HPLC法测定人血清中阿米卡星的浓度及临床应用
徐兰,汪凤华,任琦,陈集志,李刚*
1.中国人民解放军联勤保障部队第九○八医院药学科,南昌 330002;2.南昌大学第四附属医院,南昌 330003;3.江西省药品检验检测研究院,国家药品监督管理局中成药质量评价重点实验室,江西省药品与医疗器械质量工程技术研究中心,南昌 330029
阿米卡星是一种半合成氨基糖苷类抗生素,常被经验性联合青霉素类或β-内酰胺类抗菌药物用于治疗Gˉ多重耐药菌感染,且不会被普通细菌酶和低耐药性细菌所激活[1],临床上常用于呼吸道感染、骨关节感染、败血症、中枢神经系统感染、手术后感染及复发性尿路感染等[2]。但由于其具有严重的不良反应如肾毒性、听力损害[3],因而使用剂量较小且临床疗效差,特别是在重症多重耐药菌感染时使用阿米卡星非常谨慎。阿米卡星具有浓度依赖性,血浆峰浓度/细菌MIC的比值是评价抗菌活性的最好参数[4],更高的峰浓度可以获得更为理想的治疗效果[5,6],临床上需对于ICU重症感染患者给予高于常规剂量的阿米卡星。因此,对重症感染患者需进行血药浓度监测,按血药浓度监测结果及时调整给药方案,减少耐药菌株的产生,提高治疗成功率。
目前关于阿米卡星的血清浓度测定包括微生物 法[7]、荧光偏振免疫法[8]、HPLC-UV法[9]、HPLC-MS/MS法[2,10]等,但考虑到柱前或柱后衍生化法、固相萃取法操作繁琐,测定结果容易受衍生化试剂及衍生化产物稳定性的影响,微生物法准确度欠佳,而普通医院无法配备价格昂贵的液质联用仪,均无法快速有效进行阿米卡星血清浓度监测。本试验参考相关文献,采用HPLC-末端吸收法,对血样处理方法、色谱条件进行优化调整,建立了一种准确度高、快速、简便、重现性好的HPLC法测定人血清中阿米卡星浓度,并应用于本院血药浓度监测,为临床医师安全合理使用阿米卡星提供参考。
1 仪器与试药
岛津LC-15C型高效液相色谱仪(包括SPD-15C二极管阵列检测器,LC-15C泵,CTO-15C柱温箱,SIL-10AF自动进样器);AZJ-2002-C型超纯水仪(美国艾科浦国际有限公司);KQ3200E超声波清洗器(昆山市超声仪器有限公司);AUW120D型1/10万电子分析天平(日本岛津公司);TG1650-WS型高速离心机(上海卢湘仪离心机仪器有限公司);微量移液器(Thermo Fisher科技有限公司)。阿米卡星对照品(中国食品药品检定研究院,批号:130335-200204,每mg相当于655单位);辛烷磺酸钠(上海蓝季科技发展有限公司,批号:110910,分析纯);无水硫酸钠、磷酸二氢钾(西陇科学股份有限公司,分析纯);乙腈、甲醇为色谱纯,水为纯化水,其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件[11]色谱柱为Wondasil C18柱(4.6 mm×150 mm,5 μm);预柱为C18保护柱(3.0 mm×4 mm,迪马科技公司);流动相:辛烷磺酸钠1.8 g和无水硫酸钠20 g,加pH 3.0的0.2 mol/L磷酸盐缓冲液(0.2 mol/L磷酸二氢钾溶液,用0.2 mol/L磷酸溶液调节pH值至3.0)50 mL和乙腈75 mL溶解,用水稀释至1 000 mL;流速为1.3 mL/min;检测波长为200 nm;柱温为40 ℃;进样量为20 μL。
2.2 对照品溶液的配制精密称取阿米卡星对照品0.023 6 g,置25 mL量瓶中,加注射用水溶解并定容至刻度,摇匀,即得浓度为0.944 0 mg/mL的阿米卡星对照品溶液,分装于1.5 mL EP管中,置-20 ℃冰箱保存,备用。
2.3 样品处理密量取血浆样品200 μL,加入10%高氯酸溶液50 μL,涡旋振荡2 min,15 000 r/min离心15 min,取上清液,经0.45 μm微孔滤膜滤过后,进样分析。
2.4 专属性试验按“2.1”项下色谱条件测定,进样分析,色谱图见图1。由结果可知,经甲醇、乙腈、正己烷萃取的血样,阿米卡星保留时间处无峰或者峰面积非常小,提取回收率非常低,不适合阿米卡星血样处理。经10%高氯酸萃取的阿米卡星血样,色谱峰形较好,保留时间约为9.8 min,12 min左右有一杂质峰,但不干扰阿米卡星峰型,分离度大于1.5,且血清中其他内源性杂质对阿米卡星无干扰。

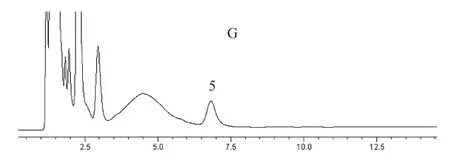
图1 HPLC色谱图
2.5 标准曲线的绘制取浓度为0.944 0 mg/mL的阿米卡星对照品溶液适量,加入超纯水稀释并配制成浓度分别为472.84、236.44、118.21、59.12、29.56、9.84、4.92、2.48 μg/mL的系列对照品溶液。精密量取空白血清150 μL,置1.5 mL离心管中,加入阿米卡星系列对照品溶液50 μL,使阿米卡星血清浓度分别为0.62、1.23、2.46、7.39、14.78、29.55、59.11、118.21 μg/mL,按“2.3”项下方法处理,进样分析,记录色谱图。以血清浓度(C,μg/mL)为横坐标,峰面积(Y)为纵坐标,绘制标准曲线,得阿米卡星的回归方程为Y=7 013.8C-6 242,r=0.999 8。定量下限浓度为0.62 μg/mL。结果表明,阿米卡星血清浓度在0.62~118.21 μg/mL范围内线性关系良好。
2.6 回收率试验分别配制低、中、高浓度为1.23、7.39、29.55 μg/mL的阿米卡星对照品血清样品,每个浓度样品各5份,按“2.3”项下方法处理,进样分析,记录色谱图,以峰面积代入回归方程计算得出各浓度的测定值,与加入浓度比较,计算方法回收率。分别配制低、中、高浓度为1.23、7.39、29.55 μg/mL的阿米卡星对照品血清样品及水溶液,每个浓度样品各5份,按“2.3”项下方法处理,进样分析,记录峰面积分别为A1、A2。绝对回收率=(血清样品峰面积/水溶液峰面积)×100%=(A1/A2)×100%。结果见表1,说明该方法符合生物样品分析要求。
表1 回收率试验结果(±s,n=5)

表1 回收率试验结果(±s,n=5)
2.7 精密度试验分别配制低、中、高浓度为1.23、7.39、29.55 μg/mL的阿米卡星对照血清样品,每个浓度样品各5份,按“2.3”项下方法处理,进行分析,测定日内5次及日间5次的精密度,结果阿米卡星的日内和日间精密度RSD均<10%,该方法符合生物样品分析要求。
2.8 稳定性试验分别配制低、中、高浓度为1.23、7.39、29.55 μg/mL的阿米卡星对照血清样品,每个浓度样品各3份,按“2.3”项下方法处理,分别考察在室温稳定性、冷藏稳定性、冻融稳定性。室温稳定性:室温放置0、2、4、6、8、12 h;冷藏稳定性:4 ℃、-20 ℃冰箱分别冷藏放置24 h;冻融稳定性:-20 ℃冰箱中冻存,取出自室温自然融化,再置-20 ℃冷冻24 h,此步骤重复2次,共进行3次冻融试验。以上样品均按“2.3”项下方法处理,进样分析,结果见表2,阿米卡星峰面积均变化不大(峰面积变化<15%,RSD<6.26%),说明阿米卡星血清样品在室温、冷藏、冻融条件下均比较稳定。
表2 血清样品阿米卡星的稳定性(±s,n=5)

表2 血清样品阿米卡星的稳定性(±s,n=5)
3 治疗药物监测
收集2019年6月至2020年6月我院ICU住院的重症感染患者16例,患者因治疗需要联合青霉素类或β-内酰胺类抗菌药物用于治疗革兰阴性多重耐药菌感染。给药方案为0.4 g加入250 mL 0.9%氯化钠注射液中静脉滴注,q12 h。在用药48~72 h血药浓度达稳态后,经外周静脉采血,谷浓度在阿米卡星静滴前30 min采血,峰浓度在阿米卡星静滴完毕后30 min采血。本试验方案经本院伦理委员会批准通过。共收集患者血清36例,测定结果为峰浓度 在21.35~43.18 μg/mL[(31.56±4.73)μg/mL],有6例样品浓度低于定量下限,其余样本谷浓度在1.05~8.59 μg/mL[(4.36±1.13)μg/mL]。
4 讨论
本试验比较了10%高氯酸、甲醇、乙腈、正己烷等几种蛋白沉淀剂对血浆样品分离效果的影响。经甲醇处理的样品,静置后进样瓶底部有白色沉淀物,且阿米卡星提取回收率较低,仅有25%左右,不能满足定量下限的要求;经乙腈处理的样品,阿米卡星保留时间处无色谱峰出现,这与张亮[9]采用乙腈进行萃取的结果不一致,分析原因可能与色谱柱、高效液相色谱仪型号不一致或者流动相选择不同有关。而经正己烷提取后的血浆中杂质峰较多,干扰阿米卡星峰;经10%高氯酸沉淀蛋白后,阿米卡星提取回收率达90%左右,且干扰峰较少,能减少血清中杂质干扰,故选择10%高氯酸作为蛋白沉淀试剂。对10%高氯酸的用量(20 μL、50 μL)进行考察,20 μL用量沉淀后的血样较浑浊,虽然提取回收率较高(达96%),但静置后底部仍有白色沉淀物,沉淀效果欠佳;50 μL用量处理的血样,上清液静置24 h后仍澄清,且色谱图干扰峰较少,提取回收率满意。
由监测结果可知,不同患者的谷、峰浓度差异比较大,其中6例患者谷浓度低于定量下限。阿米卡星检测波长为200 nm,属于末端吸收,灵敏度较低,定量下限为0.62 μg/mL。部分患者阿米卡星在体内的代谢及清除较快,给药后24 h内排泄90%以上,体内药物浓度低于0.62 μg/mL,本方法无法检测到。阿米卡星血清浓度个体化差异较大,分析原因可能与ICU重症感染患者存在影响药物体内分布和排泄的多种因素有关,比如高龄、低蛋白血症、肝肾功能损伤等,这些病理生理变化都会造成药物在体内过程发生改变,分布容积增大、药物稀释、清除增加等。而且阿米卡星主要经肾小球滤过排泄,各器官功能的下降也可引起药物代谢及清除下降,ICU重症感染患者肾功能差异较明显。这些原因都会造成阿米卡星在重症患者体内浓度存在一定的个体化差异。
阿米卡星具有耳毒性和肾毒性,因此非常有必要通过优化抗菌药物治疗方案,严密监测患者血清浓度(谷浓度>5 μg/mL为毒性阈值)。因本研究测定病例数较少,下一步研究方案拟扩大样本测定量,并监测患者肾功能、听力,将阿米卡星的血清浓度与抗菌效果、不良反应有效结合起来,提高抗感染治疗效果的同时避免阿米卡星引起的不良反应,得到优化的、个体化的给药方案应用于临床,促进抗菌药物的持续质量改进,为药学同行提供参考依据。

