新型1,3,4-噻二唑硫醚哒嗪酮衍生物的合成及生物活性
胡伟男, 朱 梅, 漆亚云, 陈 洁, 唐思雨, 唐震华, 王贞超, 2, 3*, 欧阳贵平, 2, 3*
(1. 贵州大学 药学院,贵州 贵阳 550025; 2. 贵州医科大学 药用植物功效与利用国家重点实验室,贵州 贵阳 550014; 3. 贵州大学 贵州省药物合成重点实验室,贵州 贵阳 550025)
哒嗪是一种含氮的六元杂环,具有广谱的生物活性和结构多样性,并广泛分布在医药、农药等研究领域[1],哒嗪结构被引入许多农药分子中,例如杀菌剂、杀虫剂、除草剂、植物生长调节剂等,例如广谱触杀性杀螨杀虫剂吡虫啉(Pyridaben)[2-3],有机磷杀虫剂哒嗪硫磷(Pyridaphenthion)[4-5],以及针对水稻纹枯病菌和花生白霉病菌等立枯丝核菌开发的杀菌剂二氯甲嗪(Diclomezine)[6]等。同时,1,3,4-噻二唑结构也在农药领域广泛应用,例如对水稻白叶枯病菌和柑桔溃疡病菌具有良好杀菌作用的杀菌剂叶枯唑(Bismerthiazol)[7-9]。
以上市药物Pyridaben为模板化合物,应用药物活性基团拼接原理,将1,3,4-噻二唑杂环与哒嗪酮结构通过硫醚相连接,构建出1,3,4-噻二唑硫醚哒嗪酮衍生物。以糠氯酸(1)为起始原料,与叔丁基肼盐酸盐环合制得2-叔丁基-4,5-二氯-3(2H)哒嗪酮(2)[10-11];取代苯胺或脂肪胺(3a~3k),与二硫化碳和氯甲酸乙酯反应得到异硫氰酸酯衍生物(4a~4k)[12-13]; 4肼解得硫代氨基脲衍生物(5a~5k)[14-15];5与二硫化碳在碱性条件下环合,得到5-胺基-1,3,4-噻二唑-2-硫醇衍生物(6a~6k)[16-17];6与2-叔丁基-4,5-二氯-3(2H)-哒嗪酮发生亲核取代反应,得2-取代-4-氯-5-[5-取代胺基-2-(1,3,4-噻二唑基)-巯基]-3(2H)-哒嗪酮衍生物(7a~7k, Scheme 1)[18]。所合成的新化合物经1HNMR、13CNMR、 IR、 MS(ESI)和元素分析表征。采用生长速率法,在100 mg/L浓度下,测试了化合物对小麦赤霉病菌(G.zeae)、辣椒枯萎病菌(F.oxysporum)、苹果腐烂病菌(C.mandshurica) 3种植物病原菌的抑菌活性的测定。
1 实验部分
1.1 仪器与试剂
X-4型数字显微熔点仪;QY-20型三用紫外分析仪;JEOL-ECX 500 MHz型核磁共振仪(TMS为内标);Shimadzu IRprestige-21型傅立叶红外光谱测定仪(KBr压片);Bruker maXis 4G UHR-TOF型质谱仪;Elementar Vario III型元素分析仪。
所用试剂均为分析纯或化学纯。
1.2 合成
(1) 2-叔丁基-4,5-二氯-3(2H)哒嗪酮(2)的合成
称取叔丁基肼盐酸盐3.7 g(29.7 mmol)、醋酸钠2.2 g(26.8 mmol) 溶解于60 mL水中,10 ℃下分批加入糠氯酸4.5 g(26.6 mmol),反应1 h后瓶内产生大量黄色沉淀。向体系内加入50 mL甲苯,40 ℃反应6 h, 停止加热,静置、分液,有机相依次用15% NaOH溶液洗涤一次,饱和NaCl溶液洗涤两次,无水MgSO4干燥,过滤,脱溶,重结晶,得淡黄色晶体21.72 g,收率62.7%。
(2)4a~4k的合成(以4a为例)
将苄胺2.28 g(30 mmol) 与15 mL三乙胺置于圆底烧瓶中搅拌,冰浴下加入二硫化碳2.28 g(30 mmol),滴毕后室温搅拌12 h,体系中有大量淡黄色固体出现,向体系内加入25 mL氯仿后加入少量三乙胺,冰浴下再加入氯甲酸乙酯3.26 g(30 mmol),室温搅拌6 h。反应结束后,将混合物倒入烧杯中,用1 mol/L盐酸溶液调节pH至中性,氯仿萃取分出有机相,无水硫酸镁干燥,减压蒸馏除去溶剂,重结晶得苯基异硫氰酸酯4a2.28 g,收率56.2%。
(3)5a~5k的合成(以5a为例)
往圆底烧瓶中加入80%水合肼1.13 g(18 mmol)和25 mL异丙醇,室温下向混合物中缓慢滴加溶于25 mL异丙醇的苄基异硫氰酸酯5a2.03 g(15 mmol),滴加过程中有大量白色固体析出,充分搅拌。滴加完毕后,室温搅拌2 h,过滤,干燥,无水乙醇重结晶得白色片状固体5a1.32 g,收率52.6%。
(4)6a~6k的合成(以6a为例)
称取4-苄基-3-硫代氨基脲6a1.25 g(7.5 mmol),氢氧化钾0.63 g(11.25 mmol)溶解于50 mL无水乙醇中,再加入二硫化碳0.86 g(11.25 mmol),加热回流,4 h后反应结束,减压除去溶剂,将反应混合物倒入30 mL冰水中,1 mol/L的HCl溶液调节pH至酸性,有大量类白色固体析出,抽滤,干燥,乙醇重结晶,得淡黄色针状固体6a0.82 g,收率52.0%。
(5)7a~7k的合成(以7a为例)
称取2-叔丁基-4,5-二氯-3(2H)-哒嗪酮(2)0.33 g(1.5 mmol)、无水碳酸钾0.31 g(2.25 mmol)溶解于40 mL丙酮中,分批向反应瓶中加入5-苄胺基-1,3,4-噻二唑-2-硫醇(6a)0.31 g(1.5 mmol),温室搅拌8 h,减压除去溶剂,向混合物中加入10 mL冰水,抽滤,干燥,柱层析分离纯化得淡黄色固体7a0.24 g,收率41.3%。
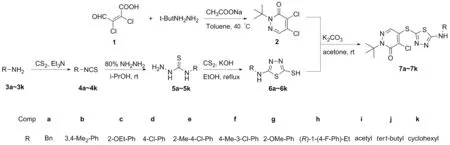
Scheme 1
2-叔丁基-4-氯-5-[5-苄胺基-2-(1,3,4-噻二唑基)-巯基]-3(2H)-哒嗪酮(7a): 类白色晶体, 收率41.3%, m.p.142~144 ℃;1H NMR(500 MHz, DMSO-d6)δ: 8.85(t,J=5.7 Hz, 1H, NH), 7.40(s, 1H, NCH), 7.36~7.34(m, 4H, Ph-H), 7.30(m, 1H, Ph-H), 4.57(d,J=5.7 Hz, 2H, CH2), 1.56(s, 9H, 3CH3);13C NMR(125 MHz, DMSO-d6)δ: 173.6, 155.3, 140.2, 139.4, 138.4, 130.7, 130.1, 129.0, 128.2, 127.9, 66.4, 48.6, 27.8; IR(KBr)ν: 3271, 3076, 2974, 2855, 1636, 1544, 1495, 1454, 1395, 1358, 1271, 1207, 1105, 937, 785, 698 cm-1; MS(ESI)m/z: 430.1{[M+Na]+}; Anal.calcd for C17H18N5OS2Cl: C 50.05, H 4.45, N 17.17, found C 50.44, H 4.41, N 16.80。
2-叔丁基-4-氯-5-[5-(3,4-二甲苯胺基)-2-(1,3,4-噻二唑基)-巯基]-3(2H)-哒嗪酮(7b): 淡黄色固体,收率39.5%, m.p.218~220 ℃;1H NMR(500 MHz, DMSO-d6)δ: 10.67(s, 1H, NH), 7.49(s, 1H, NCH), 7.36(s, 1H, Ph-H), 7.33(d,J=8.1 Hz, 1H, Ph-H), 7.13(d,J=8.6 Hz, 1H, Ph-H), 2.23(s, 3H, CH3), 2.19(s, 3H, CH3), 1.56(s, 9H, 3CH3);13C NMR(125 MHz, DMSO-d6)δ: 169.9, 155.4, 142.1, 139.1, 137.6, 131.5, 131.1, 130.6, 128.4, 126.1, 119.9, 116.2, 66.4, 27.8, 20.2, 19.3; IR(KBr)ν: 3262, 3073, 2963, 2922, 1663, 1618, 1557, 1506, 1483, 1456, 1395, 1211, 1138, 932, 810, 783 cm-1; MS(ESI)m/z: 444.1{[M+Na]+}; Anal.calcd for C18H20N5OS2Cl: C 51.23, H 4.78, N 16.60, found C 51.47, H 4.86, N 16.33。
2-叔丁基-4-氯-5-[5-(2-乙氧苯胺基)-2-(1,3,4-噻二唑基)-巯基]-3(2H)-哒嗪酮(7c): 淡黄色固体,收率40.5%, m.p.160~162 ℃;1H NMR(500 MHz, DMSO-d6)δ: 10.08(s, 1H, NH), 8.22(d,J=7.5 Hz, 1H, Ph-H), 7.47(s, 1H, NCH), 7.08~7.04(m, 2H, Ph-H), 6.99~6.96(br, m, 1H, Ph-H), 4.17~4.13(q, 2H,J=6.6 Hz, OCH2), 1.56(s, 9H, 3CH3) ,1.39(t,J=6.6 Hz, 3H, CH3);13C NMR(125 MHz, DMSO-d6)δ: 170.1, 155.4, 148.5, 143.4, 139.2, 131.1, 130.6, 129.5, 124.5, 121.1, 120.7, 112.8, 66.4, 64.5, 27.7, 15.1; IR(KBr)ν: 3265, 3132, 2982, 2933, 1639, 1599, 1537, 1472, 1454, 1395, 1369, 1250, 1207, 939, 742 cm-1; MS(ESI)m/z: 460.1{[M+Na]+}; Anal.calcd for C18H20N5O2S2Cl: C 49.36, H 4.60, N 15.99, found C 49.88, H 4.39, N 15.76。
2-叔丁基-4-氯-5-[5-(4-氯苯胺基)-2-(1,3,4-噻二唑基)-巯基]-3(2H)-哒嗪酮(7d): 白色固体,收率38.5%, m.p.231~233 ℃;1H NMR(500 MHz, DMSO-d6)δ: 10.95(s, 1H, NH), 7.68(d,J=8.0 Hz, 2H, Ph-H), 7.51(s, 1H, NCH), 7.44(d,J=8.0 Hz, 2H, Ph-H), 1.56(s, 9H, 3CH3);13C NMR(125 MHz, DMSO-d6)δ: 169.2, 155.4, 143.6, 139.3, 139.0, 131.2, 130.6, 129.6, 126.7, 120.1, 66.4, 27.8; IR(KBr)ν: 3383, 3047, 2986, 1662, 1601, 1552, 1451, 1431, 1359, 1305, 1226, 1181, 1084, 1043, 925, 813 cm-1; MS(ESI)m/z: 450.0{[M+Na]+}; Anal.calcd for C16H15N5OS2Cl2: C 44.86, H 3.53, N 16.35, found C 44.74, H 3.58, N 16.43。
2-叔丁基-4-氯-5-[5-(3-氯-2-甲苯胺基)-2-(1,3,4-噻二唑基)-巯基]-3(2H)-哒嗪酮(7e): 淡黄色固体, 收率39.5%, m.p.199~201 ℃;1H NMR(500 MHz, DMSO-d6)δ: 10.20(s, 1H, NH), 7.85(d,J=7.5 Hz 1H, Ph-H), 7.51(s, 1H, NCH), 7.29~7.24(m, 2H, Ph-H), 2.34(s, 3H, CH3), 1.56(s, 9H, 3CH3);13C NMR(125 MHz, DMSO-d6)δ: 171.7, 155.3, 143.0, 140.4, 139.2, 134.7, 131.1, 130.4, 128.7, 128.1, 126.1, 121.9, 66.4, 27.8, 15.5; IR(KBr)ν: 3300, 3098, 2978, 2926, 1641, 1601, 1580, 1545, 1479, 1367, 1267, 1209, 1105, 937, 779 cm-1; MS(ESI)m/z: 464.0{[M+Na]+}; Anal.calcd for C17H17N5OS2Cl2: C 46.15, H 3.87, N 15.83, found C 46.14, H 3.89, N 15.77。
2-叔丁基-4-氯-5-[5-(3-氯-4-甲苯胺基)-2-(1,3,4-噻二唑基)-巯基]-3(2H)-哒嗪酮(7f): 淡黄色固体, 收率37.0%, m.p.212~214 ℃;1H NMR(500 MHz, DMSO-d6)δ: 10.89(s, 1H, NH), 7.87(s, 1H, Ph-H), 7.52(s, 1H, NCH), 7.36~7.35(m, 2H, Ph-H), 2.30(s, 3H, CH3), 1.56(s, 9H, 3CH3);13C NMR(125 MHz, DMSO-d6)δ: 169.1, 155.3, 143.5, 140.1, 139.4, 139.0, 134.0, 132.1, 131.2, 129.9, 118.5, 117.2, 66.4, 27.8, 19.4; IR(KBr)ν: 3281, 3076, 2982, 2873, 1638, 1605, 1543, 1485, 1452, 1396, 1366, 1206, 1086, 935, 974, 806 cm-1; MS(ESI)m/z: 464.0{[M+Na]+}; Anal.calcd for C17H17N5OS2Cl2: C 46.15, H 3.87, N 15.83, found C 46.14, H 4.00, N 15.99。
2-叔丁基-4-氯-5-[5-(2-甲氧苯胺基)-2-(1,3,4-噻二唑基)-巯基]-3(2H)-哒嗪酮(7g): 淡黄色固体, 收率40.0%, m.p.170~172 ℃;1H NMR(500 MHz, DMSO-d6)δ: 10.24(s, 1H, NH), 8.29(d,J=7.5 Hz, 1H, Ph-H), 7.46(s, 1H, NCH), 7.10~7.06(m, 2H, Ph-H), 7.00(m, 1H, Ph-H), 3.90(s, 3H, OCH3), 1.56(s, 9H, 3CH3);13C NMR(125 MHz, DMSO-d6)δ: 169.8, 155.3, 149.1, 143.5, 139.2, 131.1, 130.5, 129.3, 124.2, 121.2, 120.2, 111.7, 66.4, 56.3, 27.7; IR(KBr)ν: 3240, 3049, 2960, 2878, 1659, 1604, 1568, 1497, 1450, 1368, 1265, 1126, 867, 752 cm-1; MS(ESI)m/z: 446.1{[M+Na]+}; Anal.calcd for C17H18N5O2S2Cl: C 48.16, H 4.28, N 16.52, found C 48.25, H 4.16, N 16.66。
(R)-2-叔丁基-4-氯-5-[5-(1-对氟苯乙胺基)-2-(1,3,4-噻二唑基)-巯基]-3(2H)-哒嗪酮(7h): 淡黄色固体, 收率36.2%, m.p.108~110 ℃;1H NMR(500 MHz, DMSO-d6)δ: 8.96(d,J=6.9 Hz, 1H, NH), 7.46~7.43(m, 2H, Ph-H), 7.30(s, 1H, NCH), 7.46~7.43(t,J=8.9 Hz, 2H, Ph-H), 4.92~4.89(m, 1H, CH), 1.55(s, 9H, 3CH3), 1.50(d,J=6.9 Hz, 3H, CH3);13C NMR(125 MHz, DMSO-d6)δ: 172.8, 160.9, 155.3, 140.1, 140.0, 139.4, 130.7, 130.1, 128.6, 115.8, 66.4, 54.5, 27.7, 23.5; IR(KBr)ν: 3308, 3063, 2976, 2930, 1641, 1549, 1497, 1456, 1368, 1260, 1209, 1146, 935, 785 cm-1; MS(ESI)m/z: 462.1{[M+Na]+}; Anal.calcd for C18H19N5OS2FCl: C 49.14, H 4.35, N 15.92, found C 49.14, H 4.40, N 15.90。
2-叔丁基-4-氯-5-[5-(N-乙酰基)-2-(1,3,4-噻二唑基)-巯基]-3(2H)-哒嗪酮(7i): 白色固体,收率44.5%, m.p.233~235 ℃;1H NMR(500 MHz, DMSO-d6)δ: 13.00(s, 1H, NH), 7.44(s, 1H, NCH), 2.23(s, 3H, CH3), 1.55(s, 9H, 3CH3);13C NMR(125 MHz, DMSO-d6)δ: 169.8, 163.3, 155.4, 149.3, 138.6, 131.6, 131.4, 66.4, 27.8, 22.9; IR(KBr)ν: 3420, 3152, 2984, 2772, 1714, 1655, 1568, 1541, 1497, 1454, 1422, 1395, 1103, 934, 785 cm-1; MS(ESI)m/z: 382.0{[M+Na]+}; Anal.calcd for C12H14N5O2S2Cl: C 40.05, H 3.92, N 19.46, found C 40.21, H 4.01, N 19.32。
2-叔丁基-4-氯-5-[5-叔丁胺基-2-(1,3,4-噻二唑基)-巯基]-3(2H)-哒嗪酮(7j): 淡黄色固体, 收率40.6%, m.p.194~196 ℃;1H NMR(500 MHz, DMSO-d6)δ: 8.19(s, 1H, NH), 7.33(s, 1H, NCH), 1.56(s, 9H, 3CH3), 1.41(s, 9H, 3CH3);13C NMR(125 MHz, DMSO-d6)δ: 171.4, 155.3, 139.7, 139.5, 130.7, 130.1, 66.4, 54.1, 28.6, 27.8; IR(KBr)ν: 3308, 3063, 2976, 2930, 1641, 1549, 1497, 1456, 1368, 1260, 1209, 1146, 935, 785 cm-1; MS(ESI)m/z: 396.1{[M+Na]+}; Anal.calcd for C14H20N5OS2Cl: C 44.97, H 5.39, N 18.73, found C 45.01, H 5.40, N 18.90。
2-叔丁基-4-氯-5-[5-环己胺基-2-(1,3,4-噻二唑基)-巯基]-3(2H)-哒嗪酮(7k): 白色固体,收率42.1%, m.p.191~193 ℃;1H NMR(500 MHz, DMSO-d6)δ: 8.36(d,J=7.5 Hz, 1H, NH), 7.33(s, 1H, NCH), 3.62~3.58(m, 1H, CH), 1.99~1.97(m, 2H, CH2), 1.71~1.70(m, 2H, CH2), 1.55(s, 9H, 3CH3), 1.34~1.27(m, 6H, 3CH2);13C NMR(125 MHz, DMSO-d6)δ: 172.8, 155.3, 139.6, 139.0, 130.6, 129.9, 66.4, 54.4, 32.4, 27.7, 25.6, 24.7; IR(KBr)ν: 3177, 3059, 2932, 2857, 1651, 1570, 1454, 1366, 1265, 1211, 1140, 934, 845 cm-1; MS(ESI)m/z: 422.1{[M+Na]+}; Anal.calcd for C16H22N5OS2Cl: C 48.05, H 5.54, N 17.51, found C 48.14, H 5.40, N 17.57。
1.3 生物活性测试
采用生长速率法[19]测试目标产物对小麦赤霉病菌(G.zeae)、辣椒枯萎病菌(F.oxysporum)、苹果腐烂病菌(C.mandshurica)的抑菌活性。
2 结果与讨论
2.1 合成
目标化合物7a~7k的合成路线如Scheme 1所示。在以中间体6a~6k合成目标化合物7a~7k的过程中探索了不同缚酸剂、溶剂、反应温度、反应时间对于产率的影响。结果发现,当以丙酮、DMF为溶剂,无水碳酸或三乙胺为催化剂时,目标化合物收率相当。另外,在DMF中进行反应时间相对较短;但与丙酮相比较,DMF后处理相对比较麻烦,且耗时较多。综合考虑后,选择丙酮/K2CO3作反应体系为宜。
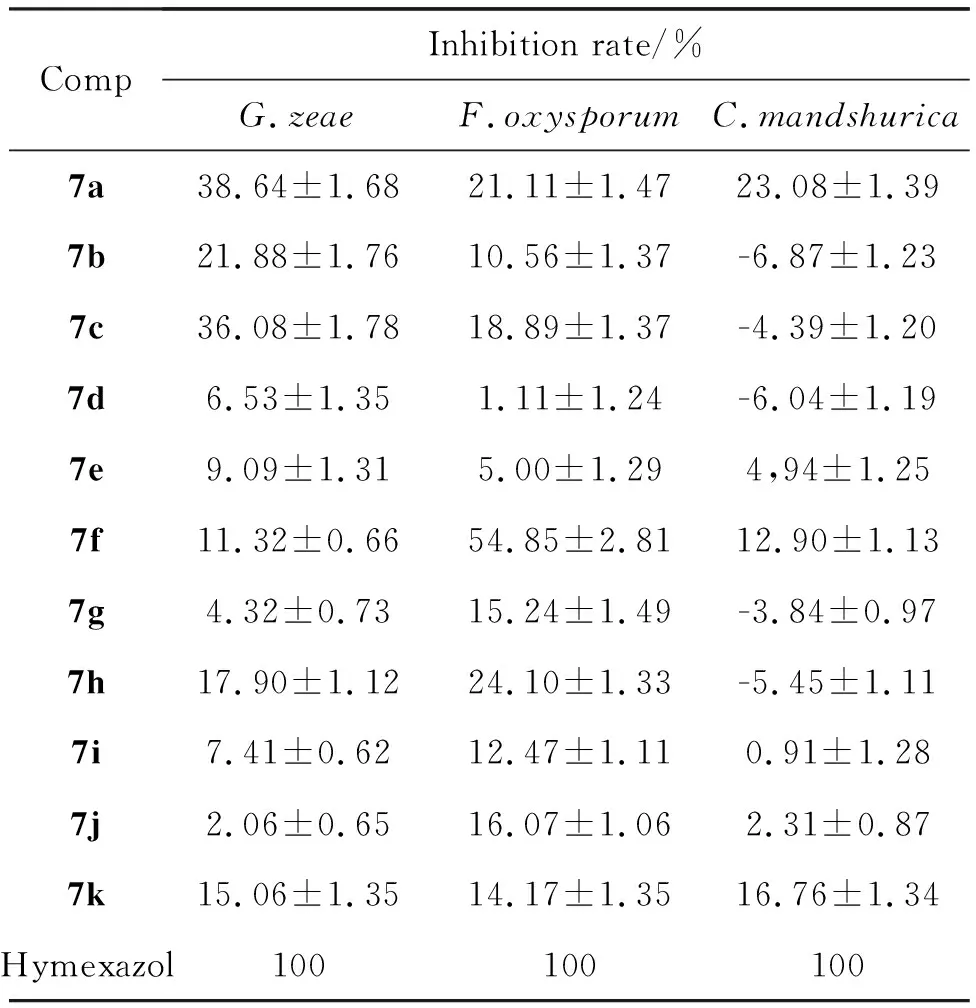
表1 部分目标化合物在100 mg/L药剂浓度下对3种植物病原菌的抑制活性
随着反应温度的不断升高,目标化合物的产率在降低。因为随着反应温度的升高,4,5-二氯哒嗪酮环位上的两个氯原子均参与了反应,生成了4,5-二取代的副产物。通过实验数据比较可知,当反应温度控制在35 ℃以下,化合物的收率较高。
2.2 抑菌活性
表1的活性数据显示,在100 mg/L浓度下,部分化合物表现出一定的抑制小麦赤霉病菌、辣椒枯萎病菌和苹果腐烂病菌的生物活性。其中化合物7a小麦赤霉病菌的抑制率为38.6%;7f对辣椒枯萎病菌的抑制率为54.9%。
2.3 化合物构效关系讨论
目标化合物活性评价的结果显示,部分化合物表现出了一定的的抗植物病原菌活性,其中取代基含有芳环的衍生物的抗菌活性,普遍强于脂肪族取代基的衍生物,在含有芳环取代的化合物中7a和7f分别对G.zeae和F.oxysporum表现出最好的抗菌活性,在不同取代的芳香性的苄基取代系列化合物中,4-甲基-3-氯苯基取代的化合物7f表现出了一定抗F.oxysporum活性,并且随着取代基的位置和取代基团发生变化时活性降低,含有供电子基取代的化合物活性普遍优于吸电子基团,在含供电子基团-CH3和-OEt的化合物7b和7c对G.zeae和F.oxysporum的抗菌活性高于含有吸电子原子Cl的7d和7e。
以糠氯酸、取代肼、芳香(脂肪)胺为起始原料,设计合成了11个新型1,3,4-噻二唑硫醚哒嗪酮衍生物,所有化合物的结构均通过1H NMR、13C NMR、 IR、 ESI-MS和元素分析的确证。对目标化合物合成条件进行了优化,确定了较优的合成条件:在室温条件下,以丙酮为溶剂,无水碳酸钾作缚酸剂,反应6~8 h,可以得到较好的收率。采用离体生长速率法,对目标化合物进行了抑菌活性的测试。结果表明:在100 mg/L浓度下,部分化合物表现出一定的抑制小麦赤霉病菌、辣椒枯萎病菌和苹果腐烂病菌的生物活性。其中化合物7a对小麦赤霉病菌的抑制率为38.6%;7f对辣椒枯萎病菌的抑制率为54.9%。构效关系分析表明,增强取代基芳环的电子云密度可加强对植物病原菌的抑制活性。

