球囊导管在后SAMMPRIS时代治疗颅内动脉粥样硬化性狭窄疾病的研究进展
唐垚 王子亮 贺迎坤 李天晓 白卫星 康晓雨 许斌 何艳艳 赵耀
一、背景
卒中目前已经成为我国成年人死亡及致残的首要原因,急性缺血性卒中约占全部卒中的80%[1]。颅内动脉粥样硬化疾病(intracranial atherosclerotic stenosis,ICAS)是引起缺血性脑卒中(ischemic stroke)的重要原因之一,2014年中国症状性颅内大动脉狭窄与闭塞研究(Chinese Intracranial Atherosclerosis,CICAS)结果显示中国缺血性卒中或短暂性脑缺血发作(transient ischemic attack,TIA)患者中颅内动脉粥样硬化发生率为46.6%,伴有ICAS的患者症状更重,住院时间更长,卒中复发率更高,且随狭窄程度而升高[2]。因此对于ICAS的治疗探索显得尤为关键。
ICAS的治疗方式仍存在争议,介入治疗作为重要的治疗方式,其发展充满曲折。目前介入治疗主要包括球囊血管成形术(percutaneous transluminal balloon angioplasty,PTBA)、球囊扩张式支架置入术、自膨式支架置入术。1980年Sundt TM等首先报道了应用PTBA治疗ICAS[3]。但对于血管夹层、弹性回缩等导致的手术失败,PTBA似乎无法解决。APOLLO支架和Wingspan支架相继成功上市以及早期美国Wingspan注册研究和美国国立卫生研究院(National Institutes of Health,NIH)Wingspan注册研究成功,使人们对于支架成形治疗寄予厚望。但在进一步的研究过程中不幸折戟沉沙:支架植入术和积极的药物治疗防止颅内动脉狭窄性脑卒中复发(stenting versus aggressive medical therapy for intracranial arterial stenosis,SAMMPRIS)试验以及维特斯缺血性脑卒中颅内支架治疗的研究试验(vitesse intracranial stent study for ischemic stroke therapy,VISSIT)均显示支架置入组围手术期并发症显著高于药物治疗组,不支持血管内支架治疗[4-5]。这无疑给发展迅速的介入治疗ICAS蒙上一层阴影。放慢脚步,重新思考,对于ICAS介入治疗手术安全是成功关键,因此在后SAMMPIRS时代,操作简单安全的球囊再次回到人们视线。材料先进、操作安全的新型颅内球囊导管不断涌现,如颅内快速交换球囊、药物涂层球囊等,给ICAS介入治疗开辟了新的临床思路,球囊成形术得以灌入新活力。本研究对球囊导管的分类、结构、性能以及球囊导管治疗颅内动脉粥样硬化性狭窄疾病的应用进展进行了综述。
二、球囊结构、分类及性能
(一)球囊结构
球囊导管的结构大同小异,主要分为球囊尖端、球囊、连接段和推送杆,球囊上有不透X线的金属焊接点,称为球囊标记。一般直径1.5 mm或更小的球囊只有一个位于中部的标记点,直径2.0 mm及以上的球囊有两个标记点,位于球囊两端。球囊尖端多为锥形并采用激光焊接技术连接。球囊目前多采用亲水涂层材料以增强通过病变的能力,推送杆由金属或高分子材料结合中心钢丝构成。球囊和推送杆中间由连接段构成,连接段影响球囊的推送性、抗折能力,通常会加入中心钢丝增强连接段的支撑力。
(二)球囊分类
球囊根据材料特点可分为顺应性球囊、半顺应性球囊和非顺应性球囊。顺应性球囊由于随压力的增大直径增加过快,遇到较硬的病变,球囊扩张不均匀,两端过度膨胀,易出现血管夹层,故临床已较少使用;半顺应性球囊多采用尼龙材料制成,球囊柔软,通过性和跟踪性好,多用于狭窄病变的预扩张处理,辅助测量病变直径、长度和形态;非顺应性球囊直径随压力增大呈均匀性增加,且增幅明显小于半顺应性球囊,可耐受较高的压力,爆破压高,主要用于支架植入后扩张处理及钙化病变处理等。目前颅内专用球囊较少,主要有半顺应性球囊Gateway、Neuro RX等。在冠脉,半顺应性球囊有Sprinter系列球囊、Ryujin球囊、Emerge球囊等,非顺应性球囊如NC Sprinter球囊、Quantum球囊等。临床工作中迫切期待更多专用于颅内的球囊上市。
根据设计特点可分为普通球囊、切割球囊、药物涂层球囊、双导丝球囊、灌注球囊以及冷冻球囊等。目前颅内动脉粥样硬化性狭窄使用最多的还是普通球囊,切割球囊和双导丝球囊应用较少。药物涂层球囊近年来逐渐开始报道使用,表现出不错的应用前景。
根据使用特点可分为同轴整体交换(over the wire,OTW)球囊、快速交换球囊和固定导丝球囊。OTW球囊易于交换钢丝,推送性能好,但操作稍复杂,需要两个术者;快速交换球囊可方便快捷地交换球囊,便于操作,缩短手术时间,只需一个术者,但不易于钢丝的重新塑形及交换钢丝,推送力不如OTW球囊好;固定导丝球囊目前已基本被淘汰。近年来颅内快速交换球囊的出现,对于优化手术操作及丰富颅内扩张球囊产品起到了一定作用。
根据冠脉和外周血管内治疗经验,按球囊直径大小,可大致分为小球囊(2~5 mm)、普通球囊(5~12 mm)和大球囊(≥12 mm)。而对于颅内血管主要使用1.5~6 mm大小的球囊。对于颈动脉、椎-基底动脉一般使用3~6 mm球囊,对于大脑中动脉、大脑前动脉及大脑后动脉多用1.5~4 mm球囊。
(三)球囊性能
球囊性能主要包括跟踪性、顺应性、推送性、灵活性以及回收性。(1)顺应性:球囊随充盈压力的增加其直径相应发生变化的性能,其高低主要取决于球囊的材料,常分为顺应性、半顺应性、非顺应性。具体使用情况上文已有叙述。(2)跟踪性:球囊在导丝指引下到达靶变的能力,理想的球囊导管具有较小的球囊外径,锥形头端设计,帮助穿过复杂的病变,以及头端与导丝密切吻合,可减少通过血管弯曲处的“鱼嘴”现象。(3)推送性:即作用于推送杆将球囊顺利到达病变的能力。球囊远近端推送杆不同设计,推送能力不尽相同。(4)灵活性:球囊的柔顺性,决定球囊通过病变的能力。灵活性、跟踪性和推送性都反映了球囊克服阻力到达病变部位的能力,三者密切相关。(5)回收性:指球囊释放后恢复其初始状态的能力。与球囊的材料及折叠方式有关,目前多为三翼折叠方式,方便扩张后的回收,对血管内膜损伤小。
三、单纯球囊血管成形术
球囊导管在治疗ICAS疾病中最主要的作用便是扩张狭窄病变。扩张狭窄又可分为直接单纯球囊血管成形、植入支架前的预扩张和植入后的后扩张。尽管早期已经成功开展单纯球囊血管成形,但受限于介入材料尚未成熟、超适应症使用冠脉球囊、术者对器械不熟练、适应症掌握不准确以及颅内血管解剖特点等原因,导致手术中出现血管夹层、破裂穿孔、侧支闭塞以及血管弹性回缩等问题,围手术期并发症率和病死率较高。由于支架成形治疗ICAS安全问题令人难以接受,单纯球囊血管成形操作简单、安全性较高,使得这一基础的术式重新回到人们视野中。后SAMMPRIS时代越来越多的研究证明单纯球囊血管成形术治疗ICAS是安全、可接受的。
(一)亚满意球囊血管成形
亚满意球囊血管成形,简单来说即在球囊血管成形治疗中选择较小直径球囊,接受适度的残余狭窄。其要求球囊大小为血管直径的50%~80%左右[6-7]。过往手术中为达到更低的残余狭窄,恢复正常血流,球囊大小选择多为血管正常直径。随着对ICAS疾病治疗的不断认识,既恢复远端组织血供,同时防止术中血栓栓塞、血管穿孔、高灌注综合征等可能比单纯追求影像结果完美更加重要。SAMMPRIS研究失败的原因是过高的围手术期并发症,并不是血流恢复不足,亚满意球囊血管成形术在限制并发症的同时恢复血流是可行的[6]。Dumont等[8]回顾性分析了41例颅内狭窄>70%的患者行亚满意单纯球囊血管成形术,30 d并发症率为4.9% (41例中出现2例并发症,1例术中穿孔,1例术后24 h内再出血),1年并发症率为9.4%。国内一项对133名接受亚满意单纯球囊血管成形术患者围手术期并发症和长期疗效进行分析[9],技术成功率97%,30 d内有9例(6.8%)出现并发症,1年的卒中和死亡率为9.0%,Kaplan-Meier分析3年无卒中生存率为87.2%。国内另一项相似研究[10]30 d卒中或死亡率2.9%,1年合并卒中或死亡率6%。日本一项对MCA主干重度狭窄的单纯球囊扩张研究[11]显示30 d卒中发生率4.2%,Kaplan-Meier分析1年无卒中和/或无死亡生存率为94.4%,2年为89.4%。一项纳入78例患者的单中心前瞻性研究[12]结果显示术后72 h内并发症率2.6%,3个月内出现缺血性卒中事件发生率1.5%,再狭窄发生率为9.2%。Okada等[13]研究显示单纯球囊血管成形治疗30 d内卒中或死亡的发生率为6.4%,30 d至1年内同侧卒中发生率为3%。
上述研究结果对比SAMMPRIS,单纯球囊扩张治疗优于SAMMPRIS支架组围手术期并发症率(14.7%),1年终点事件发生率也优于药物强化组(12.6%)。先前发表对比血管内支架置入和非亚满血管成形术的研究,后者并未在并发症率上有明显优势。这可能正是得益于亚满意球囊血管成形技术的帮助。一项对于使用亚满意球囊血管成形术的Meta分析[6]指出,该技术治疗ICAS成功率高(96.4%),30 d围术期并发症率为4.9%(95%CI:3.2%~7.5%),且前循环和后循环患者无统计学差异,30 d以上卒中或死亡率3.7%(95%CI:2.2%~6.0%)。
亚满意球囊血管成形取得成功可能得益于以下原因:(1)从解剖角度:由于颅内血管的内弹力层更厚,中膜、外膜薄且缺乏外弹力层,部分血管漂浮在脑脊液中,外壁无支撑机构,血管直径较小,病变路径迂曲,侧支循环丰富,颅内动脉粥样斑块以纤维和脂肪斑块为主,容易脱落,导致颅内血管内手术难度偏大,需要更加安全的手术方法。(2)从手术操作角度:支架植入时对血管壁的损伤,跨越狭窄时动脉粥样斑块脱落造成急性闭塞,以及金属异物引起的血管炎症反应都无疑增加了预后风险。单纯球囊血管成形减少操作,缩短手术时间,一定程度避免了不良事件的发生。(3)从球囊大小角度:使用相对正常血管直径50%~80%的球囊大小,有效防止更大球囊扩张时带来更高的血管夹层、破裂风险。(4)从有效性角度:血管成形术后从70%的狭窄改善到50%的狭窄,也相当于将血流量增加了7.29倍,结合已经存在的侧支循环,可能足以满足狭窄远端病变的代谢要求。血流量和血容量的部分恢复可能是完成血运重建的首选,这避免了狭窄患者血流量突然过大发生高灌注损伤[6]。(5)其他:球囊制造材料的发展,医生技术的提升,新型抗血小板药物,术后双抗的应用等等因素,客观上提升了手术安全性。
(二)颅内专用快速交换球囊
Gateway球囊导管在国内2006年即正式上市,但随后很长一段时间治疗颅内动脉狭窄的扩张球囊导管缺乏新型产品,临床中常常超适应证使用冠脉球囊。Gateway属于非快速交换球囊,推送能力较好,但操作复杂,需要两个术者配合,相对增加了手术难度。2016年首个获得原国家食品药品监督管理总局批准,用于颅内狭窄的快速交换球囊Neuro RX上市。快速交换球囊优点在于一位术者即可完成操作,大大减少了导丝移位的机会,节省手术时间,提高手术成功率。同时其采用双腔三折设计,回收性能优异,方便回收及再次扩张。吴等[14]比较了使用冠脉快速交换球囊与Gateway球囊预扩张,Wingspan支架成形治疗颅内动脉狭窄,结果显示使用改良快速交换预扩张球囊术后即刻残余狭窄更低、手术时间更短,但更适合于简单病变。
(三)存在的问题
单纯球囊扩张血管成形术仍存在一定问题。最常见的问题是术中发生血管夹层。但并不是所有夹层都要处理,如果前向血流无法维持时,需要植入支架补救。邓等[12]对78例患者球囊扩张后出现22例夹层(28.2%),6例无法维持稳定向前血流的给予了支架补救。Marks等纳入120例患者,25例出现夹层(20.8%),5例术中行支架补救。单纯球囊无法提供持久的径向支撑力,术后残余狭窄较高。过往研究表明单纯球囊扩张血管成形平均术后残余狭窄率约为40%[15-16]。术后过高的残余狭窄直接影响病变血管长期再狭窄的发生。Stapleton CJ等相关研究[6]指出单纯球囊扩张成形治疗ICAS长期再狭窄率为18.4%,2.7%为症状性。此外穿支闭塞、斑块脱落、血管破裂等问题也值得关注。
四、药物涂层球囊
长久以来,病人对于体内植入支架存在普遍抵触感,由此引发的焦虑抑郁情绪,对于治疗效果产生的影响不可忽视。对此“介入无植入”逐步成为我国血管介入治疗的新选择。药物涂层球囊(drug coated balloon,DCB)便是在此理念下发展而来的治疗动脉狭窄疾病的新型球囊。
(一)作用原理及部分产品
DCB原理是将抗平滑肌细胞增殖药物均匀涂层在球囊表面,通过导管输送到病变位置后扩张球囊,该球囊扩张损伤血管壁的同时,药物可向血管壁局部快速释放,经内皮细胞吸收,药物可在血管壁停留较长时间,达到抑制血管内膜增生和促进内皮化的效果,以治疗动脉狭窄。DCB已成熟地应用于治疗冠脉狭窄疾病,在治疗冠脉支架内再狭窄是首选方法之一,获得欧洲心脏病学会(European Society of Cardiology,ESC)/欧洲心胸外科协会(European Association for Cardio-Thoracic Surgery,EACTS)证据等级IA[17],《药物涂层球囊临床应用中国专家共识》推荐应用[18]。目前大多数DCB产品使用以紫杉醇为基础的涂层药物,见表1。紫杉醇无需混合后局部给药,避免了由于聚合物而引起的炎症及血栓形成;还具有良好亲脂性,能紧紧地结合到血管壁组织以抵抗被血液冲刷掉。此外,还有其他药物研究应用于DCB球囊的制备,如雷帕霉素、依维莫司、佐他莫司等。目前已上市专用于ICAS治疗的DCB仅有Aachen Resonance公司的Elutax SV球囊以及AR Baltic Medical公司的Elutax ‘3’ Neuro球囊。两款球囊都具类似的靶向沉积模式(target deposition modus,TDM),即球囊只有在与血管壁接触并受到一定压力下才能释放药物,最大限度减少DCB在路径上的药物损失[20]。
(二)药物涂层球囊治疗支架内再狭窄
血管内植入支架会引起慢性炎症反应进而导致支架内再狭窄(in-stent restenosis,ISR),患者术后需要长期服用抗血小板药物以避免晚期血栓的发生[20]。在介入治疗中,如何减少介入器械对机体的影响,降低再狭窄率,改善血流动力学,减轻炎症反应则成为了一个亟需解决的问题[21]。借鉴冠脉介入治疗丰富经验,DCB最先用于治疗颅内支架内再狭窄。Vajda等[22]最早报道了使用DCB传统球囊对脑血管病变ISR的疗效对比。发现DCB相比传统球囊在1年后再狭窄发生率上具有巨大优势(9% vs 50%)。Montorsi等[23]报道了应用DCB治疗的7例颈动脉支架术后ISR患者。结果显示DCB的技术成功率为100%。术后(6.1±1.5)个月和(13.7±1.5)个月的随访均见支架内血流通畅。Vajda等[24]联合应用DCB和自膨支架Enterparise治疗54例颅内动脉粥样硬化性狭窄,术后9个月的再狭窄率为3%,远远低于先前报道过的支架内再狭窄高发生率(24%~31%)[25-26]。
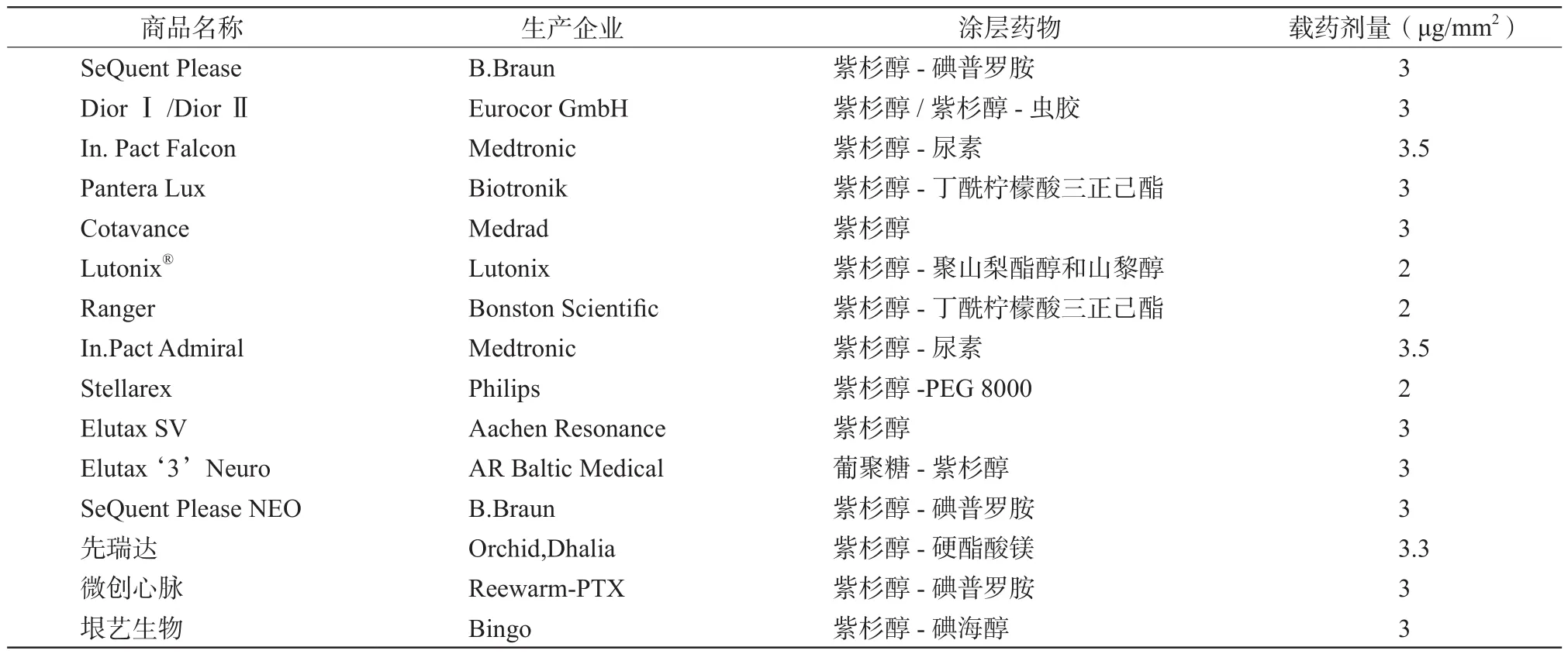
表1 国内外已上市的部分药物涂层球囊
(三)药物涂层球囊治疗ICAS
药物涂层球囊应用于颅内治疗症状性动脉粥样硬化性狭窄报道多数为回顾性单中心研究,缺乏足够样本数量,且大多数为超适应证使用,但从结果分析,DCB治疗ICAS是安全有效的(见表2)。
一项研究[27]纳入10例患者,全部接受DCB治疗,技术成功率100%,治疗后狭窄程度中位数为50%(IQR 45%~53%),无围手术期再闭塞死亡病例发生,中位随访3个月,无再缺血事件发生。国内Han等[28]报道30例患者,技术成功率100%,术后中位残余狭窄20%(10%~40%),中位9.8个月随访有1例患者出现无症状再狭窄,无症状性再缺血事件发生。Remonda等[29]研究结果显示6%患者出现围手术期并发症。平均随访9个月,总体再狭窄率为15%。Wang AYC等[30]使用DCB治疗ICAS围术期主要并发症2例(5.7%,2/35),轻度围术期并发症2例(5.7%,2/35)。病变狭窄率治疗前为76.6%±7%,DCB成形术后为32.4%±11.2%,随访时为25%±16%。随访相比术后即刻病变狭窄率有着明显降低,44%(16/36)的治疗血管管腔增益大于10%。在过往文献中,ICAS介入治疗后的管腔增大很少有报道,而在这项研究中是很常见的。从这方面看,在DCB血管成形术后放置支架似乎不一定是治疗的必须[30]。
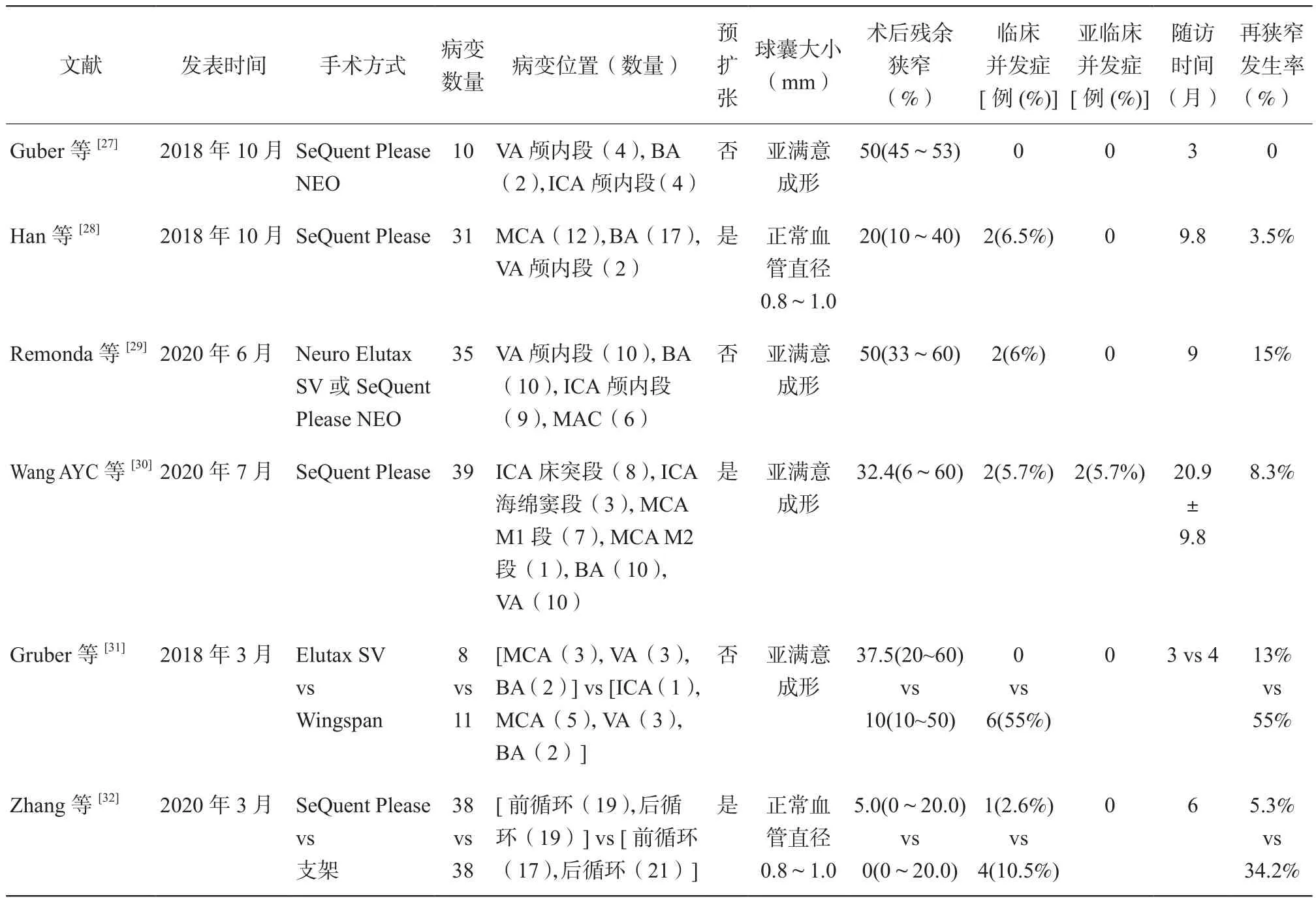
表2 药物涂层球囊应用于ICAS介入治疗的临床研究资料
进一步的研究显示可能DCB和传统支架成形相比在血管再狭窄发生率上具有优势。Gruber等[31]对比DCB和Wingspan支架对症状性颅内血管狭窄的疗效,纳入19例病人(nDCB=8,nwingspan=11),发现DCB组术后中位狭窄从81%降至37.5%,DCB相比支架有更低的复发缺血事件风险(13% vs 64%)和血管再狭窄发生率(13% vs 55%)。但DCB的技术成功率较支架组低(87% vs 100%),一定程度上体现出目前DCB产品柔顺性不足。Zhang等[32]应用1∶1倾向性匹配在前瞻性数据库中回顾性分析76名ICAS患者(DCB组38人,非DCB组38人)的治疗情况,随访结果显示在中位狭窄程度和总体再狭窄发生率上DCB更具优势。
不管是否具有ICAS治疗适应证,DCB可有效降低术后再狭窄,手术成功率高,且并发症较低。同时还具有手术操作简单,体内无异物置入,术后抗血小板时间减少,缩短手术时间,降低血栓形成风险及出血风险等优点。但由于DCB顺应性不足,缺少专门针对颅内设计的产品,适应颅内血管的球囊型号较少,多选择非迂曲、分支较少的病变部位,手术技术成功率有待进一步观察,但有理由相信DCB是一个极具期待的方向。
(四)存在的问题
目前对于DCB应用于颅内动脉狭窄治疗流程亟需规范化指导。由于DCB进入体内后受到血流冲刷影响损失,在冠脉病变要求2 min内送达病变,颅内目前还未有共识,有待进一步研究。对于DCB的扩张时间各中心也存在差异。笔者认为颅内动脉扩张时间不易过长,30~60 s即可。颅外动脉可能需要更长时间的扩张,60~80 s为宜。对于是否使用预扩张,预扩张球囊大小和DCB球囊大小的选择也存在一定分歧。目前专用于颅内的两款DCB球囊均不需要预扩张。Gruber等[27]报道的10例患者使用DCB(商品名:SeQuent Please)前未进行任何预扩张,并使用亚满意血管成形术,未出现围手术期并发症,随访有1例无症状再狭窄;而Han等[28]对30例患者全部行预扩张,在DCB(商品名:SeQuent Please NEO)选择上为正常血管直径的80%~100%,且至少比常规球囊大0.5~1 mm,围手术期并发症率2人(6.5%),随访出现1例无症状再狭窄。术后平均残余狭窄方面,后者Han等研究结果为20%(10%~40%)小于前者Gruber的50%(45%~53%)。Wang Y等[33]比较了使用小球囊(球囊与血管直径比<0.8)和大球囊(球囊与血管直径比0.8~1.0)对椎动脉开口处狭窄的血管内治疗预扩张,随后使用DCB,结果小球囊预扩组(SSBP)再狭窄的发生率明显高于大球囊预扩组(LSBP),分别为56.3%和10%。提示对于椎动脉开口处狭窄病变,保守的预扩张可能导致更差的结果。
笔者经验:(1)预扩张可以使DCB更加容易通过病变,扩张时药物均匀充分地释放到血管壁;(2)对于严重钙化或血管弹性回缩明显的病变,预扩张可以指导手术下一步方案;(3)进行预扩张及较大球囊直径可能获得更小的术后残余狭窄,但同时可能增加了手术风险。多数认为颅内血管一般不选择预扩张,颅外段椎动脉可遵循冠脉共识充分预扩张。有必要进行更大规模的临床试验以评估各种手术方式。
五、总结
后SAMMPRIS时代治疗颅内动脉粥样硬化,球囊成形治疗正在扮演更加重要的角色。回首过去40年,随着技术的提升和器械的更新迭代,从单纯球囊扩张开始,到自膨支架、球扩支架,再到今天的药物涂层球囊,从球囊成形—支架成形—球囊成形的过程,不是支架碰壁的无奈出路,而是研究思考后的不断改变。制备材料的改进,操作技术的提升,多种类球囊的涌现,球囊血管成形治疗颅内动脉粥样硬化狭窄扮演着更加重要的角色。

