离子色谱法测定复方氨基酸注射液(18AA)中阴离子含量
周敏,郭艳芳,王烜,程奇珍
江西省药品检验检测研究院,国家药品监督管理局中成药质量评价重点实验室,江西省药品与医疗器械质量工程技术研究中心,南昌 330029
复方氨基酸注射液(18AA)是含有多种氨基酸的肠外营养制剂,属于营养用氨基酸注射液,用于各种应激状态和危重患者的营养支持,临床使用较广[1]。复方氨基酸注射液引起的不良反应,涉及多个系统、器官,其临床表现复杂多样[2],其中以静脉炎最普遍,其次为过敏性休克。除使用方面的原因,静脉炎主要与药物中含山梨醇、电解质等多种成分相关,过敏性休克主要与药品在生产过程中混有其它杂质或其代谢产物及亚硫酸氢钠过敏[3,4]相关。
氯离子、亚硝酸根离子、磷酸根离子是水中常见的阴离子[5],部分氨基酸结合醋酸根离子成盐,同时制剂过程中调节pH 值时也可能引入部分醋酸根[6],乙二胺四醋酸二钠常用于注射液金属离子络合,亚硫酸氢钠、硫代硫酸钠用于注射液中作为抗氧剂,以上多种阴离子均有可能在制剂中存在,可能与用药引起的不良反应相关,为监控注射液用药安全,有必要进行检测监控。
离子色谱法需要样品量少,具有专属性、灵敏度、准确度、自动化程度高的优点,适合于分析阴离子、阳离子、有机酸、碱,特别适合分析各种离子,由于多数阴离子的紫外响应值较低,而本制剂中总离子强度较强,为减少解离,以氢氧根作为淋洗液。本次实验建立离子色谱法同时测定多种阴离子含量的方法,用于测定不同来源复方氨基酸注射液(18AA)的多种阴离子含量,从而发现潜在的隐患。
1 仪器与试药
1.1 实验仪器
戴安离子色谱(ICS-1000 系统+AS40 进样器+IONPAC AS11 阴离子交换柱+KOH 自动抑制外加水模式);Synergguv Millipore 超纯水制水机。
1.2 对照品
醋酸钠(国药集团化学试剂有限公司,批号:20150417,含量99%);乙二胺四醋酸二钠(国药集团化学试剂有限公司,批号:20170527,含量:99.0%);亚硝酸钠(国药集团化学试剂有限公司,批号:142024,含量99%);氯化钠(西陇化工股份有限公司,批号:170417,含量:99.5%);磷酸钠(西陇化工股份有限公司,批号:160106,含量:98%);硫代硫酸钠(SIGMA,批号:MKBT8948V,含量:99.5%);硫酸钠(西陇化工股份有限公司,批号:160105);亚硫酸氢钠(SIGMA,批号:MKBB5028,含量:100%)
2 实验方法
2.1 色谱条件
色谱条件色谱柱:Ion Pac AS11 Analytical(4 mm ×250 mm),保护柱:Ion Pac AS11(50 mm × 4 mm),淋洗液:20 mmol/L KOH 溶液,流速:1.0 mL/min;柱温:35 ℃,检测器:电导检测器,进样体积:25 μL。
2.2 溶液的制备
2.2.1 标准品贮备液的制备分别精密称取醋酸钠、乙二胺四醋酸二钠、亚硝酸钠、氯化钠、磷酸钠、硫代硫酸钠、硫酸钠与亚硫酸氢钠对照品适量,加超纯水制成对照品贮备液(浓度与折算见表1,乙二胺四醋酸二钠以EDTA 计)。
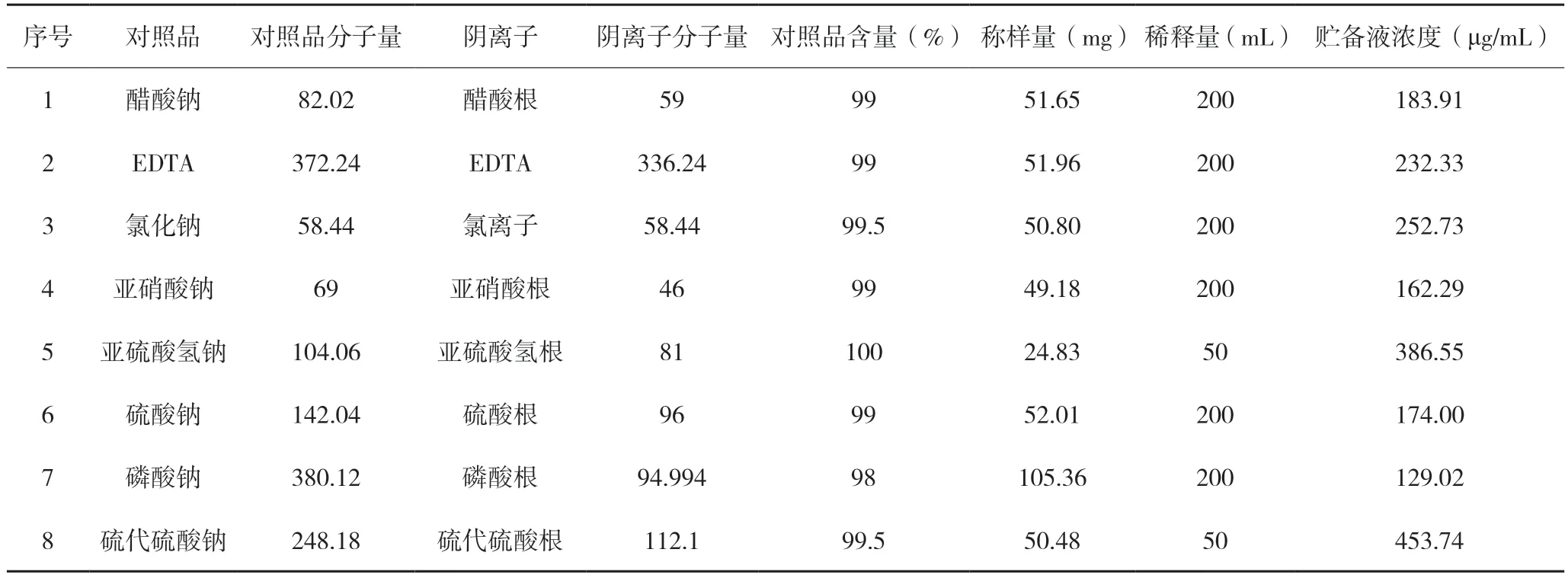
表1 标准品贮备液的浓度折算表
2.2.2 供试品溶液的制备取本品一支,用超纯水溶解并转移至25 mL 容量瓶中,定容至刻度,摇匀,即得。
2.2.3 标准曲线溶液的制备及线性考察分别精密量取适量各标准品贮备液,置同一容量瓶中,用超纯水稀释至刻度,配制成相应浓度的标准曲线溶液,见表2。混合对照品溶液离子色谱图,见图1,各成分分离度良好。线性考察结果良好,见表3。
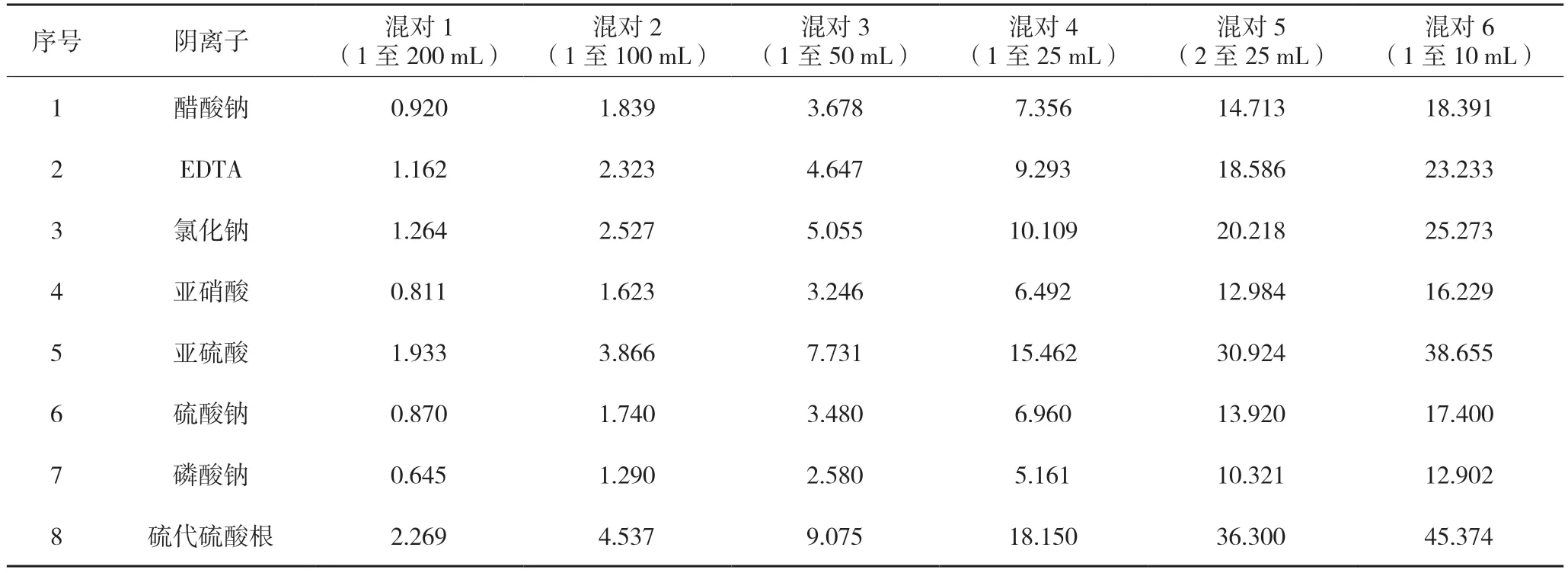
表2 混合标准曲线溶液浓度

表3 线性关系与检测限
2.3 专属性试验
分别取溶剂(超纯水)、氨基酸原料溶液(取氨基酸原料,按处方量配制混合氨基酸溶液)与复方氨基酸注射液(18AA),同法测定。结果:溶剂对样品阴离子测定均无干扰,氨基酸对照品溶液仅检测出氯离子,样品溶液色谱图中各检出阴离子峰分离度良好。方法专属性良好,见图2。
2.4 稳定性试验
取混合对照品溶液5 间隔24 h 进样,比较结果。亚硫酸氢根离子峰有较明显减小,硫酸根离子峰明显增大,其余阴离子稳定,见图3。
因亚硫酸氢根在水中不稳定,对亚硫酸氢根标准品贮备液进行稳定性试验。从结果可知亚硫酸氢根离子在水中会部分转化为硫酸根离子,且随放置时间增长而增加,见图4。
样品由于长期存放,添加的亚硫酸氢根离子同样会部分转化成硫酸根离子,从用药的安全性考虑应测定硫酸盐与亚硫酸氢盐的总和[7],试验结果见表4。
2.5 精密度试验
取六份混合对照品溶液5 分别进样,比较结果(硫酸盐与亚硫酸盐按总量计),精密度良好,见表5。
2.6 回收率试验
分别称取氨基酸原料药(混合)12 份约50 mg,置100 mL 量瓶中,加适量高纯水溶解,分别精密加入各阴离子贮备溶液0.5、1.0、2.0 mL,加高纯水稀释至刻度,摇匀,同法测定。回收率结果良好,结果见表6。

表4 亚硫酸氢根标准贮备液稳定性试验结果
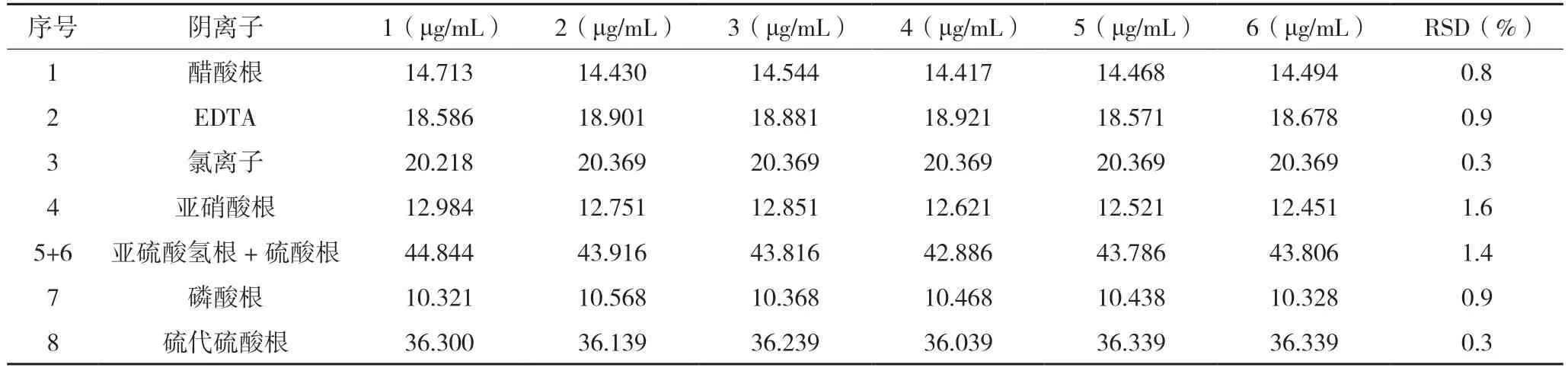
表5 精密度试验结果(n=6)

表6 加标回收率测定结果 %
2.7 检测限试验
分别精密量取1 mL 混合对照溶液2 置5、25、50 mL 量瓶中,加高纯水稀释至刻度,摇匀,同法测定。分别得各阴离子检出限浓度,见表3。
3 结果分析
本次共选取5 家企业样品(制剂A~E),各抽取三批进行测定,测定结果(三批均值,见表7)。测定结果与理论值均存在一定差异。其中:(1)原料检测结果氯离子与理论值一致,其余离子均未检出。(2)制剂中氯离子检测结果均高于处方量。根据处方,氯离子主要来源于原料中盐酸精氨酸、盐酸赖氨酸与盐酸组氨酸。其中一家企业含量明显高于处方量,推测来源:①工艺中调节pH 时使用带入;②使用注射用水中带入。天然水体中含有大量常规离子如氟离子、氯离子、硝酸盐、硫酸盐等以及其他可能的污染物。大量研究表明,对水体进行深度处理的常规消毒工艺如臭氧和二氧化氯等消毒技术的应用也越来越广泛,其中氯化消毒是我国的主要饮用水消毒方法[9]。然而,消毒剂和饮用水中的天然有机物和无机物反应可生成溴酸盐、氯酸盐和卤代乙酸等消毒产物;③本品包装使用丁基胶塞,丁基胶塞中含有氯[10],在产品贮存过程可能产生微量迁移。(3)亚硫酸氢根离子检测,5 家制剂含量在59%~96%之间,均符合现行药典标准[10]规定(不得过标示量的110.0%),但计算亚硫酸氢根离子与硫酸根离子总量却有4 家均超过了110%,说明在添加亚硫酸氢钠时可能存在实际添加量高于处方量的情况。现有药典标准使用紫外-可见分光光度法检测亚硫酸氢根含量,虽能有效监控溶液中亚硫酸氢根的含量,但从离子色谱法检测结果来看,仍存在一定的隐患。(4)磷酸根离子5 家均有微量检出,但原料溶液中未有检出,推测为药品包装中产生的微量迁移。

表7 样品测定结果(n=3) mg/mL
4 结论
本次实验研究探讨了离子色谱法对复方氨基酸注射液(18AA)多种阴离子同时进行分离测定。方法需要样品量少、自动化程度高,精密度、准确度及回收率均较满意,为该品种提供了一种较为新颖的质量控制手段,具有较好的参考和实用价值。

