响应面法优化古尼拟青霉中活性成分提取工艺
章能胜,陈晓玲,胡丰林
(1.安徽卫生健康职业学院 医学系,安徽 池州 247099;2.安徽农业大学 安徽省微生物防治重点实验室,安徽 合肥 230036)
虫生真菌古尼拟青霉(PaecilomycesgunnniLiang)为古尼虫草[Cordyceps gunnii (Berk.)Berk.]的无性型[1],其药用价值与古尼虫草相当[2]。近年来,古尼拟青霉活性研究主要集中在抗氧化[3]、镇静[4-5]、镇痛[6]和抗肿瘤[7]等。笔者前期研究发现古尼拟青霉有较强的清除自由基活性。本研究在前期研究基础上,利用响应面分析法(Response Surface Methodology,RSM )对古尼拟青霉中清除自由基活性组分超声波提取工艺进行优化,旨在为深度开发利用提供参考。
1 材料和方法
1.1 材料
1.1.1 供试菌株
供试菌株古尼拟青霉(PaecilomycesgunnniLiang),由安徽农业大学微生物防治省重点实验室提供,菌株号为RCEF4117。
1.1.2 培养基
固体培养基(g/L):葡萄糖 40,蛋白胨10,酵母浸粉10,琼脂20,配置好后用蒸馏水定容。
1.1.3 主要仪器与试剂
Spectra Max M2型酶标仪,美国Molecular device公司;KH5200型超声波清洗器,昆山禾创超声仪器公司;LRT-250G型光照培养箱,广东省医疗器械厂;化学纯葡萄糖,中国医药集团上海化学试剂公司;蛋白胨,天津大茂化学试剂厂;酵母浸出粉,英国OXOID公司;分析级甲醇,上海建信化工有限公司;分析纯三氯甲烷,无锡市亚盛化工有限公司;分析纯乙酸乙酯,安徽淮南化学试剂厂,分析纯石油醚,上海化学试剂有限公司。
1.2 实验方法
1.2.1 样品前处理
将灭菌培养基倒好培养皿后,将剪好的灭菌玻璃纸铺于培养基上,接种1 mL种子液于玻璃纸表面,放置于25℃培养箱中培养8天,刮取菌丝冷冻干燥备用。
1.2.2 清除自由基活性测定
本研究采用自由基为二苯基苦基苯肼自由基(DPPH),具体测定方法参考胡丰林的酶标仪实验法(DPPH-Microplate)[8]。
1.2.3 最佳浸提溶剂的选择
准确称取6份样品,按照料液比为1: 20分别加入水、甲醇、正丁醇、乙酸乙酯、氯仿、石油醚等六种溶剂,室温下利用超声波浸提30 min,离心取上清液,经真空浓缩冻干后进行活性测定。
1.2.4 单因素实验
以自由基清除率为考察指标,甲醇作为浸提溶剂,按照上述提取过程,分别对提取温度、提取时间和料液比进行单因素实验。提取温度(℃)设5个水平:20、40、60 、80 、100;提取时间(min)设置4个水平:10、30 、60 、120;料液比(mg/μL)设置4个水平:1:10、1:20、1:30、1:40。
1.2.5 响应面实验
在单因素实验基础上,利用design expert软件的Box-Behnken设计三因素三水平的响应面实验(见表1),对超声波提取工艺进一步优化,其中响应值为自由基清除率,自变量为影响较大的3个因子即提取温度、提取时间和料液比。

表1 响应面分析因子和水平表
1.2.6 数据处理
所有实验均重复3 次,实验结果用平均值±标准差表示,用SPSS 24.0和Design-Expert 8.06 对实验数据进行处理和分析。
2 结果与分析
2.1 单因素实验
2.1.1 最佳浸提剂的选择
本研究选取水、甲醇、正丁醇、乙酸乙酯、氯仿和石油醚等六种极性不同的溶剂提取古尼拟青霉菌丝中具有清除自由基的活性的物质。从图1可看到,供试样品的甲醇提取物活性最强,其次是正丁醇、水,石油醚提取物的活性最弱,表明供试样品的活性组分为中等偏上极性的化合物,甲醇为最佳提取溶剂。

图1 提取溶剂对自由基清除率的影响
2.1.2 提取温度对自由基清除率的影响
由图2可知,随着提取温度的升高,供试样品的清除自由基活性呈现先上升后下降的趋势。当温度达到40℃时,自由基清除率最高,随着温度继续升高,自由基清除率反而下降。出现这种现象可能是因为温度较低时,温度升高有利于样品中清除自由基活性组分的提取,温度过高时,高温会破坏活性组分的结构,导致活性下降。
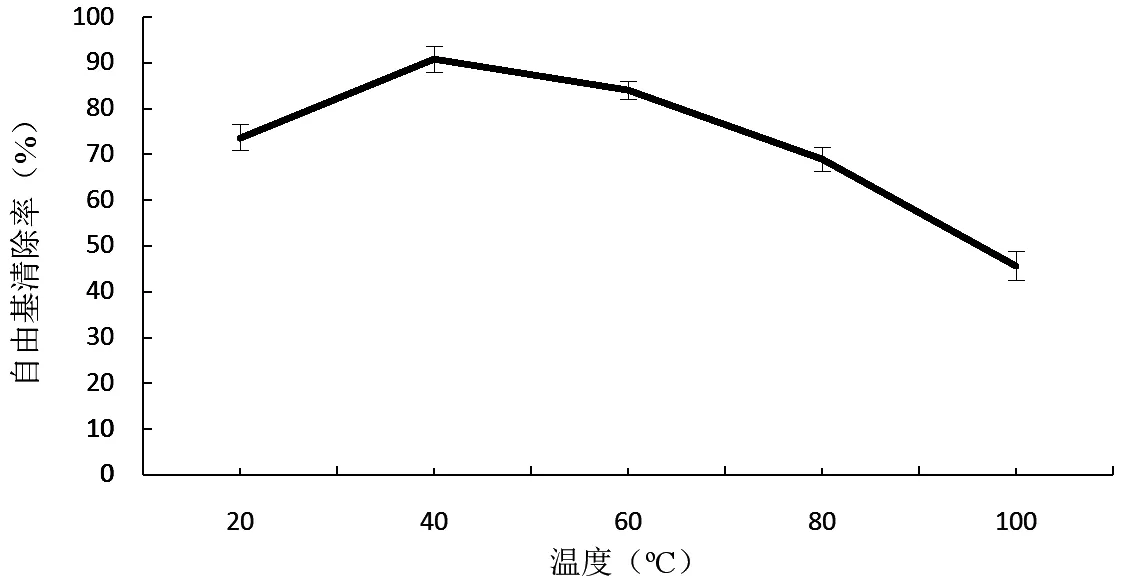
图2 提取温度对自由基清除率的影响
2.1.3 提取时间对自由基清除率的影响
由图3可知,提取时间为30 min时,供试样品中的清除自由基活性组分浸出率最高。随着提取时间的延长,活性组分浸出率没有上升,反而呈现少许下降。出现这种现象可能是由于提取时间过长,会导致过多的其他组分被浸提出,影响了供试样品的清除自由基的活性。

图3 提取时间对自由基清除率的影响
2.1.4 料液比对自由基清除率的影响
由图4可知,随着料液比增加,供试样品中的清除自由基活性组分浸出率呈现上升趋势,当料液比1:30 mg/μL时达到最大值,继续增大料液比活性组分的浸出率没有持续上升。这可能是因为料液比较小时供试样品中活性组分不能完全溶解于提取液中,若增加溶剂的比例,活性组分得率会增加;当料液比过大时供试样品中活性组分已完全被浸提出,此时再增加溶剂的比例已无意义。

图4 料液比对自由基清除率的影响
2.2 响应面分析法优化提取工艺
2.2.1 回归模型的建立与显著性分析
在单因素实验基础上,设计响应面实验优化古尼拟青霉中清除自由基活性成分提取工艺,结果见表2。运用软件中Box-Behnken进行拟合,得到响应面的回归模型的方程为:Y= 96.52 - 0.18 A + 0.029 B - 0.085 C- 0.36 A B+ 0.30 A C + 0.048 BC- 0.40 A2- 1.58 B2- 1.87 C2。

表2 响应面实验设计方案及实验结果
由表3可知,二次项B2(提取时间)、C2(料液比)对古尼拟青霉清除自由基活性有极显著的影响(P<0.01),二次项A2(提取温度)、交互项AB、AC的影响显著(P<0.05),其余项均不显著。模型P<0.0001,可见本实验选用的模型是极显著。模型的失拟相(Lack of Fit)P>0.05,表明正常误差在回归方程与实际拟合所占比例较小,表明方程拟合性强,模型是可行的。相关系数R=0.9854,表明模型推算值与实际值接近,模型的拟合度高,实验误差小,可见该模型在统计学上有现实指导意义。
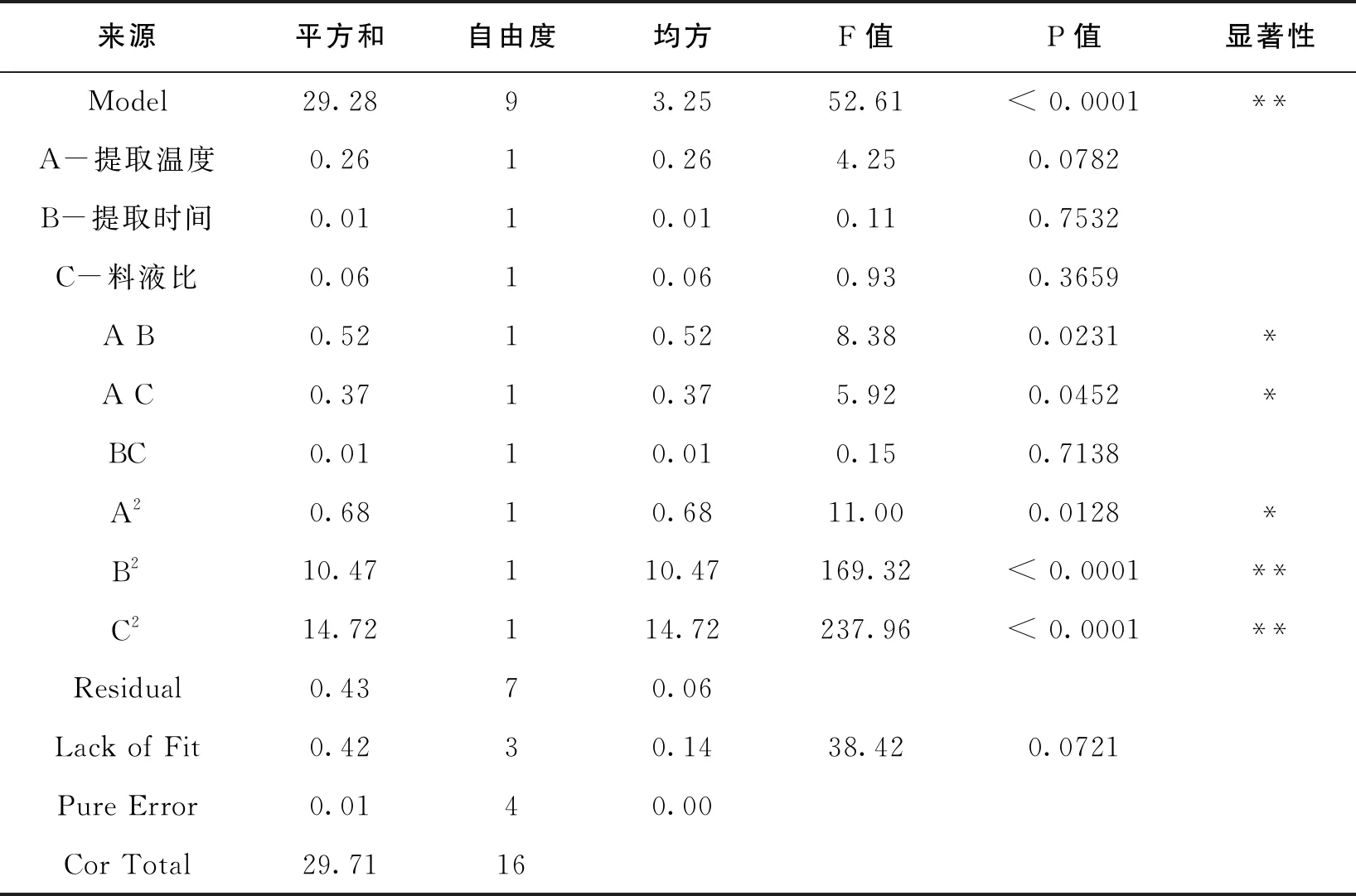
表3 回归模型显著性结果
2.2.2 响应面图分析
由响应面分析图(图5)形状(开口向下且等高线最小椭圆的中心在-1~1范围内)可知,响应面存在最大值。又因为温度和时间、温度和料液比的等高线为椭圆形状,表明提取温度、提取时间和提取温度、料液比的交互效应均显著,而时间和料液比的等高线为近圆形,表明提取时间和料液比交互效应不显著,与回归模型显著性结果相吻合。对回归方程分析得最佳提取工艺为:提取温度37℃,提取时间34 min,料液比1:30,理论最佳自由基清除率为96.61%。

图5 响应面分析图
2.2.3 验证试验
为了验证响应面法的可行性,采用上述最佳提取工艺进行了3次平行实验,得到实际自由基清除率平均为96.58%,与理论值接近,进一步表明模型的科学性。因此,响应面法优化古尼拟青霉中清除自由基活性成分提取工艺是可行的。
3 讨论与结论
目前,响应面法由于提供了响应面区域内的必要信息,较大程度上扩展了有限的资源利用效率,能够优化加工条件,降低生产成本,广泛运用于生物、化工、农业生产等领域。[9]本研究是在单因素实验的基础上,将响应面法应用于优化古尼拟青霉中清除自由基活性成分的提取。结果表明最佳提取工艺条件为:提取溶剂为甲醇,提取温度为37℃,提取时间为34 min,料液比为1:30。在最佳工艺条件下,实际自由基清除率为96.58%,与预测值非常接近,表明模型的拟合度较好,优化后提取工艺可靠、准确。

