高稳定性硅/硬碳复合负极在锂电负极中的应用
余晨露,田晓华,郑 瀚,张哲娟,孙 卓,朴贤卿
(纳光电集成与先进装备教育部工程研究中心,华东师范大学物理与电子科学学院,上海200062)
锂离子电池是当今重要的能量存储器件,具有能量密度高、功率密度高、使用寿命长、自放电率低、无记忆效应、安全低污染等优点,近年来在智能手机、便携电器、医疗电子、航空航天、电动工具、混合型动力汽车领域获得了广泛应用。随着各个领域对电池能量密度的需求飞速提高,高能量密度的锂离子电池是研究和开发的重点方向[1]。目前的负极体系中,硅的理论嵌锂容量(3500~4200 mA·h/g)约为石墨理论容量(约370 mA·h/g)的10倍,并且具有储量丰富、无毒无污染、嵌锂平台(约0.4 V)低的优势,是当前广泛研究的锂离子电池负极材料之一。但是,制约硅在锂电池负极中的应用问题也很突出:硅的电导率低,脱嵌锂时存在巨大的体积涨缩,导致硅负极的容量优势难以保持[2]。硅的体积膨胀、粉化衰减、电导率低等问题,可以通过减小硅颗粒尺寸[3]、增加硅颗粒孔隙、构建3D导电网络和结构性缓冲基体等策略进行优化[4]。其中纳米硅碳复合被证明是能有效缓解单质硅负极的体积变化、材料结构的破坏、电解液不可逆消耗、负极的功能失效等问题的策略[5]。纳米硅粉在实际应用中成本高,存在易氧化、易团聚、孔隙化处理难度大等缺点,同时粒径较小的纳米硅(<100 nm)比表面积大(>50 m2/g),在制备负极浆料时存在工艺繁复、产量低、均匀混合困难等技术挑战[6-7]。
因此,本文以太阳能光伏产业的硅废料处理得到的纳米硅颗粒(约200 nm)为原料,以市售低价碳氢化合物为碳复合前体,通过低能耗的简单工艺制备硅碳复合材料,通过对碳种类、复合含量的研究,解决锂电硅负极的应用瓶颈问题,提高硅碳复合负极材料的比容量和循环稳定性。
1 实 验
1.1 硅/硬碳复合材料的制备和测试
1.1.1 硅/硬碳复合材料的制备
以太阳能光伏电池生产中切割硅棒产生的硅废料为原材料(主要成分包括硅颗粒52%、水46%、表面活性剂2%),经酒精和去离子水清洗、过滤和100 ℃干燥后,超声分散于去离子水中,得到硅的悬浊液。同时以蔗糖(su)、可溶性淀粉(ss)、壳聚糖(c)、小麦淀粉(w)为前体碳源,以硅碳(Si∶C)质量比为9∶1 在水相中配置质量分数为2%的含碳前体溶液(其中在壳聚糖中加入质量分数2%的乙酸助溶)。将硅的悬浊液缓慢加入碳的前体溶液中,搅拌1 h后,80 ℃蒸发液体得到粉末,研磨备用。将粉末置于石英舟,放入真空管式炉(型号TCW-32B)中,在N2气氛下常压700 ℃和800 ℃各保温1 h进行碳化,升温速率为5 ℃/min。待样品自然冷却至室温,取出研磨,以su、ss、c、w为前体的硅/硬碳复合物分别命名为su@Si、ss@Si、c@Si、w@Si。
为研究碳含量对复合电极性能的影响,实验中对c@Si复合物进行二次碳复合,控制c@Si∶C比例为9∶1,工艺流程与上述一致,二次碳复合后样品标记为c2@Si,其中Si∶C比例近似为8∶2。
1.1.2 硅/硬碳/石墨(SCG0.2)复合材料的制备
以c为前体碳源,将石墨(G)作为添加材料,制备了Si/C/G 复合负极,其中控制Si∶C∶G 比例为1∶0.2∶1,石墨是直接加入至硅与壳聚糖混合液中,其余制备工艺与c@Si一致,硅/硬碳/石墨的样品标记为SCG0.2。
1.1.3 复合材料的表征
采用带铜靶Kα射线(Panalytica,PRO PW3040/60,电压为30 kV,电流为25 mA,波长为0.15418 nm)的X 射线衍射仪(XRD)分析样品的晶相。采用装有Bruker QUANTAX-400 能谱系统(EDS)的扫描电子显微镜(SEM,JEOLJSM-7610F)分析样品的形貌和元素分布。采用美国麦克(Micromeritics)公司的ASAP2020比表面积及孔隙分析仪在-196 ℃的低温下进行N2等温吸附脱附测试,通过Brunauer-Emmett-Teller(BET)方法计算得到样品的比表面积,用Barrett-Joyner-Halenda(BJH)模型对脱附曲线数据计算得到样品的孔径分布。采用热重分析仪(PerkinElmer Pyris1 TGA)在空气气氛下对样品进行碳含量分析,温度从室温到800 ℃,升温速率为10°C/min。
2 硅碳复合电极的制备及电化学性能测试
将c@Si、c2@Si、SCG0.2 复合材料分别与导电碳黑(Super-P)和羧甲基纤维素(CMC)按8∶1∶1的比例,以适量的去离子水溶剂,磁力搅拌24 h制备负极浆料;随后采用涂敷机将浆料刮涂在铜箔上,100 ℃干燥一夜得到负极片,切成φ12 mm的圆片。电极片上活性物质的质量控制在1~3 mg/cm2。
2.1 扣式半电池的组装
在氩气环境(水氧含量<0.5 ppm,1 ppm=10-6)的手套箱中(型号:米开朗罗娜),使用CR2032型的电池壳,以锂片(φ15.6 mm)作对电极和参比电极,以多孔聚乙烯聚丙烯多层膜(Celgard 2320)为隔膜,按负极片、隔膜、电解液、锂片、垫片、外壳的顺序组装扣式半电池,其中电解液配方为1 mol/L 的LiPF6溶于体积比1∶1∶1的碳酸乙烯酯(EC)、碳酸甲乙酯(EMC)、碳酸二甲酯(DMC)的三元混合物。电池组装、封口后室温下静置24 h,进行后续测试。
2.2 电极的电化学性能表征
采用CT2001A 蓝电测试系统(武汉市蓝电电子有限公司,电压量程5 V,电流量程100 mA),测试电压范围为0.005~3.0 V,对扣式半电池进行恒流充放电测试。使用AUTOLAB PGSTAT302N电化学工作站对电池进行循环伏安测试,测试范围为0~3 V,扫描速率为0.1 mV/s。采用同一台电化学工作站测试电池的电化学阻抗谱(electrochemical impedance spectroscopy,EIS),测试频率范围为0.1 Hz~100 kHz,偏压和交流振幅分别为开路电压和5 mV。
3 结果和讨论
图1为不同负极材料的SEM图像。硅颗粒[图1(a)]的尺寸为50~300 nm,形状不规则,具有棱角分明的切削界面。与纯硅相比,su@Si、ss@Si和c@Si 的形貌变化不明显,颗粒尺寸略微变大,w@Si 的形貌与硅有明显差别,颗粒具有圆润的表面,棱角呈现圆弧角,尺寸明显增大。
图2 为Si 和su@Si、c@Si、w@Si 三种复合碳硅材料的EDX mapping 图,由于ss@Si 的分布与su@Si类似,因此未另外展示。从O元素的分布可知,Si 颗粒的表面会发生氧化。与纯Si 对比可知,su@Si、ss@Si 中C 元素的分布与纯硅一致,为杂乱分布的散点,说明这两种材料中的碳含量过低,达不到检测要求。在c@Si、w@Si中,可以明确看到有C 元素的存在,并且在c@Si 中更明显。表明c@Si、w@Si 复合材料方案下碳的复合目标基本达到。

图1 硅粉(a)、su@Si(b)、ss@Si(c)、c@Si(d)和w@Si(e)的SEM图Fig.1 SEM images of(a)Si,(b)su@Si,(c)ss@Si,(d)c@Si and(e)w@Si

图2 Si(a)、su@Si(b)、c@Si(c)、w@Si(d)样品的EDX mapping图(Si、C、O元素的分布)Fig.2 EDX mappings(including element mappings of Si,C,O)of(a)Si,(b)su@Si,(c)c@Si and(e)w@Si
以上结果表明,壳聚糖和小麦淀粉作为碳源,c@Si、w@Si复合物碳含量更高。壳聚糖是甲壳素的脱乙酰化产物,分子式为(C6H11NO4)n,其化学结构C-2位上是一个氨基,在壳聚糖形成溶液后,氨基会游离成阳离子,聚电荷效应使得溶液的黏度相当高,有利于硅和前体碳颗粒的紧密黏附。另外,小麦淀粉中,淀粉分子是链状甚至分支状,在80 ℃下会发生糊化,形成黏性很高的糊状溶液,使得淀粉分子与硅的连接也相当紧密。相比之下,蔗糖在质量分数2%时黏度不及小麦淀粉糊化产物和壳聚糖溶液,而对于化学式与小麦淀粉相同的可溶性淀粉,它是由淀粉经过轻度酸或碱处理生成的,溶液的黏度也更低,因此c@Si、w@Si中的碳含量更高。
为了验证c@Si和w@Si的结构,图3(a)给出了Si、c@Si、w@Si 的XRD 图。Si 在2θ=28.4°、47.3°、56.1°、69.14°、76.39°处有5 个峰,分别对应 硅 的(111)、(220)、(311)、(400)、(311)面,在20°~27°、50°处分别有一宽峰,对应于SiO2或SiOx,表明亚微米硅颗粒经干燥处理后,表面存在一定程度的氧化。c@Si、w@Si样品中硅衍射峰尖锐且明显,表明硅碳复合后,硅的晶体结构未发生改变。另外,c@Si、w@Si的XRD谱图在20°~26°处均出现宽峰,峰中心位置约为23°,认为是SiOx的峰(21.4°)和无定形碳(26°)的衍射峰的重叠。与w@Si相比,c@Si中无定形碳的峰强度相对硅的峰强度更明显,认为该复合材料中碳的含量更高,因此,之后的研究工作以c@Si 为主。二次复合后,c2@Si 在23°的峰包更明显,表明无定形碳含量更高。
为了确定一次复合、二次复合对样品碳含量的影响,对c@Si、c2@Si 进行热重分析(TGA),以壳聚糖(chitosan)作为对比样。TGA测试曲线如图3(b)所示,c@Si 中的碳质量分数达到6.1%,低于预期的10%。二次包裹实验方案下得到的c2@Si 样品,碳质量分数可提升至约12.3%,表明二次复合可以提高碳的复合量。

图3 (a)Si、c@Si、w@Si、c2@Si的XRD图;(b)chitosan,c@Si,c2@Si的热失重曲线Fig.3 (a)XRD patterns of Si、c@Si、w@Si、c2@Si;(b)TGA of chitosan(c),c@Si,c2@Si
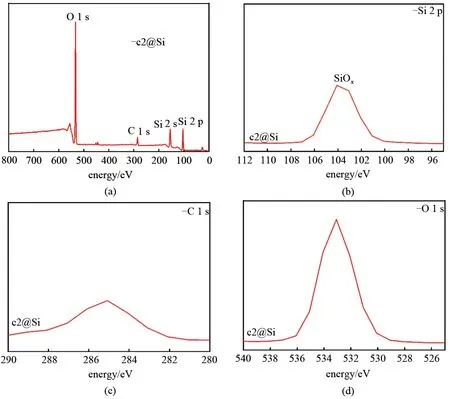
图4 c@Si(a)、Si2p(b)、C1s(c)、O1s(d)的XPSFig.4 XPS spectra of(a)c@Si;(b)Si2p;(c)C1s;(d)O1s
为进一步确定XRD 中23°的衍射峰是否有SiOx和无定形碳的贡献,实验对c2@Si进行了XPS分析(XPS 的穿透深度约为5~10 nm),如图4 所示。从图4(a)的放大图看,图4(b)在104 eV 处的峰来自SiOx[8],图4(c)的284.8 eV 处的C1s 峰证实硅碳复合材料中碳的存在;图4(d)中533 eV的较强O1s峰也表明SiOx的存在,且从C和O的相对峰强可知,在c2@Si 表面10 nm 以内,无定形碳和SiOx均存在,且后者的含量较多,这将影响到复合材料的导电性。
为了了解c@Si、c2@Si的表明孔隙结构,实验测试了两者N2吸附-脱附等温曲线图和孔径分布曲线图(图5),并以Si 为对比样。c@Si、c2@Si 的都表现为Ⅲ型的N2吸附-脱附等温线,孔隙的直径分布不集中。采用Brunauer-Emmett-Teller(BET)方法可计算出材料的比表面积、孔容和平均孔径,结果见表1。结果显示:①Si、c@Si、c2@Si 的比表面积分别为43.37、49.57 和43.23 m2/g,一次复合时,Si颗粒表面沉积了小的碳颗粒或不连续碳断层,并且碳本身的比表面积大,因此c@Si 的比表面积略增大,二次复合下,复合碳尺寸会增大,并且表面碳的连续性增强,导致复合颗粒尺寸整体会变大,因此c2@Si 的比表面积又会下降;②Si、c@Si、c2@Si的孔容呈现降低趋势,表明无定形碳可以对Si 的表面孔隙进行填充。上述数据表明,在制备c@Si、c2@Si复合材料中,复合碳将使硅碳复合材料的孔容和平均孔隙减小,并且通过二次复合增加碳的量,这一效果更甚[9]。
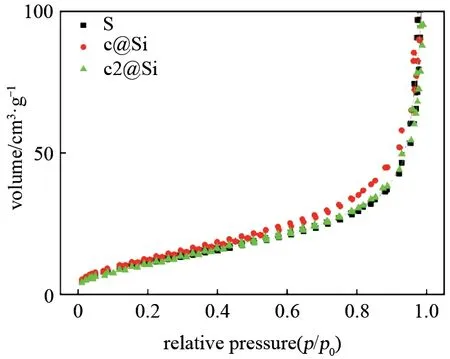
图5 硅(Si)、壳聚糖一次复合硅复合物c@Si、壳聚糖二次复合硅c2@Si的氮气吸附图Fig.5 Nitrogen adsorption isotherms of Si,c@Si and c2@Si

表1 Si、c@Si、c2@Si的比表面、孔体积和平均孔径Table 1 Specific area,pore volume and mean pore diameter of Si,c@Si and c2@Si
3.1 硅/硬碳负极(Si、c@Si和c2@Si)电池性能测试
Si、c@Si和c2@Si在200 mA/g的电流密度下的循环性能如图6(a)所示。Si 负极的首次库仑效率为52.3%,初始容量达到1082 mA·h/g,说明亚微米硅颗粒的表面氧化,使得负极比容量性能受到影响;在20次循环之后,Si负极的比容量快速衰减,说明较大尺寸的Si颗粒使得电极充放电稳定性差,无法长期高容量工作。经壳聚糖碳包裹后的c@Si 和c2@Si负极,初始比容量较低;经过约50圈活化后,随着电解液逐渐渗入,电极的内部反应活性得到提高,这要归因于硬碳材料的嵌锂特性——在循环过程中,随着锂离子的扩散深入,硬碳中的锂离子存储活性位点增加,容量在达到稳定前缓慢释放[10-13]。100次循环之后,c@Si、c2@Si复合负极的比容量分别为102 mA·h/g、225 mA·h/g,库仑效率分别为98.9%和98.6%。负极的比容量值与业内石墨、硅碳复合材料等比并不高,这主要是复合材料中存在较多的SiOx[图3(a)、图4(b)]。循环200 圈后,c@Si电极(含铜衬底)的XRD谱如图6(b)所示,晶体Si的3 个标准衍射峰消失,23.1°、39.2°和41°处存在的SiO2及SiOx衍射峰,26°处出现了LiC 衍射峰,表明循环前后负极中:①Si由晶态向非晶态转变;②SiO2和SiOx在充放电循环过程后,硅的氧化行为略增强[14];③热解碳参与了脱嵌锂反应。为了进一步研究c@Si,c2@Si 硅碳复合负极的电化学性能,图7给出了循环100圈后的c@Si和c2@Si复合负极的循环伏安曲线(CV图),以纯Si电极作为对比。
图7(a)为Si负极前3圈的CV图,在首次嵌锂过程中,在约0.7 V和0 V出现还原峰,分别对应于Li和SiOx、Si 形成合金化的过程[15]。在首次脱锂过程中,氧化峰出现在约0.3 V、0.6 V附近,对应LixSi、Liy(SiOx)z的去合金化过程,其强度(峰值电流)在后续循环过程中有所降低,峰位无明显移动,说明材料在嵌/脱锂过程中容量降低,结构稳定性不佳[16]。图7(b)显示,硅负极循环100 圈后脱嵌锂的峰不明显,电化学活性丧失,主要是由于硅颗粒的膨胀、粉化等会导致电极龟裂、脱落等现象[17-18]。

图6 (a)硅粉(Si)、c@Si、c2@Si的循环性能及库仑效率;(b)c@Si负极循环前后的XRDFig.6 (a)cycling performance and Coulombic efficiency of Si,c@Si and c2@Si;(b)XRD pattern of c@Si before and after cycling

图7 (a)Si的前三圈CV曲线;(b)Si、c@Si、c2@Si循环100圈后的循环伏安曲线Fig.7 CV profile of(a)Si from first three cycles;(b)CV profiles of Si,c@Si and c2@Si after 100 cycles
c@Si 电极的CV 曲线,在嵌锂过程中,约0.6 V、0 V 附近的还原峰对应SiOx、LixSi 的合金化过程。在脱锂过程中,约0.4 V、0.6 V 合并的宽氧化峰对应着SiOx、Si的去合金化过程。由于C质量分数仅占6%,电极中硅是主导,因此C 脱嵌锂的氧化和还原峰并不明显,Si/SiOx的嵌锂脱锂的氧化和还原峰电位相差约0.4 V,表明电极内部存在极化。在后续循环过程中,峰位无明显移动且峰强无明显变化,说明c@Si 材料在嵌/脱锂过程中的结构稳定性良好。
与c@Si相比,二次碳包裹后c2@Si的CV曲线有所不同。在阴极负扫中,约0.6 V、0 V的还原峰对应SiOx、LixSi的合金化过程,还原峰电位低了约0.2 V,这主要是因为电极材料中包裹碳含量的增加,导致还原峰向低电位移动。在阳极正扫中,负极在约0.4 V、0.6 V 出现氧化峰,对应着SiOx、Si的去合金化过程。与c@Si 相比,c2@Si 中Si 的氧化还原峰电位差较小,电极极化小,这表明更多的碳加入有利于降低电极的极化[19]。
Si、c@Si和c2@Si复合材料样品的EIS谱图如图8所示。一般而言,高频曲线与横坐标轴的截距表示欧姆阻抗,用RS表示;高频的第1个半圆代表Li+在SEI 膜中的迁移电阻,第2 个半圆表示e-在活性材料内部输运的电阻,这两个半圆易重叠,用RSEI/CSEI表示;中频区的半圆代表活性材料电极与电解质界面的电荷转移阻抗,用RCT/CCT表示;低频区的斜线表示Li+在活性材料电极内部的固体扩散过程,用Zw表示[20]。半圆的直径越小则样品的阻抗越小。从图8 可以看出,Si 和c2@Si 电极的中高频半圆均合并为一个半圆,而c@Si的SEI阻抗和电荷转移阻抗区分明显,由半圆半径可知,Si电极阻抗最大,经过一次或二次碳复合后,电极的阻抗值明显降低。说明壳聚糖热解碳可以提升硅/硬碳复合材料的导电性。c@Si电极阻抗最小,c2@Si次之,说明由于二次包裹增加热处理时间,会导致SiOx的增加,不利于电子传输。
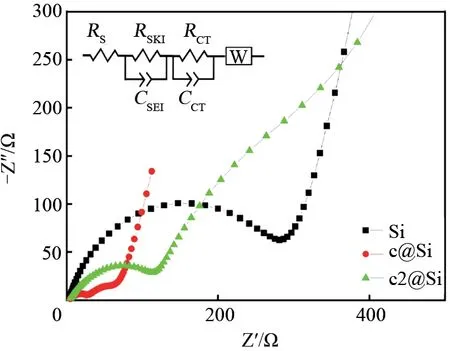
图8 Si,c@Si和c2@Si的EIS谱图(插图为c2@Si等效电路图)Fig.8 EIS of Si,c@Si and c2@Si,(inset:equivalent circuit of c2@Si)
综上所述可知,经过壳聚糖的复合,与Si 相比,c@Si 和c2@Si 负极复合电极的电导率得到提高,但是该硅碳比在该工艺下制备中会导致SiOx的大量产生,导致复合负极的比容量值不高,不利于硅/硬碳锂电负极的性能优化,具有很大改进空间。因此在水相复合步骤中,加入第二碳源石墨(G),以期弥补碳的不完全包裹和SiOx的大量生成,并对硅/硬碳/石墨复合负极的比容量和倍率性能进行测试。
3.2 硅/硬碳/石墨复合负极(SCG0.2)的比容量和倍率性能测试
以壳聚糖和石墨为碳源,与硅颗粒复合制备所得的SCG0.2 电极的循环性能曲线如图9(a)所示。SCG0.2 负极的初始比容量较低,经约50 圈左右的活化后,比容量值趋于稳定,这与上述规律一致,说明在SCG0.2 中,壳聚糖碳化产生的无定形碳使得电解液浸润、渗透缓慢,随着电池循环周期延长,内部的反应活性逐渐得以释放。在100 mA/g的电流密度下,循环100 圈之后,SCG0.2 复合负极的比容量达到617 mA·h/g,库仑效率为99.24%。SCG0.2 负极能维持较稳定的充放电特性,循环300 圈后比容量达到637 mA·h/g,容量保持率高达103.2%,说明在在壳聚糖热解碳和石墨共同作用下,Si 的体积膨胀问题得到克服,且硅碳复合负极制备中SiOx含量也得到了有效控制,因此比容量和稳定性均得到了明显提升。SCG0.2 在50、100、200、400、600、800 和1000mA/g电流密度下的比容量分别为629、609、570、522.9、487.1、452、427.1 mA·h/g[图9(b)]。SCG0.2 复合负极的倍率特性再次证明,壳聚糖作为碳源,加入石墨的碳复合策略下,有效解决了Si 负极的体膨胀、粉化等问题,改善了SiOx含量高的问题,获得了具有良好循环稳定性的高容量负极。

图9 (a)SCG0.2负极的循环比容量和库仑效率;(b)SCG0.2负极在不同电流密度下的下的比容量Fig.9 (a)cycling performance and Coulombic efficiency of SCG0.2;(b)rate capacity of SCG0.2 at different current density
4 结 论
利用光伏产业回收的硅废料,以价格低、无污染的壳聚糖为碳复合前体,通过水相包裹、低温碳化两步简单工艺制备了硅/硬碳复合材料。研究发现:
(1)碳以填充方式与硅颗粒复合,当硅碳质量比为9∶1 时,实际碳质量分数为6%,二次复合可以提高复合物中碳的含量;
(2)该复合策略下,与Si 相比,c@Si 和c2@Si 负极的导电性得到提升,可实现100 圈以上的稳定循环,但是其中SiOx含量高,硅的比容量优势无法发挥;
(3)在此基础上,通过加入石墨,降低硅含量,SCG0.2负极在稳定后,库仑效率达到99.24%,循环300 圈后比容量达到637 mA·h/g,容量保持率高达103.2%,在400 mA/g 的电流密度下比容量达到522.9 mA·h/g,硅负极的衰减问题得到有效改善,硅/硬碳/石墨复合负极在保证稳定性的基础上进一步提高了比容量,在锂电储能中具有较大的潜在应用价值。

