新型冠状病毒(SARS-CoV-2)的生物检测技术研究进展
梅艳秋,罗 燕,钟 斌,林小凤,邝 莹,易小庆,曾卫佳,杨 民,黄启同,6,8,9
(1. 赣南医学院2020级硕士研究生;2. 赣南医学院科研中心;3. 赣南医学院第一附属医院;4. 赣南医学院医用信息工程学院;5. 赣南医学院基础医学院;6. 江西省油茶医药保健及功能产品开发工程研究中心;7. 赣南医学院药学院;8. 江西省医用组织工程材料与生物制造重点实验室;9. 心脑血管疾病防治教育部重点实验室,江西 赣州 341000)
目前,席卷全球的新型冠状肺炎(COVID-19)主要由严重急性呼吸系统综合征冠状病毒2(SARS-CoV-2)引起的,SARS-CoV-2是β冠状病毒属的新成员,其与严重急性呼吸综合征—冠状病毒(SARS-CoV)等密切相关,是第七个可感染人类的冠状病毒[1-3]。图1为美国首例新冠肺炎患者体内分离出SARS-CoV-2 的透射电镜(TEM)图,TEM 显示其结构为直径在80~220 nm的微球形,具有囊膜和12~24 nm 的棒状刺突,具有典型的“冠状”病毒的形态特征[4]。目前COVID-19 的主要感染源是COVID-19感染者、潜伏期感染者和无症状感染者,其主要的传播途径包括:飞沫传播、接触传播、气溶胶传播以及其他可能的传播途径,如粪口传播等[5-7]。截至2020年12月1日,全球累计确诊63 751 110人,累计死亡人数达到1 477 200。由于COVID-19 具有非常强的传染性和致死性,目前全球各个国家都在寻求有效的预防和治疗方法,而预防的关键在于对患者的早诊断、早隔离、早治疗。
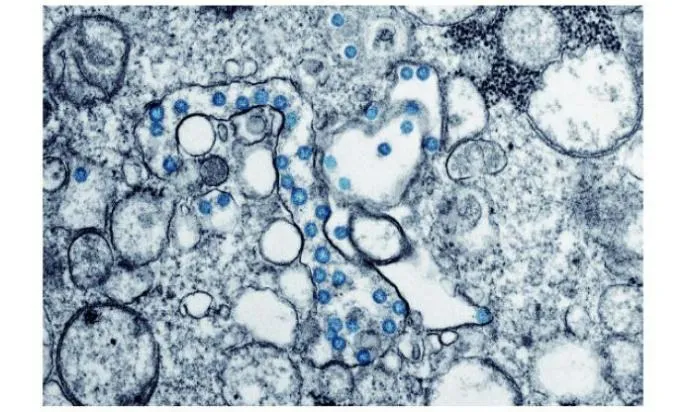
图1 SARS-CoV-2的TEM图[4]
开发快速、灵敏、简单、准确地检测SARS-CoV-2方法对于疫情防控至关重要。2003年的SARS-CoV、2012 年的中东呼吸综合征(MERS-CoV)以及现在流行的SARS-CoV-2 均属人类冠状病毒(HCoV),只是他们所处的菌株型不同,但是菌株结构大同小异,所以可借鉴之前对其他HCoV 的检测方法对SARS-CoV-2 进行检测。目前我国国家药品监督管理局(NMPA)批准了至少11 种基于核酸的方法和8种抗体检测试剂盒来检测SARS-CoV-2[8]。随着对COVID-19研究的不断深入,新的生物化学检测手段也被不断地开发出来,目前对SARS-CoV-2 的测定最有效的手段是通过核酸或者抗体检测(图2)[9]。本文对目前已有的SARS-CoV-2 的生物化学检测方法进行了总结。
1 SARS-CoV-2核酸检测
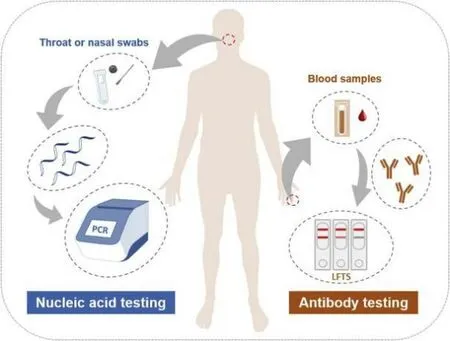
图2 用于SARS-CoV-2的两种主要测试方法:核酸和抗体检测[9]
核酸检测是作为诊断COVID-19 的主要方法,目前常用的核酸检测法包括宏基因组学测序[10-12]、聚合酶链反应(PCR)[13]、逆转录PCR(RT-PCR)[14-16]和核酸生物传感器[17]等,这些技术的发展为COVID-19的临床诊断和预防提供了重要的技术支持。
1.1 宏基因组学测序技术用于检测SARS-CoV-2宏基因组学测序技术无须对病毒微生物进行分离培养即可实现对病毒微生物的鉴定与临床诊断,基于宏基因组学测序得到SARS-CoV-2 病毒全基因组序列,为SARS-CoV-2列为β冠状病毒属的新成员提供了依据。因此,在疫情暴发早期阶段,SARS-CoV-2病毒的宏基因组测序作为确定COVID-19 患者的主要手段。张永振教授团队率先完成第一个SARS-CoV-2 基因组的测序工作,并系统比对了SARS-CoV-2基因与其他类冠状病毒基因的差异性,其与SARS 病毒基因组的相似度达到了89.1%,为SARS-CoV-2 的演化来源提供了依据[10]。随后,LU等[11]对获得了8个完整的SARS-CoV-2 基因组序列,并与其他冠状病毒的基因组序列进行了详细比对,系统分析了其与其他病毒基因的相似片段与差异性片段。目前,国家卫健委已将基因组测序中得到与已知的SARS-CoV-2 高度同源的结果,作为COVID-19 临床确诊的依据之一[12]。虽然宏基因组学测序成本较高,但是宏基因组学测序不仅为SARS-CoV-2的来源、发病机制的分析提供了技术支撑,还为新型SARS-CoV-2 检测方法的开发奠定了基础。
1.2 RT-PCR 用于检测SARS-CoV-2RT-PCR 是使用呼吸道样本(鼻咽拭子、口咽拭子、鼻咽洗液、鼻腔抽吸物、痰液、灌洗液以及气管吸出物等)诊断COVID-19 的 最 主 要 方 法[14-16]。 RT-PCR 将SARS-CoV-2 RNA 反转录为互补DNA(cDNA)链,然后扩增cDNA 的特定区域。设计过程通常包括两个主要步骤,一为序列比对和引物设计;二为分析条件的优化和测试。CORMAN 等[14]在与SARS 相关的病毒基因组分析中设计了双“引物—探针”体系。第一个引物组可以普遍检测许多冠状病毒,而第二个引物组只能检测SARS-CoV-2。之后优化测定条件(试剂条件、孵育时间和温度),随后进行PCR 测试,以此实现对SARS-CoV-2 RNA 测定。RT-PCR 可分为一步法或两步法进行测定。在一步测定中,反转录和PCR 扩增被整合为一个反应,这种测定方法为高通量分析提供了快速且可重复的结果。缺点在于逆转录和扩增步骤同时进行,优化过程很难实现,从而导致靶标扩增子的产量降低。在两步测定中,反应在单独的试管中依次进行,这种形式的分析法比单步分析法更敏感,但需要更多的时间去进行其他参数的优化。
RT-PCR 可用来诊断COVID-19,但是实际测试的敏感性和特异性相差很大,缺乏一致性,AI 等[15]研究表明其准确率仅为66%~80%,与此同时,AREVALO-RODRIGUEZ 等[16]也得出其检测结果假阴性率在2%~29%之间,其准确性低大致是因为检测时病毒载量低于最低检测值、专业人士操作不佳、所用核酸提取方法不适当、靶向DNA 序列未检测、探针和引物设计不良等诸多因素导致。
1.3 核酸生物传感器用于检测SARS-CoV-2生物传感器在病毒检测等领域已得到了广泛的应用,其是一种能产生与被分析物浓度成比例的可量化信号的分析装置。它们由换能器和生物活性元件或材料组成,如核酸、酶和抗体等,它们可通过特异性的相互作用实现对目标物的检测与分析[17-19]。目前,生物传感器主要包括荧光、光散射、表面增强拉曼散射、电化学和表面等离子体共振等技术[17-21]。由于生物传感器廉价、简单、灵敏、经济、快速等优点,可为非专业人员和公众提供切实可行的分析技术,因此,其受到了研究学者的广泛青睐。
JIAO 等[22]制备了基于DNA 纳米支架杂交链反应的新型DNA 荧光传感器,并成功地应用于SARS-CoV-2 RNA 的测定。首先DNA 纳米支架由长DNA 单链(RCA)和一些H1 探针(由立足点序列F1、发夹结构S'C1S 和尾部T1 组成)通过杂交组成。然后用5-羧基荧光素(FAM)染料和其猝灭剂(BHQ1)分子标记以形成自淬灭探针,发夹打开时荧光将恢复。当目标SARS-CoV-2 RNA 存在时,它会触发沿DNA 纳米支架的级联反应。在不添加目标的情况下,其具有弱的荧光信号,当存在SARS-CoV-2 RNA的情况下,游离的H1 和H2 能够相互杂交以触发杂交链式反应(HCR),从而导致荧光的恢复。由此构建出新型的荧光DNA 生物传感器,实现对SARS-CoV-2 RNA 的灵敏检测,检测限(LOD)达到了0.96 pM(图3)。该方法具有高信号增益、反应时间短、特异性高、室温响应、方便检测等优点。
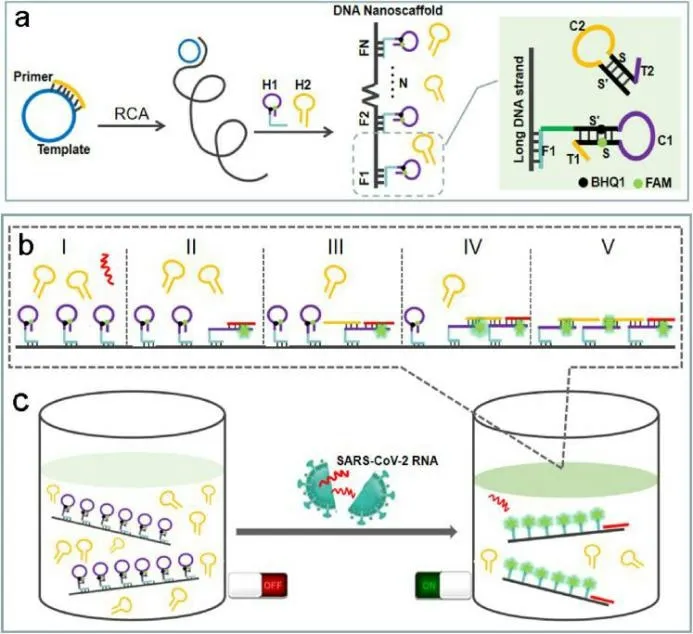
图3 基于DNA纳米支架杂交链反应的新型DNA荧光传感器用于测定SARS-CoV-2 RNA[22]
QIU 等[23]构建了等离子体光热效应(PPT)和局部表面等离子体共振(LSPR)传感转导相结合的双功能等离子体生物传感器。该传感器主要是基于二维金纳米粒子(AuNIs),并通过DNA 互补杂交技术,实现对SARS-CoV-2 中的选定序列进行敏感检测,其LOD 达到0.22 pM,并允许在多基因混合物中精确检测特定靶点。该项研究为PPT-LSPR 生物传感器在SARS-CoV-2检测方面提供了新的思路。
ZHU 等[24]开发了一种多重逆转录环介导的等温扩增(mRT-LAMP)与基于纳米颗粒的侧流式生物传感器(mRT-LAMP-LFB)相结合,用于诊断COVID-19,能在1 小时内快速检测出病毒中的ORF1ab 和核蛋白基因(N)。BROUGHTON 等[25]针对SARS-CoV-2开发了一种基于CRISPR/Cas12的LFB 生物传感器,比mRT-LAMP-LFB 传感器的检验时间缩短了半小时。
ZHAO 等[26]使用杯芳烃官能化的氧化石墨烯与靶向SARS-CoV-2 RNA 的合成了一个超三明治型电化学传感器(图4),该传感器用于临床标本SARS-CoV-2 RNA检测时的LOD低至200 copies·mL-1。基于此传感器也开发了一种即插即用的方法,甚至可用在智能手机上,实现无须RNA 扩增即可灵敏、准确、快速地检测各种临床中的SARS-CoV-2 样品,从而提供了一种简单、低成本检测方法。TRIPATHY等[27]利用无标签电化学检测DNA 杂交合成了一种微型电化学生物传感器,可作为一种潜在的方法用于COVID-19 的诊断。这个方法简单且便携,可以摆脱笨重的检测设备,能在现场即时操作,基于这个优点,为开发出快速诊断和即时诊断检测设备提供了参考。
CHAIBUN 等[28]开发了一种结合等温滚圈放大(RCA)的电化学生物传感器,用于对SARS-CoV-2进行高灵敏度和特异性的检测。利用RCA 的高扩增能力和高灵敏性的电化学检测方法,使我们能在合成的线性靶标和/或临床标本中检测到病毒的N和S基因,整个实验耗时不到2小时,该方法对临床样本的检验性能可与RT-PCR 相比较。该传感器可用于COVID-19的现场实时诊断。
总之,随着核酸检测技术的不断发展,越来越多的检测技术被开发用于SARS-CoV-2 的测定,表1显示了截至目前为止部分SARS-CoV-2 核酸测定的方法,通过不同方法的对比,希望后续研究学者能够开发出更加灵敏、快速、经济以及准确的COVID-19核酸测定方法。
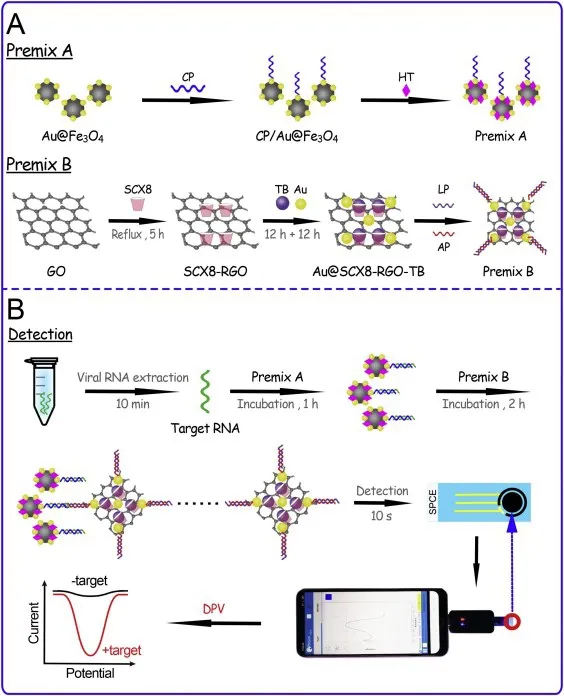
图4 三明治型电化学传感器检测SARS-CoV-2 RNA 的示意图[26]

表1 SARS-CoV-2核酸测定的方法对比
2 SARS-CoV-2蛋白检测
虽然SARS-CoV-2 核酸测定已得到了广泛的研究,但从SARS-CoV-2 的蛋白结构图(图5)可以看出,将整个病毒颗粒或其相应的表面抗原表位作为传感器检测标志物也可有效地实现对SARS-CoV-2的测定[39]。许多研究表明,IgM 抗体在症状发作后约5~10天开始可检测到并迅速升高,然后紧接着是IgG 抗体反应,这些血清转化通常发生在总抗体症状发作后的前3 周内,平均时间为9~11 天(IgM 为10~12 天,IgG 为12~14 天)[40],这些病毒感染后的免疫反应为SARS-CoV-2 的蛋白检测提供了可能,所以可利用病毒自带的蛋白质(例如S蛋白)或者患者样品中的抗体(例如IgM和IgG)进行检测。

图5 SARS-CoV-2结构示意图[39]
ZHANG 等[41]针对SARS-CoV-2 核衣壳蛋白(N蛋白)制备了DNA 适体。N 蛋白是最丰富的结构蛋白之一,它可作为准确、灵敏地检测SARS-CoV-2 的诊断标记。他们通过使用四个DNA 序列(亲和力低于5 nM)分别生成了四对适体,而且这四对适体由于三明治型相互作用,可以先后与N 蛋白结合,在ELISA 和胶体金免疫色谱条中使用这些夹心的适体,能够实现超灵敏地(1 ng·mL-1)检测N蛋白。
MAVRIKOU 等[42]制备了一种基于便携式无标签细胞的生物测定方法,可检测SARS-CoV-2的突触蛋白抗原S1。该生物传感器以超快速的方式(3 min)提供结果,检测极限为1 fg·mL-1,此外,没有观察到与N 蛋白的交叉反应性。无须事先对样品进行处理,就能大规模筛选SARS-CoV-2 表面抗原,为及时监测冠状病毒提供了依据。
FABIANI 等[43]建立了一种快速、智能检测唾液中SARS-CoV-2 的电化学免疫分析方法(图6)。以磁珠为免疫链载体,以碱性磷酸酶为免疫标记物的二级抗体为免疫标记物,建立了检测棘突蛋白(S 蛋白)或核衣壳蛋白(N蛋白)的电化学方法。用炭黑纳米材料修饰的丝网印刷电极检测酶副产物萘酚。该方法对S 蛋白和N 蛋白的检出限分别为19 ng·mL-1和8 ng·mL-1,将该方法用于唾液样本中SARS-CoV-2的直接检测,其检测结果与实时PCR 的检测结果一致。该方法具有检测限低,分析快速(30 min),仪器小型化,便携性好,使用方便,无创采样,且可用于检测未经处理的唾液中的SARS-CoV-2,该分析工具具有很高的市场准入潜力。
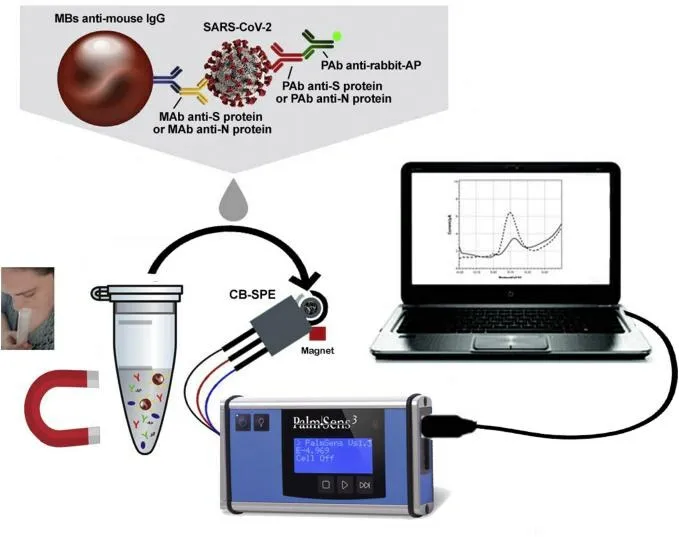
图6 磁珠为免疫链载体,以碱性磷酸酶为免疫标记物的二级抗体为免疫标记物,建立了检测S 蛋白或N 壳蛋白的电化学方法[43]
SEO 等[44]合成了一种基于场效应晶体管(FET)的生物传感设备,能检测临床样品中的SARS-CoV-2。它是通过S蛋白的特异性抗体覆盖在FET 的石墨烯片制成的。该传感器具有良好的灵敏度:培养基中的SARS-CoV-2(LOD:1.6×101pfu·mL-1)和临床样品(LOD:2.42×102pfu·mL-1)都被成功检测出,说明该FET生物传感器具有非常优异的潜在使用性。
目前,蛋白的检测虽然已取得了可观的进展(表2),我国国家药品监督管理局目前也已经批准了8 种用于SARS-CoV-2 抗体检测的试剂盒,但目前仍有假阴性或者假阳性的情况出现,因此,结合核酸检测和CT检测,将弥补蛋白检测的这一缺点。

表2 SARS-CoV-2蛋白测定的方法对比
3 结论与展望
迅速、灵敏、准确地实现SARS-CoV-2 检测对疫情的控制与监测非常重要。目前,无论是核酸检测还是蛋白检测仍存在不足,因此,通过两种目标物的测定,结合CT 检测,将有效地预防假阳性或者假阴性的产生。本次疫情的严重性也提醒我们有必要为未来任何病毒或其他致病性微生物暴发做好准备。其中,快速检测方法的不断开发是预防和管理未来可能发生的流行病的关键。因此,开发出廉价、快速、高通量和便携式筛查技术显得尤为重要。基于功能材料、纳米技术的新型传感器具有灵敏度高和成本低的优势,此类传感器在未来的应用前景将会得到不断重视。同时,新的智能传感方法将生物传感器的超高灵敏度与人工智能和物联网相结合,有助于更好地发现和预防潜在的传染性疾病。总之,随着检测技术的不断完善和疫苗的即将问世,COVID-19在不久的将来必将得到有效控制。

