CO2辅助好氧菌煤炭脱硫工艺的实验
王瑞,刘自勇,王琪,彭翠娜,陈中合,李福利,王晓龙,杨成
(1 济南大学化学化工学院,山东济南250022;2 中国科学院青岛生物能源与过程研究所生物燃料重点实验室,山东青岛266101;3 中国华能集团清洁能源技术研究院有限公司煤基清洁能源国家重点实验室,北京102209)
随着现代工业的迅猛发展,大量消耗煤、石油、天然气等不可再生能源,其燃烧产生的SO2、H2S 等污染性气体,对环境、社会等造成严重影响。近年来,利用微生物进行煤炭燃前脱硫技术因其反应条件温和、价格较为便宜、有害副产物少等特点一直受到各国政府、产业界和学术界的重视[1]。
工业应用微生物脱硫技术的关键难点在于,生物脱硫过程反应周期长和适用温度范围窄。国内外学者针对以上两个难点进行了大量研究,主要研究利用氧化亚铁硫杆菌、氧化硫硫杆菌、铁氧化钩端螺旋菌等除去煤中的无机硫,利用假单胞菌、大肠杆菌、埃希氏菌、红球菌属、芽孢杆菌属等脱除煤中有机硫,利用硫化裂片菌属、嗜酸热硫化叶菌、嗜酸硫杆菌等脱除煤中无机硫和有机硫组分[2−6]。嗜 酸 氧 化 亚 铁 硫 杆 菌 (Acidithiobacillus ferrooxidans) 及 嗜 酸 氧 化 硫 硫 杆 菌(Acidithiobacillus thiooxidans)两菌种,Juszczak 等[7]采用A.ferrooxidans 在初始铁离子浓度15g/dm3下脱硫反应7d,脱除煤中硫化铁硫,脱除率为54%,总硫脱除率为62%。Cardona等[2]采用A.ferrooxidans与A. thiooxidans 混合共培养技术,并在煤浆浓度10%、30℃、脱硫反应30d 后脱除煤中硫化铁硫达85%~95%,总硫31%~51%。Ohmura等[8−9]研究发现A. ferrooxidans 在H2/Fe3+、H2/S0、S0/Fe3+的厌氧呼吸模式及H2/O2的有氧呼吸模式下均可生长,且当培养过程中无CO2,菌种无明显生长,说明CO2可有效为A.ferrooxidans菌种的生长提供关键碳源。
围绕嗜酸氧化亚铁硫杆菌(A.ferrooxidans)和嗜酸氧化硫硫杆菌(A. thiooxidans)混合菌群对高硫煤生物脱硫,本文较为系统地研究了A.ferrooxidans 和A.thiooxidans两菌种混合共培养对煤炭脱硫的影响。研究探讨混合共培养的脱硫工艺条件,构建了CO2辅助A.ferrooxidans和A.thiooxidans协同脱硫的新工艺,探究CO2对生物脱硫效果的影响,并对CO2辅助两菌生物脱硫反应机理进行了探讨。煤炭清洁利用是当前资源环境领域面临的重大问题,CO2辅助好氧菌脱硫有望发展一条经济、高效的煤炭生物脱硫新工艺技术。
1 材料和方法
1.1 材料
本研究所用煤样产自山西高平,将煤块粉碎、过筛,90℃干燥24h后,放入干燥器,待用。依据GB/T 215—2003[10]、GB/T 212—2008[11]、GB/T 213—2008[12]等标准得到原煤、对照组及脱硫组煤样的热值、硫化铁硫含量、工业分析与元素分析数据,结果见表1。
由于生物脱硫产生的黄钾铁矾沉淀固定下的硫为硫酸盐形式,脱硫前后煤样中总硫含量有少量降低,但脱硫后氧元素明显增加近70%,主要是煤中单质硫与硫铁矿FeS2转变为SO42−离子,这与混菌21d后无机硫的70%脱除率吻合。
1.2 培养基配制
实验所用A.ferrooxidans和A.thiooxidans菌群来自山东大学微生物重点实验室林建强老师实验室保藏的菌株,两菌种将分别在Starkey−S0培养基和9K培养基中进行培养,并在9K 培养基中混合共培养进行脱硫。其中10×Starkey−S0培养基[13]的配制:母液配制的最终浓度为(NH4)2SO4(2g/L)、KH2PO4(3g/L)、MgSO4·7H2O (0.05g/L)、FeSO4·7H2O (0.01g/L)、CaCl2·2H2O(0.25g/L),并用6mol/L HCl 调节培养基的初始pH 为2;称量硫粉,加入配制的1×Starkey−S0培养基母液中,使得最终浓度为S(4g/L)。
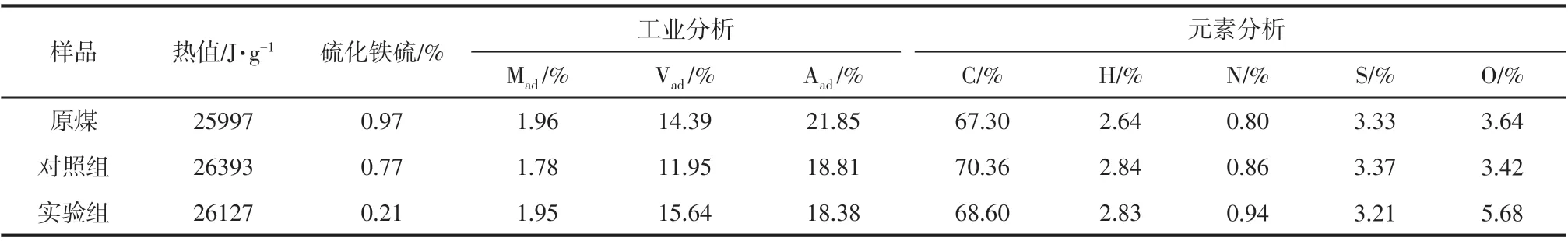
表1 原煤、对照组及脱硫组煤样的热值、硫化铁硫含量、工业分析与元素分析
10×9K 培养基[2]的配制:A 液配制的最终浓度为(NH4)2SO4(30g/L)、KCl(1g/L)、K2HPO4(5g/L)、MgSO4·7H2O (5g/L)、Ca(NO3)2(0.1g/L),并 用6mol/L HCl 调节培养基的初始pH 为2,121℃灭菌20min或0.22μm的滤膜过滤除菌;称取FeSO4·7H2O,与配制的A 液混匀,使得最终浓度为FeSO4·7H2O(50g/L)。
1.3 脱硫实验
1.3.1 对照组实验
依据10%煤浆浓度,在250mL 锥形瓶中加入10mL 10×9K 培养基A 液、90mL pH=2 盐酸溶液及10g 原煤,恒温水浴30℃下,150r/min 搅拌7d、14d、21d,同条件平行实验3次。
1.3.2 空气氧化环境脱硫实验
依据10%煤浆浓度、10%接种量,在250mL锥形瓶中加入10mL 10×9K 培养基A 液、10mL A.ferrooxidans 原 液、10mL A.thiooxidans 原 液、70mL pH=2盐酸溶液及10g原煤,其余同对照组实验条件,平行实验3次。
1.3.3 CO2气氛辅助脱硫实验
依据10%煤浆浓度、10%接种量,在250mL锥形瓶中加入10mL 10×9K 培养基A 液、10mL A.ferrooxidans 原 液、10mL A. thiooxidans 原 液、70mL pH=2盐酸溶液及10g煤,向锥形瓶中30mL/min持续通入CO2气体,其余同对照组实验条件,平行实验3次。
1.4 脱硫率测定
脱硫结束后,样品经8000r/min 离心5min,将离心后的固体煤样经90℃干燥24h后,将煤样按1g煤∶10mL 盐酸的比例加入0.3mol/L HCl 溶液,将煤与盐酸的混合液60℃水浴4h,尽可能除去生物脱硫产物中的NH4Fe(SO4)2(OH)6黄钾铁矾沉淀,随后依据GB/T 215—2003[10]中的原子吸收分光光度法测定煤中硫化铁硫的含量。其中测得实验所用原煤样中的硫化铁硫含量为0.9%~1.0%。
1.5 实验仪器及条件
以下测试样品均为FC−300 型粉碎机粉碎,80目筛分,90℃干燥24h处理后得到的煤样。
S−2500 型扫描电子显微镜(SEM)测试条件:加速电压为10.00kV,放大倍数分别为5000 倍和40000倍,工作距离分别为9mm和18mm。
VERTEX 70型傅里叶变换红外光谱仪(FTIR)测试条件:扫描范围为4000~450cm−1,分辨率为4cm−1,扫描次数为16 次,KBr∶样品=100∶1,图谱用透射率表示。
D8·FOCUS 型X 射线衍射仪(XRD)测试条件:Cu靶陶瓷管,扫描范围为10°~80°,扫描步宽为0.04。
Thermo Fisher Scientific ESCALAB 250型X射线光电子能谱仪(XPS)测试条件:X 射线源为Al靶,通过能为200eV,30eV高分辨率扫描,CAE分析模式,Large Area XL 镜头模式。使用C 1s(284.8eV)峰作为内标进行校正,使用XPSPEAK软件对S 2p、Fe 2p谱图进行分峰拟合。
2 结果与讨论
2.1 A. ferrooxidans & A. thiooxidans 对煤炭硫化铁硫脱除的协同作用
在初始pH 为2、转速150r/min、温度为30℃、煤粒度180 目的条件下,用A. ferrooxidans、A. thiooxidans 以 及A. ferrooxidans 和A. thiooxidans混菌,分别对煤样脱硫7d。从图1 可以看出,A. ferrooxidans 和A. thiooxidans 两菌种共同脱硫的硫化铁硫脱除率达到32%,比A. ferrooxidans、A.thiooxidan 各自单菌的硫化铁硫脱除率分别提高了5%、20%,两种嗜酸氧化菌表现出一定的协同优势。后续实验均采用A.ferrooxidans 和A.thiooxidans混合菌种培养进行煤中硫化铁硫的脱除。
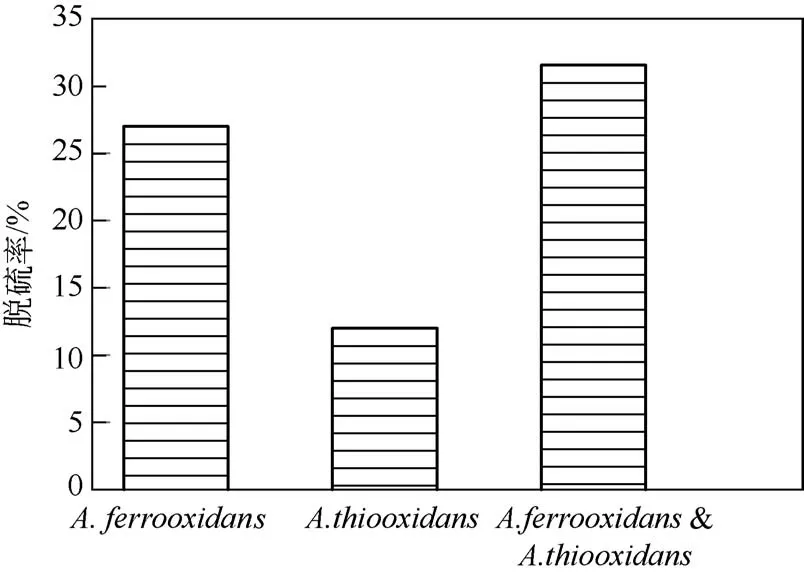
图1 不同菌种对于煤炭生物脱硫的影响
2.2 CO2气氛辅助微生物脱硫工艺初探
影响生物脱硫过程的主要因素有初始pH、温度、煤浆浓度、煤粉粒度、煤中黄铁矿的含量与分布状态、菌种、煤种等[2]。其中煤粉粒径、脱硫周期等对生物脱硫影响较大[5],对这两个工艺参数进行研究优化具有重要价值。图2 为保持初始pH 为2、转速为150r/min、温度为30℃,煤粉粒径大小、脱硫周期对煤中硫化铁硫脱除效果的影响。由图可见,煤粉粒径越小,脱硫周期越长,煤中硫化铁硫的脱除率越高。其中,煤粉粒径D<0.18mm,脱硫21d时,煤中硫化铁硫脱除率为60%左右;当煤粉粒径D<0.08mm,脱硫21d时,煤中硫化铁硫脱除率比同周期煤粉粒径D<0.18mm 时高出约15%,脱硫率最高达到77%。
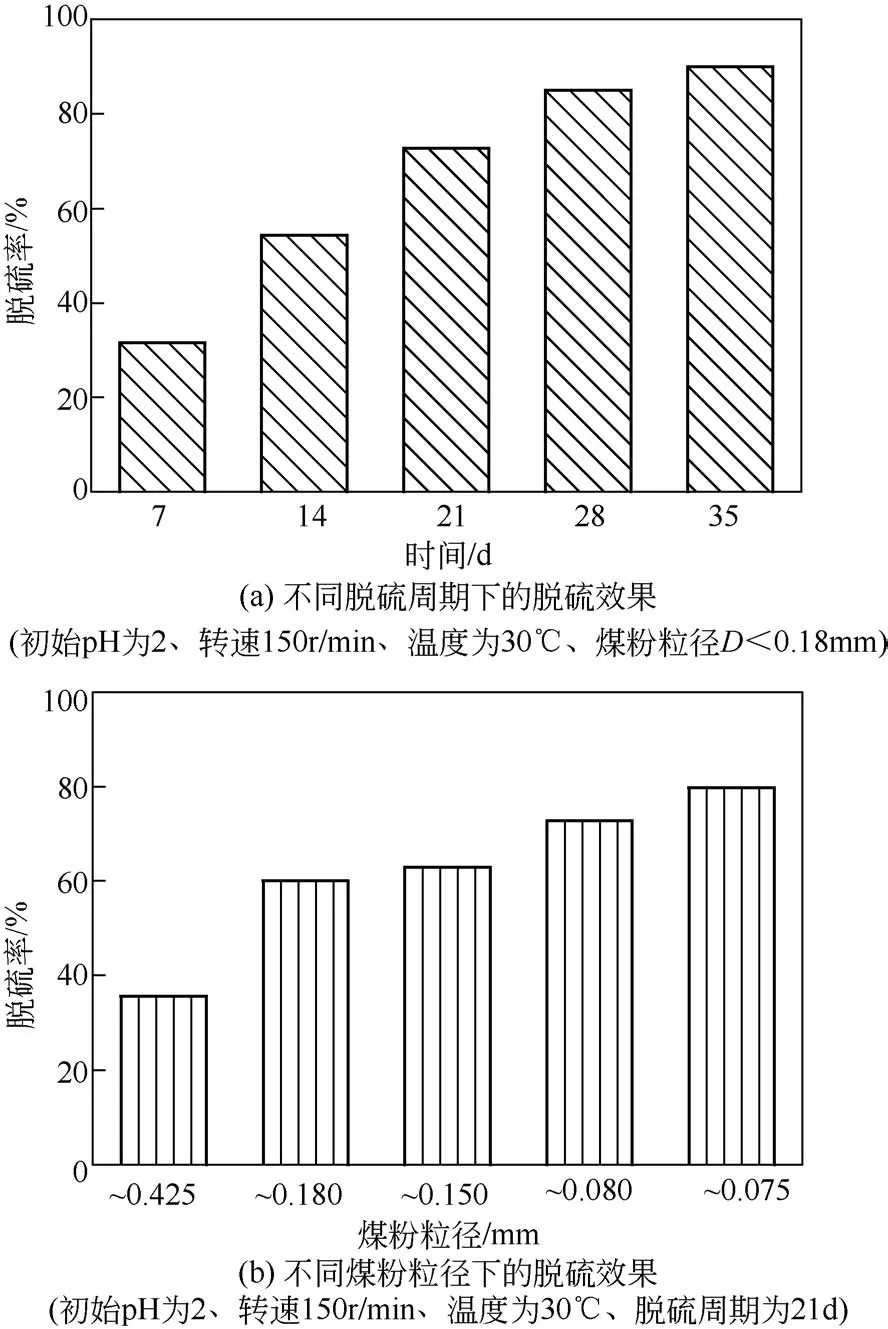
图2 不同煤粉粒径和脱硫周期对煤中硫化铁硫脱除效果的影响
文献报道,A.ferrooxidans 和A.thiooxidans 菌群能以CO2作为关键生长碳源[8−9,14],并可在25~30℃和常压下具有较高的脱硫效率。如前所述,本文作者课题组研究发现两菌种混合培养菌群的硫脱除效果优于单一菌种,因此采用A.ferrooxidans和A.thiooxidans进行混合脱硫研究。分别在空气氧化环境、CO2辅助气氛下进行为期21d 的脱硫实验,进一步研究CO2对煤炭脱硫的影响。图3 为不同气氛对煤中硫化铁硫脱除效果的实验数据,可以看出CO2辅助下硫化铁硫脱除率普遍高达90%,相较于空气氧化环境下的脱硫效果,平均提高了约20%的硫化铁硫脱除率。这一结果表明,CO2气氛辅助下A.ferrooxidans 和A.thiooxidans两菌混合能够明显提高硫化铁硫的脱除率。
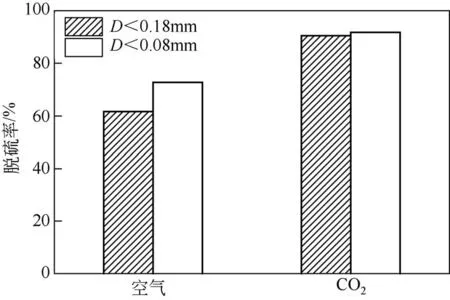
图3 不同气氛对煤中硫化铁硫脱除效果的影响
2.3 CO2气氛辅助微生物脱硫机理分析
2.3.1 SEM表征分析
图4为脱硫前后煤炭的SEM图。为了更好地观察生物脱硫对煤炭微观结构的影响,采用SEM 揭示煤炭脱硫前后的表界面变化。当使用0.3mol/L HCl除去表面覆盖的黄钾铁矾沉淀时,发现原煤表面较为平整,只出现少许破碎,这是由于盐酸与煤中的黄铁矿反应造成少许破碎;对比发现,脱硫后各煤样的表面均出现凹陷或不同程度的破碎情况,说明脱硫过程中微生物对煤炭表面形貌造成一定影响。随着CO2气氛引入到生物脱硫反应,SEM图显示煤表面凹陷和破碎程度更为明显,其中图4(e)中煤样表面的凹陷及破碎程度要比图4(d)明显得多,碎片也更为细碎,这说明CO2气氛的引入对A.ferrooxidans 和A.thiooxidans两种菌群的混合培养对煤表面形貌的影响更为显著,CO2气氛的引入对生物脱硫过程有较明显的增强效果。

图4 脱硫前后煤炭的SEM图
2.3.2 FTIR&XRD表征分析
有文献[15]表明黄钾铁矾在1188cm−1、1083cm−1和630cm−1处有特征峰。图5 中煤样在1200cm−1、1087cm−1和634cm−1出现的峰与标准黄钾铁矾的峰相对应,且吸收峰的强度随着CO2辅助气氛的引入而 有 所 增 强, 表 明CO2对A. ferrooxidans 和A.thiooxidans 两菌混合培养脱硫过程有明显促进作用,CO2充足时将加快脱硫反应进程。由图6可知,A.ferrooxidans 和A.thiooxidans混合培养脱硫后煤样的XRD 谱图中可以看到黄钾铁矾特征峰的存在,且随着在A.ferrooxidans和A.thiooxidans脱硫过程中引入CO2辅助脱硫,黄钾铁矾在28.966°、28.680°及17.408°处的衍射峰峰强度明显增强,这与实验结果中CO2加入后混菌脱硫率增强的趋势相一致。
2.3.3 XPS表征分析
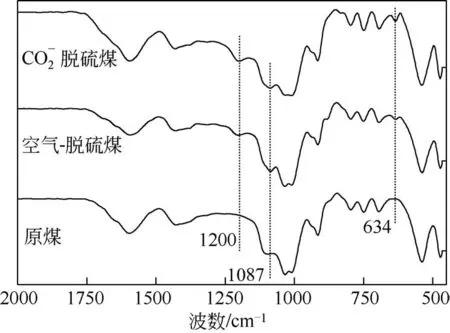
图5 不同气氛下脱硫煤样的FTIR谱图
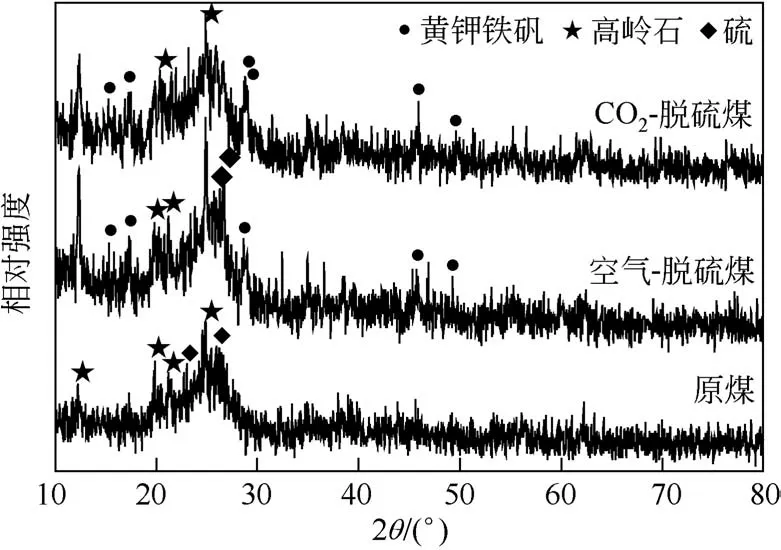
图6 不同气氛下脱硫煤样的XRD谱图

表2 生物脱硫前、后煤样表面无机硫的含量
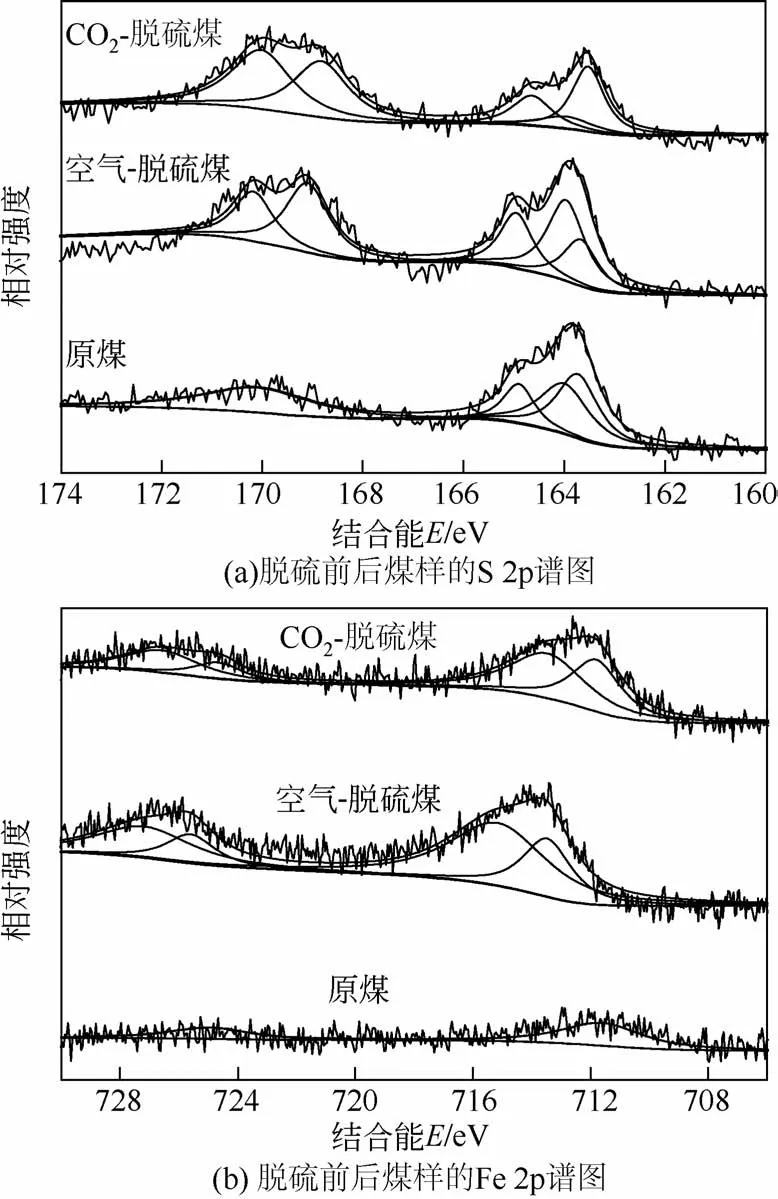
图7 脱硫前后煤样的S 2p、Fe 2p谱图
其中,163.3eV±0.4eV 为硫化物中硫的特征峰,169.5eV±0.5eV 为 硫 酸 盐 硫 的 特 征 峰[16]。A.ferrooxidans 和A.thiooxidans两菌对煤中硫的脱除主要集中在硫化铁硫等无机硫的脱除,并在表2中列出了生物脱硫前后煤样表面的无机硫含量变化。由图7 可知,原煤的S 2p 谱图经拟合后有4 个峰,其中归属于硫化物的163.7eV、164.0eV处特征峰峰面积较大,硫酸盐类的峰面积占比相比硫化物类的小26.5%。以原煤为基准比较两类硫的峰面积占比发现,空气氛围下脱硫样、CO2气氛辅助下脱硫样的硫酸盐硫占比的增加与硫化物硫占比的减少之间均达到了近似平衡,且CO2气氛辅助下脱硫煤样表面的硫酸盐峰面积占比明显比空气氛围下脱硫煤样的高了19%,这与本文中测得的CO2气氛辅助下脱硫效果比空气氧化环境下脱硫效率提高了约20%的数据相吻合。
同时,由图7可知,Fe3+的2p1/2、2p3/2轨道的对应特征峰处结合能为726.5eV、713eV,Fe2+的两对应特征峰较Fe3+的两特征峰均向低场移动了2~3eV[17]。由表3 中Fe(Ⅲ)∶Fe(Ⅱ)的峰面积比可知,原煤表面几乎没有Fe3+存在;随着生物脱硫的进行,Fe2+转化为Fe3+并向煤样表面以黄钾铁矾形式富集,包覆在煤样表面,阻碍微生物对煤样内部脱硫的继续进行,这与文献[2]中提及的现象相符合。
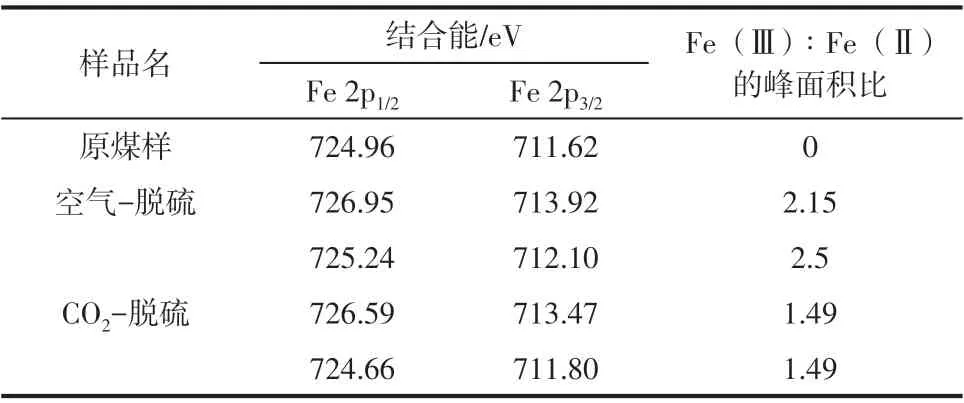
表3 生物脱硫前、后煤样表面Fe价态变化
CO2气氛辅助下脱硫煤样表面Fe(Ⅲ)∶Fe(Ⅱ)的峰面积比明显低于空气氧化环境下脱硫煤样,即CO2气氛辅助下脱硫煤样表面的Fe3+占比减少。根据SEM、FTIR、XRD 和XPS 的分析结果,初步发现在CO2气氛辅助下微生物A. ferrooxidans 和A.thiooxidans 两菌的混合脱硫过程中,CO2溶于水生成C使得溶液H+离子浓度变化,使得部分生成的Fe3+脱离煤表面,进入培养基中,从而减少煤样表面沉淀的累积,利于微生物对煤样内部的脱硫反应持续进行。
2.3.4 CO2气氛辅助微生物协同脱硫机理探讨
关于A.ferrooxidans脱硫过程中CO2的引入对脱硫的影响作用,当前报道较少且结论不尽相同[18]。图3 可知,当在CO2气氛辅助下脱硫21d,A.ferrooxidans 和A.thiooxidans两菌混合脱硫率可达到90%;比较同条件下空气氛围脱硫的脱硫率提高了约20%,CO2气氛辅助脱硫效果显著,在相同脱除率下CO2气氛的脱硫周期缩短30%。
无机硫占煤中总硫的60%~70%,大多以硫化铁硫的形式存在。硫化铁硫中的硫元素、铁元素经过复杂的多阶段物理化学过程,最终转化为硫酸及高价铁的可溶性硫酸盐,实现了硫化铁硫的溶解脱除。目前微生物对煤中硫化铁硫的脱除原理大致分为直接作用与间接作用两类。其中,直接作用为微生物吸附于煤中黄铁矿(硫化铁硫)表面能较低的凹陷上,直接把黄铁矿氧化成Fe3+和SO,反应过程见式(1)、式(2)。
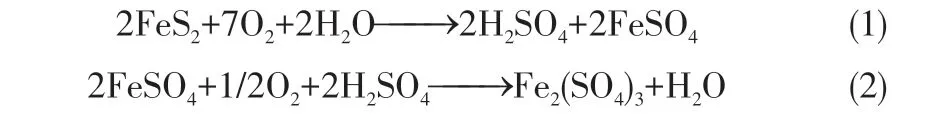
间接作用为微生物将溶液中Fe2+直接氧化为Fe3+,并与煤中黄铁矿反应,进一步生成Fe2+和H2SO4来实现煤炭中硫化铁硫的去除,反应过程见式(3)、式(4)。
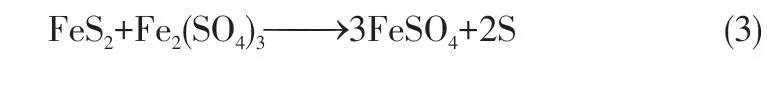
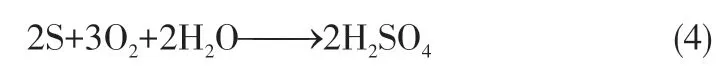
大多数学者认为煤中硫化铁硫的微生物脱除既有直接作用也有间接作用[19]。A.ferrooxidans 将Fe2+氧化为Fe3+及还原性硫化物,维持系统中Fe3+/Fe2+的高比率;A.thiooxidans氧化单质硫或还原态硫化物产生酸,降低pH,保持溶液中的离子形态[20−21],从而一定程度上降低了黄钾铁矾等在煤表面的沉淀等影响。
黄钾铁矾晶格中的K+常被Ag+、N、Na+、H3O+取代形成黄钾铁矾类矿物,已知Fe2+的氧化速率影响黄钾铁矾的形成,A.ferrooxidans可能是通过提高矿物表面微区内Fe3+的供应速度促使黄钾铁矾快速结晶[22]。故认为CO2在一定程度上影响矿物表面H+浓度及H3O+浓度,进而影响黄钾铁矾类矿物的沉积速度,减小黄钾铁矾沉淀在煤粒表面的吸附密度,为菌种对煤表面的下一步脱硫反应争取时间,使得脱硫效果提高。同时从培养基的配制可以发现,培养基中只有氮源、磷源等,没有碳源,CO2可以作为两菌种生长的碳源。实验结果表明引入的CO2为两菌的生长提供了充足的碳源,两菌生长状况较好,提高了煤炭脱硫效果。
3 结论
本文研究发现,在空气氧化环境下,A.ferrooxidans 和A.thiooxidans混合菌群表现出一定的协同作用,比A. ferrooxidans、A. thiooxidan 各自单菌的硫化铁硫脱除率分别提高了5%、20%。脱硫周期的延长明显提高了煤中硫化铁硫的脱除率,A.ferrooxidans 和A.thiooxidans混合菌群在空气氧化环境下脱硫21d,硫化铁硫脱除率可达70%。CO2气氛的引入能显著提高有氧条件下菌群的脱硫效率,脱硫21d时硫化铁硫脱除率可达90%,比空气氧化环境下的硫脱除率提高了约20%,在相同脱除率下CO2气氛的脱硫周期缩短30%。初步的机理分析表明在CO2气氛下黄钾铁矾沉淀在煤粒表面的吸附密度的降低是其促进脱硫的重要原因之一。本研究技术有望发展一条经济、高效的煤炭生物脱硫新工艺技术,促进实现煤炭清洁利用。
致谢:感谢山东大学微生物技术重点实验室为本研究提供的A.ferrooxidans及A.thiooxidans菌种;感谢山东省自然科学基金委与山东省科学院联合基金项目(ZR2016YL010)、山东国宇能源集团有限公司对本研究的支持。

