DETC在创面愈合过程中对炎症反应的调控作用及机制研究进展
陈成 胡晓红 梁光萍 贺伟峰
上皮内淋巴细胞(intraepithelial lymphocytes,IEL)是构成皮肤黏膜免疫系统的重要组成部分,其中包含了大量的γδT细胞[2]。树突状表皮T 淋巴细胞(dendritic epidermal T lymphocytes,DETC)作为γδT细胞家族的一员,是小鼠表皮内最重要的T细胞(占CD3 阳性T细胞的95%以上)[3],它们特异性地表达Vγ3Vδ1(Garman 命名体系)(根据Tonegawa 命名体系又称Vγ5Vδ1)T 淋巴细胞受体(T lymphocyte receptor,TCR)[4-5],并与角质形成细胞、朗格汉斯细胞共同构成抵御外界各种伤害的重要屏障[6]。近年来,人们发现DETC 可以通过分泌角质细胞生长因子(keratinocyte growth factor,KGF)促进再上皮化从而在创面修复过程中发挥重要作用[7-8]。然而创面愈合不止涉及再上皮化,还包括以炎症细胞浸润和迁移为特征的炎症阶段、以胶原沉积和血管生成为主的增殖阶段和涉及炎症消退和瘢痕成熟的重塑阶段[9]。其中,炎症反应作为创面修复的始动环节,可以为创面招募包括中性粒细胞、巨噬细胞和淋巴细胞在内的各种炎症细胞。这些炎症细胞分泌相应的炎症因子和细胞因子参与创面组织修复及重塑的全过程,并在其中发挥重要作用。尽管炎症是创面愈合过程中必不可少的关键环节,但过度的炎症反应会使创面发展为迁延不愈的慢性溃疡[10]。DETC在激活后可产生多种趋化因子和炎症因子抵御病原体并趋化各种炎症细胞扩大炎症反应。另外,在炎症反应后期,DETC 似乎也能抑制创面炎症细胞从而调节过度炎症反应带来的损伤。本文就DETC在创面修复过程中对炎症反应的调控作一介绍。
一、DETC 的发育与激活
DETC 即分布于表皮内的树突状的γδT 淋巴细胞,小鼠的γδT 淋巴细胞根据TCR 的不同分为Vγ1 到Vγ7T 淋巴细胞7个亚群,而DETC 是特异地表达Vγ3δ1 TCR 的γδT细胞亚群[1]。其来源于胸腺前体细胞并在胚胎期迁移至表皮并在此定殖。在DETC 发育过程中,TCR 和白细胞介素(IL)-15可为其长期存活提供必要的刺激[11],在静息状态下,DETC表现为部分激活,可持续低水平表达各种趋化因子、炎性细胞因子和包括KGF、胰岛素样生长因子(insulin-like growth factor-1,IGF-1)在内的生长因子,使其在维持表皮组织稳态中发挥重要作用[12]。当皮肤受到损伤后,受损角质细胞表达的未知抗原可与DETC 上的TCR 受体结合启动DETC 进入半激活状态[13]。而JAML-CAR、NKG2D-H60c 等共刺激分子则进一步促使DETC 完全激活[14-15],使之由树突状变为圆形。与小鼠不同的是,在人体内,γδT细胞习惯上根据TCRδ 链划分,主要为Vδ+1 T 淋巴细胞和Vδ2+T 淋巴细胞两大类,分别主要存在于人体的皮肤和外周血中。其中,Vδ+1 T淋巴细胞因其不具备树突状结构并且主要存在于真皮,因此不能称为树突状表皮内T 淋巴细胞。但因为其与小鼠表皮内的DETC在功能上具有相似性,例如分泌IGF-1 促进创面愈合、对肿瘤细胞产生细胞毒作用,常将其认为是人体内与小鼠DETC 相对应的γδT细胞[16-18]。
二、炎症反应对创面愈合的影响
创面愈合过程的炎症反应具有双重作用。在炎症反应初期,中性粒细胞和巨噬细胞迅速浸润到损伤组织部位并吞噬入侵病原微生物和坏死组织细胞碎片并释放大量抗菌活性物质抵御外来病原微生物的入侵以预防创伤后感染[19-20]。随后,M1型极化为M2型巨噬细胞并产生转化生长因子-β、转化生长因子-α、碱性成纤维细胞生长因子、血小板衍生生长因子等各种生长因子促进血管生成和细胞增殖以启动组织修复[20-21]。然而,炎症反应却是组织病理性修复-瘢痕形成的必要前提。胎儿的伤口修复缺乏典型的炎症反应,几乎无疤痕再生[22],但在胎儿伤口发炎时,疤痕的形成会加速[23],也有研究表明炎症反应中的淋巴细胞对疤痕形成有一定影响[24]。另外,各种炎症细胞释放的包括基质金属蛋白酶在内的蛋白酶可以水解促修复的介质来延缓创面愈合[25],以中性粒细胞为主所产生的大量活性氧和蛋白酶可直接损伤宿主细胞造成进一步损伤[10,26]。创面CD4+αβT细胞主要由Treg细胞组成(占70%)并致力于创面的炎症消退和组织重塑[27]。CD8+T细胞则因其细胞毒作用则延迟创面愈合[28]。
三、DETC 调节普通创面炎症
不同于上述免疫细胞,DETC 常驻于表皮组织,主要通过局部增殖进行自我更新,并不依赖于骨髓来源的前体细胞补充[1]。它们在损伤后的第一时间即可直接识别相关抗原,从而充当炎症反应发生的引发者。而通过对巨噬细胞和αβT细胞的趋化,DETC 可间接诱导创面愈合的炎症期向增殖期转变,最终达到促进创面愈合的目的。虽然目前关于DETC对创面愈合作用的研究多集中于再上皮化,对炎症阶段调控的研究尚不全面,但多项研究表明DETC 具有强大的免疫调节功能,其可以抵抗皮肤感染但它也是导致炎症性皮肤病、皮肤移植排斥反应等不可或缺的原因[29-31]。目前已证实DETC 对创面愈合炎症阶段调式方式包括趋化因子、炎症因子、透明质酸和NO,而这些调节方式所涉及的信号通路以及其他潜在的调节方式还有待探讨。
(一)趋化因子
DETC在激活后能大量表达包括巨噬细胞炎症蛋白-1α、巨噬细胞炎症蛋白-1β、T细胞激活性低分泌因子和淋巴细胞趋化因子等趋化因子,参与诱导炎症细胞的迁移。其中,CCL3、CCL4 和CCL5 属于CC 类趋化因子,主要参与巨噬细胞的趋化,也可参与T细胞和其他免疫细胞的诱导。XCL1则属于XC 趋化因子类,是DETC 产生的促迁移能力最强也是最多的趋化因子,可与CD8+αβT细胞上的XCR1受体结合,诱导CD8+αβT细胞向创面迁移,但对中性粒细胞和巨噬细胞无趋化活性[32]。
(二)炎症因子
除趋化其他炎症细胞外,DETC 也可直接产生促炎性细胞因子扩大炎症。早在1993年,Mastue 等[33]就检测到DETC 能 产 生IL-1β、IL-2、IL-3、IL-6、IL-13、GM-CSF、TNF-α、IFN-γ 在内的多种促炎性细胞因子,以及IL-4、IL-10、TGF-β 等抑炎性细胞因子。在促炎性细胞因子中,IL-6 可通过IL- 6-STAT3-Skint通路提高角质细胞的增殖和迁移能力[4]。另外,IL-17A 与角质细胞和朗格汉斯细胞来源的IL-1β、IL-23 组成的IL-1β/IL-23-IL-17A 轴在扩大炎症反应方面的作用广受关注[34]。DETC 作为损伤早期表皮IL-17A 的重要来源,可在IL-1β、IL-23 刺激下进一步增加IL-17 的表达[35-36]。同时Vγ4 产生的IL-17A 又能刺激IL-1β、IL-23表达从而形成正反馈环路,间接促进DETC 产生IL-17A[37]。然而,有研究者发现低剂量的IL-17A 促进伤口愈合,而高剂量的IL-17A 作用却相反[36-37]。这可能是因为DETC 产生的IL-17A不仅能诱导角质细胞产生β 防御素3、S100A8 以及Reg Ⅲγ等抗菌肽抵御病原体的入侵[38],还能适度地促进炎症反应促进伤口愈合。而高剂量的IL-17A 造成过度炎症反应阻碍伤口愈合。
(三)透明质酸
炎症细胞向损伤部位的迁移离不开细胞外基质的协助,而细胞外基质中的透明质酸因其本身的化学性质以及与相应炎症细胞表面受体(CD44、ICAM-1、RHAMM)结合的能力,成为促进炎症细胞迁移的重要成分[39]。Jameson 等[40]用打孔伤小鼠模型证明DETC 具有促进巨噬细胞迁移作用,这主要与DETC 介导分泌的透明质酸有关。DETC 分泌的KGF-1/FGF-7 和KGF-2/FGF-10 可与角质细胞表面的FGFR2 Ⅲb 受体结合,增加透明质酸合成酶2 和透明质酸合成酶3 的表达从而促进透明质酸的产生[8,40]。另一方面,DETC 本身也有产生透明质酸的能力,但这些透明质酸对中性粒细胞迁移的影响不大,可能其他中性粒细胞强趋化因子掩盖了它们的作用。另外,透明质酸还能促进TNF-α、IL-1β和IL-8 的产生,并诱导内皮细胞和树突状细胞产生趋化因子[41]。然而,透明质酸也可通过与TSG-6/IαI 复合体结合,促进IαI 对基质金属蛋白酶和其他蛋白酶的激活来降解细胞外基质中的炎症介质,从而阻止炎症细胞产生的自由基对组织的损害[42]。
(四)一氧化氮(NO)
NO 在创面愈合的各个方面都很重要,不仅能促进再上皮形成、伤口闭合和胶原蛋白沉积,也有助于炎症细胞如中性粒细胞和巨噬细胞的募集[43]。巨噬细胞作为NO 产生的重要来源,主要通过合成诱导型一氧化氮合酶来催化L-精氨酸产生NO。DETC 则可增强巨噬细胞NO 的产生,这使得创面IL-1β、巨噬细胞炎症蛋白-1α 和粒细胞集落刺激因子等炎症因子的水平增加,但单核细胞趋化蛋白的水平降低[44]。
(五)其他潜在调节方式
除促进创面愈合的作用外,DETC 也可在其他疾病中发挥免疫调节作用,此外,作为γδ 家族的一员,DETC 与其他γδT细胞的功能有许多相似之处,这其中涉及到的相关分子机制也许能为探讨DETC 对创面愈合过程中炎症反应的调节方式提供方向。
1.胸腺肽β4:类似于NO,胸腺肽β4 创面愈合多个过程中均能发挥相应作用,如促进血管生成、胶原沉积、再上皮化以及抵抗炎症反应等,目前已被广泛应用于皮肤创面的临床治疗[45]。Tβ4 的抗炎作用主要体现在可抑制中性粒细胞的聚集,以及通过促进自噬和抑制多种促炎因子如TNF-α 的表达来减轻炎症反应[46],此外,其也能通过抗凋亡作用和抑制活性氧的产生来减轻组织损伤[45]。既往研究表明Tβ4 主要存在于创面聚集的血小板中,但有研究者在皮肤炎症模型中了解到DETC在静止期和激活期也能表达Tβ4,Tβ4 由局限于淋巴组织的剪接异构体(splice-variant limited to lymphoid tissue,LTβ4)和广泛存在的肌动蛋白结合蛋白(ubiquitous actin-binding protein,UTβ4)两种成分组成,其中,LTβ4 在DETC 激活后水平和抑制炎症的作用高于UTβ4,提示LTβ4在缓解炎症反应中占主导地位[47]。因此,DETC 是否会在创面愈合过程中释放Tβ4 从而促进炎症期向增殖期的转变值得探讨。
2.细胞毒作用:在感染李斯特菌的小鼠模型中,终末分化的巨噬细胞会激活外周γδT细胞,使之对巨噬细胞产生细胞毒作用促进其凋亡从而调节免疫反应,减轻组织损伤[48]。DETC 也能通过穿孔素和颗粒酶等细胞毒作用直接杀死肿瘤细胞[29],也能够通过该途径清除创面终末分化的巨噬细胞来抑制炎症反应。
四、DETC 调节烧伤创面炎症
烧伤因其独特的热损伤和体液大量丢失与其他皮肤损伤有所不同。热损伤导致的创面损伤加重和烧伤毒素的产生可进一步加重创面愈合的局部和全身免疫反应,烧伤小鼠创面的炎症细胞和炎性细胞因子的浸润高于非烧伤创面[44,49-50],DETC 对烧伤创面的调节作用也与普通创面略有区别。
(一)T 淋巴细胞
如前所述,DETC 是诱导αβT细胞至创面的重要因素[32],但不同类型创面T细胞的浸润情况仍有所不同。普通创面浸润的T细胞以γδT细胞为主,而烧伤创面则以αβT细胞为主[51]。在烧伤创面中,DETC表达的CD69、TLR2、TLR4和TLR9 增加,提示烧伤创面可通过线粒体损伤相关分子模式(DAMPs)激活DETC[51-52]。与之相反的是,αβT细胞TLR和CD69 等激活相关分子表达下降,这可能与烧伤相较其他损伤产生更多的NO[53],而NO 与抑制T细胞增殖和其他功能有关[54]。DETC 又有助于创面NO 的产生,这进一步加强了对T细胞的抑制[44]。
(二)巨噬细胞
与上述得到的DETC 可诱导巨噬细胞在创面浸润的实验结果相反,Rani 等[50]观察到烧伤的野生型小鼠创面的巨噬细胞和髓样抑制细胞低于δTCR-/-小鼠,其中,髓样抑制细胞可由烧伤早期的巨噬细胞转化而来,主要发挥免疫抑制功能。二者结果的差异部分原因可能是二者的损伤模型不同,烧伤创面可能促使DETC 抑制巨噬细胞的募集或使其诱导巨噬细胞向髓样抑制细胞转化。同为烧伤模型,Daniel 等[49]实验结果也与Rani 相反,这可能是二者取样方式的差异导致的。Rani 从皮肤全层获取的细胞包括来自外周血的浸润细胞和皮肤中固有的常驻细胞,而Daniel 从创面皮肤下海绵获取的细胞只涉及浸润细胞,这提示DETC 可能对烧伤后皮肤中的浸润炎症细胞和常驻炎症细胞存在差异性调节,虽然可以趋化浸润细胞,但也可以抑制创面中的常驻细胞发挥及时终止炎症反应的作用。(图1)
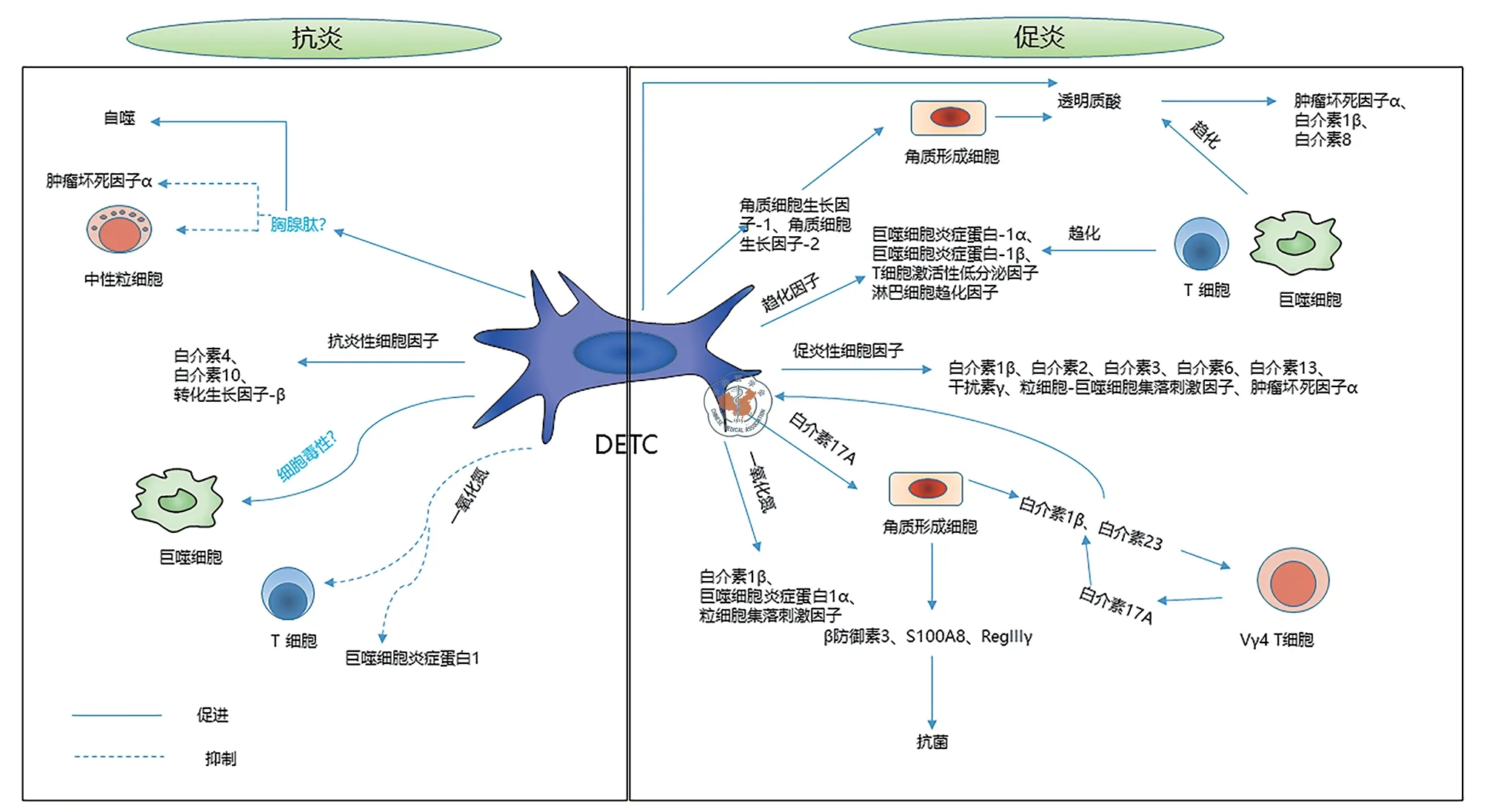
图1 DETC 对创面愈合炎症反应的调控机制
五、展望
创面的修复一直以来都是困扰医学界的难题。在创面愈合过程中炎症反应的不足会导致创面发生感染、转变为迁延不愈的慢性炎症。而过度的炎症反应则会导致瘢痕组织过度增生从而影响愈合后组织的形态与功能。甚至一些严重烧伤和创伤患者的死亡原因一定程度上也可以归因于免疫系统的调节紊乱。DETC在创面愈合的炎症阶段发挥启动和扩大炎症反应的作用,然而,在发生某些感染和炎症性皮肤病的情况下,DETC 也可以抑制炎症反应。这提示其对炎症反应可能存在差异性的调控,也许DETC在创面愈合过程中可及时终止炎症反应。尽管具体机制还有待研究,但DETC 对再上皮化的影响以及对炎症反应的调控表明了其在创面愈合和重度烧伤和创伤患者的救治方面具有广阔的应用前景。

