醇酸降解淀粉制备糊精的研究
刘子隽 邓 翀 胡秀婷 金征宇
(南昌大学食品学院,南昌 330047)(江南大学食品学院,无锡 214122)
将淀粉降解为分子量较小的糊精是提高淀粉水溶性的有效手段之一。广义的非环状糊精是指淀粉经不同方法降解所得到的产物,但不包括单糖和低聚糖。淀粉的降解是制备糊精的经典方法,包括淀粉的酶法降解和酸法降解。然后,淀粉酶对淀粉颗粒降解程度较低,而传统水体系酸降解淀粉易产生较多的低分子糖。近年来,淀粉醇酸降解制备糊精引起学者们的兴趣。淀粉的醇酸降解即将淀粉分散于小分子醇体系中,加入酸对淀粉进行降解,醇酸降解与传统水介质的淀粉降解相比具有产物得率高、产生的小分子量糖少、降解产物分子量分布窄等特点[1]。这表明醇酸降解淀粉可能是一种高效制备糊精的方法。研究表明,醇酸降解产物的最终平均分子量取决于醇的类型,相同降解条件下,不同醇酸降解淀粉的最终产物平均分子量顺序如下:甲醇>乙醇>异丙醇>正丁醇,这可能是因为不同醇介质体系导致渗入淀粉颗粒的酸浓度存在差异[2]。此外,醇酸降解淀粉的最终产物平均分子量还取决于淀粉来源、水分含量、酸的类型、酸的浓度和降解温度[3-5]。目前,关于醇酸降解淀粉的研究主要集中于醇酸降解对不同来源淀粉理化性质和结构的影响,包括流变性质、糊化性质、晶体结构、分子结构等[6-12],然而采用醇酸降解淀粉制备糊精的研究主要集中于工艺的优化[13]。因此,本研究以水溶性为指标,筛选适宜制备糊精的醇酸降解条件,从淀粉颗粒结构、晶体结构和分子结构等变化探究醇酸降解制备水溶性糊精的过程。
1 材料与方法
1.1 材料与试剂
木薯淀粉、大米淀粉、高直链玉米淀粉;乙醇、异丙醇、正丁醇和盐酸;分析纯。
1.2 主要仪器
Quanta-200扫描电子显微镜,Laser S3500激光粒度分析仪,D8-Advance X射线衍射仪,高效尺寸排阻色谱联合多角度激光检测器和示差检测器(HPSEC-MALLS-RI):LC-10AD输送泵、Dawn DSP-F多角度激光散射仪、Waters 2414示差折光检测器,高效液相排阻色谱柱Styragel HMW7和Styragel HMW6串联,TU-1901型双光束紫外可见分光光度计。
1.3 方法
1.3.1 淀粉的醇酸降解
称取(25±0.01)g淀粉分散于无水醇(乙醇、异丙醇、正丁醇),搅拌,水浴加热至40 ℃,加入1 mL浓盐酸,反应4 h、8 h、12 h、16 h、20 h、24 h、2 d、3 d、4 d、5 d、6 d和7 d。加入14 mL的1 mol/L NaHCO3溶液中和并且冰水浴以停止反应,然后将样品进行离心(5 000 r/min,10 min),收集沉淀后用50%乙醇溶液洗涤干燥,即可获得醇酸降解的淀粉,称重,计算糊精得率。
1.3.2 溶解性的测定
称取(0.5±0.000 1)g醇酸降解的淀粉(干基),加入10 mL蒸馏水,搅拌的同时加热至90 ℃,在90 ℃继续搅拌保温30 min,使得降解的淀粉充分溶解,冷却至25 ℃,置于25 ℃水浴锅保温4 h,在5 000 r/min下离心20 min,取上清液置于130 ℃烘箱干燥、称重。溶解性定义为溶解的淀粉部分(上清液中的淀粉部分)与总淀粉质量之比。
1.3.3 淀粉颗粒形貌分析
在室温下,将木薯淀粉和干燥后的醇酸降解木薯淀粉分别固定在样品台上,镀金(10 nm)处理后在加速电压下用扫描电镜观察,并拍下扫描图片。
1.3.4 淀粉颗粒粒径分布测定
分别将约100 mg木薯淀粉和醇酸降解的木薯淀粉分散于5 mL蒸馏水中,在200 r/min下搅拌10 min。然后,分散液立刻转移到激光粒度分析仪的样品池中测定,水的流速为60 mL/s,运行30 s。通过该粒度分析仪可以获得淀粉颗粒分布,包括体积平均尺寸(MV),数均平均尺寸(MN)和面积平均尺寸(MA)。本研究采用体积平均尺寸代表淀粉颗粒的平均粒径。
1.3.5 X-射线衍射仪分析
采用X-射线衍射仪(XRD)测定淀粉的晶型和相对结晶度。将淀粉样品平铺于样品池中,置于X-射线衍射仪中,选用铜靶Cu Kα(λ=0.154 06 nm),功率为1 600W(40 kV×40 mA),采用NaI晶体闪烁计数器测量X-射线的强度,扫描范围为4°~35°,扫描速度为4°/min。
1.3.6 分子质量的测定
参考Yokoyam等[14]的方法测定淀粉的分子量,称取木薯淀粉和醇酸降解淀粉溶于50 mmol/L NaNO3的DMSO溶液,沸水浴30 min使得淀粉完全溶解,再在25 ℃下搅拌24 h,配制合适的浓度,将得到的溶液过0.45 μm有机滤膜,采用HPSEC-MALLS-RI系统测定样品的分子质量。进样量:0.1 mL;流动相:50 mmol/L NaNO3-DMSO溶液(过0.45 μm有机滤膜,超声30 min脱气);柱温:35 ℃;流速:0.6 mL/min。MALLS的光源气体使用氦气和氖气,波长选用632.8 nm。流动相的折光指数取1.479,淀粉在溶液中的折光指数增量(dn/dc)为0.066。采用配套的Astra 5.3.4软件对激光散射信号和示差折光检测器信号进行采集,进而分析和计算淀粉的重均分子质量(Mw)、数均分子质量(Mn)和峰值分子质量(Mp)。
1.3.7 淀粉-碘全波长扫描分析
分别称取75 mg木薯淀粉和醇酸降解的木薯淀粉溶于15 mL DMSO溶液中,沸水浴1 h,取0.1 mL淀粉溶液加入0.2 mL碘溶液(1 mL碘液含有20 mg KI和2 mg I2),加蒸馏水定容至10 mL,室温下静置15 min,以0.2 mL碘溶液直接加蒸馏水定容至10 mL为空白,采用可见光-紫外光扫描仪在400~800 nm进行全波长扫描。
1.3.8 数据分析
采用Origin 7.0处理数据和绘制图形。结果用平均值±标准差的形式表示,指标比较采用最小显著差异法,取95%置信度(P<0.05)。所有实验平行测定3次。
2 结果与讨论
2.1 醇酸降解淀粉的溶解性
降解淀粉的得率均在90%以上,且在不同条件下无显著差异,这与文献报道一致,即醇酸降解淀粉的得率较高。如图1所示,在大米淀粉、高直链玉米淀粉和木薯淀粉醇酸降解过程中,随着降解时间的延长至3 d,淀粉的溶解性均显著增加,而降解时间进一步延长,淀粉溶解性缓慢增加。对于同一种淀粉,经正丁醇-盐酸降解之后溶解性最高,经异丙醇-盐酸降解之后溶解性次之,而经乙醇-盐酸降解之后溶解性最低。在相同的醇酸降解条件下,三种淀粉中木薯淀粉溶解性最大,大米淀粉溶解性次之,高直链玉米淀粉溶解性最低。通过比较溶解性,选择正丁醇-盐酸降解的木薯淀粉实验对象,阐明淀粉醇酸降解制备糊精的过程。
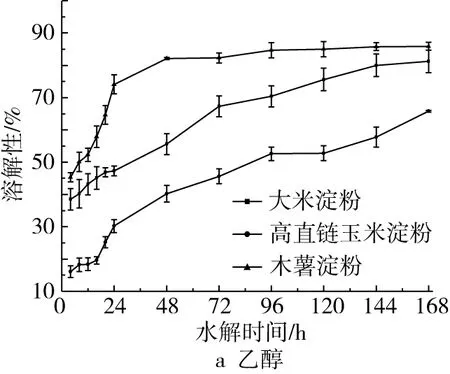
图1 淀粉酸醇降解过程中溶解性的变化
2.2 SEM分析
如图2所示,天然木薯淀粉颗粒呈椭球形,表面光滑。经正丁醇-盐酸降解4 h,淀粉颗粒保持原有的椭球形状,但淀粉颗粒表面变得粗糙,出现些许碎片,这表明正丁醇-盐酸降解破坏了木薯淀粉的颗粒结构。随着降解时间延长至3 d,淀粉颗粒表面出现凹陷,出现更多的碎片。随着降解时间的进一步延长,木薯粉颗粒破坏程度更加严重,大部分淀粉颗粒均失去了原有的颗粒形状。

图2 木薯淀粉正丁醇-盐酸降解过程中颗粒形态变化
2.3 淀粉粒径分析
如图3所示,天然木薯淀粉粒径分布在2.75~73.99 μm范围内,平均粒径为15.55 μm。经正丁醇-盐酸降解4 h后,木薯淀粉粒径和平均粒径均无显著变化。随着降解时间的进一步延长,大颗粒的木薯淀粉逐渐减少。经正丁醇-盐酸降解7 d后,木薯淀粉平均粒径下降了42.0%。SEM和粒径分析结果发现,木薯淀粉颗粒被正丁醇-盐酸的破坏导致了淀粉粒径的下降。然而与分散于水相中降解相比,木薯淀粉的粒径变化轻微,这与文献报道一致[7]。在醇酸降解过程中,糖苷键的断裂需要水分子的参与,而醇酸降解淀粉体系中水分含量少,因而正丁醇-盐酸只是轻微地破坏淀粉颗粒。然而与大米淀粉和高直链玉米淀粉相比,木薯淀粉的粒径下降程度更高、颗粒破坏更显著,这可能是因为三者淀粉颗粒结构不同导致正丁醇-盐酸处理对木薯淀粉的降解程度更高,从而导致其产物水溶性更高。
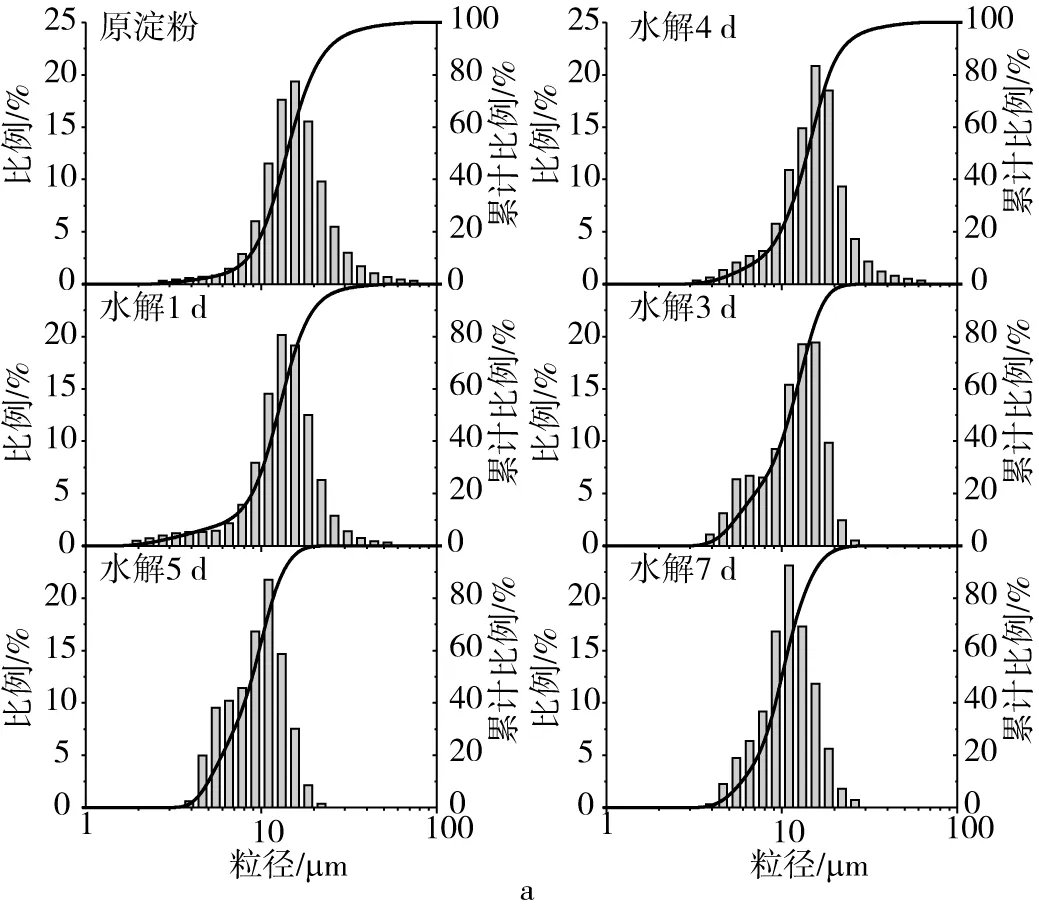
图3 木薯淀粉和正丁醇-盐酸降解木薯淀粉的粒径分布和平均粒径
2.4 XRD分析
图4为木薯淀粉在正丁醇-盐酸降解过程中结晶性的变化。木薯淀粉在15.1°和22.9°处出现显著的特征衍射峰,在17°和17.9°出现双重峰。根据文献报道,木薯淀粉作为薯类淀粉的一种,为C-型淀粉[15]。C-型淀粉被认为是A-型晶体和B-型晶体的混合体。由图3和图4可以发现,木薯淀粉中A-型晶体含量远多于B-型晶体,导致木薯淀粉特征衍射峰与A-型更接近,而无显著的B-型晶体峰。木薯淀粉的降解过程中,其结晶含量先升高,这表明正丁醇-盐酸降解了木薯淀粉的无定型区,随后结晶含量略有下降,表明正丁醇-盐酸破坏了木薯淀粉结晶区。降解后木薯淀粉在20°处出现特征峰,为V型晶体特征峰[16]。因此可以推断,在木薯淀粉的正丁醇-盐酸降解过程中形成了直链淀粉-正丁醇络合物,该络合物为V-型晶体,这与文献报道一致[17]。此外,木薯淀粉在醇酸降解过程中,V-型淀粉含量呈先上升后下降的趋势,这表明醇酸处理亦可破坏淀粉络合物。
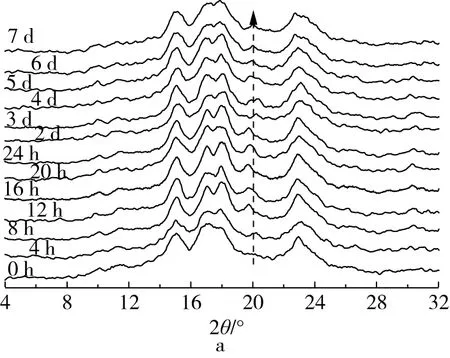
图4 木薯淀粉和正丁醇-盐酸降解木薯淀粉的XRD图谱和相对结晶性
2.5 分子质量的测定
木薯淀粉和醇酸降解的木薯淀粉分子质量见表1。木薯淀粉的Mw为3.024e +7 u。经正丁醇-盐酸降解4 h后,Mw急剧下降到6.331e+5 u,随着降解时间延长至3 d,Mw逐渐下降到2.308e+4 u,随着降解时间的进一步增加,Mw无显著变化。由此推测,盐酸在4 h内已经扩散至整个淀粉颗粒,并且类似内切酶作用于糊化淀粉的方式降解支链淀粉,从而导致淀粉平均分子质量急剧下降。结合XRD分析结果发现,与传统酸降解淀粉一样,正丁醇-盐酸以较快的速率降解淀粉无定型区的支链淀粉部分。此外,正丁醇-盐酸对淀粉的降解作用在3 d后几乎停滞。这可能有两方面的原因,一方面,根据XRD结果,在淀粉的正丁醇-盐酸过程形成直链淀粉-正丁醇络合物,淀粉的无定型区被降解导致淀粉结晶性提高,直链淀粉-正丁醇络合物和淀粉结晶区比游离的淀粉和淀粉的无定型区对酸更有抗性;另一方面,反应体系中水分子完全被消耗,在醇酸降解体系中,含水量非常有限,主要包括醇中的水分、淀粉中的水分和酸中的水分[18, 19]。
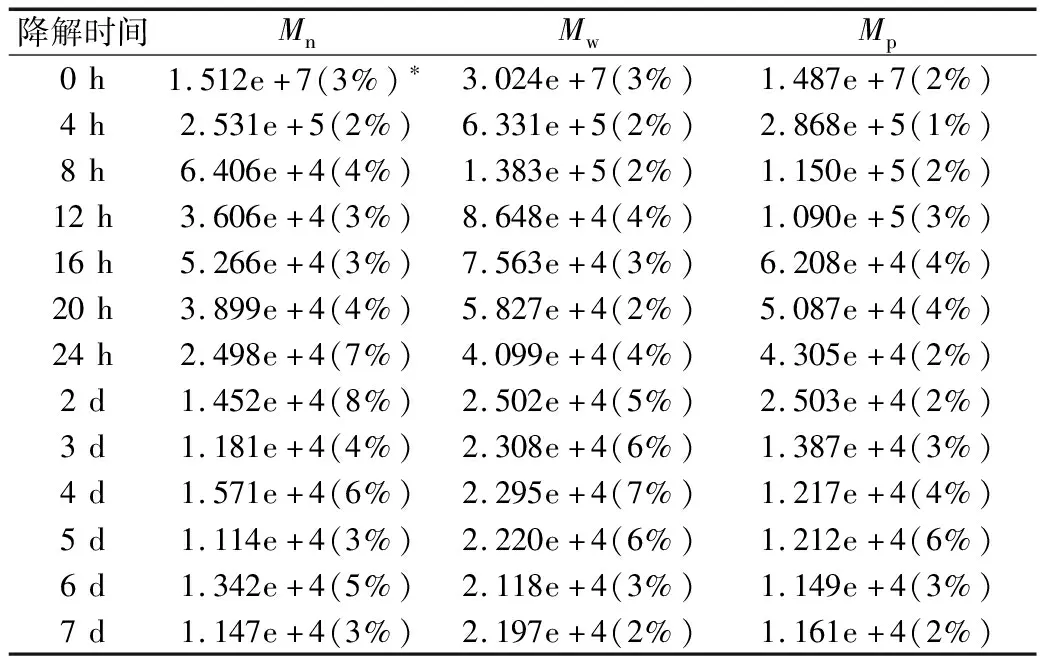
表1 木薯淀粉和正丁醇-盐酸木薯淀粉的分子质量信息
2.6 全波长扫描
淀粉与I2作用后可以形成颜色是淀粉重要的性质之一。直链淀粉遇碘呈蓝色,支链淀粉遇碘呈红紫色,淀粉在逐渐降解过程中遇I2可能会呈现紫色、红色,棕色,最后没有颜色,不同的颜色在可见光范围对应不同最大吸收波长(λmax),因此,淀粉-I2复合物的λmax可以表征直链淀粉的聚合度和支链淀粉侧链的平均链长[20]。因此,采用淀粉-I2复合物全波长光谱图反映淀粉在醇酸降解过程中平均分子量的变化。图5表明,经正丁醇-盐酸降解3 d后,木薯淀粉-I2复合物的λmax从584.1 nm蓝移至517.1 nm,随着降解时间的进一步延长,λmax无显著变化。这与分子质量的测定结果一致。而在相同条件下须降解4 d后大米淀粉和高直链玉米淀粉分子量趋于稳定[18, 19],表明醇酸处理对木薯淀粉降解的速率快于其对大米淀粉和高直链玉米淀粉的降解速率。
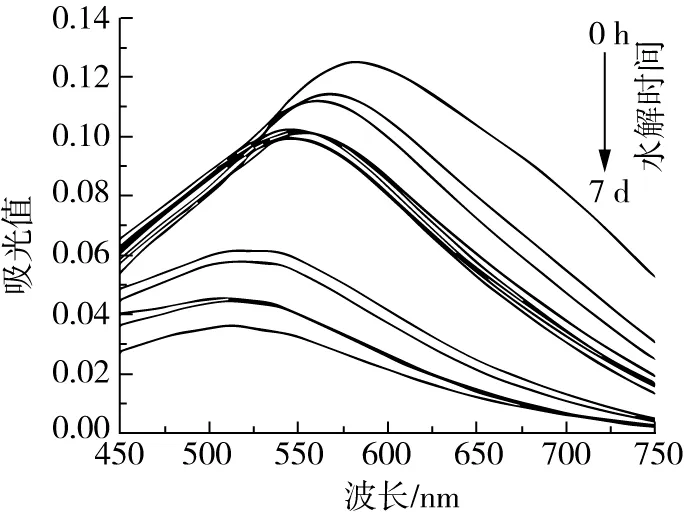
图5 木薯淀粉和正丁醇-盐酸降解木薯淀粉与I2复合物的可见光图谱
3 结论
醇酸降解过程中,不同的醇对淀粉的溶解性影响如下:正丁醇>异丙醇>乙醇;在相同条件下,正丁醇-盐酸降解的木薯淀粉溶解性最大,且在降解3 d时趋于稳定。在正丁醇-盐酸降解木薯淀粉过程形成了直链淀粉-正丁醇络合物,这可能是淀粉醇酸降解产物小分子糖含量少、分子量分布窄的原因。木薯淀粉的分子量在正丁醇-盐酸降解4 h后急剧下降,当降解时间进一步延长至3 d后,淀粉平均分子量无显著变化。因此,采用正丁醇-盐酸降解木薯淀粉3 d为制备糊精的最佳条件。

