不同钛源改性HZSM-5耦合低温等离子体放电催化生物油提质反应的性能
樊永胜, 侯光喜, 熊永莲, 蔡忆昔, 赵卫东
(1.盐城工学院 汽车工程学院,江苏 盐城 224051;2.江苏大学 汽车与交通工程学院,江苏 镇江 212013)
生物质热解可获得高附加值石油燃料替代品和基础化工原料,受到众多学者关注。目前,生物质催化热解液化和液化生物油品质提升成为研究的热点[1]。其中,HZSM-5分子筛因催化生物油提质效果明显而得到广泛关注[2]。生物油提质在HZSM-5催化下主要发生裂化和芳构化反应:生物油分子首先在L酸中心的作用下断裂脱氧或脱氢生成碳正离子,然后在B酸中心上经过β位断裂生成以C1~C4烯烃为主的碎片,然后继续在B酸中心的作用下发生齐聚环化反应,最后在L酸中心上环脱氢生成芳香烃。然而,在生物油催化提质过程中,常规HZSM-5易结焦失活[3],且催化产物中多环芳香烃含量过高[4]而不能满足要求,因此需要对HZSM-5进行改性以提升其性能。
迄今,众多研究者对HZSM-5进行了化学改性,引入P、B等非金属元素和Zn、Ni、Co、Ga等金属元素[5-8],在一定程度上提高了催化剂的选择性,增强了稳定性。然而,目前对HZSM-5进行Ti改性的研究仍然有限。Li等[9]对ZSM-5进行了Ti改性研究,发现Ti在催化过程中会发生价态变化,该过程中的电子迁移有利于促进碳正离子反应的进行;同时,Ti离子较高的价态和较小的半径使其具有较强的极化能力,可明显增强催化剂性能。在本课题组前期研究中,利用Ti/HZSM-5进行了生物油的提质研究,发现对HZSM-5进行Ti改性可明显提高催化剂对轻质烃的选择性,延缓催化剂结焦失活[10]。
低温等离子体放电(Cold Plasma Discharge, CPD)协同催化是将高压放电所引发的自由基反应与催化反应进行有机结合的一种新型催化处理技术。其中,高压电场提供了大量能量,用于分解、激发和电离反应物原子和分子,使反应体系内富含电子、离子、自由基和激发态分子,改变了反应物在催化剂表面的化学吸附行为,提升了催化剂活性和化学反应的选择性[11]。当HZSM-5催化剂催化反应过程中耦合CPD技术后,会在催化剂孔道及颗粒之间产生微放电,产生能量直接活化和解离反应物分子;同时,CPD技术产生的高能活性电子、离子等会撞击催化剂表面形成等离子体鞘,减少催化剂结焦,提高催化效率。
在本课题组前期研究中,将CPD技术引入生物油催化裂解过程,设计了以介质阻挡放电为工作原理的生物油催化提质反应器,构建了基于CPD的在线催化提质系统[12]。研究表明:CPD的协同作用使催化剂有效工作温度从550 ℃左右下降至400 ℃,且催化脱氧性能提升;在CPD作用下Ti改性HZSM-5对单环芳香烃和轻质脂肪烃的选择性较高;然而精制生物油产率与燃料品位很难同时得到提升,Ti改性的作用机制及改性催化剂与CPD的耦合作用机制尚不明确;并且催化剂使用后结焦焦炭会出现“同构化”,即不同类型焦炭的热分解规律趋于一致。
因此,笔者对HZSM-5进行不同Ti源改性,制备不同钛改性催化剂,考察不同钛改性催化剂耦合CPD对精制生物油产率、燃料品位及化学组成的影响。同时,为更好地分析钛改性的作用机制,对反应过程中产生的高能活性自由基进行在线监测;并分析使用后催化剂的结焦特性,探究不同钛改性对催化剂稳定性的影响及作用机制,为实现生物油高效提质提供依据。
1 实验部分
1.1 原料
所用油菜籽壳采自江苏省盐城市某农场,将干油菜籽壳粉碎成粒径为0.1~1.0 mm的颗粒,于105 ℃干燥24 h,保存备用。油菜籽壳的热挥发组成、元素组成及高位热值(HHV)如表1所示。一般而言,生物质或生物油的高位热值越大,燃烧所能释放的热能就越多,燃料的品位相对越高。因此,生物油高位热值的大小可以在一定程度上反映其燃料品位的高低。

表1 油菜籽壳的热挥发组成、元素组成及高位热值(HHV)Table 1 Thermal volatile composition, elemental composition and HHV of rapeseed shell
1.2 改性HZSM-5制备及表征
1.2.1 改性催化剂的制备
将硅/铝原子比为50的HZSM-5原粉在550 ℃煅烧2 h后,将其分别浸渍到金红石型TiO2和锐钛型TiO2的水分散液(2种TiO2粉体粒径约为1.6 μm),以及TiCl3和TiCl4的盐酸溶液中,于80 ℃恒温搅拌4 h,过滤、洗涤,于105 ℃干燥4 h以除去水分和盐酸,最后于马弗炉中550 ℃高温焙烧4 h,得到Ti质量分数占HZSM-5的5%改性催化剂。分别将金红石型TiO2、锐钛型TiO2、TiCl3和TiCl4改性催化剂记为TiRH-5、TiAH-5、Ti3H-5和Ti4H-5。
1.2.2 改性催化剂的表征
采用德国布鲁克AXS D8 Advance型X射线衍射(XRD)仪测定催化剂物相,以CuKα(λ=0.15406 nm)为辐射源,管电压为40 kV、管电流为30 mA,扫描速率为5°/min,扫描范围为2θ在5°~50°。
采用北京彼奥德SSA4300型分析仪进行液氮吸附-脱附测定催化剂比表面积和孔体积。由BET模型计算催化剂的比表面积;由BJH模型计算催化剂孔体积。
采用美国赛默飞Frontier型红外光谱仪配合真空吡啶吸附-脱附系统测定催化剂的Brönsted酸和Lewis酸分布。
1.3 生物油催化提质实验系统和方法
1.3.1 实验系统
生物油在线催化提质系统如图1所示。该系统包括生物质热解反应器、催化反应器、连接管路、过滤装置、冷凝收集装置、集气装置、稳压筒、真空泵以及温控装置等。催化反应器采用介质阻挡放电(DBD)原理设计成同轴双介质结构,具体结构参数见文献[12],催化剂层置于放电区中。实验时通过调压阀调节体系内部压力。此外,在催化反应器中填装催化剂时,利用带筛孔的石英玻璃薄片沿径向隔开,形成一条细小的光学透光通道,用来实时检测反应自由基中间体。

图1 生物油在线催化提质系统Fig.1 Diagram of experimental apparatus of bio-oils online catalytic upgradingDBD—Dielectric barrier discharge
1.3.2 实验方法
生物质先在反应器下段进行热解,产生的热解气在真空泵抽吸作用下进入反应器上段进行催化提质反应,然后经过滤、冷凝等,得到液相生物油。用二氯甲烷萃取分离液相生物油中的有机物,得到精制生物油。实验条件:催化剂层高度为30 mm;催化温度为400 ℃;生物质热解终温为500 ℃;升温速率为20 ℃/min;体系压力为5 kPa;加载等离子体电源进行高压高频放电,输出功率为800 W,输出电流为30 mA。此条件下,热解和催化过程均达到较优状态[13]。
实验过程中,采用美国海洋光学USB4000光纤光谱仪进行反应生成自由基分析,以美国海洋光学DH-2000为光源,检测波段为350~1050 nm。
以生物质原料质量为基准,计算精制生物油产率。为便于分析,将HZSM-5、TiRH-5、TiAH-5、Ti3H-5和Ti4H-5催化得到的精制生物油分别记为 RB(0)、RB(R)、RB(A)、RB(3) 和RB(4)。对使用3次后的催化剂进行分析以评价其稳定性。
1.4 精制生物油及催化剂分析
1.4.1 精制生物油分析
采用意大利Euro Vector EA3000型元素分析仪测定精制生物油的元素组成。
采用美国赛默飞世尔Trace DSC II型气-质联用分析仪(GC/MS)测定精制生物油组成。GC条件:载气为高纯He,流量为1 mL/min,进样口温度为250 ℃,不分流,进样量1 μL;MS条件:离子源温度为230 ℃,MS传输线温度为250 ℃,电离方式为EI,电子轰击能量为70 eV,扫描质荷比范围为30~500,扫描时间为1 s;升温程序:30 ℃保持2 min,以15 ℃/min升温至100 ℃,然后以 10 ℃/min 升至250 ℃并保持3 min,溶剂(CH2Cl2)延迟时间为3 min。
1.4.2 催化剂结焦分析
采用美国赛默飞世尔TGA/DSC 1型同步热分析仪对结焦催化剂进行热重分析。采用荷兰飞利浦CM200型透射电子显微镜(TEM)观察结焦催化剂上的焦炭分布及特征,点分辨率为0.235 nm。
2 结果与讨论
2.1 改性催化剂表征分析
2.1.1 XRD分析
钛改性前后催化剂X射线衍射谱如图2所示。由图2可见,各催化剂X射线衍射谱(JCPDS card:PDF 44-0003)基本一致,并未发生明显的衍射峰位置偏移,表明钛改性催化剂结构完整,未发生晶相取代。对于TiRH-5,在2θ为27.45°、54.32°和36.09°等位置有微弱的衍射峰,归属于金红石型TiO2(JCPDS card:PDF 21-1276);对于TiAH-5,在2θ为25.28°、48.05°和37.80°等位置的衍射峰由锐钛型TiO2(JCPDS card:PDF 21-1272)引起;对于Ti3H-5,由XRD图可以确定HZSM-5负载TiCl3改性,催化剂上引入了多种中间价态的钛氧化物,包括Ti2O3(JCPDS card:PDF 10-0063)和Ti3O5(JCPDS card:PDF 09-0309)等;对于Ti4H-5,XRD衍射峰分析表明,HZSM-5负载TiCl4改性,催化剂上引入的是常规TiO2((JCPDS card:PDF 65-5714)。
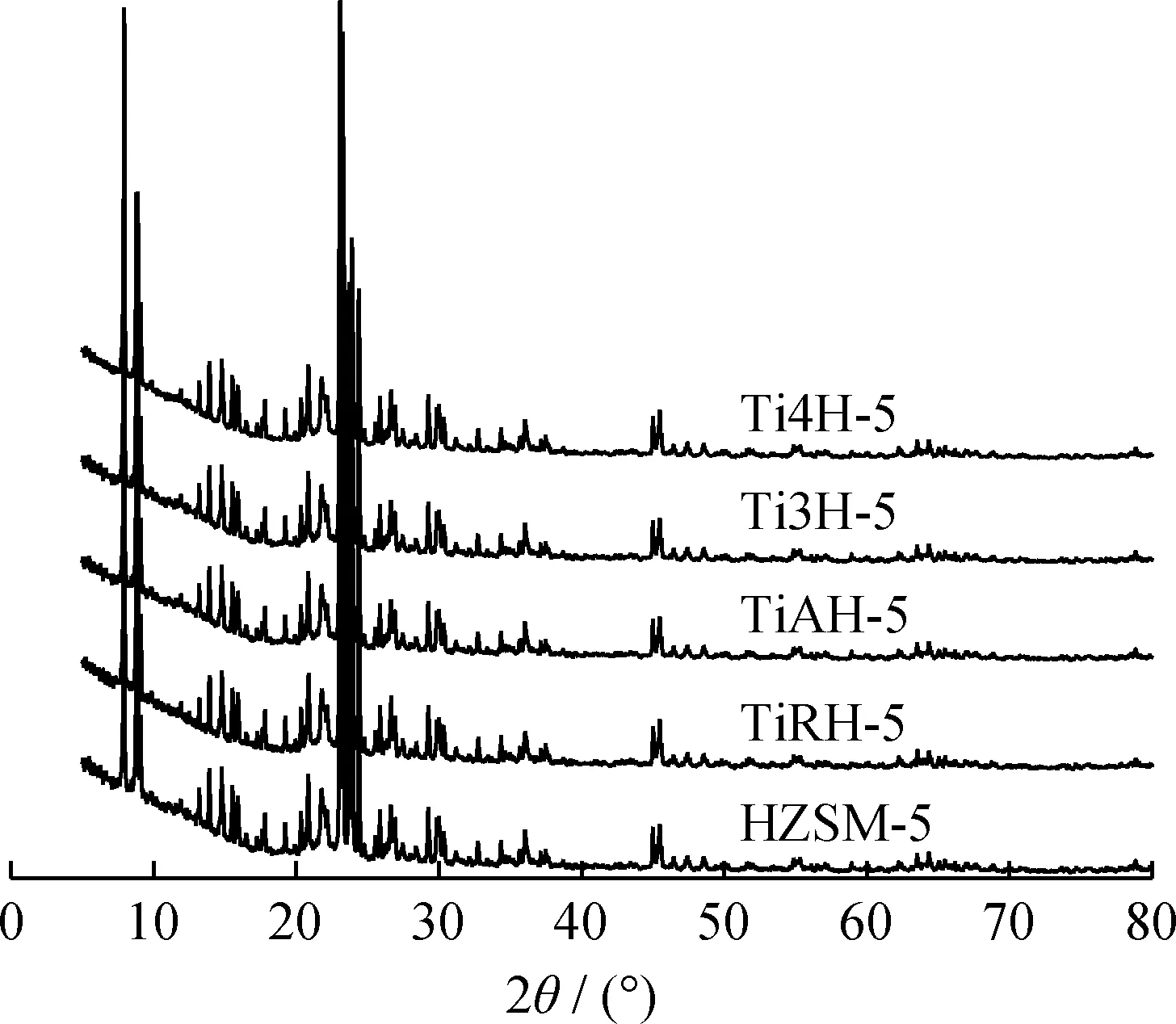
图2 改性前后催化剂的XRD谱Fig.2 XRD patterns of catalysts before and after modification
2.1.2 催化剂的比表面积和孔体积
钛改性前后催化剂的比表面积和孔体积参数如表2所示。由表2可见,金红石型和锐钛型TiO2改性的TiRH-5和TiAH-5催化剂比表面积及孔体积有所降低;TiCl3和TiCl4改性的Ti3H-5和Ti4H-5催化剂比表面积和微孔孔体积亦降低,但总孔体积明显增大。这是因为TiCl3和TiCl4改性过程中,溶液中的HCl会去除晶间堆积通道中的非晶态颗粒,使孔径增大。
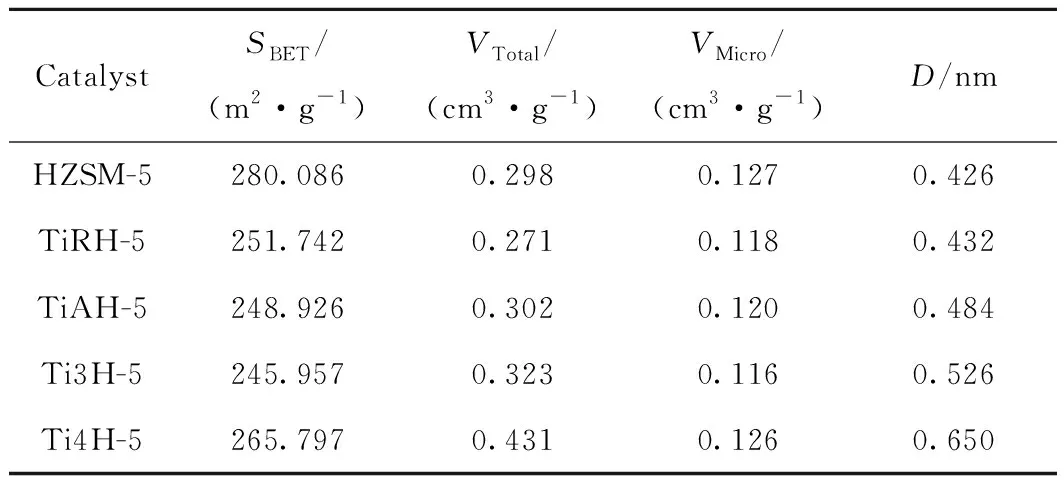
表2 钛改性前后催化剂比表面积及孔体积Table 2 Specific surface area and pore volume results ofcatalysts before and after modification
2.1.3 Py-IR分析
钛改性前后催化剂的吡啶红外脱附谱如图3所示。其中,波数在1450 cm-1和1616 cm-1附近的吸收峰代表弱L酸中心;1545 cm-1附近的吸收峰代表强B酸中心;而1490 cm-1附近的吸收峰则为弱B酸中心和较强的L酸中心的共同特征峰,这部分酸中心催化作用较弱,一般不进行半定量分析[14]。B酸和L酸酸性的半定量分析结果如表3所示。由表3可见,金红石型和锐钛型TiO2改性使催化剂各酸性位点减少,金红石型TiO2改性降低了催化剂的B/L酸量比,而锐钛型TiO2改性提高了催化剂的B/L酸量比。在用TiCl3和TiCl4改性过程中,催化剂经过盐酸处理,使B酸酸量明显增加;同时氢离子与金属离子的交换,使部分B酸中心向L酸中心转化[15];此外,催化剂骨架Al能与金属离子作用也产生L酸中心[16],使催化剂的L酸中心增加显著。因此,用TiCl3和TiCl4改性,催化剂的B酸和L酸中心都增加,但n(B)/n(L)降低。

图3 钛改性前后催化剂吡啶红外脱附谱Fig.3 Py-IR desorption spectra of catalystsbefore and after modification
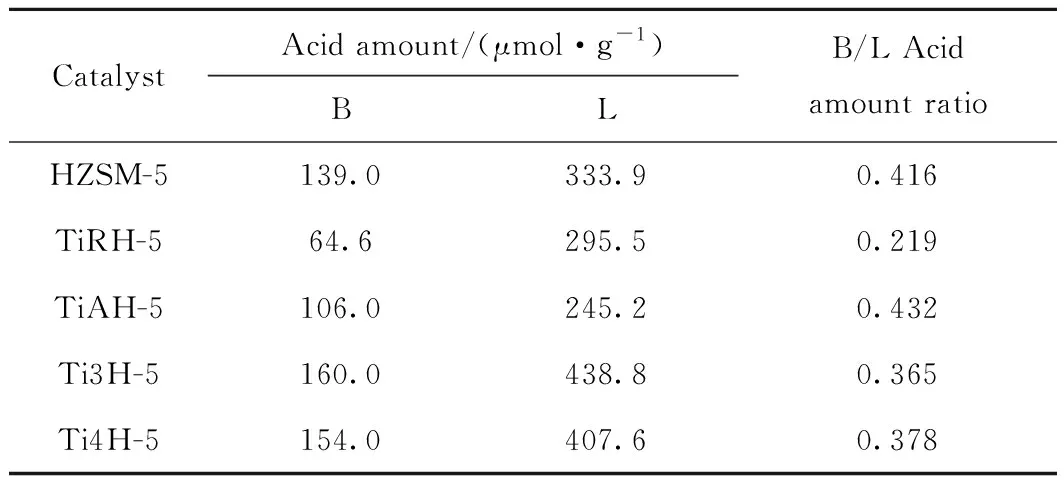
表3 吡啶红外半定量钛改性前后催化剂上酸量Table 3 Py-IR semi-quantitative results of catalystsbefore and after modification
2.2 在线光谱分析
使用不同钛源改性催化剂时反应体系的在线光谱分析结果如图4所示。由图4可见:位于431 nm位置的发射线归属于CH自由基[17];位于486 nm和656 nm位置的发射线归属于Hβ和Hα原子自由基[18];位于516 nm和590 nm位置的发射线分别对应C2烃和C自由基[19];而位于777 nm和844 nm位置的发射线则归属于高活性O自由基[18]。一般而言,谱峰强度越大表明自由基浓度越高,因此可以将谱峰强度作为半定量分析依据。当以TiRH-5、TiAH-5和Ti4H-5为催化剂时,主要自由基的发射线强度较用HZSM-5时变化不大,甚至还有所减弱。这是因为锐钛型、金红石型以及常规TiO2中钛元素的价态及键构较稳定,与CPD的协同作用较弱,难以产生更多活性自由基;同时,由于改性物掩盖了HZSM-5部分酸性位点,削弱了催化剂酸性位点与CPD的协同作用。而当以Ti3H-5为催化剂时,大部分自由基的发射线强度较高,原因在于用TiCl3改性引入了中间价态的钛,其倾向失去电子而被进一步氧化,消耗O自由基,从而促进了CPD诱导的生成O自由基反应,而O自由基增多会促使长链大分子有机物断链分解,产生更多的H和C自由基[20]。此外,CPD诱导过程中释放的高能电子会还原被O自由基氧化的钛,使中间价态的钛处于被氧化、还原的动态反应过程中,从而促进自由基反应。因此,以TiCl3改性的催化剂Ti3H-5对反应体系中生成活性自由基的促进作用最强。

图4 不同钛源改性催化剂催化反应体系的在线波谱Fig.4 Online spectra of reaction system with differentTi sources modified catalysts
2.3 精制生物油分析
2.3.1 精制生物油产率及元素组成
采用不同钛源改性催化剂耦合CPD技术的生物油提质反应中,提质精制生物油的产率、元素组成、有效氢碳比(nH/nC)[12]和HHV见表4。由表4可见,与RB(0)相比,RB(R)产率提高但HHV降低,主要原因在于HZSM-5负载金红石型TiO2的改性催化剂TiRH-5活性下降,导致生物油提质反应进行不彻底,保留了很多含氧有机物;虽然表观产率升高,但改性效果很差。
RB(A)的产率最高,为14.57%;其nH/nC和HHV均明显升高。这是因为锐钛型TiO2是一种高性能光催化剂,由其改性的TiAH-5催化剂在耦合CPD技术时会产生驱动TiO2光催化作用的紫外光[21]。光生电子易被含氧有机物捕捉,促使有机物的活化或分解,形成更多的碳氢碎片;而空穴则更易吸附和转化有机物和活性自由基[22]。此外,TiAH-5催化剂L酸中心的脱氢作用较强,锐钛型TiO2改性使TiAH-5的n(B)/n(L)升高,生物油提质反应倾向于保留氢元素,使高nH/nC的烃含量增加。
RB(3)的产率较高,其nH/nC和HHV提高最明显。这主要得益于Ti3H-5催化剂上中间价态的钛处于“氧化-还原”的动平衡状态,有利于提升自由基反应效率,产生更多的H和C自由基,促进生物油催化提质反应[9]。与RB(0)相比,RB(4)的产率降低,nH/nC和HHV略有升高,但不明显;RB(4)与RB(A)和RB(3)相比,其产率、nH/nC和HHV均显著降低,表明常规TiO2与CPD之间亦无明显的协同作用。因此,以TiCl3改性的催化剂Ti3H-5能同时提升精制生物油产率和燃料品位。

表4 精制生物油产率及元素组成Table 4 Yields and elemental compositions of refined bio-oils
2.3.2 精制生物油的组成
生物油提质精制产物主要为烃类化合物和含氧化合物。其中,烃类化合物主要有单环芳香烃(MAHs)、多环芳香烃(PAHs)和轻质脂肪烃(LAHs);含氧化合物主要有呋喃类(FUR)、酚类(PHE)、醇类(ALC)、醛/酮类(ALD/KET)和酯/醚类(EST/ETH)化合物。
不同催化剂催化生物油提质反应的产物组成如表5所示。由表5可见:与RB(0)相比,RB(R)中MAHs和PAHs含量有所降低,而LAHs有所增加,烃类化合物总含量降低,表明TiRH-5的芳构化性能变差;含氧化合物除了FUR含量降低之外,其他均不同程度增加,而FUR的减少是由于TiRH-5的n(B)/n(L)降低导致部分呋喃开环生成了羟基[23]。
RB(A)的烃类化合物总含量升高,氧含量降低,使HHV升高;而烃类含量升高又以LAHs和MAHs增加为主,其氢含量相对较高,因而使产物的nH/nC升高;同时,RB(A)中含羰基的ALC和ALD/KET含量均较低,主要是因为羰基氧的电负性很强,在锐钛型TiO2的光催化作用下被捕获并附着在光生空穴上,空穴将其转化为水或碳氧化物,进而除去产物中氧[22]。

表5 不同催化剂催化精制生物油的产物组成Table 5 Components of refined bio-oils catalyzed with different catalysts
RB(3)中烃类化合物总含量增加,MAHs显著增加,PAHs稍有增加,而LAHs明显减少;各类含氧化合物含量均明显降低。主要原因有2点:一是中间价态钛元素消耗更多的O自由基,产生更多的H和C自由基参与催化反应,使含氧化合物减少、烃类增加;二是B/L酸量比降低,即L酸中心相对数量升高,促进环烷烃脱氢生成芳环。
RB(4)的烃类化合物总含量略有增加,并以LAHs增加为主,原因在于改性后的催化剂上具有较强的裂解脱氢作用的L酸中心显著增加、但具有成环作用的B酸中心减少;含氧有机物中FUR、ALC和ALD/KET含量有不同程度降低,PHE和EST/ETH含量则明显升高,表明Ti4H-5的脱氧催化能力有限,部分含氧有机物转化并未形成烃类,而是转化了其他含氧有机物。
因此,以TiCl3改性的催化剂Ti3H-5对烃类化合物的选择性最强,对含氧有机物的转化能力最好。
对精制生物油中烃的碳数分布进行分析,结果如表6所示。以汽油(C4~C12)和柴油(C10~C22)的碳数分布为分界依据,将精制生物油中烃化合物的碳数分布划分为C4~C、C10~C12和C13~C22等3个区域。精制生物油中烃碳数均在C7~C19范围内,符合燃料的碳数要求。由表6可知,与RB(0)相比,RB(R)碳数分布变化不大;RB(A)中C4~C9烃明显增加,C4~C12烃的质量分数为47.34%,可作为汽油添加剂或替代组分;而RB(3)中C10以上的烃显著增加,C10~C22烃质量分数达76.42%,得益于芳香烃含量的大幅增加,可作为柴油添加剂或替代组分;RB(4)中3个区域的烃质量分数相对均衡,说明Ti4H-5对芳香烃的选择性降低,而对LAHs烃选择性升高。

表6 烃类化合物的碳数分布Table 6 Carbon atom distribution of hydrocarbonsin bio-oil products
因此,锐钛型TiO2改性的催化剂TiAH-5催化生物油提质,可以得到较高产率的汽油添加剂或替代组分;以TiCl3改性的催化剂Ti3H-5催化生物油提质,可以得到较高产率的柴油添加剂或替代组分。
2.4 改性催化剂抗结焦性能分析
2.4.1 TG-DTG分析
反应后催化剂的TG和DTG曲线如图5所示。由图5(a) TG曲线可知:使用后催化剂在低于 250 ℃ 的质量损失主要为催化剂上吸附的水分和轻质小分子化合物;250~700 ℃内的质量损失由催化剂上的焦炭氧化分解引起。对DTG曲线进行Gaussian分峰拟合,计算得到HZSM-5、TiRH-5、TiAH-5、Ti3H-5和Ti4H-5的总结焦量依次为7.93%、4.56%、2.81%、1.76%和6.29%,因此,催化剂稳定性顺序由高到低依次为Ti3H-5、TiAH-5、TiRH-5、Ti4H-5、HZSM-5。
一般而言,生物油催化提质后催化剂上会产生2种类型的焦炭:低温下结焦的含氧型焦炭和高温下结焦的纯碳型焦炭。含氧型焦炭多为丝状,多分布于催化剂表面,而纯碳型焦炭无固定形状,多位于催化剂孔道内[24]。对于Ti3H-5,由于中间价态的钛与CPD之间的相互作用,使含氧型焦炭难于在其上结焦,因此反应后Ti3H-5上的焦炭为纯碳型焦炭,分解温度相对较高。对于TiAH-5,由于锐钛型TiO2的光催化作用有利于羰基的转化和去除,减少了含氧型焦炭的生成;同时,锐钛型TiO2改性使催化剂的B/L酸量比升高,倾向于保留氢元素,使高氢/碳比烃类增加,减少了纯碳型焦炭,因此反应后TiAH-5上的焦炭较少。含氧型焦炭分解温度相对偏低,而纯碳型焦炭分解温度偏高[12]。对于HZSM-5、TiRH-5和Ti4H-5,反应后焦炭主要由低温含氧型焦炭和少量高温纯碳型焦炭组成[25]。
2.4.2 TEM分析
反应后催化剂的透射电镜照片如图6所示。由图6可见,反应后HZSM-5结焦量较高而使催化剂透明度较低,其表面明显附着丝状含氧型焦炭。反应后TiRH-5和Ti4H-5的透明度与HZSM-5接近,说明催化剂表面焦炭含量较高。TiRH-5上未观察到明显的丝状含氧型焦炭,而Ti4H-5表面观察到明显丝状含氧型焦炭,说明常规TiO2与CPD之间缺乏相互作用。锐钛型TiO2的光催化作用使TiAH-5结焦量下降,使TiAH-5颗粒上部分区域的透明度提高。对于反应后Ti3H-5,只有少量焦炭

图5 反应后催化剂的TG和DTG曲线Fig.5 TG and DTG profiles of catalysts after reaction(a) TG; (b) DTG

图6 反应后催化剂的透射电镜照片Fig.6 TEM images of different catalysts after reaction(a) HZSM-5; (b) TiRH-5; (c) TiAH-5; (d) Ti3H-5; (e) Ti4H-5
点缀于催化剂颗粒上。这是因为中间价态钛元素与CPD的相互作用,使钛处于“氧化-还原”的动平衡状态,提升自由基反应效率,使O自由基增多,有利于分解焦炭前驱物,因此Ti3H-5上结焦较少。
3 结 论
以锐钛型TiO2改性的TiAH-5耦合CPD可以提升精制生物油产率至最高值14.57%,但对高位热值的提升作用不是最显著,精制生物油中 C4~C12烃质量分数为47.34%,较适合制成汽油添加剂或替代组分。
以TiCl3改性的Ti3H-5耦合CPD对生物油的催化提质性能最优,精制生物油产率和HHV分别达到14.22%和36.47 MJ/kg,烃质量分数达到了80.78%,其中C10~C22烃质量分数达76.42%,适合用作柴油添加剂或替代组分。TiCl3改性引入的中间价态钛元素与CPD相互作用使Ti3H-5结焦量最低,稳定性最好。
以金红石型TiO2改性催化剂TiRH-5性能变差。负载常规TiO2改性催化剂Ti4H-5酸性增强,但与CPD无协同作用,催化剂性能变化不明显。

