氢还原处理棒状纳米CeO2光催化特性研究
夏雪雯 李军旗 陈朝轶 兰苑培 毛锡嵩 柏富生 王咪艳
摘 要:采用水热法制备棒状纳米CeO2并研究氢气还原处理对其能带结构及亚甲基蓝光催化降解率的影响。研究结果显示:在600 ℃氢气气氛下,因Ce4+ → Ce3+转化,棒状纳米CeO2的失重率较空气气氛下高;氢气还原后,棒状纳米CeO2的漫反射光谱出现蓝移,未焙烧及在600 ℃空气和氢气气氛焙烧后的棒状纳米CeO2的能带间隙分别为2.882 eV、3.019 eV和3.260 eV;氫气还原后,棒状纳米CeO2对亚甲基蓝的光催化降解率从61.16 %提高至90.09 %,反应速率常数提高至0.015 72 min-1。采用氢还原处理虽使棒状纳米CeO2的带隙变宽,但其光催化降解率有明显提升。
关键词:棒状CeO2;氢气还原;能带结构;光催化性能
中图分类号:O614.332;O643
文献标识码: A
CeO2因其优异的氧化还原能力(Ce4+→ Ce3+)、化学稳定性和无毒性成为备受关注的光催化材料[1]。为进一步提升CeO2的光催化性能,研究人员主要采用的方法有掺杂金属/非金属离子[2]和复合其他半导体材料[3]等。
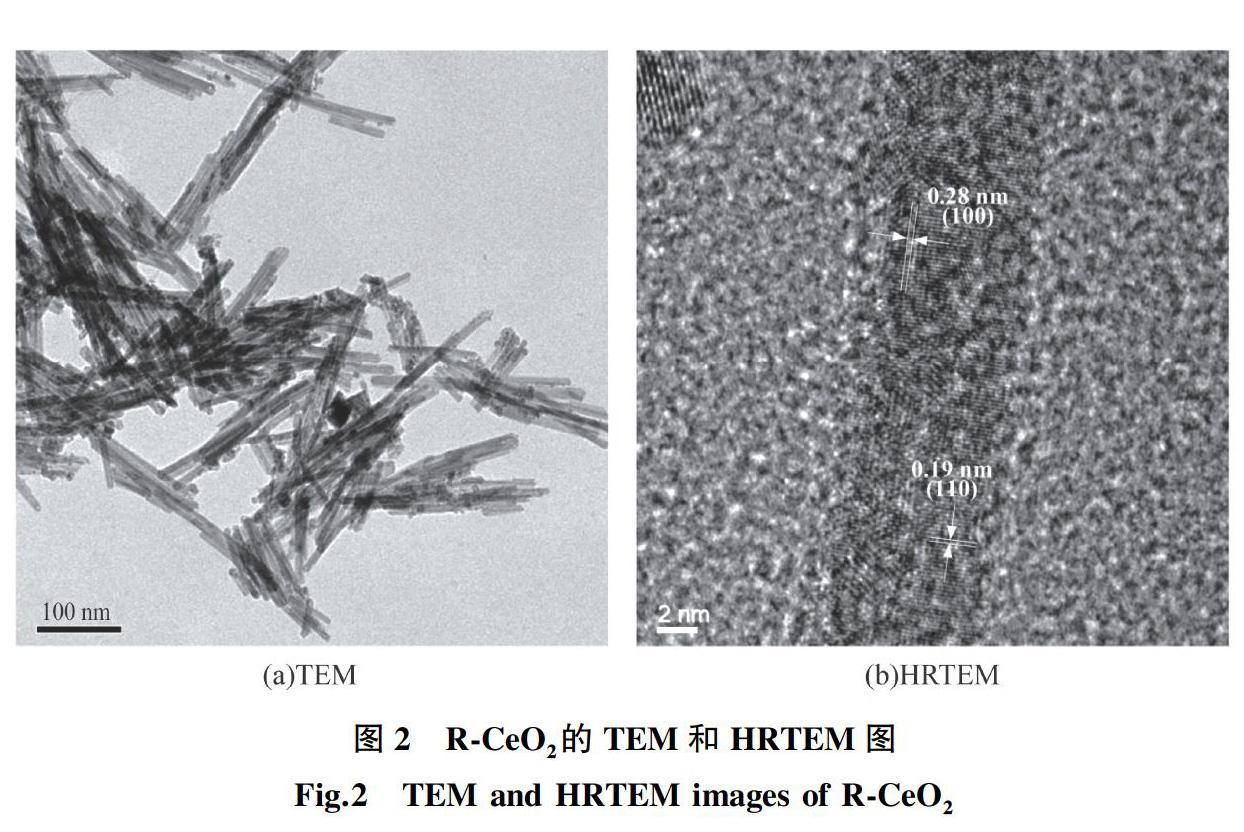
CeO2的形貌会影响其光催化性能[4]。CeO2晶体主要暴露(111)、(100)和(110)晶面,各晶面的催化活性不同,其中(111)<(100)<(110)[1-4]。棒状纳米CeO2因暴露(110)和(100)晶面而受到广泛关注[5]。此外,CeO2晶格中产生的Ce3+或形成的氧空位亦可提升其光催化性能[6]。可见,制备晶格中存在Ce3+或氧空位的棒状纳米CeO2有提升CeO2光催化性能的潜力。在CeO2晶格中引入Ce3+的途径主要包括高温退火[7]、X-射线照射[8]、Ar+轰击[9]和表面刻蚀[10]等。有报道[11-12]称采用中低温H2处理可使CeO2表面还原生成Ce3+,但目前鲜有H2还原对棒状纳米CeO2光催化性能影响的研究。
因此,本文采用水热法制备棒状纳米CeO2,通过热重曲线分析在不同气氛(空气/氢气)中棒状纳米CeO2的质量变化和Ce4+→Ce3+转化,并以此为依据在不同气氛下对棒状纳米CeO2进行焙烧处理。结合紫外-可见漫反射光谱和光催化降解亚甲基蓝溶液实验,研究空气及氢气气氛焙烧对棒状纳米CeO2能带结构及其光催化特性的影响。
1 实验
1.1 棒状纳米CeO2制备与焙烧处理
所用实验原料六水合硝酸铈(Ce(NO3)3·6H2O,99.95 %)和氢氧化钠(NaOH,99.9 %)均购置于阿拉丁公司(上海)。
水热法制备棒状纳米CeO2的方法[13]具体如下:将35 mL NaOH溶液(6 mol/L)缓慢滴入溶有0.868 g Ce(NO3)3·6H2O的5 mL水溶液后搅拌30 min;将形成的乳白色悬浊液转移至50 mL聚四氟乙烯内衬的不锈钢高压反应釜中,在100 ℃下反应24 h后取出并冷却至室温;对得到的淡紫色沉淀物用去离子水和无水乙醇交替洗涤、超声、过滤数次,后在60 ℃下干燥24 h,最终得到淡黄色CeO2粉末(R-CeO2)。
将铺于氧化铝瓷舟中的R-CeO2置于管式炉(合肥科晶gsl-1600x)内,以10 ℃/min升至一定温度,分别在空气和氢气气氛下焙烧2 h。其中,氢
气(高纯氢,99.999 %)流量为400 mL/min,通入氢气前反复将炉管抽真空并以氩气排气。焙烧后待炉温降至150 ℃时,关闭氢气并通入氩气直至室温,得到R-CeO2-H2;将管式炉两端法兰打开与大气相通,空气气氛下焙烧得到R-CeO2-Air。
1.2 材料表征和光学性能分析
室温下,使用Rigaku D/Max-2200 V X射线衍射仪对样品进行物相分析,采用Cu靶Kα辐射(λ=0.154 06 nm),扫描角度范围为5~90°,扫描速度为0.02 (°)/s,获得X射线衍射(X-ray diffraction,XRD)图谱。采用∑SIGA扫描电子显微镜(scanning electron microscope,SEM)拍摄SEM图像,采用Tennai G2 F20透射电子显微镜(transmission electron microscope,TEM)拍摄TEM图像和高分辨率透射电子显微镜(high resolution transmission electron microscope,HRTEM)图像,以观察微粒的形貌和尺寸。空气和氢气气氛下,采用Mettler TGA/SDTA 851e进行R-CeO2的热重分析测试,温度测试范围为室温至1 000 ℃,升温速率为10 ℃/min。采用紫外-可见分光光度计(PE lambda 750S)测试紫外-可见漫反射光谱,测试范围为200~800 nm,并以BaSO4作为参比。
以亚甲基蓝(methylene blue,MB)溶液的降解率评价催化剂的光催化性能;采用250 W氙灯(北京泊菲莱 PLS-SXE300)为测试光源,发射波谱范围为190~1 100 nm。催化性能测试步骤如下:将20 mg样品分散于80 mL MB溶液(10 mg/L)中;在光反应前,将其置于黑暗环境下搅拌30 min,使催化剂和MB溶液达到吸附-解吸平衡;随后,在氙灯光源下反应2 h,每30 min取5 mL悬浊液离心并收集上清液,用分光光度计(VIS-7220N)在664 nm下测定不同时刻其对应浓度。
2 结果与讨论
2.1 物相及形貌分析
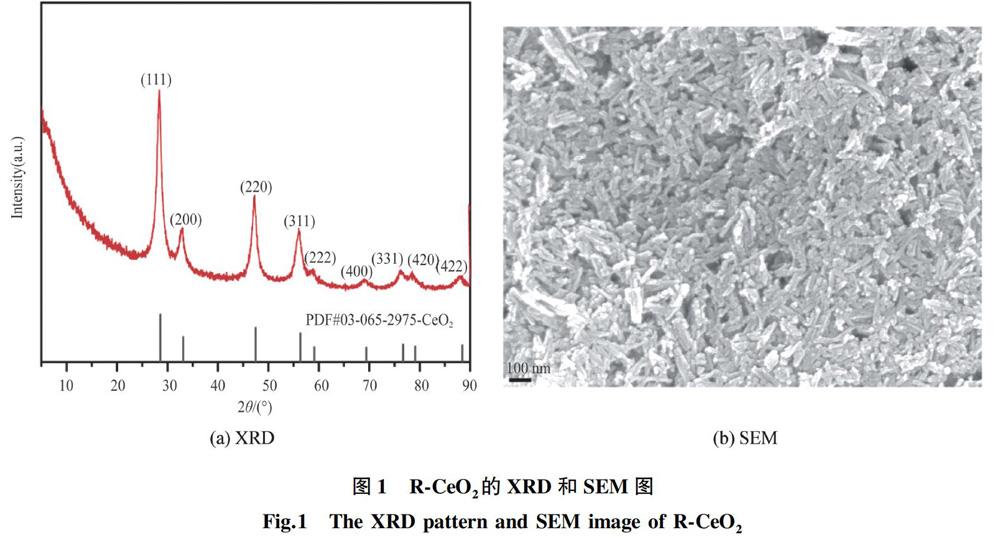
图1是R-CeO2的XRD和SEM图。由图1(a)可知:R-CeO2的衍射图谱具有典型CeO2晶体特征[14],其具有面心立方萤石结构,属于Fm3-m空间群;主要衍射峰所在位置为28.534°,33.105°,47.376°,59.059°,分别对应CeO2晶面(111),(200),(220)和(311)。通过Rietveld精修得到R-CeO2的晶格常数为0.542 4 nm(拟合值为1.070 3),比稳定化学计量CeO2的晶格常数(0.541 1 nm)[1]大。这可能是因为R-CeO2未经焙烧,微粒中存在少部分未反应的Ce(OH)4。由图1(b)可知:制备得到的R-CeO2具有均匀棒状结构,其长约为100 nm,宽约为10 nm。
2.2 不同气氛热稳定性分析及焙烧温度确定
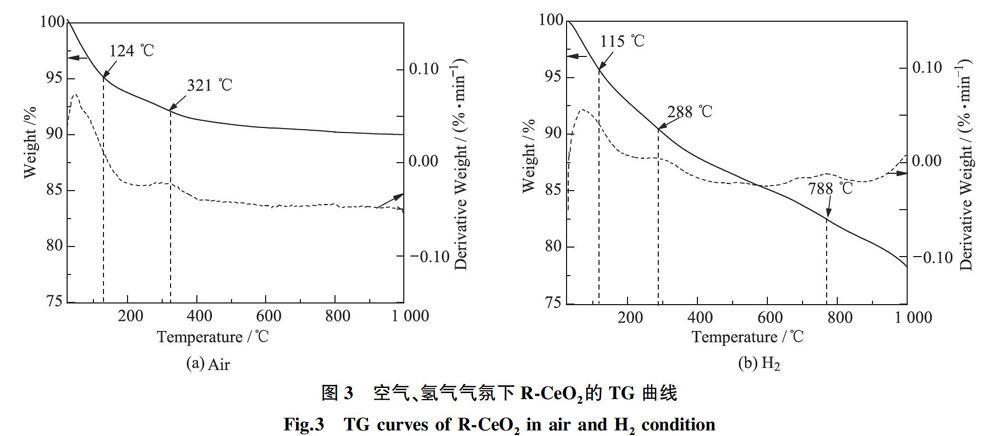
图3为空气和氢气气氛下R-CeO2的热重(thermogravimetry,TG)曲线,分别对各曲线进行微分处理,利用微分热重法提高TG的分辨率。图3(a)显示:在空气气氛下,随着温度的升高,R-CeO2的质量变化过程可分为3个阶段。第一阶段应为自由水的脱除,温度范围为室温至124 ℃,因R-CeO2样品疏松,含水量较高,其失重率约为5.65 %;温度>124~321 ℃为第二阶段,R-CeO2的失重率约为3.212 %,此过程应为少部分未反应的Ce(OH)4发生分解;温度>321 ℃为第三阶段,此时R-CeO2的质量变化较为稳定,并逐渐变成稳定的化学计量CeO2。
从表1和图5可知:R-CeO2-H2在120 min时使MB溶液降解了90.09 %,反应速率常数达到0.015 72 min-1;相比于在空气中焙烧的R-CeO2-Air,氢气还原处理使得棒状CeO2的光催化性能显著提高。未焙烧的R-CeO2的光催化性能较差,这可能是R-CeO2未经焙烧,在光反应过程中微粒团聚,使其接触MB溶液的有效面积减小导致。
CeO2的光催化性能受到比表面积、尺寸、形貌、能带间隙、光生载流子迁移/复合速率和降解溶液与催化剂反应产生的活性离子、自由基等因素的影响。其中,通过窄化CeO2能带结构和提高光生载流子迁移效率,使CeO2对紫外光和可见光均敏感,能显著提升CeO2光催化活性[24]。当催化剂受到大于其能带能量的光照后,价带电子受激发跃迁到导带,在价带留下空穴。产生的电子和空穴在扩散作用下分别迁移至催化剂表面。
氧空位的出现(Ce4+→Ce3+)会促进H2O和O2的吸附,并作为电子陷阱捕获光生载流子,然后转变为具有强氧化性和还原性的超氧自由基和羟基自由基以光催化降解有机物质[25]。YOUNIS等[26]报道称富Ce3+的CeO2可有效提高光生载流子迁移效率并降低光生电子-空穴的复合率,显著提高其光催化效率。因此,采用氢气还原棒状纳米CeO2,可使CeO2表面产生较大浓度Ce3+,在提升催化材料吸附效率的同时,提高CeO2光生载流子的迁移速率并减慢电子和空穴的复合效率。虽然氢气还原处理后棒状纳米CeO2的能带间隙变宽,但其光催化降解效率仍有显著提升。
3 结论
采用水热法制备的棒状纳米CeO2在600 ℃氢气气氛下易被还原;600 ℃氢气气氛下焙烧2 h后,棒状纳米CeO2的能带间隙增至3.260 eV,较未焙烧或相同温度空气气氛下焙烧的CeO2的能带间隙宽,但其对亚甲基蓝的光催化降解效率显著提升,为90.09%,且反應速率常数较空气条件下焙烧的样品提高了97.5%。
参考文献:
[1]XIE S L, WANG Z L, CHENG F L, et al. Ceria and ceria-based nanostructured materials for photoenergy applications[J]. Nano Energy, 2017, 34: 313-337.
[2]MA R, ZHANG S, WEN T, et al. A critical review on visible-light-response CeO2-based photocatalysts with enhanced photooxidation of organic pollutants[J]. Catalysis Today, 2019, 335: 20-30.
[3]ARUL N S, MANGALARAJ D, KIM T W. Photocatalytic degradation mechanisms of CeO2/Tb2O3 nanotubes[J]. Applied Surface Science, 2015, 349: 459-464.
[4]JIANG D, WANG W, ZHANG L, et al. Insights into the surface-defect dependence ofphotoreactivity over CeO2 nanocrystals with well-defined crystal facets[J]. ACS Catalysis, 2015, 5(8): 4851-4858.
[5]LIU B, LI C M, ZHANG G Q, et al. Oxygen vacancy promoting dimethyl carbonate synthesis from CO2 and methanol over Zr-doped CeO2 nanorods[J]. ACS Catalysis, 2018, 8(11): 10446-10456.
[6]YUN S, XU B, ZHANG Q T, et al. Development of the visible-light response of CeO2-x with a high Ce3+ content and its photocatalytic properties[J]. Chem Cat Chem, 2018, 10(6): 1267-1271.
[7]PANLENER R, BLUMENTHAL R, GARNIER J. A thermodynamic study of nonstoichiometric ceriumdioxide[J]. Journal of Physics Chemistry of Solids, 1975, 36(11): 1213-1222.
[8]QIU L M, LIU F, ZHAO L Z, et al. Comparative XPS study of surface reduction for nanocrystalline and microcrystalline ceria powder[J]. Applied Surface Science, 2006, 252(14): 4931-4935.
[9]GONZLEZ-ELIPE A, FERNANDEZ A, HOLGADO J, et al. Mixing effects in CeO2/TiO2 and CeO2/SiO2 systems submitted to Ar+ sputtering[J]. Journal of Vacuum Science & Technology A-vacuum Surfaces and Films, 1993, 11(1): 58-65.
[10]GAO W, ZHANG Z Y, LI J, et al. Surface engineering on CeO2 nanorods by chemical redox etching and their enhanced catalytic activity for CO oxidation[J]. Nanoscale, 2015, 7(27): 11686-11691.
[11]BRAUER G, GINGERICH K, HOLTSCHMIDT U.ber die oxyde des cers—IV: die sauerstoffzersetzungdrucke im system der ceroxyde[J]. Journal of Inorganic Nuclear Chemistry, 1960, 16(1/2): 77-86.
[12]兰苑培. 纳米二氧化铈颗粒的制备及氧空位对其性能的影响研究[D]. 重庆: 重庆大学, 2017.
[13]MAI H X, SUN L D, ZHANG Y W, et al. Shape-selective synthesis and sxygen storage behavior of ceria nanopolyhedra, nanorods and nanocubes[J]. Journal of Physical Chemistry B, 2005, 109(51): 24380-24385.
[14]ONN T M, MONAI M, DAI S, et al. High-surface-area, iron-oxide films prepared by atomic layer deposition on γ-Al2O3[J]. Applied Catalysis A: General, 2017, 534: 70-77.
[15]PERRICHON V, LAACHIR A, BERGERET G R, et al. Reduction ofcerias with different textures by hydrogen and their reoxidation by oxygen[J]. Journal of the Chemical Society Faraday Transactions, 1994, 90(5): 773.
[16]BINET C, BADRI A, LAVALLEY J C. A spectroscopic characterization of the reduction of ceria from electronic transitions of intrinsic point defects[J]. The Journal of Physical Chemistry B, 1994, 98(25): 6392-6398.
[17]BRUCE L A, HOANG M, HUGHES A E, et al. Surface area control during the synthesis and reduction of high area ceria catalyst supports[J]. J Applied Catalysis A: General, 1996, 134(2): 351-362.
[18]WANG J, ZHU H, QIN Z, et al.Pd/CeO2-TiO2 catalyst for CO oxidation at low temperature: a TPR study with H2 and CO as reducing agents[J]. Journal of Catalysis, 2004, 225(2): 267-277.
[19]LEE Y, HE G, AKEY A J, et al. Ramananalysis of mode softening in nanoparticle CeO2-δ and Au-CeO2-δ during CO oxidation[J]. Journal of the American Chemical Society, 2011, 133(33): 12952-12955.
[20]ANSARI S A, KHAN M M, ANSARI M O, et al. Band gap engineering of CeO2 nanostructure using an electrochemically active biofilm for visible light applications[J]. Rsc Advances, 2014, 4(32): 16782-16791.
[21]XIA X W, LAN Y P, LI J Q, et al. Facile synthesis of nanoceria by a molten hydroxide method and its photocatalytic properties[J]. Journal of Rare Earths, 2019, 38(9): 951-960.
[22]MURALI A, LAN Y P, SOHN H Y. Effect of oxygen vacancies in non-stoichiometric ceria on its photocatalytic properties[J]. Nano-Structures & Nano-Objects, 2019, 18: 100257.1-100257.13.
[23]LIU B, ZHAO X J, TERASHIMA C, et al. Thermodynamic and kinetic analysis of heterogeneous photocatalysis for semiconductor systems[J]. Physical Chemistry Chemical Physics, 2014, 16: 8751-8760.
[24]TAMBAT S, UMALE S, SONTAKKE S. Photocatalytic degradation ofmilling yellow dye using sol-gel synthesized CeO2[J]. Materials Research Bulletin, 2016, 76: 466-472.
[25]YANG H, XU B, YUAN S, et al. Synthesis of Y-doped CeO2/PCN nanocomposited photocatalyst with promoted photoredox performance[J]. Applied Catalysis B Environmental, 2018, 243: 513-521.
[26]YOUNIS A, CHU D, KANETI Y V, et al. Tuning the surface oxygen concentration of {111} surrounded ceria nanocrystals for enhanced photocatalytic activities[J]. Nanoscale, 2016, 8(1): 378-387.
(責任编辑:周晓南)

