以猪胆囊为原料提取胆红素
顾文杰,朱 旗,舒春鸽,李 超,张 宇,薛洪宝,,高 敏,刘志祥
(1.蚌埠医学院公共基础学院,安徽蚌埠233030;2.安徽宏业药业有限公司生产技术部,安徽蚌埠233045)
中医药典籍《中华本草》曰:猪苦胆自然阴干,阴阳瓦微火焙干,研末冲服,具有清热、润燥、解毒以及主热病燥渴、大便秘结、咳嗽、哮喘、目赤、目翳、泄痢、黄疸、喉痹、聤耳、痈疽疔疮、鼠瘘、湿疹、头癣的功效。《本草纲目》《本草汇言》也有类似记载。胆色素为胆汁中的色素总称,包括胆红素和胆绿素,也是胆结石的主要成分,其化学结构见图1[1]。本实验以猪胆囊为原料提取胆红素。
胆红素(Bilirubin)作为猪胆囊中的主要成分,其分子是由四个吡咯环通过亚甲基和次甲基连在一起的开链所组成的。血红蛋白的原卟啉经氧化使α-次甲基键断开,形成胆绿素,再经还原为胆色素的其他成分。胆色素可以分为四类,即胆色烷、次甲胆色素、二次甲胆色素和三次甲胆色素,它们分别含有0、1、2 和3 个次甲桥。除胆色烷无色外,其他皆有颜色。胆红素是二次甲胆色素,胆绿素为三次甲胆色素,图1可反映其结构。
胆红素为橙色至暗红棕色的粉末或结晶体[2-3],加热时逐渐变黑但不熔融。0.001%的氯仿溶液,在波长400~490 nm 处有选择性吸收,最大吸收波长在449~451 nm 处。胆红素具备多种药理作用,是制造人工牛黄的主要原料,具有抗氧剂以及有效的过氧化氢基清除剂的功能,保护细胞膜脂质免于活性基的氧化作用。胆红素为干燥固体时较稳定,在氯仿溶液中避光保存也较稳定,在碱溶液中或遇Fe3+等极不稳定,很容易被氧化。
胆红素的主要来源及提取方法包括以下部分:从人的胆汁中提取胆红素的直快法,因涉及到伦理道德方面,不为人类社会所允许;高分子树脂型胆红素常温制取工艺方法,目前技术尚不成熟;狗、棕熊、活猪体等生物体引流提取胆红素的方法涉及到伤害野生动物方面,不为人类社会所允许;利用人的废胆结石提取胆红素的方法,由于利用人体病变组织,有感染其他病毒、细菌等风险,且涉及到伦理道德方面,亦不能推广;酶法合成胆红素,目前技术尚不成熟;猪、牛等家畜胆汁提取胆红素的生产工艺是目前的主要来源途径,且成本低廉[4-5];此外,其他技术如双管体内合成胆红素的技术、獭狸胆红素和獭狸血红素及其制取技术、血液分解法生产胆红素新技术等受到成本较高、技术不成熟等因素限制,尚不能推广。
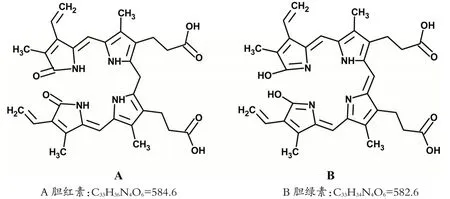
图1 胆色素化学结构Fig.1 Chemical structure of bile pigment
胆红素不溶于水,溶于苯、氯仿、氯苯、二硫化碳,微溶于乙醇、乙醚等有机溶剂,且分子中有两个丙酸基侧链,呈弱酸性,能与碱土金属离子如Ca2+生成不溶性盐(习惯上称胆钙盐)。这种不溶性盐与强酸如盐酸反应,可置换出胆红素,这是本实验的主要提取方法。
1 材料与方法
1.1 实验材料
仪器设备:DF-101S 型集热式恒温加热磁力搅拌器,河南省巩义市予华仪器有限责任公司;250 mL电热套,上海越众仪器设备有限公司;水浴系列JC-ZFRE5000 型旋转蒸发仪,山东省青岛聚创环保集团有限公司;SHZ-D(Ⅲ)型循环水式多用真空泵,河南省郑州科丰仪器设备有限公司。
试剂材料:猪胆囊,新采集或冰箱冷冻存放,安徽省某肉类联合加工厂有限公司;氧化钙,分析纯,天津市大茂化学试剂厂;亚硫酸氢钠,分析纯,天津市大茂化学试剂厂;浓盐酸,优级纯,天津市大茂化学试剂厂;95%的乙醇,分析纯,天津市大茂化学试剂厂;氯仿,分析纯,河南祥德商贸有限公司;乙醚,分析纯,天津市大茂化学试剂厂;纯化水,电导率≥18 Ω。
1.2 工艺路线
提取工艺路线参照某公司原有猪胰脏来源胆红素原料药提取工艺基础上进行优化,见图2。
1.3 提取步骤
(1)制钙盐
取新鲜猪胆汁200 mL,加入3~4倍量的澄清饱和石灰水搅拌均匀。加热至沸,撇取浮于液面的橙红色胆钙盐(内含胆色素钙盐),趁热压干[6-7]。
(2)酸化
于钙盐中加入适量水,捣成糊状,过65 目筛,加入1%的亚硫酸氢钠[8]。在搅拌下缓缓滴加浓盐酸溶液,至pH 值为1~2,静置30 min。用双层纱布沥去酸水,得泥状物。
(3)乙醇处理
泥状物中加入95%的乙醇捣成稀糊状,再加入约20 g 95%的乙醇和0.01 g亚硫酸氢钠水溶液,充分搅拌均匀。乙醇液的pH 值约在3.0~3.5。于约3℃静置沉淀18 h。去除上层乙醇。于下层中加入45℃~50℃温水,静置分层,富集胆红素的悬浮物即浮于液面[9],去除下层废水。
(4)提取
于悬浮物中加入氯仿约30 g,回流提取2 h。将提取液置于分液漏斗中分层,下层氯仿液过滤后,于常压下蒸发出氯仿,尽量蒸干。于残余物中加入适量95%乙醇,继续蒸发至馏出乙醇中几乎不带氯仿气味。过滤分取胆红素,在过滤器上用温热的乙醇和乙醚洗涤,抽干,即得成品胆红素[10-11]。
2 结果与讨论
实验产物呈橙色或淡黄色粉末,不溶于水,可溶于氯仿等有机溶剂,从物理化学性质方面判断与胆红素性质相同。
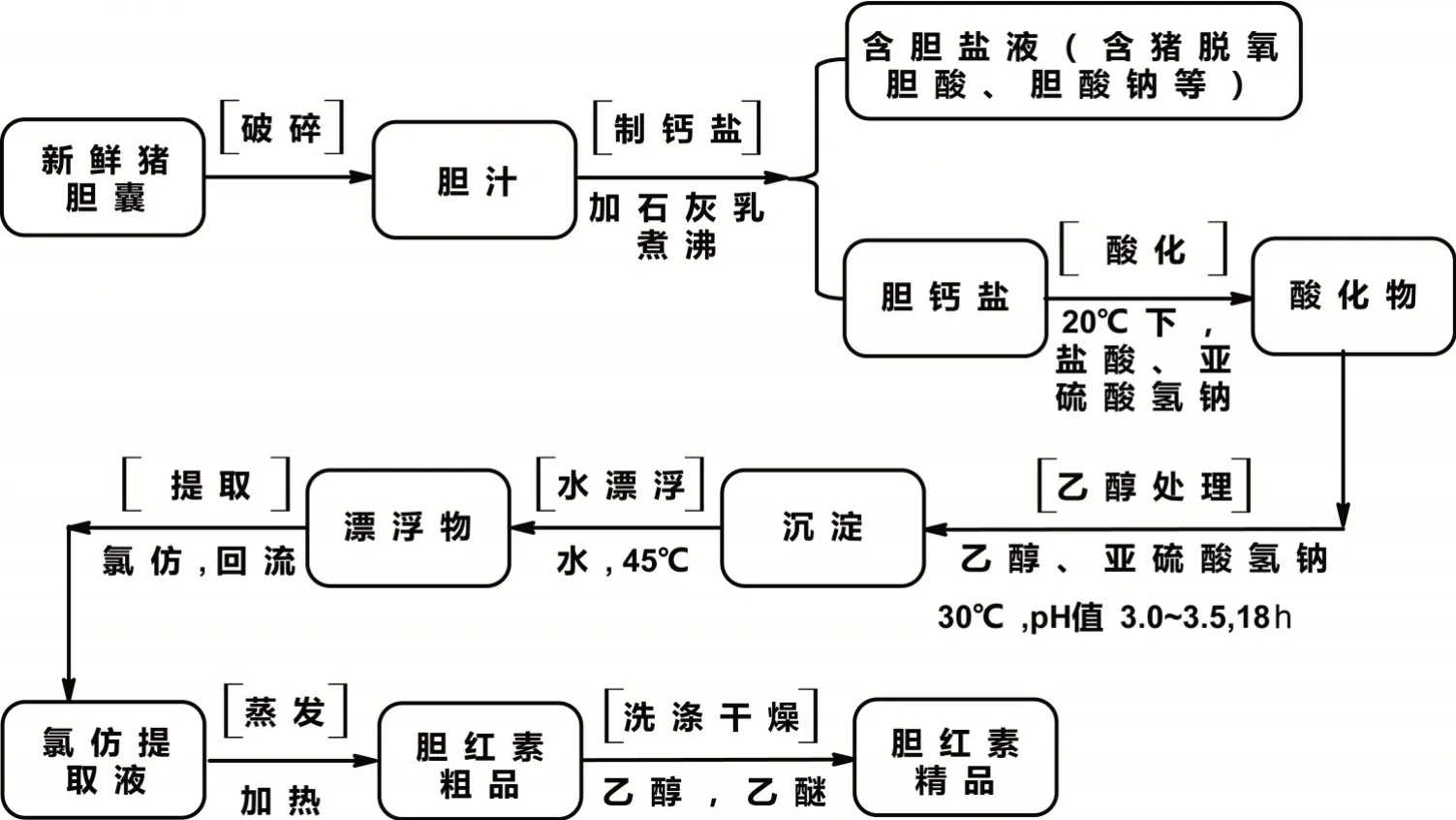
图2 猪胰脏来源胆红素原料药提取工艺路线框图Fig.2 Extraction process roadmap of bilirubin from pig pancreas
胆红素和重氮化的对-氨基苯磺酸反应,产生偶氮染料。这种偶氮染料在强酸中呈蓝紫色,在pH 值2.0~5.5之间呈红色,在pH值5.5以上则呈绿色。
(1)重氮化试剂的配制
溶液甲:对-氨基苯磺酸10 g,加浓盐酸15 mL,水985 mL。
溶液乙:0.5%亚硝酸钠溶液。
临用时取10 mL甲溶液加0.3 mL乙溶液,混匀。
(2)胆红素标准曲线的绘制[11-12]
精密称取胆红素标准品10.0 mg,用氯仿溶解后,转移至100 mL棕色容量瓶中,加氯仿至刻度。量取氯仿溶液10 mL,置于50 mL容量瓶中,加乙醇至刻度,此即为标准品溶液,标准溶液胆红素为0.000 02 g/mL。精密量取标准品溶液0 mL、1 mL、2 mL、3 mL、4 mL、5 mL于带塞比色管中,分别加入乙醇9 mL、8 mL、7 mL、6 mL、5 mL、4 mL,使总体积均为9 mL,再加入重氮化试剂1 mL,混匀。于20℃暗处静置60 min(或30℃暗处静置30 min)后,于波长520 nm处测定吸收度。以吸收度为纵坐标,以各管中胆红素的量为横坐标,绘制标准曲线图,见图3。线性相关系数为R2=0.993 99,线性方程:Y=1.020±0.035 46×X+0.028±0.013 81,检测下限:1.38×10-7g/mL。

图3 胆红素含量测定标准曲线Fig.3 Standard curve of bilirubin content determination
(3)样品测定[13]
另精密称取供试品25.0 mg,用氯仿溶解后,转移至250 mL容量瓶中,边加氯仿边振摇,使溶解完全并加至刻度。量取氯仿溶液10 mL,置于50 mL 容量瓶中,加乙醇至刻度,摇匀。精密量取5 mL于带塞比色管中,加乙醇4 mL,使总体积为9 mL,混匀,再加入重氮化试剂1.0 mL。与标准品在相同条件下显色后,于波长520 nm处测定吸收度。可由标准曲线对应的线性方程直接计算出供试品的含量。
3 结论
经多次平行试验知,猪胆囊提取之前要保证新鲜,以免有效成分损失,提取过程中不能有铁器接触猪胆囊,以防产品氧化、变性,提取过程中使用的澄清石灰水在空气中极容易变质,使用时需现用现配,浓度过低或杂质过多可能会导致钙盐不能全部漂浮出来,影响最终产品的收率。提取过程产生的强酸、强碱性物质后处理不善可能会对环境造成不利影响[12]。在实验室小试阶段过程中以浓盐酸替代1∶1 的工业级盐酸效果更佳。胆汁液沸腾后要立即趁热过滤,因为胆钙盐的溶解度会随温度的升高而降低。如果温度过低,橙红色的胆钙盐溶解在溶液中,不易析出,导致成品产率较低。回流过程中要注意设备的密闭性,以防氯仿外泄;回流过程中不能完全蒸干,否则会导致产品过热而分解变质,收率明显降低。
通过实验证明,以猪胆囊为原料生产胆红素工艺技术路线可行,为肉类联合加工企业的生产废料——猪胆囊的无公害资源化处理,即以其为原料生产胆红素提供了技术参考。

