乳腺癌患者血清E-cadherin、sE-cadherin 水平与临床分期及化疗疗效的相关性
王 超,舒诚荣,曹爱玲,乐 玲
(咸宁市中心医院,湖北科技学院附属第一医院肿瘤科,咸宁 437100)
乳腺癌(breast cancer,BC)最常见于导管和小叶,从导管发展的癌症被称为导管癌,而从小叶发展的癌症被称为小叶癌[1,2]。此外,还有超过18 种其他亚型的乳腺癌;其中一些癌症,如原位导管癌,是从侵袭前病变发展而来的[3]。其治疗方法根据癌症分期和患者年龄不尽相同,主要包括手术、放疗、化疗、内分泌治疗和靶向治疗;其中手术类型从乳房保留术到乳房切除术各不相同[4]。但这些治疗都需在活组织检测确诊和确定癌症是否已经扩散后实施,尚未有有效的血清指标已表征这种癌症的分期和治疗效果。研究表明,56 %的小叶乳腺癌中上皮细胞钙粘附蛋白(E-cadherin)的CDH1 基因失活,84 %小叶乳腺癌中E- cadherin 表达完全丧失[5,6]。因而本研究旨在探讨E-cadherin 和可溶性上皮细胞钙粘蛋白(sE-Cadherin)在不同临床分期患者中的表达情况,并分析其化疗效果,详述如下。
1 资料与方法
1.1 研究对象收集我院2017 年1 月~2018 年11 月接受治疗的患者资料,纳入标准:确诊为乳腺癌[7],为首次接受治疗,KPS 评分大于60[8];排除标准:合并其他脏器功能不全,患免疫系统疾病,患内分泌疾病,临床治疗不完整。将符合标准的100 例患者纳入研究,根据TNM 分期不同分为Ⅰ期组(n=29)、Ⅱ期组(n=41)和Ⅲ期组(n=30),一般资料见下表1,各组间资料差异不显著(P>0.05)。

表1 患者一般资料
1.2 临床分期根据TNM 分期系统进行,其中T 表示肿瘤体积及周围受累范围情况,T0 至T4 情况逐步加深;N 表示淋巴结受累情况,N0 至N3 受累范围逐渐扩大;M 表示是远处转移情况。M0 表示无远处转移,M1反之。再将患者T、N 和M 分期情况进行汇总,分期从Ⅰ至Ⅳ期不等,如Ⅰ期为T1、N0 和M0,ⅡB 期为T2、N1、M0 或T3、N0、M0。
1.3 血清E-cadherin、sE-cadherin水平检测 在化疗前后检测患者E-cadherin、sE-cadherin 及其他指标水平。取患者清晨(8:00 前)空腹8 小时外周静脉血5 mL,加入抗凝管静置2 小时,后3 000 r/min 离心10 分钟取血清,-20℃保存待测。使用ELISA 法检测其中E-cadherin、sE-cadherin 和HMGB1 水平,按照试剂盒(均购于上海内含子生物)说明中步骤操作。
1.4 化疗及其效果评估
1.4.1 化疗治疗方式全部患者推荐使用蒽环联合紫杉醇(PTX)化疗(EC-P)方式,表柔比星(批准文号:H2012039,依比威药品)90 mg/m2,静脉滴注,21 天为一个周期;上述完成4 周期后,序贯PTX(批准文号:H20059378,海正辉瑞)175 mg/m2,在心电监护下3 hrs 静脉滴注,也为21 天一个周期进行4 个周期;全部方案完成为8 个周期。滴入PTX 之前30 min,给予苯海拉明(批准文号:H41021264,天津药业集团)20 mg,肌肉注射;给予盐酸昂丹司琼(4 mg/片,批准文号:H10960146,宁波天衡药业)2 片,口服。化疗进行7 天后,检测血常规,若血红蛋白大于等于80 g/L、中性粒细胞计数大于等于1.5*109L-1,、血小板大于等于7.5*1010L-1,则继续使用PTX 化疗;若不在上述范围内,改用粒细胞集落刺激因子(G-CSF,新瑞白,批准文号:S20150013,齐鲁制药),待骨髓抑制后继续化疗。
1.4.2 结果判断化疗前后,使用B 超采用最大直径法检查乳腺原发灶大小,病理完全缓解患侧原发肿瘤区无浸润癌细胞,临床完全缓解(CR)检查时肿瘤消失,临床部分缓解(PR)肿瘤最大直径*最大垂直径减少50%以上,病情稳定(SD)肿瘤最大直径*最大垂直径减少少于50 %或增加小于25 %,病情进展(PD)肿瘤最大直径*最大垂直径增加大于等于25 %。将全部患者按照化疗临床效果进行分组,临床完全缓解和部分缓解(CR+PR)一组,病情稳定和病情进展(SD+PD)一组。
1.5 数据分析删除无效数据(信息缺失比例>20%)后导入SPSS 22.0 进行统计分析。计量数据以mean±SD 表示,采用配对t 检验进行组内比较,采用独立样本t 检验进行组间比较;计数资料以n(%)表示,经过半定量化处理后使用χ2或Fisher 精准概率法检验;依据数据是否服从二元正态分布分别采用spearman 或pearson相关分析各监测指标间的相关性。如无特殊说明,显著性水准α=0.05,所有P 值均表示双侧概率。
2 结果
2.1 不同临床分期患者血清E-cadherin、sE-cadherin水平患者血清E-cadherin 水平随着临床分期升高而明显降低(P<0.01),sE-cadherin 和HMGB1 水平则随着临床分期升高而明显升高(P<0.01),见表2。
2.2 血清E-cadherin、sE-cadherin 水平与临床分期相关性血清E-cadherin 水平与临床分期呈负相关,sE-cadherin 水平与临床分期呈正相关(P<0.05),相关系数分别为-0.357 和0.382,见表3。

表2 不同临床分期患者血清E-cadherin、sE-cadherin水平

表3 血清E-cadherin、sE-cadherin水平与临床分期相关性
2.3 血清E-cadherin、sE-cadherin 水平与化疗疗效相关性化疗后,CR+PR 组E-cadherin 水平明显高于化疗前(P<0.01),sE-cadherin 和HMGB1 水平明显低于于化疗前(P<0.01),而SD+PD 组合与化疗前无明显差距(P>0.05)但明显异于CR+PR 组(P<0.01),见表4。
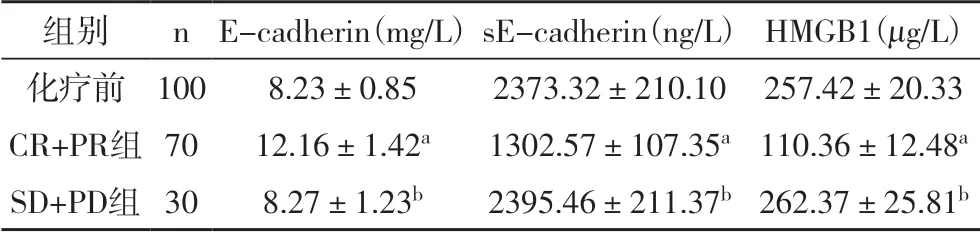
表4 血清E-cadherin、sE-cadherin水平与化疗疗效相关性
2.4 血清E-cadherin、sE-cadherin 水平与化疗疗效相关性血清E-cadherin 水平与化疗疗效呈负相关,sE-cadherin 水平与临床分期呈正相关(P<0.05),相关系数分别为-0.310 和0.326,见表5。

表5 血清E-cadherin、sE-cadherin水平与化疗疗效相关性
3 讨论
在世界范围内,BC 是威胁女性生命安全的主要癌症类型,约占全部病例的四分之一[9,10]。BC 的症状包括乳腺肿块、乳腺形状变化、乳头溢液,或皮肤改变、乳头乳晕异常和腋窝淋巴结肿大等;在疾病远处传播的患者中,可能存在骨痛、淋巴结肿大、呼吸短促或皮肤发黄等现象;但是一些症状,如皮肤浅凹和乳头凹陷,其症状不明显不易及时发现,因而需要更灵敏的指标表征[10,11]。
本研究分别检测不同癌症临床分期患者血清E-cadherin、sE-cadherin 和HMGB1 指标发现,相较于Ⅰ期患者,Ⅲ期组患者血清E-cadherin 水平明显更低,且与临床分期呈负相关。E-cadherin 是一种由肿瘤抑制基因CDH1 编码的钙黏蛋白,CDH1 基因的突变与胃癌,乳腺癌、结肠直肠癌、甲状腺癌和卵巢癌相关;E-cadherin 表达和功能的丧失被认为通过增加增殖、侵袭和/或转移促进癌症的进展。Favaretto 和Kato 等人[12,13]认为,E-cadherin 是上皮癌的生物标志物。报道显示,正常组织中E-cadherin 阳性表达明显高于肿瘤增生组织和癌组织,说明随着组织癌变,其中E-cadherin 表达逐渐减少,与本文血清E-cadherin 水平随着TNM 分期增加而减少的结果一致[14]。
其后我们对比了不同T N M 患者血清中s Ecadherin 和HMGB1 含量,我们发现其二者水平均随着TNM 分期增加而增加,即呈正相关。sE-cadherin 是E-cadherin 的细胞外一游离形式分布的降解片段,微量存在于血清中;近年研究表明,sE-cadherin 在肿瘤患者血清中含量升高,说明其可能在肿瘤发生、发展和扩散中扮演重要角色,与本文研究结果一致[14,15]。而HMGB1 是一种重要的染色质蛋白,由免疫细胞通过无前导分泌途径分泌,作为其细胞因子介质在炎症和损伤机制中起作用;另外巨噬细胞移动抑制因子可以通过激活HMGB1 / TLR4 /NFκB 轴促进乳腺癌转移[16]。因而TNM 分期越高的患者,血清内HMGB1 含量越高。
我们随后将全部接受化疗的患者按照化疗效果进行区分,CR 和PR 作为效果明显的一组,而SD 和PD 作为效果不理想的一组,对比两组血清指标我们发现,血清E-cadherin 水平与化疗疗效呈负相关,sE-cadherin和HMGB1 水平与临床分期呈正相关,这提示化疗效果越好的患者血清E-cadherin 含量越高,sE-cadherin 含量越低,这与其各自在机体内作用结果一致。
虽然本文发现乳腺癌患者血清E-cadherin 和sEcadherin 变化趋势,但由于收集的患者资料时间和完全度问题,未进行化疗后随访,因而未能分析血清指标变化与患者无进展生存期(PFS)、总生存期(OS)和无病生存期(DFS)之间的关系。因而下一步,我们需要对取得联系的患者进行随访,直至其联系丢失或因癌死亡。随后统计随访数据,分析血清E-cadherin 和sE-cadherin是否为影响乳腺癌患者化疗后PFS、OS 和DFS 等指标的危险因素。
综上所述,不同TNM 分期患者血清E-cadherin、sE-cadherin 水平不同,E-cadherin 水平与临床分期呈负相关,sE-cadherin 与临床分期呈正相关;化疗前后检测血清E-cadherin、sE-cadherin 水平可帮助表征乳腺癌预后和复发情况,为临床诊断和治疗提供依据。

