小梁切除术联合人工晶体植入对原发性青光眼患者成功率及功能性滤过泡形成的影响
林水龙,林美英,伍蓝洁
(晋江市医院眼科,晋江 362200)
青光眼是一类以病理性神经凹陷、萎缩和视野缺损为主要特点的眼部疾病,对患者视力损害具有不可逆转性[1]。目前临床多以降眼压为主要目的进行治疗,当药物和激光不能有效控制病情时需采用手术治疗[2]。小梁切除术是治疗青光眼的首选术式,术中通过在手术区球结膜下形成滤过泡,然后被滤过泡周围毛细血管或淋巴管吸收来解除病理引流障碍,从而降低眼压。但小梁切除术后常出现滤过泡瘢痕化、浅前房和巩膜瓣粘连等引发眼压再次升高,导致手术失败[3]。随着对青光眼研究进展,发现晶状体浑浊、增厚也在青光眼发病中起到重要作用。超声乳化人工晶体植入可代替患者原膨胀增厚的晶状体,解除瞳孔阻滞和对前房角挤压,从而降低眼压[4]。本次研究以我院收治的117 例原发性青光眼患者为研究对象,探究小梁切除术联合人工晶体植入对原发性青光眼患者手术成功率和功能性滤泡形成的影响。
1 资料与方法
1.1 一般资料选取2016 年1 月~2019 年1 月我院收治的117 例原发性青光眼患者,纳入标准:(1)患者均确诊为原发性青光眼,参考《我国原发性青光眼诊断和治疗专家共识》[5];(2)年龄18 岁以上;(3)药物和激光无法有效控制病情或患者对药物不耐受无法坚持治疗者;(4)患者知情并签署知情同意书。排除标准:(1)存在眼部手术史;(2)患者为继发性青光眼;(3)存在链球菌疾病、葡萄糖膜炎、自身免疫疾病或糖尿病等;(4)患者为瘢痕体质或对透明质酸钠过敏等;(5)患者无法耐受或后期无法配合随访等。入选患者按照随机数字法分为观察组(59 例64 眼)和对照组(58 例62 眼),观察组男12 例12 眼,女47 例50 眼,年龄(68.4±7.3)岁,64 眼中有开角型19 眼,急性闭角型30 眼,慢性闭角型15 眼;对照组男10 例10 眼,女48 例52 眼,年龄(67.9±7.0)岁,62 眼中有开角型17 眼,急性闭角型29 眼,慢性闭角型16 眼,两组患者一般资料比较无显著差异(P>0.05)。本次研究提交我院医学伦理委员会审核并通过。
1.2 方法所有患者进行眼部状况、血压、心电图、血尿等术前常规检查,手术前3d 给予抗生素及非自体滴眼液点眼,术前30min 以硝酸毛果芸香碱滴眼液缩瞳和卡替洛尔眼液点眼,部分病情较为严重患者可先行前房穿刺术释放部分房水以降低术后并发症。(1)观察组行小梁切除术联合人工晶体植入治疗。丙美卡因眼液表面麻醉后,采用开睑器撑开眼睑,封上直肌牵引线固定眼球,于角膜缘右上方制作长约6mm 的结膜瓣。然后适当暴露准备做巩膜瓣区域,烧灼器适当烧灼止血,做一个约4mm×3mm×半个巩膜厚度的长方形巩膜瓣,以角膜缘为基底向前分离,直至清亮角膜区内1mm。然后于角膜缘12 点位下穿刺进入前房缓慢释放部分房水,注入粘弹剂加深前房、撕囊、注入平衡液行水分离及分层;采用超声乳化仪(美国MTP 公司,MTP Model2000 型)将皮质、晶状体核吸除,植入人工晶状体,在巩膜瓣下切除约1mm×2mm 小梁组织,显微剪刀减去周边虹膜并冲洗,然后采用10-0 尼龙线间缝合切口,检查无漏水后涂上妥布霉素地塞米松眼膏,沙垫覆盖眼部。(2)对照组行常规小梁切除术。丙美卡因眼液点眼麻醉后撑开眼睑,角膜缘右上方制作制作结膜瓣,适当灼烧巩膜表面止血,以角膜缘为基地制作巩膜瓣,并向清亮基底分离1mm,穿刺释放部分房水,加入粘弹剂后撕裂,水分离,切除约1mm×2mm 小梁组织,剪除周边虹膜并冲洗,然后缝合切口,检查无漏水后涂妥布霉素地塞米松眼膏,沙垫覆盖眼部。所有患者术后均给予妥布霉素地塞米松眼液、托吡卡胺眼液局部给药,并根据患者情况酌情增减。
1.3 观察指标和疗效判定于手术前和术后7d、1月、3 月、6 月检测患者眼压、功能性滤泡形成情况,于术前和术后6 个月分别评价最佳矫正视力,于术后6 个月时评价手术成功率及并发症情况。采用国际标准视力表评价患者最佳矫正视力,采用非接触性眼压计检测患者眼压。手术成功标准[6]:(1)完全成功:术后无需抗青光眼药物就能维持眼压正常;(2)部分成功:术后需1~3 种降压药才能维持眼压正常;(3)失败:眼压无法维持正常,需再次进行手术者。手术成功率=(完全成功+部分成功)/总眼数×100%。统计为功能性滤过泡的眼数,滤过泡可分为分为Ⅰ-Ⅳ型[7]:Ⅰ型,隆起呈小囊泡贫血状,Ⅱ型,扁平弥散状,Ⅲ型,发生瘢痕化,Ⅳ型,包囊囊泡型,其中Ⅰ-Ⅱ型为功能性滤过泡。
1.4 统计方法采用SPSS 22.0 统计软件包进行数据分析,符合正态分布计量资料以均数±标准差表示,组间比较采用t 检验;计数资料如最佳矫正视力、功能性滤泡形成、并发症以百分率“%”表示,组间比较采用χ2检验。记P<0.05 为差异有统计学意义。
2 结果
2.1 两组手术成功率比较观察组手术成功率高于对照组,差异具有统计学意义(98.4%vs87.1%,P<0.05),见表1。
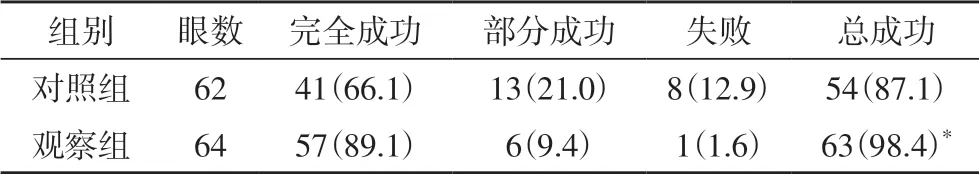
表1 两组手术成功率比较[n(%)]
2.2 手术前后两组视力情况比较术后两组视力较术前均有所改善,最佳矫正视力>0.5 人数较术前明显增加,但组间比较均无显著差异(P>0.05),见表2。
2.3 手术前后两组眼压比较术后7d 时,两组眼压无明显差异(P>0.05),术后1月、3 月、6 月时,观察组眼压低于对照组,差异具有统计学意义(P<0.05),见表3。
2.4 两组功能性滤过泡比较术后7d 时,两组功能性滤过泡无明显差异(P>0.05),术后1月、3 月、6 月时,观察组功能性滤过泡数高于对照组,差异具有统计学意义(P<0.05),见表4。

表2 手术前后两组视力情况比较(n)

表3 术前后两组眼压比较(mmHg)

表4 两组功能性滤过泡比较[n(%)]
2.5 两组术后并发症比较两组术后前房内均未出现明显渗出物,观察组术后前房出血、浅前房、低眼压及恶性青光眼发生率均未高于对照组,且组间比较无显著差异(P>0.05),见表5。

表5 两组术后不良反应及并发症比较[n(%)]
3 讨论
原发性青光眼是眼科的一种常见疾病,是世界第二大致盲眼病。且青光眼发病原因较为复杂,治疗难度较大[8]。青光眼对视力具有不可逆转损伤,因此寻找一种较为有效的治疗方法尤为重要。眼压升高是青光眼对视神经造成损伤的重要原因,目前临床治疗多以降低眼压为目的,如抑制房水生成及促进房水排除进行治疗[9]。其中激光、药物及手术是目前治疗青光眼的主要方法,当激光和药物治疗无法控制病情时,患者需采取手术治疗。小梁切除术是青光眼首选手术,多项研究发现,小梁切除术能通过制作房水引流通道使其自巩膜瓣下引至球结膜下,形成功能性滤过泡从而降低眼压[10-11]。但术后易并发前房浅、眼压低等症,且患者后期常因形成滤过道瘢痕引发房水流出受阻,导致眼压再度升高。随着临床对青光眼研究进展,发现晶状体也在青光眼发病过程中起到重要作用。患者随年龄增长晶状体体积逐渐膨胀,加重前房浅和瞳孔阻滞情况,使房角变窄,引发眼压升高[12]。因此可通过摘除已有晶状体缓解眼前节拥挤状态,同时植入较薄的人工晶状体代替,从而改善眼部压力状态。
本次研究中发现,观察组手术成功率明显高于对照组,且术后1 月、3 月、6 月时,观察组眼压明显低于对照组,提示患者术后眼压控制较好,视神经没有被进一步损伤。原因可能是:(1)通过采用薄的人工晶状体代替患者原本增厚的晶状体,缓解了晶状体引发的瞳孔阻滞和前房角挤压,同时加深了前房深度,开放前房角同时降低了眼压。(2)晶体植入前先采用的超声乳化仪产生的压力和灌注液的冲洗,有利于闭塞的房角开放和虹膜周边平坦,促进房水流出的通畅。同时也能清除房角和小梁网上的色素颗粒和炎性介质脱落,促进小梁网内细胞吞噬功能的加强,增加小梁网通透性,利于房水循环[13]。此外,仪器震荡过程可抑制睫状体的分泌功能,从根本上减少房水的生成,从而降低眼压。眼压过高情况得到改善后,可有效保护患者的视功能,因此术后两组最佳矫正视力较术前明显改善。小梁切除术通过在手术区球结膜下形成滤过泡,然后被滤过泡周围毛细血管或淋巴管吸收来解除病理引流障碍,从而降低眼压。手术成功与否很大程度上取决于术后伤口的愈合和瘢痕形成,而临床实践发现,手术引发的组织创伤可刺激炎症反应和成纤维细胞的增生,造成滤泡瘢痕化,造成引流障碍,引发手术失败。而植入人工晶体后,滤过泡内部能保持一定张力,从而维持结膜下滤过腔的留存,协助滤过泡的形态和功能的留存[14]。已有研究发现,在小梁切除术中联合植入人工晶体可使功能性滤泡数形成数明显增加[15]。我们发现术后1月、3 月、6 月时,观察组功能性滤过泡数明显高于对照组,与相关研究报道一致。而两组术后并发症发生率无显著差异,但观察组在前房出血、浅前房、低眼压及恶性青光眼发生率均未高于对照组,提示小梁切除术联合超声乳化植入人工晶体后对传统手术中并发浅前房、低眼压、脉络膜脱离等长期潜在的感染风险控制较好,减少患者多次手术产生疼痛及手术费用方面的经济负担。
综上所述,小梁切除术联合人工晶体植入治疗原发性青光眼能有效提高手术成功率,促进功能性滤过泡的形成,同时在降低眼压和改善视功能方面具有良好效果,是一种较为安全有效的治疗方法。

