腹腔镜技术在肠梗阻治疗中的应用效果观察
胡爱民,周新红,魏征,易杰明,郑祖祥,曾长江
(长江大学附属仙桃市第一人民医院普外科,湖北 仙桃 433000)
肠梗阻是外科常见的急腹症之一。由于其具有病因复杂、病因诊断困难,且病情发展迅速,死亡率高等特点,常给临床医师对其诊断及治疗带来困惑,在明确病因及保守治疗不佳的条件下,手术成为一种重要的治疗方案。目前,腹腔镜技术已应用于外科的多个领域,但其在肠梗阻治疗中的应用仍饱受争议,肠梗阻仍被列为腹腔镜手术的相对禁忌证[1]。随着腹腔镜技术的成熟,其作为一种新型的微创技术在临床上得到广泛应用,不仅有效地减少了传统开腹手术给病人带来的创伤,而且能够降低术后再粘连的复发率,效果明显[2-3]。笔者于2014年1月至2019年9月间对本院收治的98例肠梗阻手术病人(包括良恶性疾病)进行回顾性对比研究,现报道如下。
资料与方法
一、临床资料
回顾性分析2014年1月至2019年9月长江大学附属仙桃市第一人民医院普外科收治的肠梗阻病人临床资料,按纳入排除标准,共98例手术病人纳入研究,分为腹腔镜组(50例)和开腹组(48例)。纳入标准:①病人术前做好评估,非具备明显急诊开腹指征病人;②术前行相关检查基本明确梗阻原因,包括粘连和肿瘤;③经非手术治疗效果欠佳,但未出现腹腔间隔室综合征(ACS);④腹腔镜手术主刀医生具备熟练腹腔镜操作技术。排除标准:①老年病人合并有心肺、肝肾疾患或功能障碍不能耐受手术者;②具备明显开腹指征,如急性肠梗阻伴有弥散性腹膜炎、既往有因肠梗阻已行2次以上的开腹手术、ACS出现等。本研究经本院伦理委员会批准。
二、术前准备
依据腹部立位平片及临床症状,对于肠梗阻诊断明确的病人,入院后完善全腹部CT平扫+增强、胸片、心电图、血细胞五分类、血型、血生化、凝血功能全套、肿瘤标志物、感染性疾病筛查、尿常规等常规检查,对于老年病人以及合并有高血压、冠心病、慢性肺部疾病病人需完善心肌酶谱、心肌钙蛋白、心脏彩超及血气分析等;通过CT影像对腹腔梗阻原因初步判断、肠管扩张情况、肠管血运情况、腹腔内压变化估计,必要时行结肠镜或钡剂灌肠检查了解梗阻部位及原因。治疗上首选予以抗感染,胃肠减压,给予生长抑素,维持水、电解质及酸碱失衡等对症治疗。治疗观察期间对病情严密观察,对症状不能缓解和长期反复发作病人,必要时复查腹部CT,了解情况后和家属沟通选择手术方式,若病情发展急速直接急诊行手术治疗。
三、术中探查情况
其中50例经腹腔镜探查及治疗(粘连性肠梗阻32例,结肠肿瘤9例,小肠肿瘤5例,肠扭转4例)。其中4例腹腔镜中转开腹手术原因:2例为腹腔肠粘连过重,1例左半结肠梗阻肿瘤浸润腹壁,1例为乙状结肠扭转复位困难。另外48例病人经开腹手术治疗(粘连性肠梗阻31例,结肠肿瘤10例,小肠肿瘤4例,肠扭转3例)。
四、术式选择
肠梗阻因病情复杂,实施手术时较为困难,肠梗阻手术实施者为具有丰富经验的副主任医师,腹腔镜手术也为从事腹腔镜技术10年以上、掌握了熟练的腹腔镜操作技术医师实施。腹腔镜手术操作要点:①手术病人均采用全麻,行气管插管;体位根据术中要求变化。②建立气腹。一般病人选择脐部上、下以气腹针穿刺建立气腹,既往有手术史的病人,观察孔Trocar位置应根据术前判断选择,常规仍以脐部上下为宜,便于腹腔探查,尽量避开上次手术瘢痕区,最好距离原瘢痕区域6 cm以上,直视下置入观察孔Trocar建立气腹(Hasson法),其他Trocar在腹腔镜直视下置入,位置以病变部位为中心,成扇形分部,操作器械尽量位于观察孔前方,便于手术操作。③术中尽量使用无损伤钳,应用超声刀分离,避免使用尖锐的器械,如分离钳、电钩等;术中如发现副损伤应及时处理,以免遗漏;对发现需行肠切除、肠吻合的病变时,可就近行小切口于腹壁外完成,技术熟练者也可直接在腹腔镜下执行;如病情复杂、腹腔镜下操作困难,应及时中转开腹手术。④防粘连剂的使用。术毕于腹腔内均匀涂抹防粘连剂或者防肠粘连液,术后嘱病人早期活动,防治肠梗阻复发。
五、统计学方法

结 果
两组病人术前一般资料包括性别、年龄、体质量指数(BMI)、白蛋白水平、是否放置胃肠减压管、本次发病至手术开始保守治疗时间,对比情况见表1,差异均无统计学意义(均P>0.05),具有可比性。
术中探查原因通过分析差异均无统计学意义(均P>0.05),腹腔镜组有4例中转开腹,统计数据见表2。术中情况比较两组手术时间、术中出血量无明显差异,胃肠道功能恢复时间、住院时间腹腔镜组少于开腹组(表3)。术后随访1~3年,腹腔镜组2例复发(2例均为粘连性肠梗阻),开腹组9例复发(7例为粘连性肠梗阻,2例为结肠肿瘤),11例复发病人(2例结肠肿瘤经腹部CT检查未见肿瘤复发)均保守治疗出院,未再次手术。术后并发症无明显差异(表4)。其中腹腔镜组肠漏为小肠漏,术后再次开腹,发现为手术分离粘连带时损伤未及时发现,行穿孔修补后治疗痊愈。开腹组肠漏1例,为左半结肠吻合口漏,保守治疗后炎症局限,引流管口有分泌物流出,换药2个月后用负压封闭引流(VSD)治疗窦道闭合;1例为直肠吻合口漏,经引流管及肛管冲洗等保守治疗1个月后痊愈。
讨 论
肠梗阻变化快,需要早期作出诊断、处理。诊治的延误可使病情加重,甚至出现肠坏死,腹膜炎等严重情况,有些病人可能发生多器官功能障碍甚至衰竭,危及病人生命[4]。肠梗阻的治疗应得到临床外科医生的高度重视。
曾经作为诊断疾病的腹腔镜技术,目前已经广泛应用于外科手术的各个领域。由于其具有创伤小、恢复快的特点,受到越来越多医生的青睐和病人认可。腹腔镜肠梗阻手术技术难度较大、风险较高且争议颇多[1]。其主要原因有:①腹腔内广泛而致密粘连,建立气腹困难,既往因急性弥漫性腹膜炎行开腹手术尤甚;②肠管扩张使腹腔内操作空间狭小,肠管梳理受限,行结肠肿瘤游离时困难;③肠管扩张、水肿,肠壁脆性增加,器械操作容易造成副损伤而导致严重的后果。一旦穿孔,术中未及时发现,术后将会引起严重后果。O′Connor等[5]曾经报道腹腔镜下治疗肠梗阻手术中肠壁穿孔的发生率为6.6%,其中84%能及时发现,另有16%被疏忽。我们在腹腔镜组也出现1例小肠漏未及时发现,二次开腹才明确原因。
对于肠梗阻的诊断,我们皆是通过严格询问病史、临床症状(痛、吐、胀、闭)、体格检查(腹部触诊和肠鸣音听诊)、辅助检查等综合判断。本组资料术前辅助检查均接受腹部CT平扫+增强检查,因CT对急性肠梗阻病人的诊断准确率(98.17%)高于腹部X线平片(70.12%),且CT对急性肠梗阻病因确诊率(96.34%)高于腹部X线平片(50.61%)[6]。明确原因后按照严格的手术适应证,选择合适的手术时机由熟练的医师进行腹腔镜下手术,一般能顺利完成(本组中转率8%,4/50)。有资料显示提高腹腔镜手术技术,尽量避免开腹手术,腹腔镜手术可以减少腹膜的损伤和术中缝合的机会,减少粘连的形成。如果腹腔镜技术水平低或者术后出现损伤等并发症,则术后再粘连以及新粘连的机会增加[7]。本研究中腹腔镜手术皆是由腹腔镜技术10年以上的副主任医师实施。两组手术时间、术中出血量、术中副损伤(腹腔镜组有2例在分离粘连带时小肠浆膜层破损,于腹腔镜下直接缝合,开腹组发现后直接缝合)无明显差异(P>0.05),并发症也无明显增加(P>0.05)。
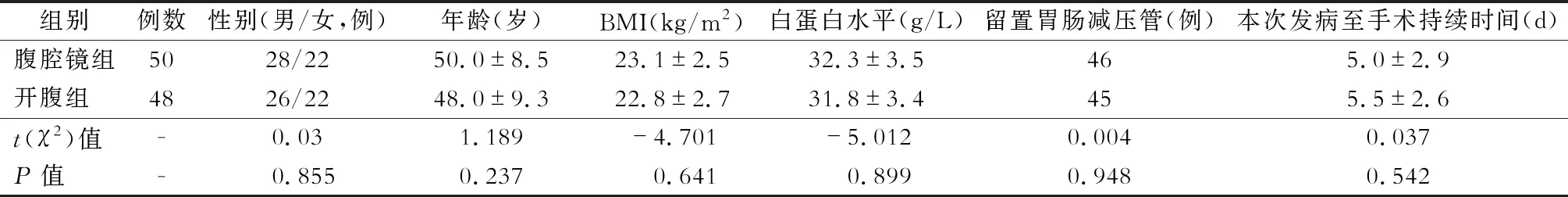
表1 腹腔镜组与开腹组术前一般资料比较
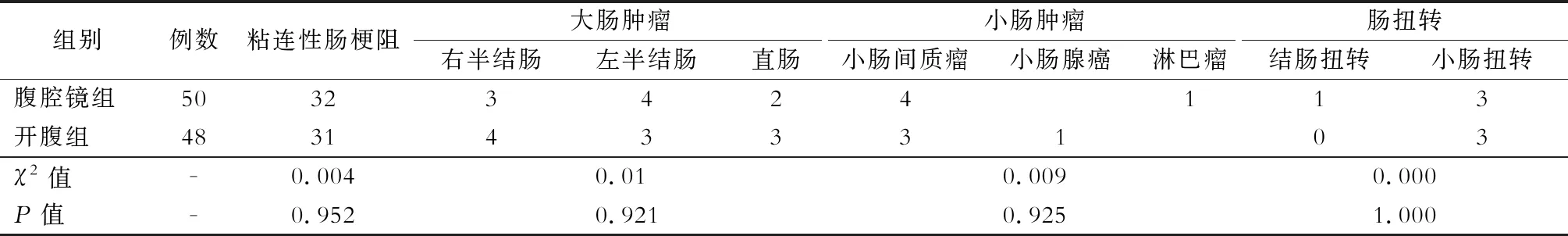
表2 入组病人术中肠梗阻探查梗阻原因(例)

表3 两组术中及术后相关指标比较
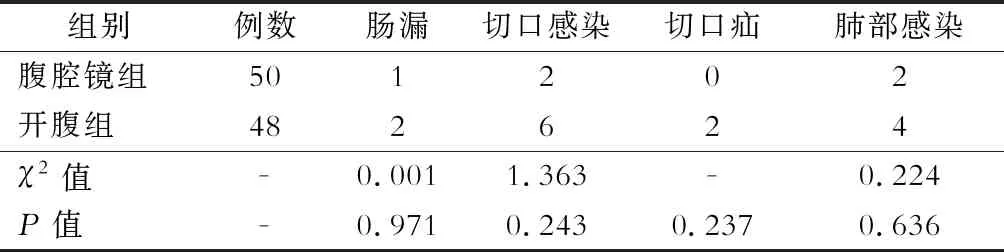
表4 两组术后并发症比较(例)
本研究中病例按肠梗阻原因主要分为两种类型:粘连型和肿瘤型。对于粘连性肠梗阻而言,除了少数由先天性肠粘连、肠系膜发育不良(文献报道原因可能为家族性,与第9号染色体重复的基因座有关[8])引起,大约有4/5的粘连性肠梗阻病人有腹部手术史。 如果再行开腹手术则更加重了粘连的发生和带来的其他严重并发症。而一般的非手术治疗只是缓解症状,长期反复发作给病人增加痛苦,不能根除病因,为此传统开腹手术和一般的非手术治疗对于粘连性肠梗阻均不是特别的理想[9]。我们选择肠粘连手术适应证为:①既往有腹部手术史,半年内发作过2次以上的肠梗阻症状;②腹部影像学检查提示局限性1~2处肠管扩张;③经非手术治疗,临床症状得不到缓解。对于肿瘤型肠梗阻,一般分为小肠肿瘤和结肠肿瘤,小肠肿瘤以间质瘤为主,恶性肿瘤较少,文献报道小肠原发肿瘤仅占胃肠道肿瘤的3%,约占全身肿瘤的0.5%。发病率低可能与通过小肠的食物为液体状、通过速度快、和致癌物质接触时间短、对肠道的刺激小及小肠的细菌负荷少有关[10-11]。小肠肿瘤引起的肠梗阻因小肠比较游离,行腹腔镜操作较为容易,而肠粘连因病例都有开腹手术史而显得稍加困难。结肠肿瘤本组病理皆为腺癌,因其特殊部位,目前介入技术的发展,可以通过支架植入解除消化道梗阻症状,再行腹腔镜手术可提高手术成功率和肿瘤一期切除+重建的概率[12],因基层医院技术的局限性,本组病例中所有结肠肿瘤都没有行支架植入,而是根据病情评估和家属意愿选择手术方式。术前两组一般情况如性别、年龄、BMI等没有明显差异(P<0.05),术前治疗上采用抗感染、胃肠减压、给予生长抑素、肠外营养(TPN)常规治疗,部分不全性肠梗阻以腹痛为表现,腹腔未见明显腹胀而没留置胃管,生长抑素每位病人均使用,因其对全消化道分泌作用的抑制所形成的“内减压”,可有效缓解腹腔特别是解除梗阻部位近端肠管的压力,改善病人的生理机能[13-14],同时也为病人行腹腔镜治疗创造条件。
术后恢复上,腹腔镜组与开腹组比较,术后胃肠道功能恢复时间、住院时间较传统手术有明显缩短,复发率也大大降低。本研究腹腔镜手术后肠梗阻的复发率低于开腹组(P<0.05),仅有2例复发。2014年,Sallinen等[15]发表了一项前瞻性、多中心、同等条件下随机分组实验研究,认为腹腔镜肠梗阻手术在术后并发症发生率、术后恢复时间、住院时间等方面与开腹手术相比具有优势,且差异有统计学意义。原因可能是腹腔镜能减少对腹壁的创伤,尤其是腹膜的损伤,对腹腔干扰较小,腹腔内肠管处于腹腔封闭的空间中,避免了肠管长期暴露于空气中体液丢失,自主节律恢复困难,加之腹腔镜手术疼痛较轻,可以早期下床活动,促进肠道功能恢复。而传统开腹手术术后再粘连的发生率较高,10年肠梗阻复发率为6%~19%,并随着开腹次数的增加,概率也增高,40%的肠梗阻病人都是因为术后粘连造成,有粘连需要再次住院进行第2次手术的病人约占35%,常常形成“粘连-手术-再粘连-再手术”的恶性循环[16-17]。预防术后肠粘连也很重要,我们手术时术中用大量的温生理盐水冲洗腹腔,以稀释和清除腹腔壁上的纤维蛋白原和炎性介质;在肠管表面和壁层腹膜均匀涂抹透明质酸钠,有资料表明透明质酸还有清除作用及抗氧化剂作用,在腹膜炎症时增加γ干扰素水平,抑制炎性反应蛋白,以及减少致炎因子例如IL-1、IL-8 及TNF-α[18-19]等。Johns等[20]的一项多中心的随机﹑三盲对照研究结果显示,透明质酸可以减轻术后粘连。术中尽量不留置引流管, 避免放置引流管本身导致的粘连性肠梗阻复发[21],同时将大网膜覆盖受损的肠管表面及腹膜创面,鼓励病人早期下床活动,可以预防粘连性肠梗阻的发生[22],预防术后肠粘连及肠梗阻复发也一直是我们努力的方向。
综上所述,腔镜手术在肠梗阻治疗中的应用是微创理念的一次创新,即使采用小切口辅助手术也能达到微创的目的[23],但术中遇到粘连广泛、肠管扩张明显、病变处理困难情况下,及时中转开腹,保障病人安全,避免术中或术后造成严重并发症。本研究可以看出如果能够严格掌握腹腔镜肠梗阻治疗的时机和操作流程,进行肠梗阻的腹腔镜治疗是安全的、可行的,并且能使病人获益。但是,本研究由于病例数较少,随访时间短,分组未采用盲法,尚未对远期的并发症及症状改善情况进行详细的研究,还需进一步探讨。

