帕博利珠单抗联合化疗治疗晚期肺腺癌不良反应的护理
崔承盼,蒲瑾,沈华,韦文,李雪莹
(海军军医大学第一附属医院,上海)
0 引言
肺癌居我国恶性肿瘤发病率和死亡率的第一位,每年新发病约73.3万例,死亡约59.1万例[1]。多数患者发现时已处于晚期,丧失手术机会,而传统的治疗方式以全身化疗、放疗和靶向治疗为主。近年来,免疫治疗,作为一种新型的治疗肿瘤的手段,成为全世界的研究热点。
程序性死亡受体-1(Programmed death-1,PD-1)抗体主要作用于T细胞膜上的抗PD-1分子,阻断其与PD-L1及PD-L2配体的结合,促进特异性T细胞增殖和细胞因子释放,从而增强有效的抗癌活性。抗PD-1抗体已在恶性黑色素瘤、非小细胞肺癌、膀胱癌、肾癌、乳腺癌、霍奇金淋巴瘤、卵巢癌及其他恶性肿瘤的治疗中取得了良好的效果[2]。PD-1/PD-L1家族中最著名的当属大名鼎鼎的K药(帕博丽珠单抗,Keytruda),目前美国FDA已批准为用于黑色素瘤及晚期非小细胞肺癌中。而Keytrudal联合AC(培美曲塞+卡铂)已经被批准为晚期非小细胞肺腺癌一线治疗方案。
尽管包括抗PD-1/PD-L1抗体在内的肿瘤免疫治疗已经取得了非常好的抗肿瘤疗效,联合化疗有效率显著高于单纯化疗组,但通过阻断免疫检查点增强肿瘤特异性免疫反应的同时,也会非特异性地激活免疫系统导致免疫稳态被破坏,导致与治疗相关的特殊炎症不良反应,即免疫相关不良反应(Immune-related adverse events,irAEs)[3]。阻断PD- 1通路引起的irAEs主要影响皮肤、消化道、内分泌腺体、肝脏和肺等重要脏器,但同时也几乎对其他任何器官组织具有潜在的影响[4-5],且可发生在应用免疫疗法的任意时间[6]。
国内目前对于应用抗PD-1单克隆抗体后患者出现免疫相关不良反应的观察和护理文献报道较少,尤其是针对晚期肺癌患者,为此,我们将2018年1月至2020年6月本科室20例采用抗PD-1单克隆抗体治疗,共进行178次输注的肺癌患者的护理体会报告如下:
1 临床资料
1.1 研究对象
选取2018年1月至2020年6月期间在我院呼吸与危重症医学科收治的晚期肺腺癌患者共20例,其中IIIb期9例,V期11例,男性12例,女性8例,年龄41-72岁,平均 (60岁),20例患者均为经过病理组织学或细胞学确诊为IIIb/Ⅳ期肺腺癌患者。
1.2 研究方法
根据指南,经病理证实为腺癌,驱动基因阴性,PD-1>50%的晚期肺腺癌患者,PD-1抑制剂联合AC方案为一线首选,因此,20例患者均采用PD-1抑制剂(帕博利珠单抗注射剂,Keytruda)联合AC方案(培美曲塞 800mg/kg d1+卡铂 AUC=5 d1)的治疗方案,3周为1个疗程,每个疗程用药按Keytruda、培美曲塞、卡铂的给药顺序静滴,其中Keytruda采用推荐剂量2mg/kg,配合全身化疗,每3周1疗程。将Keytruda加入100mL生理盐水中,输液泵控制滴速,30min滴完,输注前后用生理盐水冲管,用药期间若出现严重不良反应或无法耐受的毒性时予以减量或停药。
2 结果
采用RECIST 1.1版(实体瘤疗效评估标准)对临床疗效进行评估,其中1例完全缓解(CR),10例部分缓解(PR),9例疾病稳定(SD)。依据美国国家癌症研究所(NCI)不良事件常用术语评定标准4.0版本,对用药过程中出现的免疫相关性不良事件的严重程度进行分级,治疗过程中出现不良反应包括:发热(2例)、皮疹(5例,其中3例轻度,1例为重度)、乏力(5例)、胃肠道反应(4例)、骨髓抑制(2例,1例为II级,1例为V级)、甲状腺功能减退(1例)、免疫性肺炎(1例),不良反应中有19例完全缓解,1例部分缓解。
3 护理
3.1 心理护理
癌症患者不仅要承受身体上的痛苦,更要面临心灵上的打击。研究表明,国内癌症相关抑郁(CRD)的发病率可高达65%-78%,以妇科肿瘤、鼻咽癌和肝癌相对高发[7],而精神压抑会导致癌症患者内分泌失调、免疫力降低,使病情恶化[8]。美国医师学会建议对妇科癌症患者进行随访时,要着重评估患者的负性情绪如焦虑、抑郁、自杀倾向等,早期发现并给予相应的心理支持和药物治疗,进而延长患者的生存时间,提高患者生活质量[9]。用药前,首先与家属和患者进行充分的沟通,建立相互信赖、医患关系,向患者及家属介绍帕博利珠单抗,培美曲塞和卡铂这三个治疗药物,详细解答治疗过程、用药注意事项、可能出现的药物不良反应、以及相应的处理方法,疏导患者对于化疗的恐惧和紧张的情绪。
3.2 用药护理
化疗前对于患者进行全面的评估,如血常规、肝肾功能、尿粪常规、心电图等,根据说明书配置溶液:配置好的溶液是透明至轻微乳白色、无色至浅黄色,给药前目测配置溶液有无颗粒物和变色。配置好的溶液在室温下等待时间不超过6h,包括输注的持续时间。不要在同一个输液器中同时输注其他药物。用药过程严格监测患者的生命体征,密切观察病情,一旦发现异常情况,立即报告负责医生并做好相应的记录。
3.3 不良反应的护理
3.3.1 皮疹的护理
皮肤不良反应,是最常见的免疫相关性不良反应,约40%的患者有不同程度的皮肤不良反应[10],大部分皮肤不良反应为轻中度,通过对症支持治疗可以得到控制[11],而少数严重的皮肤不良反应,可能危及患者的生命,如Steven-Johnson综合征,大炮性类天疱疮等[12]。
本组有5例患者出现皮疹,均表现为红色斑丘疹样皮疹。其中4例轻度,1例重度。4例轻度患者表现为用药后1-2周后出现局部的斑丘疹样皮疹,伴皮肤瘙痒,躯干部多件,予以口服开瑞坦、外用止痒地霜外涂1-2周,同时给予患者相应的护理指导:保持心情舒畅,避免进食辛辣刺激食物(如:辣椒、浓茶、咖啡、酒等);避免穿着紧身衣裤,以全棉透气为主;保持皮肤干燥,剪短指甲,避免用手抓破皮肤,引起皮肤感染;平日少用对皮肤有刺激性的清洁剂,清洗干净后可分次外涂止痒乳膏,4例患者在以上治疗1周后皮疹自行消退。另1例重度患者,静滴完Keytruda药物1天后出现全身多处皮肤瘙痒,随后出现全身多发红色斑丘疹样皮疹,躯干及四肢较多,但无明显呼吸困难、气急等喉头水肿症状,配合上述护理要点的同时,静脉应用糖皮质激素:甲强龙20mg静推,非那根肌注抗过敏处理,同时给予口服强的松序贯,口服抗组胺药物,外涂洁肤乳膏,2周后该患者皮疹逐渐消退,强的松予以减量至停用。
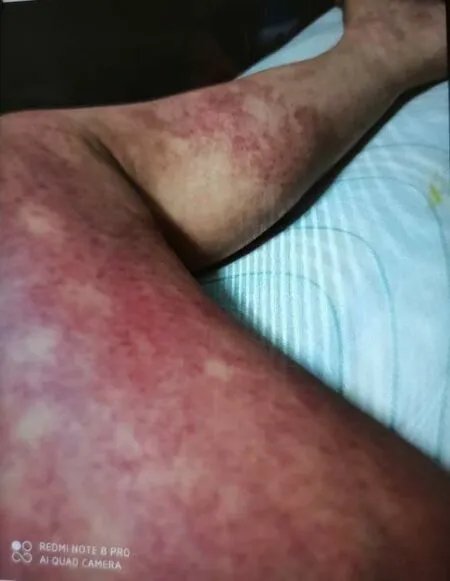
图1 重症皮疹患者下肢皮疹表现
3.3.2 发热的护理
发热是另一个较多见的免疫不良反应。发生的原因与细胞因子释放和免疫反应的非特异性活化有关[13]。多数患者表现为第一次输注时,以低热为主,极少数表现为高热。护理上,用药前可先于患者沟通,告知其用药后可能会出现发热等副作用,用药期间注意规范输液流程,避免输液感染的情况出现。用药后密切监测患者体温情况,对于轻症患者可予以对症处理,对于高热同时伴有寒战的患者,要考虑到输液反应的可能性,必要时行血培养,并应用糖皮质激素对症处理。
本组有2例患者出现发热,均为用药后出现低热,发热前均无明显畏寒寒战,精神状态好,较逍遥,饮食胃口均未受影响,嘱多喝水,吃些新鲜水果蔬菜,物理降温(冰袋、温水擦浴)。1例体温37.5度,用药后6小时左右体温下降至正常。另1例体温38度的这例患者给予消炎痛栓30mg纳肛对症处理,约半小时后患者出汗后体温逐渐将至正常。
3.3.3 乏力的护理
本组有5例在输注药品之后产生了疲乏感,由于本研究为Keytruda联合AC方案治疗,考虑乏力与应用细胞毒药物相关可能性大,护理上与患者多沟通,充分告知可能出现的不良反应,嘱患者治疗期间多休息,适当活动,减少过度消耗体力的活动,补充营养,可给予高热量、高蛋白、高维生素饮食,少食多餐。
3.3.4 胃肠道反应的护理
本组有4例患者出现轻度胃肠道反应,主要表现为轻度恶心、食欲下降,无腹泻腹痛病例,胃复安等处理后可缓解,4例患者在用药后3天胃肠道反应完全消失,其余16例患者无明显不适,耐受性好。由于本组患者均选用Keytruda联合培美曲塞和卡铂治疗,因此出现的胃肠道反应可能也与化疗药物的毒副反应有相关性。饮食上,建议患者进食清淡、易消化的软食,少食多餐,用药前可给予中枢止吐药物如:托烷司琼预处理。
3.3.5 甲状腺功能异常的护理
接受PD-1单克隆抗体治疗的患者中,10%被观察到出现了不同级别的免疫相关内分泌病症[14]。甲状腺功能减退是常见的内分泌系统免疫相关不良反应,发病率为11%,中位发病时间是2.9个月[15]。
本组出现1例甲状腺功能减退,但无明显自觉症状,仅在抽血复查后发现TSH升高,FT3、FT4下降。护理上需告知患者定期随访甲状腺功能,如血清促甲状腺激素(TSH)、血清游离甲状腺素(FT4)、游离三碘甲状腺原氨酸(FT3),每2周1次,若出现甲状腺功能减退者,可适当补充甲状腺激素,如:优甲乐12.5ug1/早,根据复查的甲状腺功能调整药物剂量。
3.3.6 骨髓抑制的护理
骨髓抑制是免疫抑制剂联合化疗最严重的副反应之一。通常出现在化疗后7-10天到达低谷。本组出现2例骨髓抑制,1例轻症,表现为化疗后1周复查血象,白细胞降低至3.8×109/l,中性粒细胞计数降至1.8×109/l,常规给予口服利可君片、地榆升白片升白细胞,护理上嘱患者避免去人群聚集的地方,注意佩戴口罩,保持室内空气流通,平日注意保暖休息,补充营养,避免感染,治疗后1周左右复查白细胞,若白细胞显著下降可予以皮下注射重组人粒细胞刺激因子。
另1例为重症,治疗后7天复查血常规,白细胞将至1.2×109/l,中性粒细胞计数降至1.4×109/l,血小板降至40×109/l,但患者无发热畏寒,无咽喉肿痛,无咳嗽咳痰,无皮下淤血瘀斑,无牙龈出血,无呕血黑便等并发症,立即收治入院,予以病房紫外线消毒一日两次,医护查房交接班时均佩戴口罩,谢绝亲友探视,固定陪护人员1名;注意加强口腔护理,观察口腔黏膜及皮肤完整性,若出现口腔黏膜破损,可给予贝复济外用促进表皮生长;加强会阴护理,预防尿路感染发生;观察有无皮下出血、牙龈出血、呕血咯血等活动性出血情况,尽量平卧,保持大便通畅,避免用力过度致消化道出血等。治疗上,皮下注射重组人粒细胞刺激因子(惠而血)升白细胞,皮下注射白介素-11升血小板,必要时可输注单采血小板。若合并有活动性出血症状,止血对症处理。经治疗和护理,该患者约6天后白细胞及血小板逐渐回升,10天后恢复正常。
3.3.7 免疫相关性肺炎的护理
抗PD-1单克隆抗体引起的免疫相关性肺炎,主要表现为非特异性间质性肺炎,多出现在0.5-24.3个月,中位发病时间为2.6个月[16]。
本组出现1例免疫相关性肺炎,该患者Keytruda联合AC方案治疗两个疗程后,因出现咳嗽咳痰,伴有胸闷气急,胸部CT提示两肺多发网状状斑片影,两肺间质性肺炎。立即收治入院,予以静脉滴注甲强龙80mg1/日×3天,第4天起甲强龙减量至40mg1/日×3天,同时因痰培养提示白色念珠菌,予以口服SMZ预防感染,伏立康唑抗真菌感染。7天后患者胸闷气急症状缓解后,复查胸部CT,两肺间质性肺炎较前吸收,遂停用甲强龙,改强的松40mg1/日口服序贯,治疗期间辅以多索茶碱平喘、沐舒坦化痰、小剂量速尿利尿剂减轻组织水肿、营养大袋营养支持和维持水电解质平衡等对症治疗,护理上积极口腔及会阴护理,避免继发感染和二重感染的发生,帮助患者翻身、排痰,鼓励患者自主咳嗽,必要时予以吸痰保持呼吸道畅通;给予低流量氧疗,检测患者血氧饱和度,隔日行动脉血气分析;观察患者有无端坐呼吸、咳粉红色泡沫痰等心衰症状,及时汇报医生处理。
4 总结
本组实验虽然样本量偏小,所得结果可能缺少全面性,仍可以得出以下结论:帕博利珠单抗联合AC方案化疗在大多数患者中耐受性良好,重度严重的不良反应少见。肿瘤免疫治疗是激活肿瘤患者T淋巴细胞的抗肿瘤反应以提高其对肿瘤细胞的杀伤功能,其核心机理为阻断免疫抑制通路,因此引起的免疫相关不良反应,可累及绝大多数正常组织,且可以发生在疾病治疗的任何一个阶段,复杂多样。对于临床护理工作而言,对不良反应需要提高警惕,在掌握了常见的免疫相关不良反应后,应用于实际工作中,做到早发现早诊断早治疗,将不良反应控制在低级别,降低危险,改善预后,帮助患者顺利完成治疗正过程。

