测定空气中氧气含量实验的改进
河北省涉县鹿头中学 李树兵 张树卫
【实验原型】教科版教材第二章第一节“测定空气中氧气含量”的实验原理:利用燃料的方法,可燃物燃烧消耗瓶内空气中的氧气,产生内外压强差,通过进入瓶内的水的体积,反映空气中氧气的含量。装置如图1所示。

图1
【操作细节】1.首先需要将燃烧匙中的红磷在酒精灯上加热到燃烧。
2.将燃烧匙快速插入集气瓶中,以防瓶内气体受热膨胀被挤出集气瓶。
3.塞紧瓶塞,防止漏气。
4.待反应完全后,装置冷却至室温时打开止水夹,观察烧杯中水进入集气瓶中的量,得出空气中氧气的含量。
【实验弊端】1.将燃烧匙中的红磷在酒精灯上加热至燃烧时,放出大量的热,会烫手且冒出大量的白烟,散发到空气中不但会造成人体伤害,还会对空气有污染,违背绿色化学的理念。
2.被点燃的燃烧匙中的红磷,要迅速插入集气瓶中,但由于瓶口较小,很容易碰到瓶子,使瓶子骤然受热而炸裂。
3.移动燃烧着的红磷的过程中很容易将红磷撒出烫伤身体或引起火灾。
【创新设计】鉴于该实验操作复杂、难以掌握,很容易引起实验结果不准确。因此,为了更好地开展实验教学,消除安全隐患,让学生在实验中感受化学的魅力,特对该实验的装置进行改进。
【方案一】如图2 所示装置,利用凸透镜对太阳光会聚将红磷点燃完成实验。该设计的优点有:
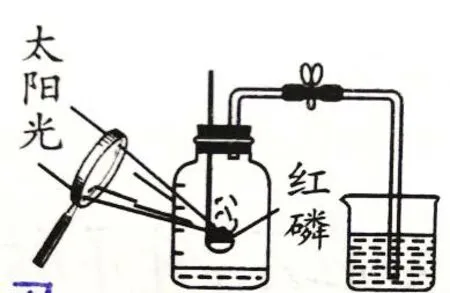
图2
1.不再用酒精灯加热,操作简单,没有点燃移动等环节,非常安全,还无空气污染。
2.在密闭环境下实验,减少了空气热胀逸出的影响,实验结果准确度大大提高。
3.在化学实验中应用物理学科中凸透镜对光线的会聚作用提高温度,实现了不同学科之间的知识渗透,可以提高学生的学科素养。
【方案二】如图3 所示装置,由注射器、铜丝、玻璃管和酒精灯组成。
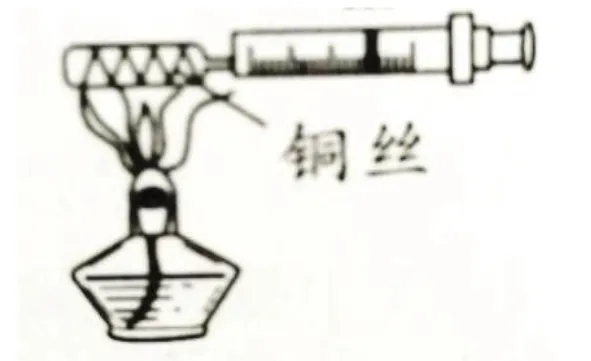
图3
原理:加热铜丝,铜丝与氧气反应,消耗玻璃管内氧气,压强减小,大气压将注射器活塞推入,测出消耗氧气的体积。
优点:测量准确,伴随有明显的化学现象:铜丝由红色变为黑色。
注意事项:1.管中的铜丝要足量,保证能消耗完管中氧气。
2.反应过程中来回推动活塞,让管内氧气充分反应。
3.采用分度值更小的注射器能准确测出空气中氧气的体积,提高实验的测量准确度。
科学需要不断探索,敢于质疑、敢于实践是推动科学进步的力量源泉,希望广大中学生能在学习中勤于思考、勇于探索。

