降钙素原、乳酸联合APACHEⅡ评分对脓毒性休克合并弥散性 血管内凝血的预测价值
何习斯,陈燕宏,文莎,李豪丽,吴明,3*,冯永文*
1广州医科大学研究生院,广州 511400;2深圳市第二人民医院重症医学科,广东深圳 518037;3广东医科大学研究生院,广东湛江 524023
弥散性血管内凝血(DIC)是感染性疾病中常见的、可危及生命的并发症。研究发现,30%~50%的脓毒症患者会发生DIC,脓毒症并发DIC的病死率达28%~43%[1-2]。DIC是脓毒性休克患者发生多器官衰竭(MOF)和死亡的强预测因子[3]。脓毒性休克相关DIC的特征为内皮功能障碍导致炎性因子释放,引起全身凝血激活,凝血、抗凝及纤溶系统失衡,导致微小血栓形成,严重者迅速发展成MOF甚至死亡[4-5]。因此,炎症反应及凝血反应在脓毒症和脓毒性休克的发病过程中起着至关重要的作用[6]。 脓毒症和脓毒性休克患者的降钙素原(PCT)水平升高,可反映炎症反应的活跃程度[7]。Becker等[8]发现,PCT可诱导白细胞的促炎作用,如增高细胞表面标志物的表达和促炎细胞因子的浓度,且PCT与D-二聚体水平和血小板计数密切相关,提示PCT与止血功能障碍有关。急性生理学与慢性健康状况评分Ⅱ(APACHEⅡ评分)是临床常用的危重症评分系统,其评分越高,表明患者病情越重,预计病死率越高。但APACHEⅡ评分系统缺乏出-凝血相关指标的评价,而目前尚无单一生物标志物能有效诊断脓毒性休克患者合并DIC。本研究探讨炎性指标、乳酸和APACHEⅡ评分对脓毒性休克合并DIC的预测价值,以协助早期诊断DIC并降低其病死率。
1 资料与方法
1.1 研究对象 回顾性分析2015年1月1日-2018年12月31日于深圳市第二人民医院重症医学科就诊的164例脓毒性休克患者的临床资料。脓毒性休克诊断标准[9]:脓毒症患者经过积极的液体复苏治疗后,仍需升压药物维持平均动脉压(MAP)≥65 mmHg且血乳酸水平>2 mmol/L。排除标准:①年龄<18岁;②心脏骤停、心肺复苏者;③休克超过24 h或入ICU少于24 h;④既往有风湿免疫性疾病、血液病、肿瘤病史;⑤存在血栓性疾病,如急性脑梗死、急性肺栓塞、急性心肌梗死;⑥合并心源性休克;⑦临床资料不全。所有纳入患者根据是否发生DIC分为DIC组和非DIC组。DIC诊断标准为2001年国际血栓与止血协会(International Society of Thrombosis and Haemostasis,ISTH)评分标准[10-11]。该DIC诊断积分系统主要采用凝血酶原时间(PT)、血小板(PLT)、纤维蛋白原和D-二聚体等指标进行积分,积分≥5分为显性DIC,积分<5分为非显性DIC。本研究通过深圳市第二人民医院伦理委员会审批(批准文号:20160115004)。
1.2 方法 收集患者的年龄、性别、住院时间、 感染源、是否机械通气等资料,血常规、凝血功能、肝肾功能、血气分析等实验室指标,对所有患者住院第一个24 h进行APACHEⅡ评分和ISTH DIC评分。
1.3 统计学处理 采用SPSS 24.0软件进行统计分析。符合正态分布的计量资料以表示,组间比较采用独立样本t检验;不符合正态分布的计量资料以M(Q1,Q3)表示,组间比较采用Mann-WhitneyU检验。采用logistic回归分析脓毒性休克患者合并DIC的危险因素;绘制受试者工作特征曲线(ROC)确定PCT和APACHEⅡ评分预测发生DIC的灵敏度、特异度,计算最佳截点。P<0.05为差异有统计学意义。
2 结 果
2.1 脓毒性休克非DIC组和DIC组一般资料比较 共纳入脓毒性休克患者261例,根据排除标准,最终纳入164例,其中男97例(59.1%),女67例(40.9%),年龄19~99(64.1±18.9)岁。根据ISTH评分标准分为DIC组(n=58,35.4%)与非DIC组(n=106,64.6%)。两组年龄、性别、ICU住院时间、是否机械通气和感染源差异均无统计学意义(P>0.05,表1)。患者筛选流程如图1所示。
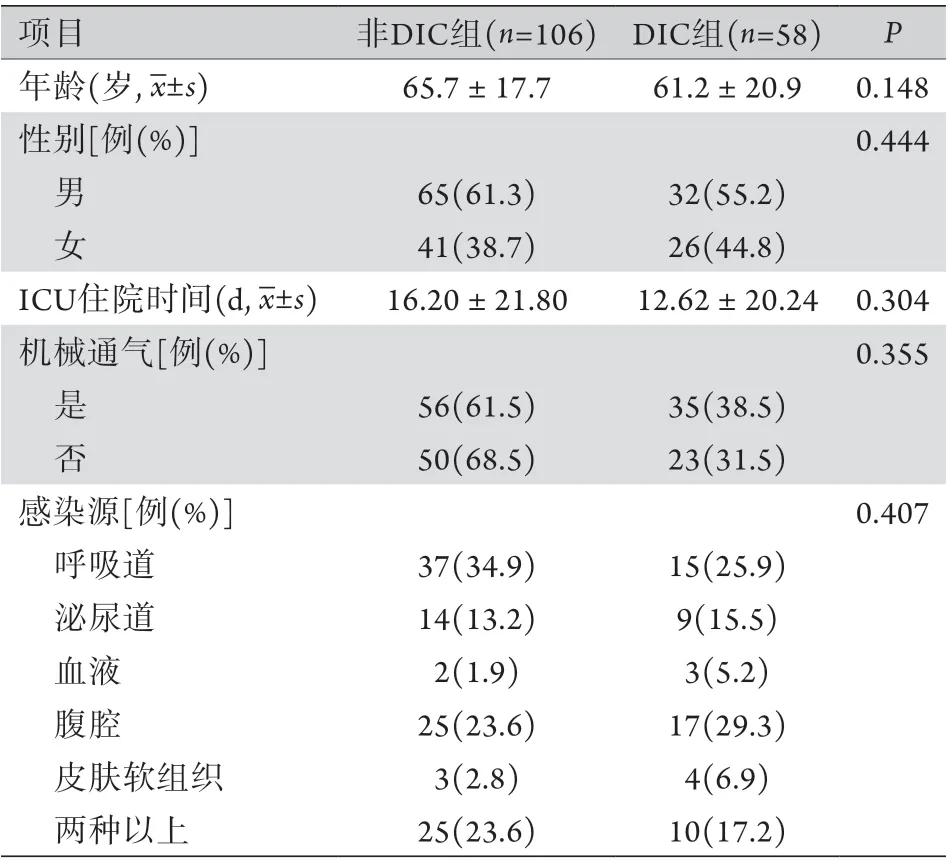
表1 两组脓毒性休克患者一般资料比较Tab.1 Comparison of the general data between non-DIC and DIC patients induced by septic shock

图1 脓毒性休克患者筛选流程Fig.1 Flow diagram of screening subjects
2.2 脓毒症休克合并DIC的单因素分析 脓毒性休克DIC组PCT、胆红素、谷丙转氨酶、谷草转氨酶、乳酸、APACHEⅡ评分、ISTH评分均高于非DIC组,差异有统计意义(P<0.05)。两组白细胞计数、淋巴细胞计数、中性粒细胞计数、C反应蛋白、白蛋白、肌酐、尿素氮、氧合指数差异均无统计意义(P>0.05,表2)。
表2 脓毒性休克患者合并DIC的单因素分析(±s)Tab.2 Univariate analysis of clinical indicators of non-DIC and DIC patients induce by septic shock (±s)

表2 脓毒性休克患者合并DIC的单因素分析(±s)Tab.2 Univariate analysis of clinical indicators of non-DIC and DIC patients induce by septic shock (±s)
项目 非DIC组(n=106)DIC组(n=58) P白细胞计数(×109/L) 15.66±10.31 15.26±10.30 0.813淋巴细胞计数(×109/L) 1.29±2.22 1.09±1.26 0.529中性粒细胞计数(×109/L) 13.70±9.31 13.45±9.63 0.869 C反应蛋白(mg/dl) 129.16±77.91 130.48±72.66 0.916 PCT(ng/ml) 43.75±64.75 92.95±83.50 <0.001白蛋白(g/L) 25.46±6.80 23.91±7.50 0.180总胆红素(μmol/L) 22.88±36.38 50.22±83.78 0.021谷丙转氨酶(U/L) 61.21±104.70 601.62±1428.61 0.006谷草转氨酶(U/L) 85.10±111.86 11 157.97±2514.81 0.002肌酐(mmol/L) 172.57±161.22 230.05±207.97 0.051尿素氮(mmol/L) 12.15±8.82 14.03±7.52 0.171乳酸(mmol/L) 3.48±1.80 6.70±6.21 0.000氧合指数(mmHg) 238.75±97.25 228.11±106.16 0.518 APACHEⅡ评分(分) 21.80±8.41 26.62±10.26 0.003 ISTH评分(分) 3.12±0.70 5.57±0.76 <0.001
2.3 脓毒症休克合并D I C 的多因素分析 多因素logistic回归分析结果显示,PCT、乳酸、APACHEⅡ评分可能是脓毒性休克患者发生DIC的独立影响因素(P<0.05,表3)。
2.4 预测脓毒性休克合并DIC的ROC曲线分析 ROC曲线分析结果显示,PCT预测脓毒性休克合并DIC的ROC曲线下面积(AUC)为0.701(95% CI0.619~0.784,P<0.001),最佳截点为41.18 ng/ml, 敏感度为6 0.3 4%,特异度为7 2.6 4%。乳酸预测脓毒性休克合并DIC的AUC为0.669(95% CI 0.579~0.759,P<0.001),最佳截点为4.2 mmol/L,敏感度为51.70%,特异度为77.40%。APACHEⅡ评分预测脓毒性休克合并DIC的AUC为0.643(95% CI 0.550~0.736,P=0.002),最佳截点为28.5分,敏感度为53.45%,特异度为74.53%。三者联合预测脓毒性休克合并DIC的AUC为0.772(95% CI 0.697~0.848,P<0.001),敏感度为65.50%,特异度为80.20%。相对单独指标,三者联合预测脓毒性休克合并DIC的敏感度和特异度最佳(图2)。
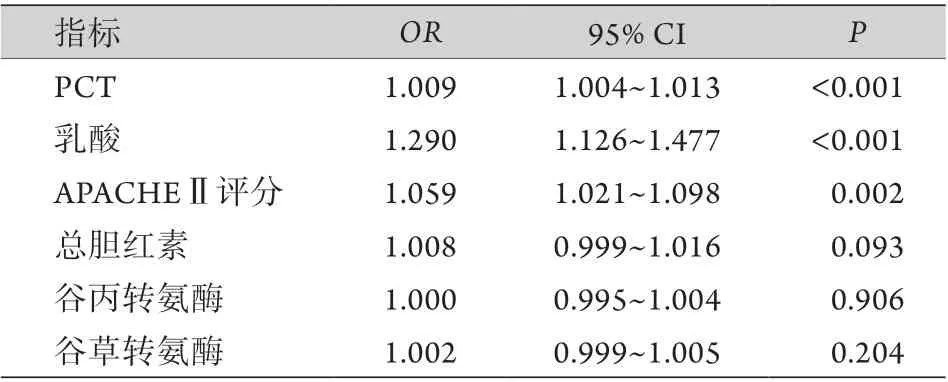
表3 脓毒症休克患者合并DIC的多因素分析Tab.3 Multivariate regression analysis of the clinical indicators for DIC induced by septic shock
3 讨 论
凝血激活和炎症反应是脓毒性休克宿主抵抗感染的基本反应,但同时也会对宿主造成伤害。Levi等[12]在脓毒症相关DIC中观察到凝血激活、纤维蛋白溶解过度和抗凝系统紊乱,其病理生理过程为大量纤维蛋白沉积在微小血管,造成多脏器衰竭[13]。 在脓毒性休克中,机体释放大量炎性因子,促使PCT释放入血,PCT水平升高也可导致炎性因子水平升高,持续增多的炎性因子刺激血管内皮释放血管性血友病因子,促进微血栓形成,进一步加重凝血功能紊乱[3],这可能是PCT作为脓毒性休克患者发生DIC早期预测指标的机制。本研究结果显示,与非DIC组相比,脓毒性休克合并DIC组PCT水平明显升高,高PCT水平是脓毒性休克发生DIC的高危因素,可用于临床早期识别DIC并指导治疗。因此,血浆PCT不仅可预测脓毒性休克,还可预测患者是否发生DIC。此外,PCT可能在早期风险分层及整体发病率和病死率预测中具有潜在作用。本研究ROC曲线分析结果显示,PCT预测脓毒性休克合并DIC的AUC为0.701,高于乳酸的0.669和APACHEⅡ评分的0.643,预测能力更强,其最佳截点为41.18 ng/ml,敏感度为60.34%,特异度为72.64%。
血清乳酸是微循环障碍常用的监测指标。DIC持续性微血栓形成引起的微循环功能障碍可导致流向组织的血液减少,并在后期引起器官功能障碍,可能与组织缺氧、高乳酸血症和最终死亡有关[14]。此外,一系列观察研究发现,凝血激活和纤溶抑制直接导致组织缺氧,但与潜在的混杂因素无关,表明脓毒性休克导致DIC可使微血管阻塞,加重组织缺氧,且与高乳酸血症有关,有助于解释器官系统衰竭的发生[15-16]。本研究结果显示,乳酸是脓毒性休克合并DIC的独立危险因素,对脓毒性休克合并DIC有预测价值。
APACHEⅡ评分系统是一种广泛应用于重症监护室患者预后评估的评分模型。APACHEⅡ评分分值越高,表明病情越重、病死率越高,与危重患者的预后密切相关[17-18]。但该评分系统不涉及凝血指标,忽略了凝血激活过程对大多数患者预后的意义。本研究结果显示,APACHEⅡ评分对预测脓毒症休克合并DIC有临床诊断意义,表明APACHEⅡ评分和DIC存在相关性,且PCT、乳酸联合APACHEⅡ评分预测脓毒性休克合并DIC的敏感度(65.50%)和特异度(80.20%)最佳。三者联合的ROC曲线显示AUC为0.772,较单一指标的AUC更大,说明三者联合应用对脓毒性休克合并DIC患者更有预测价值。
综上所述,PCT、乳酸和APACHEⅡ评分可作为预测脓毒性休克合并DIC的早期诊断指标,三者联合可提高早期预测的准确性,为预警和救治脓毒性休克早期患者提供临床依据。本研究为单中心、小样本研究,故仍须进一步大规模随机对照研究来证实。

