微量元素Se的生物活性及检测技术研究进展
马风伟,许 粟,程永友,陈海江,费 强,马立志
(1.贵阳学院 食品与制药工程学院,贵州 贵阳 550005;2.贵州省果品加工工程技术研究中心,贵州 贵阳 550005)
硒(Selenium,Se)为人体不可缺少的微量元素,其最早引起人们的注意是因其过量摄入而产生的毒副作用,过量的硒摄入会产生呼气大蒜味、腹痛、严重者呼吸困难并导致死亡。[1]Schwarz等[2]在1957年提出动物体内缺硒与蛋白质不良症密切相关,硒作为人体的必需微量元素被人们关注。1981年我国黑龙江省克山县发生的地方性心脏病—“克山病”被证实为缺硒所致,硒与人类健康的关系受到越来越多的重视。[3]硒作为和硫(Sulphur,S)元素同族的元素,其物理化学性质与S元素有相似性,也有多个价态,在自然界的存在方式可呈现出有机态和无机态,不同的硒价态和形态与生物活性差别很大。[4]人体对硒的日需求适宜量为60~250 μg[5-6],相对于常量营养元素,如此微量的需求对分析检测技术的要求很高,为了准确定量食物中硒的含量,研究者开发了多种检测手段,从最初的滴定法、化学比色法到最新的质谱分析,对硒的检测也是从微量到痕量。[7]本文对硒的生物活性以及分析检测进行综述,以期为硒相关的深入研究提供参考。
1 硒的存在形式
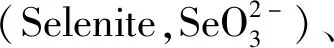

图1 常见的硒化合物
2 硒的生物活性
2.1 硒的毒性


图2 亚硒酸盐在机体内的代谢途径
2.2 硒的益处
虽然过量的硒对人体有毒害作用,但硒作为人体必需的微量元素是机体内很多酶和蛋白的活性中心,对人体正常机能的正常运行起到非常重要的作用[13],如抗氧化[14]、抗癌、免疫调节[15]、维护甲状腺功能、重金属解毒等。
2.2.1 抗氧化作用
GSH-Px是人体重要的过氧化物分解酶,其活性中心就是硒代半胱氨酸[16],机体内GSH-Px活力的大小可以反映出人体是否缺硒。人体GSH-Px酶系可分为4种[17-19],分别为胞浆GSH-Px(GPX1,由203个氨基酸组成,活性中心为U49)、血浆GSH-Px(GPX3,由226个氨基酸组成,活性中心为U73)、磷脂氢过氧化物GSH-Px(GPX4,由197个氨基酸组成,活性中心为U73)和胃肠道专属性GSH-Px(GPX2,由190个氨基酸组成,活性中心为U40)。GSH-Px在人体内的作用主要是分解过氧化物,使其转变为无毒的羟基化合物,进而保护细胞膜的结构完整和功能。

注:*为活性催化中心-硒代半胱氨酸图3 人类4种谷胱甘肽过氧化物酶的氨基酸序列
2.2.2 抗癌作用
硒元素的抗癌机理虽然并不完全清楚,但流行病学调查发现癌症高发区居民的血硒水平普遍偏低,同时发现癌症组织中硒蛋白P的含量较正常组织低。[20-21]硒元素抗癌的作用机理可能有以下几个方面:a硫氧还蛋白还原酶1(Thioredoxin reductase 1, TrxR1)作为一个含硒蛋白可以激活肿瘤抑制因子p53蛋白的表达;[22]b位于内质网的硒蛋白15(Selenoprotein 15,Sep15)被发现在多个肿瘤组织细胞中的表达减少,其可通过调节细胞周期在肿瘤发生发展过程中起着重要作用;[23]c谷胱甘肽过氧化物酶GSH-Px2分布于小肠上皮细胞,可通过上调Nrf2/Keap1(NF-E2-related factor 2/Kelch-like ECH-associated protein 1)信号通路的表达对致癌物进行脱毒,对结肠癌的发生有预防作用。[24]
2.2.3 免疫调节作用
在机体内,硒存在于多种免疫器官中,如胸腺、骨髓、脾、淋巴结等;在细胞内,硒存在于多种免疫细胞中,如淋巴细胞、单核/巨噬细胞、粒细胞等。[25]机体缺硒会导致T细胞数目减少[15],并致使免疫反应减弱,如人类致命的强毒性流感病毒在中国缺硒地区进化[26],小鼠试验显示,柯萨奇病毒更易在缺硒的机体内发展为致命的心脏毒性反应。[27]
2.2.4 其他作用
甲状腺是人体组织中含硒浓度最高的器官,脱碘酶(Deiodinase)有三种类型,均为含硒酶,缺硒会影响甲状腺功能;硒通过形成重金属-硒-蛋白复合物来拮抗有毒重金属对机体的毒害作用。[28]
3 硒的含量检测
硒作为人体必需的微量元素,人体血液或毛发中的硒含量很低,这就为分析检测增加了难度,研究者开发了多种分析检测方法对硒元素进行检测。
3.1 滴定法
滴定法测定样品中的硒含量采用的是氧化还原滴定法,其原理是利用亚硒酸离子氧化碘离子(I-)生成碘分子(I2),通过硫代硫酸钠滴定碘来定量样品中硒的含量。其反应方程式如图4所示,硫代硫酸钠与亚硒酸钠的化学计量比为4∶1,通过滴定消耗的硫代硫酸钠体积及浓度可以计算样品中硒的含量。
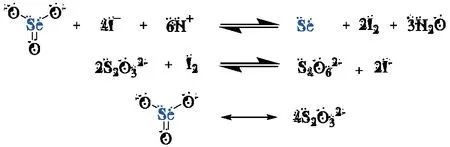
图4 氧化还原滴定法测定样品中硒的反应方程式
3.2 化学比色法
化学比色法测定硒含量的方法比较多,如2,3-二氨基萘法、3,3’-二氨基联苯胺法、钼蓝法、硫氰化钾-罗丹明B法等,其原理为高温消解样品,然后加入还原剂使硒转变为+4价,通过与发色团吸光物质发生化学反应,生成络合物(图5),该络合物在一定条件的颜色深度与硒浓度呈正比关系,然后根据最小二乘原理建立回归曲线,对溶液中硒含量进行测定。化学比色法的优点是操作简单,不需要昂贵的仪器,缺点是灵敏度低,其无法对不同价态的Se进行分析。
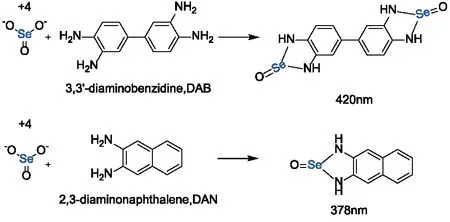
图5 化学比色法测定样品中的硒
3.3 气相色谱法
硒(IV)与邻苯二胺发生反应生成具有挥发性的产物(图6),通过用有机溶剂萃取后,可以进行气相色谱分析[29],色谱柱可分为键合型和非键合型,其中非键合型色谱柱内径较大,柱内有固定液和担体(support)组成,用于硒分离的固定液多为非极性的,如100%聚甲基硅氧烷(100% dimethyl polysiloxane)或含5%苯基的聚甲基硅氧烷(5% phenyl dimethyl polysiloxane);担体多为高纯度硅藻土(SiO2·nH2O)。检测器一般不选择氢火焰离子化检测器(flame ionization detector,FID),而是选择灵敏度高的电子捕获检测器(electron capture detector,ECD),若选择溴代或硝基取代的邻苯二胺类似物发生反应,可进一步提供灵敏度。

图6 气相色谱法测定样品中的硒
3.4 原子光谱法
硒的特征发射波长为196.0nm,通过特征谱线的波长和强度可以进行定性和定量分析,但实际应用中,多采用硒原子的吸收光谱法进行定量分析,因基态原子能量最低,也最稳定,定量分析时基线平稳,外层电子吸收能量跃迁至较高能级,也会瞬间回到基态,谱图上表现为锐利的尖峰。Kubota等[30]采用钼酸盐型阴离子交换树脂富集水中痕量的不同价态的Se,然后直接导入石墨炉原子化进行原子吸收检测,取得良好的检测结果。
由于硒化氢(H2Se)具有沸点低、易原子化的特点,一般多采用氢化物发生装置使硒化物还原生成硒化氢,然后进行原子吸收光谱法检测。[31]
硒原子还有一个特性,其吸收特定波长的电磁波后,由基态跃迁至激发态,在从激发态返回至基态过程中,会发射特征的荧光,通过检测荧光强度进行定量分析,具有灵敏度高,且专属性强的特点。Deng等人[32]采用原子荧光法测定食物中Se的含量,定量限达到0.050 ng/mL。
3.5 质谱法
质谱作为一个新的检测离子的技术,具有快速、灵敏的特点,硒在自然界有6种同位素(表1),其丰度有很大差异,故相对原子质量为78.96。质谱分析中多采用78Se进行定量,同时以82Se为内标参照。

表1 自然界中硒元素的同位素
硒的离子化一般选择电感耦合等离子体(inductively coupled plasma,ICP)技术,ICP具有温度高、电子密度高、化学惰性等优点,既可以作为离子源又可以作为原子化器,在元素分析中有重要应用。
样品的前处理可以选用电热蒸发(electrothermal vaporization)法,其优点是操作简单,可固体取样。[33-34]Liu等人[35]采用电热蒸发原子吸收法测定水果汁中的Se含量,通过考察不同基质改性剂最终可实现Se的定量限为28 pg。
3.6 硒的形态分析
硒的形态分析研究多数限于无机硒和有机硒的简单分析,或对有机硒的形态进行初步分析。分析方法多采用HPLC或阴离子交换色谱(anion-exchange LC)进行分离,然后采用ICP-MS与标准样品进行比对分析[36-37],也可采用分子质谱对硒形态进行辅助分析。对硒蛋白的检测分离也可以采用凝胶电泳(gel electroghoresis),然后采用ICP-MS分析。[34]Jorge[38]等人采用HPLC-ICP-MS同时对富硒区产的干果(巴西栗)Se含量和Se形态进行的分析,最低定量限可达到0.014 ppm,Se形态分析发现巴西栗中含有SeMet和SeCys2,并通过轨道阱质谱确证了巴西栗中不含有SeOMet。
3.7 其他分析方法
中子活化分析是一种放射分析方法,以中子或质子照射引发局部微小核反应,激发活化的复合核产生辐射γ射线,根据波峰进行定性,根据辐射强弱进行定量分析。[39]Mohammed等人[40]采用放射化学中子活性技术对薄荷样品中Se含量进行检测,发现阿尔及利亚地区薄荷中Se的含量为0.037ppm。
4 展望
随着人们对硒的研究深入,对其生物活性的机理机制有了更深入的了解,同时随着现代分析仪器的研制和迭代,灵敏度、专属性越来越好,但对硒的分析检测还有待改进,今后可以从以下两个方面开展工作:(1)自动化、一体化、联用化的检测设备研制和开发,不需要样品前处理或仅仅简单的样品处理,就可以实现样品的在线、准确的定量分析;(2)硒的形态分析需要更精细的分离手段,开发专属性更好的色谱分离技术。

