急性加重高风险慢性阻塞性肺疾病患者的睡眠质量及相关因素
吴云萍, 胡罗燕
台州市路桥区中医院医疗服务共同体内科(浙江台州 318000)
慢性阻塞性肺疾病(简称“慢阻肺”)是一种具有气流受限特征的可以预防和治疗的疾病,任何存在呼吸困难、慢性咳嗽或咳痰并伴有危险因素暴露史的患者,都应考虑慢阻肺的诊断。我国慢阻肺患者人数约1亿[1],其中存在大量的慢阻肺急性加重高风险患者,即每年≥2次急性加重或≥1次因急性加重住院的患者。慢阻肺的急性加重是导致肺功能进行性下降,病死率和病残率升高,生活质量下降的最主要因素。其机制是慢性炎症基础上发生的急性炎症加重,并与气道和全身的炎症增加有关,而睡眠质量下降作为慢阻肺的重要合并症,会影响免疫功能,增加炎症介质,释放过量的应激物质,增加氧化应激和炎症反应,导致患者呼吸道症状加重。此外,慢阻肺易合并睡眠呼吸障碍,最常见的是慢阻肺合并阻塞性睡眠呼吸暂停低通气综合征(OSAHS),被称为重叠综合征。研究表明,OSAHS会加剧气道炎症并导致慢阻肺急性加重[2]。急性加重高风险慢阻肺患者由于反复发作,病情进展迅速,预后不佳,目前对其研究主要集中于白日症状变化,鲜有研究关注其夜间睡眠情况。王玮等[3]观察了30例慢阻肺患者的白日动脉血气及夜间血氧水平,并与正常对照组进行比较,发现慢阻肺患者睡眠时血氧水平较正常人明显下降,尤以快动眼睡眠期显著。申慧等[4]的研究进一步发现与单纯日间血氧饱和度相比,昼夜血氧变异率更能反映慢阻肺患者的病情及预后。睡眠相关低氧血症常见于晚期慢阻肺患者中,即使在清醒时氧合正常也可发生,并对慢阻肺患者产生危害。McNicholas等[5]发现存在低氧血症的慢阻肺患者在急性加重期夜间的死亡风险会更高。这种夜间低氧血症还会导致慢阻肺患者发生肺动脉高压[6]。慢阻肺患者夜间症状、睡眠紊乱的负担可能仍然被低估,而了解其夜间睡眠情况有助于准确评估急性加重高风险患者的病情,为个体化治疗提供帮助。本研究将观察急性加重高风险慢阻肺患者及重叠综合征患者的主、客观睡眠质量,探究合并OSAHS对其睡眠质量的影响,探讨影响主、客观睡眠质量参数的相关因素。
1 资料与方法
1.1 一般资料 选取我院呼吸内科2017年1月至2019年5月住院的急性加重高风险慢阻肺患者26例,其中男21例,女5例,年龄45~77岁,平均(67±8)岁。所有患者均行整夜多导睡眠监测并完成相关问卷。根据整夜睡眠监测结果将患者分为单纯慢阻肺组[12例,其中男9例,女3例,年龄(69±6)岁]和重叠综合征组[14例,其中男12例,女2例,年龄(65±9)岁]。选取同期于本院行多导睡眠监测者27例,根据多导睡眠监测结果分为对照组[13例,其中男6例,女7例,年龄(60±7)岁]和OSAHS组[14例,其中男10例,女4例,年龄(64±4)]岁。去除个人标识信息。
入选标准:符合GOLD2018中慢阻肺诊断标准,且每年≥2次急性加重或≥1次因急性加重住院的符合急性加重高风险慢阻肺的患者;通过多导睡眠监测诊断OSAHS,即每晚7 h睡眠过程中呼吸暂停及低通气反复发作30次以上,或睡眠呼吸暂停低通气指数(AHI)≥5次/h;年龄>40岁;能接受整夜睡眠监测及配合完成问卷调查。
排除标准:合并其他影响患者气流的肺部疾病,合并其他影响睡眠质量的疾病如发作性睡病等,严重的心肌梗死、心律失常、肿瘤(需服用镇痛药物)、严重肝肾功能不全等严重疾病;严重的精神疾患及认知沟通障碍,不能完成问卷患者;服用影响睡眠的药物如镇静催眠药等。
1.2 方法
1.2.1 慢阻肺病情评估 采用慢阻肺自我评估测试(CAT)问卷评价患者日常症状,共含8个项目,每个项目0~5分。各项目分数相加得总分,其分值为0~40分。采用英国医学研究委员会呼吸困难量表(mMRC)评价患者呼吸困难程度:分为0~4级,分数越高呼吸困难越严重。
1.2.2 肺功能测定 采用肺功能仪(Master Screen,德国)进行测定,监测并记录1 s用力呼气容积(FEV1%)、用力肺活量(FVC%)、1 s率(FEV1/FVC%)、用力呼气流量(FEF25%~75%)、最大呼气流速(PEF)、最大呼气流量占正常预计值的百分比(PEF%)。
1.2.3 主观睡眠质量评定 通过匹兹堡睡眠质量(PSQI)量表完成,包括主观睡眠质量、主观睡眠潜伏期、主观睡眠时间、主观睡眠效率、睡眠障碍、催眠药物及日间功能障碍等项目。分数范围0~21分,分数越高,睡眠质量越差。
1.2.4 日间嗜睡评估 采用Epworth嗜睡量表(ESS)评估日间嗜睡情况,分值为0~24分。
1.2.5 多导睡眠监测 对入组者采用多导睡眠仪(Respironics,Alice PDX)行整夜睡眠监测,监测脑电图、下颌肌电图、胸腹运动、鼾声、口鼻气流、血氧饱和度等。监测数据由计算机记录并自动分析,再由同一名医师进行人工校正,记录包括总睡眠时间(TST),慢波睡眠占总睡眠时间的百分比,第1阶段和第2阶段睡眠占总睡眠时间的百分比,快动眼睡眠占总睡眠时间的百分比,睡眠潜伏期,睡眠效率,觉醒次数,入睡后清醒时间、AHI、夜间最低血氧饱和度、夜间平均血氧饱和度、氧饱和度≤90%的时间占总监测时间的百分比(SIT90%)。通过此结果进行客观睡眠质量评定和OSAHS诊断。

2 结果
2.1 各组间一般情况的比较 与对照组相比,单纯急性加重高风险慢阻肺患者ESS评分明显升高(P<0.05)。见表1。

表1 一般临床资料
2.2 各组间PSQI评分结果、多导睡眠监测结果的比较 与对照组相比,单纯慢阻肺组PSQI评分升高,重叠综合征组较OSAHS组PSQI评分明显升高,提示慢阻肺的存在影响主观睡眠质量。从客观评估角度来看,单纯慢阻肺组较对照组总睡眠时间缩短,睡眠效率下降,觉醒次数、睡眠期总觉醒时间增多。重叠综合征组的慢波睡眠时间也明显减少,见表2。

表2 整夜睡眠监测结果
2.3 急性加重高风险慢阻肺患者主、客观睡眠参数相关因素分析 将PSQI、总睡眠时间、睡眠效率、睡眠潜伏期、觉醒次数、睡眠期总觉醒时间、第1阶段和第2阶段睡眠(%TST)、快动眼睡眠(%TST)、慢波睡眠(%TST)分别与年龄、性别、体质指数、过去1年急性加重次数、FEV1%、FEF25%~75%、PEF%、CAT、mMRC、ESS、AHI、夜间平均血氧饱和度进行相关分析,发现PSQI评分与过去1年急性加重次数、呼吸困难指数、ESS评分呈正相关,睡眠期总觉醒时间与CAT、mMRC评分呈正相关,快动眼睡眠占总睡眠时间百分比与FEF25%~75%、PEF%,慢波睡眠占总睡眠时间百分比与AHI呈负相关,见表3。
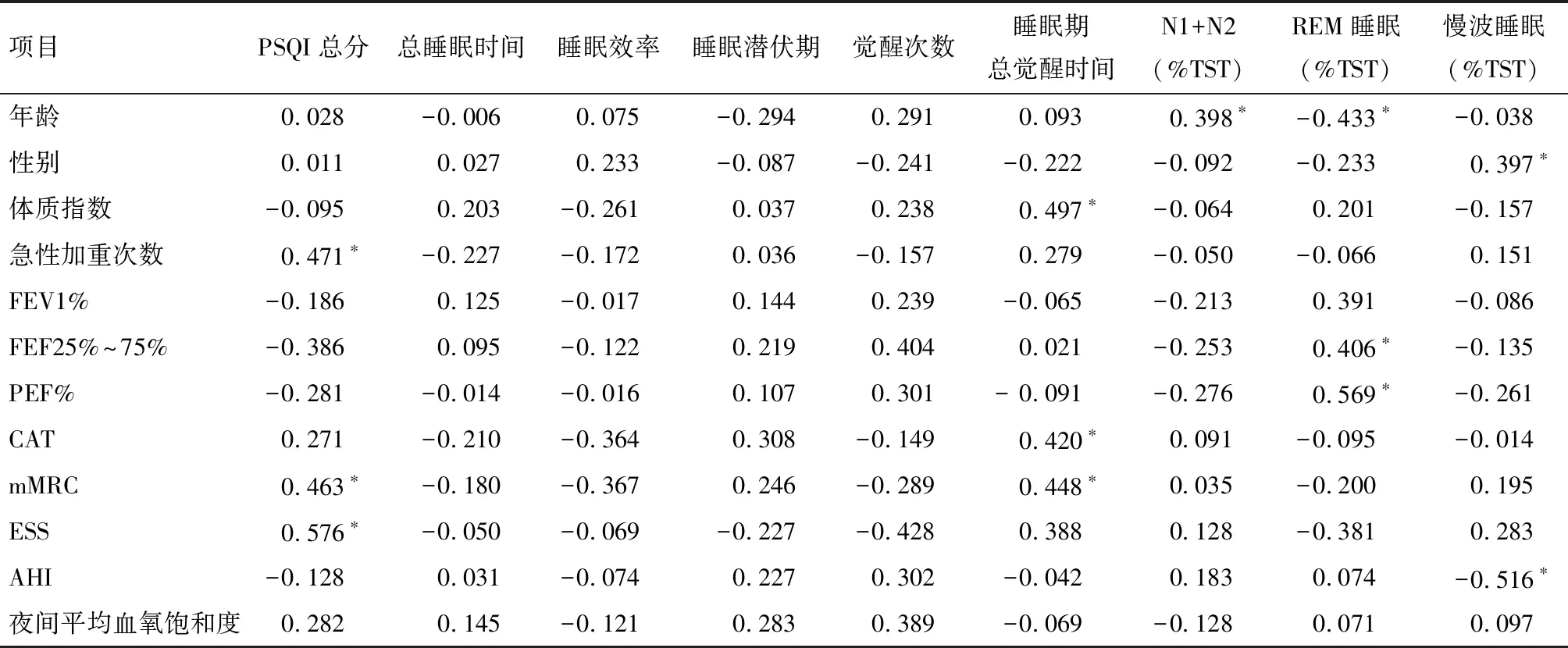
表3 急性加重高风险慢阻肺患者主、客观睡眠参数相关因素分析 r值
3 讨论
慢阻肺患者经常合并睡眠障碍,出现睡眠质量下降。Phillips等[7]对15例稳定期男性慢阻肺患者实施睡眠剥夺并与自身对照后发现睡眠缺失会导致其1 s内FVC%和FEF25%~75%减少。睡眠质量受损会增加慢阻肺患者高血压、糖尿病、心血管疾病等合并症的风险[8],还会造成慢阻肺患者认知功能下降,抑郁水平增加,使其经历更多的疲劳和嗜睡,进一步影响其健康状态、日间功能、生活质量以及治疗依从性[9],甚至造成慢阻肺的急性加重,增加死亡风险。然而临床上慢阻肺患者睡眠质量下降、夜间睡眠障碍的发生并未引起相应重视,Ding等[10]的研究表明,除了治疗日间症状,还需解决慢阻肺患者夜间睡眠障碍,才能真正改善患者的生活质量。Sanders等[11]分析了1 138例伴有轻度气流阻塞的社区稳定期慢阻肺患者的多导睡眠监测和肺功能数据,发现这些患者和健康对照组在睡眠质量和结构方面仅存在微小差异,而Valipour等[12]分析了52例轻中度稳定期慢阻肺患者较对照者睡眠时长明显缩短,睡眠效率显著下降。Akinci等[13]对1 117例中重度慢阻肺患者入组时、入组后3个月、入组后12个月行PSQI量表调查,发现中重度慢阻肺患者合并睡眠质量下降的概率较高,半数患者的睡眠质量在12个月内保持不变。然而现有研究多从不同程度稳定期患者着手,未有针对急性加重高风险患者睡眠质量的研究,故本研究以慢阻肺急性加重高风险患者为研究对象,探究其睡眠质量情况及相关影响因素。研究结果显示慢阻肺急性加重高风险患者的主、客观睡眠质量均较差,单纯慢阻肺患者主要表现为总睡眠时间减少,客观睡眠效率减低,觉醒次数增多,入睡后清醒时间增加,且伴有日间嗜睡。可能与慢阻肺急性加重高危患者急性发作频率较高、咳嗽咳痰、呼吸困难症状较重、气流受限严重、治疗药物如肾上腺皮质激素的使用等有关,一旦合并OSAHS,睡眠质量进一步下降,表现为客观入睡潜伏期延长,觉醒次数增多,睡眠障碍更严重,甚至睡眠结构发生改变,慢波睡眠减少。
目前研究认为,慢阻肺患者的咳嗽、咳痰、呼吸困难等夜间呼吸道症状、高碳酸血症、低血氧饱和度等都可对睡眠质量产生影响[14]。本研究发现呼吸困难指数越高,PSQI分值越高,即慢阻肺患者睡眠质量越差;呼吸困难等级越重,患者入睡后清醒时间越长,可能是因为外周气道堵塞,呼气困难,患者机体过度充气,增加的吸气负荷增加了呼吸功,并通过刺激胸壁和下呼吸道的机械感受器引发觉醒[15]。此外,本研究还显示CAT评分与慢阻肺患者入睡后清醒时间呈正相关,表明慢阻肺患者日间症状确实可影响其睡眠情况。对于急性加重高风险的慢阻肺患者,相关分析显示除了呼吸困难指数,过去一年急性加重次数、ESS评分也与慢阻肺急性加重高风险患者PSQI总分相关。一项加拿大研究对574例慢阻肺患者行PSQI量表调查,并随访记录之后18个月的急性加重次数,结果显示睡眠质量差可增加慢阻肺患者18个月后病情恶化的风险[16]。Ajili等[17]发现合并睡眠障碍的慢阻肺患者平均每年急性加重次数较未合并睡眠障碍者增多,可能与睡眠障碍本身可以增加气流阻塞程度,从而导致急性加重有关。慢性睡眠缺失会增加炎症标志物水平,还可引起免疫缺陷,每晚睡眠不超过5 h或有睡眠障碍的成年人更易患普通感冒和感染性疾病(包括流感、肺炎和耳部感染)[18],因此,慢阻肺患者合并睡眠质量下降可能更易出现急性加重。慢阻肺患者在急性加重状态时气道病原体负荷高,会使其具有更高水平的促炎细胞因子,而全身炎症水平增加与氧化应激可激活交感神经进而影响睡眠[19]。急性加重还可能通过加重症状,加重低氧血症和高碳酸血症,增加药物如茶碱、激素的使用来影响睡眠质量。因此睡眠质量下降与慢阻肺急性加重两者相互促进,形成恶性循环。
本结果还显示ESS评分与急性加重高风险慢阻肺患者PSQI总分密切相关。临床上,医生可通过ESS量表筛查睡眠质量下降及合并睡眠障碍的慢阻肺患者并加以适当干预,以改善患者生活质量。目前慢阻肺患者睡眠障碍与气流阻塞是否相关存在争议。Krachman等[20]调查25例重度慢阻肺患者的睡眠质量情况,发现气流阻塞与睡眠质量相关,而In等[21]的研究认为慢阻肺患者的睡眠障碍独立于气流受限,与气流阻塞无关。本研究数据表明快动眼睡眠占总睡眠时间百分比与FEF25%~75%、PEF%正相关,可能因为慢阻肺患者外周气道堵塞、峰流速下降,导致慢阻肺患者出现呼吸短促,激活网状激活系统,释放儿茶酚胺,引起睡眠结构异常[22],而睡眠质量与FEV1%、FVC%无关,这与Chang等[23]、Cleutjens等[24]关于睡眠质量与肺功能关系的研究一致。
慢阻肺急性加重的科学认识和规范治疗是延缓疾病进展的重中之重。本研究以急性加重高风险慢阻肺患者为目标人群,发现其主、客观睡眠质量下降,易合并OSAHS,一旦两者并存,睡眠质量进一步下降,且睡眠结构受损,提示临床医生应对这类患者予以足够的关注,应早期识别慢阻肺患者的睡眠异常并进行适当干预,以改善患者的生命质量和预后。

