轮状病毒减毒活疫苗感染性滴度一步法RT-qPCR检测方法的建立*
杜加亮,刘悦越,张 永,赵荣荣,赵一荣,韩 菲,刘 艳
(中国食品药品检定研究院肠道病毒疫苗室,北京 102629)
轮状病毒是世界范围内导致5岁以下儿童严重腹泻的最主要病原体。自2001年轮状病毒疫苗问世以来,全球已经有100多个国家和地区在使用。在疫苗问世之前,轮状病毒相关胃肠炎(RVGE)在5岁以下儿童中每年导致超过50万死亡病例[1]。虽然疫苗的问世减少了死亡病例,但是在低收入国家,RVGE每年仍然导致超过20万死亡病例[2]。轮状病毒疫苗可有效降低RVGE的负担,因此,对疫苗的评价显得尤为重要,尤其是多价疫苗的鉴别和效力评价。常用的检测方法为使用特异性抗体,通过荧光灶试验(FFA)、空斑试验或细胞培养半数感染量(CCID50)等来实现[3-5],但是这些方法均涉及特异性抗体制备困难、操作复杂且要求高、耗时长、主观性大、通量小等不足,不利于多价疫苗产品的精准配制和生产全过程的质量控制。相比之下,基于核酸的定量检测方法具有试剂材料可及性强、可操作性强、一致性高、耗时短、通量大、结果更加客观等优点,已经成功应用于甲型肝炎、腮腺炎病毒疫苗的滴度检测[6-7]。MSD RotaTeq使用的就是基于细胞感染的核酸定量检测方法[8],但由于疫苗毒株不同,基因序列不同,细胞感染特点也不同,该方法需要针对不同疫苗毒株进行不同设计。轮状病毒流行株因地区和年份而不同,G1、G2、G3、G4、G9型构成了我国的主要流行株[9]。国内某企业生产的五价人-牛重配轮状病毒减毒活疫苗涵盖了以上5种主要流行株。本研究针对该疫苗,参考现有方法[10],设计一步法反转录实时荧光定量聚合酶链反应(RT-qPCR),用于多价轮状病毒疫苗的鉴别和效力评价。
1 材料与方法
1.1材料与仪器 单价轮状病毒参考品由国内某企业提供,病毒滴度分别为G1:1.04×107CCID50/mL,G2:1.05×107CCID50/mL,G3:1.76×107CCID50/mL,G4:3.96×107CCID50/mL,G9:3.45×107CCID50/mL。一步法荧光定量PCR试剂盒(RR064)和一步法反转录PCR试剂盒(RR057)购自TaKaRa公司,QIAamp Viral RNA Mini Kit购自QIAGEN公司。细胞培养液为Gibco RPMI Medium 1640(1×)+1%(v/v)谷氨酰胺+1%(v/v)双抗+10%(v/v)胎牛血清。病毒稀释液为Gibco RPMI Medium 1640(1×)+1%(v/v)谷氨酰胺+1%(v/v)双抗+5 μg/mL胰酶。荧光定量PCR仪(7500)购自Thermofisher Scientific公司;恒河猴肾细胞MA104为实验室保存。
1.2引物探针设计和质粒参考品制备 分别吸取200 μL G1、G2、G3、G4和G9型单价病毒原液,按照QIAGEN QIAamp Viral RNA Mini Kit试剂盒说明书的步骤提取病毒RNA。利用通用型VP7引物VP7-F和VP7-R扩增各型单价病毒原液的VP7基因,见表1。目的条带经1%琼脂糖凝胶电泳鉴定回收后,与pEASY-T3载体连接。转化DH5a大肠埃希菌感受态后,经过蓝白斑筛选、PCR鉴定、酶切鉴定和测序验证。测序结果经序列比对后,选择型别间差异明显的区段进行引物和探针设计(表1),并由生工生物工程(上海)有限公司合成。质粒纯度符合要求(A260/A280为1.8~2.0)后作为备用参考品原液。质粒拷贝数(copy/μL)按照以下公式计算:(6.02×1012)×(质粒浓度ng/μL×10-9)/(质粒长度bp×660)。本研究中使用稀释至107、106、105、104、103、102copy/μL的质粒作为参考品。

表1 本研究中使用的探针/引物信息
1.3细胞培养和病毒接种 取生长密度合适的MA104细胞,消化制成浓度约为1.2×106个细胞的悬液,铺96孔细胞培养板,每孔200 μL,置于37 ℃ 5%CO2培养箱中培养3~5 d后使用。使用病毒稀释液进行待测病毒稀释,置于37 ℃培养箱中活化60 min。取出预先铺有MA104细胞的96孔细胞培养板,弃掉细胞维持液。把活化后的病毒加到相应的细胞培养孔中,每孔40 μL,每个稀释度4孔,置于37 ℃ 5%CO2培养箱中培养18~20 h。每孔中加入4.5% Triton X-100工作液10 μL,置于-70 ℃放置至少1 h。
1.4RT-qPCR 感染板室温放置20 min直至解冻,1 000 r/min振荡10 s,1 000 r/min离心1 min,从每孔中吸取15 μL溶液进行40倍稀释作为RT-qPCR的模板。RT-qPCR反应体系为12.5 μL Buffer、0.5 μL反转录酶、0.5 μL Taq酶、上下游引物(10 μmol)各0.4 μL、探针(10 μmol)0.4 μL、5 μL模板、加水补足至25 μL。反应条件为42 ℃ 5 min;95 ℃ 15 s;95 ℃ 5 s,60 ℃ 34 s(收集荧光),40个循环。结果解释:Ct值≤35且扩增曲线呈S型为阳性,否则为阴性。
1.5特异性检测 每个血清型毒株特异性引物/探针对每个重配株的单价培养物进行RT-qPCR来确定方法的特异性。每对引物/探针都应选择性地使G1、G2、G3、G4和G9重配株的VP7基因片段序列扩增。所有引物/探针只能对特异型扩增,对其他型无扩增或选择性差异≥210倍。将灭活的其他肠道病毒[柯萨奇病毒A(CA16)、肠道病毒71型(EV71)和脊髓灰质炎病毒]进行RT-qPCR,Ct值≥35或无扩增。
1.6线性和范围检测 将单价轮状病毒参考品以1∶15的稀释倍数首次稀释,然后以2.5倍倍比稀释4种稀释度,以基于细胞感染的RT-qPCR进行轮状病毒体外感染效力测定。以Ct值对被测物浓度制图,用最小二乘法进行线性回归。回归方程的相关系数(r2)≥0.950 0。确定Ct值与被测物浓度呈线性关系的浓度范围。
1.7重复性检测 使用上述稀释倍数的标本,采用RT-qPCR分析病毒感染效力。使用5个型的轮状病毒特异性引物探针对每个型进行定量检测,试验重复3次,每次试验4个重复,每个型的每个稀释度共得到12个Ct值,其变异系数(CV)不超过10%。

2 结 果
2.1特异性 每个血清型毒株特异性引物/探针对每个重配株的单价培养物进行RT-qPCR来确定方法的特异性。每对引物/探针都应选择性地使G1、G2、G3、G4和G9重配株的VP7基因片段序列扩增。所有引物/探针对其特异型扩增的Ct值与其对其他型扩增的Ct值比较,选择性差异≥210倍。对其他型扩增的Ct值≥35或无扩增(图1)。

图1 特异性扩增曲线

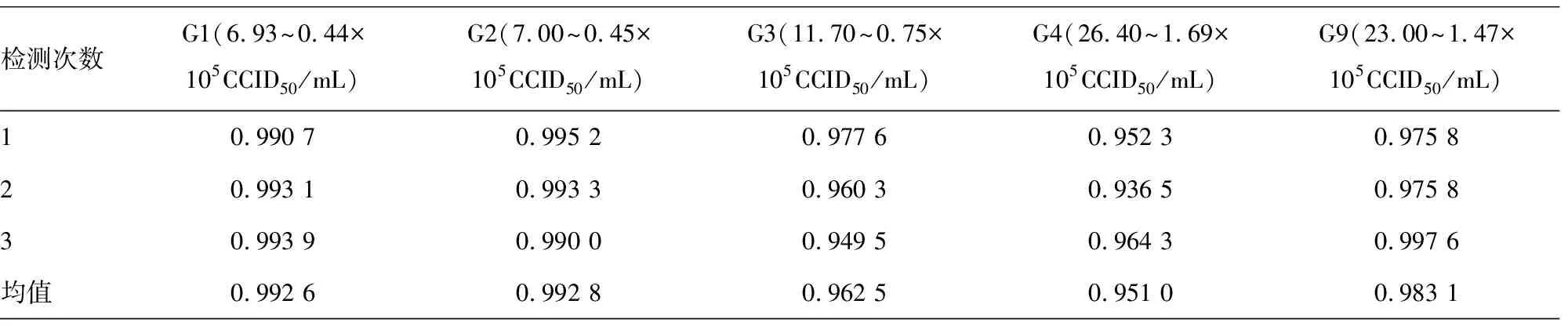
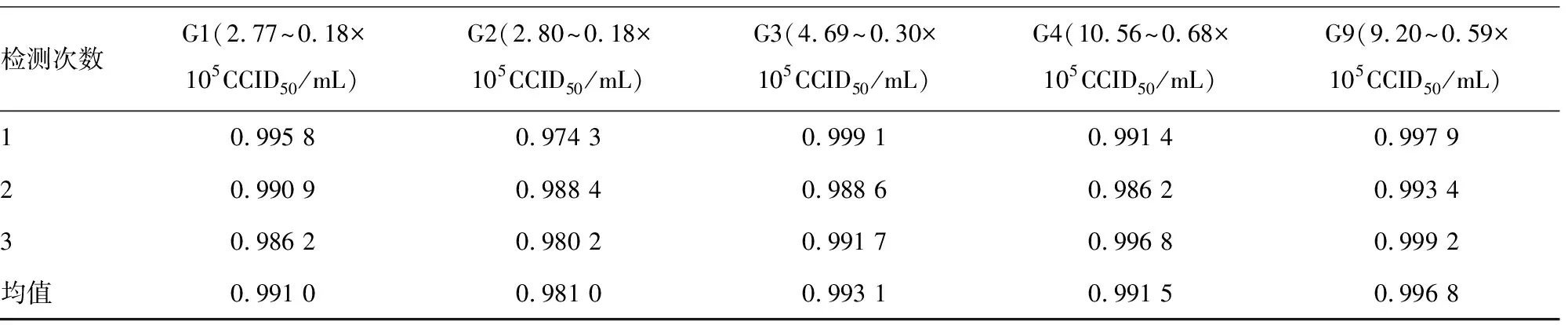
表2 不同稀释倍数和Ct值的线性相关系数(r2)
检测次数G1(6.93~0.44×105CCID50/mL)G2(7.00~0.45×105CCID50/mL)G3(11.70~0.75×105CCID50/mL)G4(26.40~1.69×105CCID50/mL)G9(23.00~1.47×105CCID50/mL)10.990 70.995 20.977 60.952 30.975 820.993 10.993 30.960 30.936 50.975 830.993 90.990 00.949 50.964 30.997 6均值0.992 60.992 80.962 50.951 00.983 1
检测次数G1(2.77~0.18×105CCID50/mL)G2(2.80~0.18×105CCID50/mL)G3(4.69~0.30×105CCID50/mL)G4(10.56~0.68×105CCID50/mL)G9(9.20~0.59×105CCID50/mL)10.995 80.974 30.999 10.991 40.997 920.990 90.988 40.988 60.986 20.993 430.986 20.980 20.991 70.996 80.999 2均值0.991 00.981 00.993 10.991 50.996 8
2.2线性和范围 当使用全部5种稀释度的检测数值进行计算时,G1、G2、G3、G4、G9型的稀释倍数和Ct值的线性r2为0.957 6~0.993 5;当使用前4种稀释度的检测数值进行计算时,G1、G2、G3、G4、G9型的稀释倍数和Ct值的线性r2为0.951 0~0.992 8;当使用后4种稀释度的检测数值进行计算时,G1、G2、G3、G4、G9型的稀释倍数和Ct值的线性r2为0.981 0~0.996 8(表2)。
2.3重复性 如表3所示,G1、G2、G3、G4、G9型重配株第1、2、3天重复检测结果的CV值为0.65%~6.71%、0.72%~10.10%、0.05%~8.10%,不同日间结果的CV值为2.05%~13.54%,一般认为重复性尚好(CV<15%)。经统计学分析,同一日重复检测结果和日间结果比较,差异均无统计学意义(P=0.917、0.746)。不同稀释度间的检测结果差异有统计学意义(P<0.001),说明本研究中选择的稀释度可以有效反映不同感染剂量的病毒复制。不同血清型之间的检测结果差异无统计学意义(P=0.345),说明各个血清型的疫苗毒株感染MA104细胞后具有相似的复制特征。

表3 重复性检测结果
3 讨 论
对于经黏膜途径感染的病毒来说,与天然病毒具有相同感染和复制方式的减毒活疫苗仍然是最有效的激发机体免疫保护的方式[11]。对于其他可经传统方法制备的灭活病毒疫苗来说,生产工艺中也必然少不了存在活病毒的灭活前阶段[12]。因此,开发快速、简便的滴度检测方法显得尤为重要。本研究初步建立了一种快速、灵敏、特异的检测多价轮状病毒减毒活疫苗病毒滴度的技术,该方法对其他肠道病毒(CA16、EV71和脊髓灰质炎病毒)无扩增,特异性符合要求;当使用前4种稀释度的检测数值进行计算时,5种型别的稀释倍数和Ct值的线性r最高,均在0.980 0以上,故选择前4种稀释度作为该方法的线性和范围;重复性检测结果显示,该方法在同一工作日内和不同工作日间均能得到差异无统计学意义的结果,重复性符合要求;不同稀释度和不同血清型之间的统计学分析结果也显示该方法在线性和范围内可有效反映不同病毒株的复制情况。因此,该方法具有一定的推广应用价值。
另外,轮状病毒流行株因地区和年份而不同,G1、G2、G3、G4、G9型构成了我国的主要流行株[11],G8型也时有检出[12]。我国多家企业都在进行多价轮状病毒疫苗的研发。多价轮状病毒疫苗是以动物来源的轮状病毒为母本,是将其主要抗原成分VP7和/或VP4替换成人源轮状病毒的相应组分制备而成的。正是多价疫苗各个毒株之间的这种微小差异(主要抗原成分不同),使多价疫苗的鉴别和效力检测需要用到型别特异性单克隆抗体[4-6]。但是基于特异性单克隆抗体的检测方法存在多种影响检测结果和操作过程的因素,不利于多价疫苗产品的精准配制和生产全过程的质量控制。与基于特异性单克隆抗体的检测方法相比,一步法荧光定量PCR不仅缩短了检测时间,而且极大地减少了操作步骤,使检测结果具有更好的一致性和客观性。另外,该方法还具有以下2个方面的优势,一是该方法建立在细胞感染的基础上,疫苗中的活病毒得以复制和扩增,而死病毒无法复制,最终检测结果能够客观反映病毒滴度;二是整个操作过程省去了核酸提取的步骤,避免了核酸提取步骤中存在的核酸损失情况造成的误差。
本研究在进行重复性验证时,临时使用了质粒参考品,但是在正式使用过程中,需要制备一批性质均一,且能长期稳定保存的标准疫苗作为标准品对待测品进行赋值[8-9],从而可以在疫苗生产工艺的各个环节(包括病毒液的收获时间、半成品及成品的配制等)进行生产指导和质量控制。
4 结 论
对于病毒疫苗的质量控制来说,滴度或者效价的检测是最重要的指标。RT-qPCR的建立和后续的适用性研究将为滴度或者效价检测提供简便、快速的方法,将更加有利于不同企业生产的相同品种的病毒疫苗之间结果的可比性研究。

