HPLC-ELSD 法同时测定康寿丸人参皂苷Rg1、Re、Rb1 的含量
黄天山,杨洁瑜,顾利红
广州市药品检验所,国家药品监督管理局中成药质量评价重点实验室,广州,510160
康寿丸质量标准目前收载于《卫生部药品标准》中药成方制剂第十一册,处方由何首乌、人参、熟地黄、地骨皮等八味药组成,主要用于气血两虚,精血两虚,精血不足导致的身体瘦弱,神疲乏力,眩晕健忘,失眠多梦等症。现行质量标准中仅对人参进行薄层鉴别[1],为了更好地控制产品质量,保证临床疗效,拟对方中人参进行含量测定研究。《中国药典》多采用HPLC-UV 法测定人参中人参皂苷Rg1、人参皂苷Re 和人参皂苷Rb1的含量,分析时间较长,效率较低[2-4]。本文建立了HPLC-ELSD 法同时测定康寿丸中人参皂苷Rg1、人参皂苷Re 和人参皂苷Rb1含量的方法,为康寿丸的质量控制提供了实验依据。
1 仪器与试剂
万分之一电子天平(瑞士梅特勒托利多公司);安捷伦1260 高效液相色谱仪(配置四元泵、自动进样器、柱温箱和Alltech 3300 蒸发光散射检测器),OpenLab CDS 色谱工作站。
人参皂苷Rg1对照品(批号为110703-201933,含量以93.4%计);人参皂苷Re 对照品(批号为110754-201827,含量以93.4%计);人参皂苷Rb1对照品(批号为110704-202028,含量以93.1%计);均由中国食品药品检定研究院提供。乙腈为色谱纯(德国 Merck),水为超纯水,其他试剂均为分析纯(广州化学试剂厂)。康寿丸样品共10 批,分别由企业A 和企业B 提供。
2 方法与结果
2.1 色谱条件色谱柱:Waters CORTECS T3 C18(柱长150 mm,内径4.6 mm,粒径2.7 μm),以乙腈为流动相A,水为流动相B,按下表中的规定进行梯度洗脱;采用蒸发光散射检测器,漂移管温度为50 ℃,载气流速为1.6 L/min,倍增系数为4。理论板数按人参皂苷Rg1峰计算不低于10 000,与相邻色谱峰的分离度不低于1.5。

表1 梯度洗脱程序
2.2 对照品溶液的制备取人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1对照品适量,精密称定,加甲醇制成每1 mL 含人参皂苷Rg1180 μg、人参皂苷Re80 μg、人参皂苷Rb1100 μg 的混合溶液,即得。
2.3 供试品溶液及阴性对照溶液的制备取本品粉末(过四号筛)约3.5 g,精密称定,置锥形瓶中,加乙醚50 mL,加热回流1 h,放冷,滤过,弃去乙醚液,药渣挥干乙醚,连同滤纸移至锥形瓶中,精密加入水饱和正丁醇50 mL,称定重量,加热回流1 h,放冷,再称定重量,用水饱和正丁醇补足减失的重量,摇匀,滤过,精密吸取续滤液25 mL,蒸干,残渣加甲醇溶解,转移至5 mL 量瓶中,加甲醇稀释至刻度,摇匀,即得。
按处方取不含人参的各药味饮片,经粉碎按处方量及制法混合制成阴性样品,同供试品溶液的制备方法制备人参阴性对照溶液。
2.4 专属性试验分别精密吸取供试品溶液和人参阴性对照溶液各2 μL,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1混合对照品溶液各5 μL,依法测定,记录HPLC 色谱图,见图1。结果显示,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1与其他组分峰的分离度均大于1.5,人参阴性对照溶液色谱中在与人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1对照品色谱峰相应的位置上,未见有色谱峰,说明阴性样品无干扰,方法具有专属性。

图1 HPLC色谱图
2.5 线性关系考察取人参皂苷Rg1对照品8 mg、人参皂苷Re 对照品8 mg、人参皂苷Rb1对照品10 mg,精密称定,置10 mL 量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得对照品溶液①。精密吸取对照品溶液①5.0 mL 置10 mL 量瓶中,加甲醇稀释至刻度,摇匀,即得对照品溶液②。精密吸取对照品溶液②5.0 mL 置10 mL 量瓶中,加甲醇稀释至刻度,摇匀,即得对照品溶液③。精密吸取对照品溶液③5.0 mL 置10 mL 量瓶中,加甲醇稀释至刻度,摇匀,即得对照品溶液④。精密吸取对照品溶液④4.0 mL置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得对照品溶液⑤。精密吸取对照品溶液⑤5.0 mL置10 mL 量瓶中,加甲醇稀释至刻度,摇匀,即得对照品溶液⑥。分别精密吸取对照品溶液①~⑥各4 μL 进样,依法测定,以峰面积积分值A 对数值为纵坐标,进样量C(μg)对数值为横坐标,绘制标准曲线,得到回归方程和相关系数,见表2。表明人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1线性关系良好。
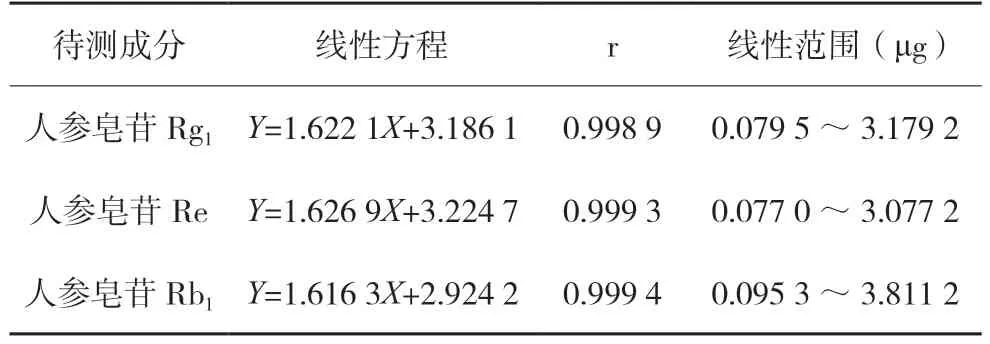
表2 人参皂苷Rg1、Re、Rb1线性考察结果(n=6)
2.6 精密度考察精密吸取对照品溶液(浓度:人参皂苷Rg185.27 μg/mL;人参皂苷Re 78.27 μg/mL;人参皂苷Rb196.03 μg/mL),连续进样6 次,记录峰面积,计算RSD。结果:人参皂苷Rg1RSD为1.9%,人参皂苷Re RSD 为1.9%,人参皂苷Rb1RSD 为1.6%,说明仪器的精密度良好。
2.7 重复性试验取同一批(批号:B07009)样品,精密称取6 份,依法制备供试液,进样测定,结果人参皂苷Rg1平均含量为0.29 mg/g,RSD 为2.2%;人参皂苷Re 平均含量为0.33 mg/g,RSD 为1.9%;人参皂苷Rb1平均含量为0.43 mg/g,RSD 为1.1%,表明本方法的重复性良好。
2.8 稳定性试验取同一份供试品溶液(批号190901),在室温放置0、4、8、12、16、20、24 h后分别进样,依法测定,人参皂苷Rg1含量平均值为0.138 mg/g,RSD 为1.5%;人参皂苷Re 含量平均值为0.194 mg/g,RSD 为1.9%;人参皂苷Rb1含量平均值为0.280 mg/g,RSD 为1.5%。表明供试品溶液在24 h 内测定结果稳定。
2.9 加样回收试验取已知含量(批号:B07009)的样品6 份,每份约1.75 g,精密称定,各精密加入混合对照品溶液(人参皂苷Rg1:0.255 3 mg/mL;人参皂苷Re:0.315 1 mg/mL;人参皂苷Rb1:0.402 8 mg/mL的混合溶液)2 mL,在水浴上挥干溶剂,自“加乙醚50 mL,”起同法制成供试品溶液,依法测定,人参皂苷Rg1、Re、Rb1的平均回收率分别为99.8%、100.9%、99.8%,RSD 分别为1.0%、1.7%、1.3%。
2.10 样品测定取所收集的A、B 两家企业共10批样品,按“2.3”项下方法制备供试品溶液,依法测定,计算结果见表3。
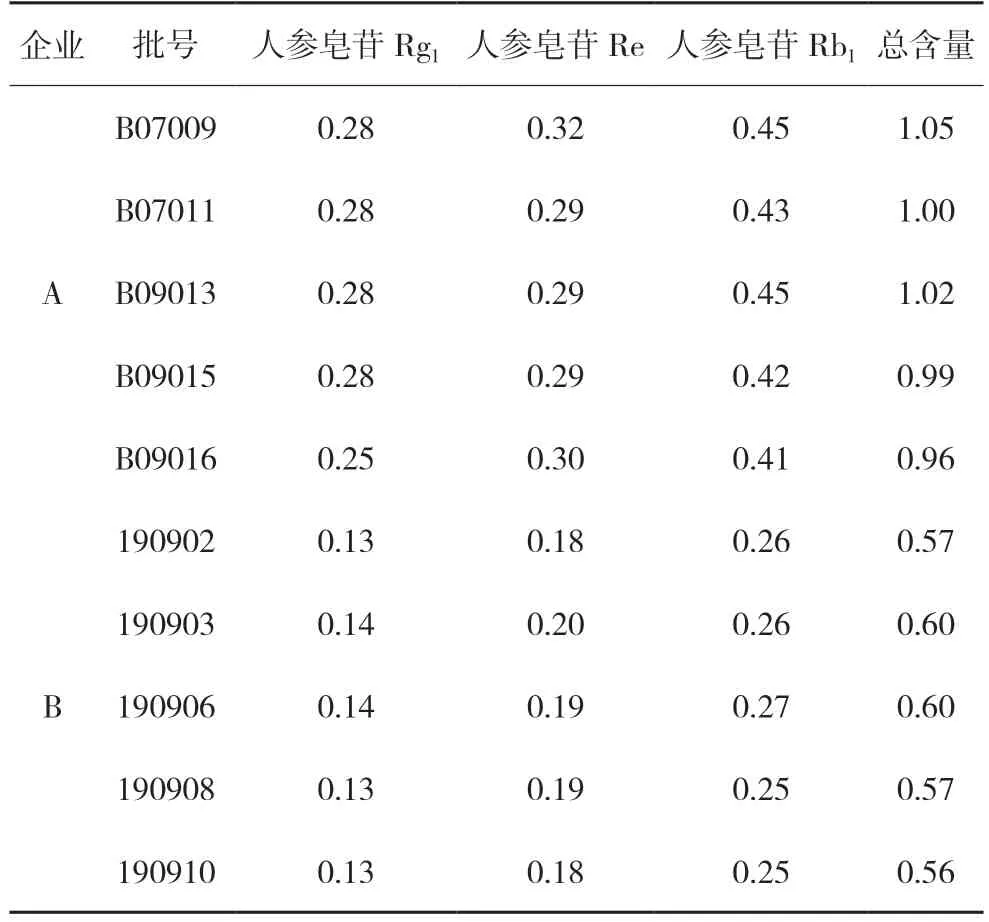
表3 人参皂苷Rg1、Re、Rb1含量测定结果 mg/g
3 讨论
康寿丸组方复杂,若选择HPLC-UV 法,检测波长常为203 nm,属于紫外末端吸收,天冬、麦冬中的皂苷类成分及杂质会产生干扰,不宜选择紫外检测器。蒸发光散射检测器作为一款通用的检测器,无紫外末端吸收的干扰,有广泛的梯度和溶剂兼容性,图谱基线平稳[5],适用于人参皂苷类成分的检测[6-9],故本实验采用HPLC-ELSD 法对康寿丸中的人参皂苷类成分进行分析。
比较了三氯甲烷、二氯甲烷和乙醚的脱脂效果,发现不同溶剂脱脂后制备的供试液各液相色谱图在目标峰(人参皂苷Rg1、Re、Rb1)附近杂质干扰无明显差异,乙醚毒性较小,从绿色环保考虑,采用了乙醚除脂。同时还比较了甲醇、正丁醇和水饱和的正丁醇三种溶剂的提取效果,发现水饱和的正丁醇提取效果最好,故选择以水饱和的正丁醇作为提取溶剂。最后还对提取方式与时间进行了研究,发现回流提取比超声提取效果好,回流60 min 能最大限度地提取完全。
本方法采用了可以在普通液相使用的微粒径色谱柱,显著缩短了人参皂苷类成分的分析时间,比较了样品在不同色谱柱(Waters CORTECS T3 C18、YMC Meteoric C18、Agilent InfinityLabPoroshell SBC18)和不同柱温(25 ℃、30 ℃、35 ℃)对分离效果和分析时间的影响,发现不同色谱柱和不同柱温均能获得良好的分离度,含量测定结果无明显差异。
本文对收集到的两家企业共10 批康寿丸样品进行了人参三个皂苷成分的含量测定,结果发现两家企业的人参皂苷含量差异较大,同一企业的不同批次样品含量差异不大,表明两个企业的投料来源比较稳定,但人参原药材质量存在一定差异。

