影响冷榨核桃油货架期内稳定性因素的研究
李亚萍
(安康学院 化学化工学院,陕西 安康 725000)
研究发现, 在常见的植物油中,核桃油中的α-亚麻酸占比最高,同时富含亚油酸,这两种物质在人体内可衍生出脑黄金DHA。核桃油中还含有黄酮和磷脂,黄酮可以缓解头痛、耳鸣等病状;磷脂具有促进造血、保护脑神经的功能[1~2]。核桃油良好的生物活性, 使其在食品、药品以及化工等领域逐步被广泛应用,前景广阔。采用冷榨工艺提取核桃油,更有利于保持它的生物活性,但会使核桃油中形成一定量的水包油乳状液[3],而水包油乳状液的不稳定,使得核桃油整体稳定性降低,易产生浪费变质而浪费。所以本论文利用乳状液粒径分布及其变化来研究几种因素对水包核桃油乳状液货架期内稳定性的影响, 为核桃油的储存和应用提供理论依据。
1 材料与方法
1.1 仪器试剂及材料
KH-250DE数控超声波清洗器,昆山禾创超声仪器有限公司;101-2AB电热鼓风干燥箱,天津市泰斯特仪器有限公司;MODEL0406-1低速离心机,上海医疗器械有限公司手术器械厂;DK-2000-ШL电热恒温水浴锅,天津市泰斯特仪器有限公司;UV-1700A紫外分光光度计,上海奥析科学仪器有限公司。试验所用试剂均为分析纯。冷榨核桃油由陕西烨林现代生态农业发展有限公司提供。
1.2 试验方法
1.2.1 水包核桃油乳状液的配制 利用电子分析天平,在50 mL水中称取0.5 g乳化剂,采用磁力搅拌仪搅拌3 min速度为2 000 r·min-1,使水与表面活性剂充分混合。取500 mL烧杯加1.0 g油及表面活性剂水溶液,加水至500 mL,使用磁力搅拌器2 000 r·min-1的转速对其进行乳化剪切5 min,高压均质两次,得到水包核桃油乳状液。
1.2.2 油浓度—吸光度标准曲线的制作 准确称取0.1 g核桃油,用石油醚定容至100 mL,配成标准溶液,浓度为1mg·mL-1。放在冰箱中备用。取0、2、4、6、8 mL标准溶液,用石油醚定容至100 mL,最终质量浓度分别为0、200、400、600、800 ug·mL-1。测定配制的核桃油标准液在波长为510 nm时的吸光度,制作标准曲线。
1.2.3 水包油乳状液稳定性的表征 采用高速离心分析法,该方法利用高速离心作用(2000 r·min-1),加快水包核桃油乳状液中油滴上浮和水相下沉降速度,从而达到快速分析乳状液稳定性的目的[4,5],以稳定性性系数表示不同因素对乳状液稳定性的影响程度。乳状液的稳定系数=A1/A2(1)
式中 A1——离心后乳状液吸光度值
A2——离心前乳状液吸光度值
1.3 影响水包核桃油乳状液稳定性的单因素试验
1.3.1 温度的影响 取1.5 g冷榨核桃油,置于250 ml的烧杯中,添加1.0 g十二烷基苯磺酸钠,加蒸馏水至250 mL,采用磁力搅拌仪乳化剪切5 min、剪切速度为2 000 r·min-1,密封避光静置。将配置的乳状液分别放置在不同温度(0℃、20℃、25℃、30℃、40℃)下,静置1 d、3 d、7 d、15 d、30 d后分别测定其吸光度。取不同温度下的乳状液10 mL于离心管中,以2 000 r·min-1离心5 min后(后期离心速度、离心时间均相同),取下层液于比色皿中,测定吸光度值A。测定吸光度后根据公式(1)计算乳状液的稳定性系数。
取静置后的下层液体于分液漏斗中,用石油醚对下层液中的核桃油进行萃取,测量其吸光度A。测量吸光度后根据公式(2)计算油浓度五组不同温度下核桃油乳状液的油浓度(mg·L-1)。
1.3.2 乳化剂种类的影响 试验选用三种不同的乳化剂:十二烷基苯磺酸钠、十六烷基三甲基溴化铵和乳清分离,实验开始时使用不同的乳化剂配制核桃油乳状液,取不同乳化剂各1 g,核桃油1.5 g,500 mL水,剪切离心后,乳状液的静置时间同1.3.1。测定吸光度后计算其稳定系数。
1.3.3 乳化剂浓度的影响 按1.3.2的结论,本次试验的乳化剂选用十二烷基苯磺酸钠。
取三个500 mL烧杯,分别加入核桃油1.5 g,加入浓度为0.05%、0.10%、0.50%的乳化剂,剪切离心后,静置时间同上。测量其吸光度再计算乳状液稳定系数。
1.3.4 水相pH的影响 取三个500 mL烧杯,分别加入1.5 g核桃油、1.0 g十二烷基苯磺酸钠,依次加蒸馏水调节pH为4.0、7.0和10.0。剪切离心静置参数均同上,测量其吸光度,计算稳定性系数。
1.4 不同因素对水包核桃油乳状液稳定性的正交试验
以温度、乳化剂浓度、水相pH等单因素试验为依据,以水包核桃油乳状液稳定性系数为试验指标,按三因素三水平L9(34)正交试验设计。
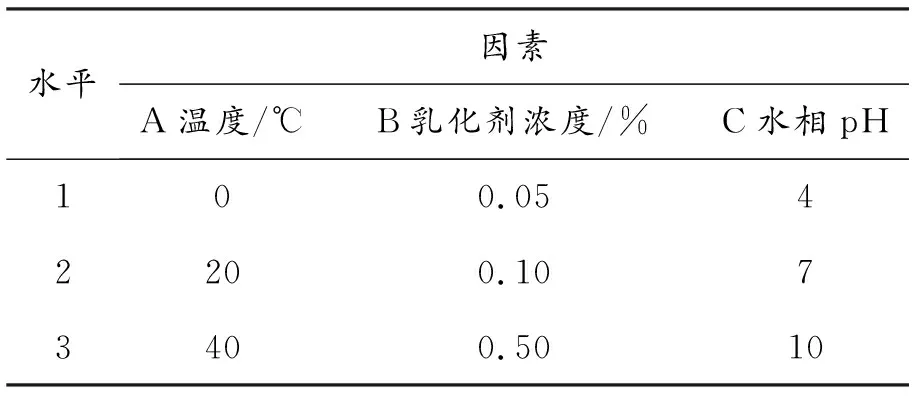
表1 水包核桃油乳状液稳定性影响因素正交试验设计
2 结果与分析
2.1 油浓度与吸光度标准曲线
按照1.2.2配制不同浓度的核桃油石油醚溶液,于510 nm处测其吸光度,标准曲线如图1所示,油浓度与吸光度之间的关系式:
C=(A-0.0961)×m/0.0127
(2)
式中 A——吸光度
C——含油浓度 mg·L-1。
2.2 温度对水包核桃油乳状液稳定性的影响
按照1.3.3 进行试验,得出水包核桃油的稳定性系数随温度的变化规律如图2所示,油浓度随温度的变化规律如图3所示。
由图2的变化趋势看,随着温度的不断升高,水包核桃油乳状液的稳定性系数在不断变小;由图3可知水包核桃油乳状液的油浓度随着温度的持续升高逐渐降低,乳状液稳定性持续下降。因此,随着温度的升高水包核桃油乳状液的稳定性逐渐降低。
2.3 乳化剂种类对水包核桃油乳状液的影响
按照1.3.4 进行试验,得出水包核桃油的稳定性系数随乳化剂种类的变化规律如图4所示,油浓度随乳化剂种类的变化规律如图5所示。
由4可知不同乳化剂中以十二烷基苯磺酸钠的稳定性系数最高,且随时间变化相比于其它两种乳化剂更为缓慢,由图5可知油浓度随静置时间变化较小,十二烷基苯磺酸钠为乳化剂时,油浓度最大,且乳化液中随着油浓度变大,油滴散布越均匀,乳状液稳定性越高;所以主乳化剂选用十二烷基苯磺酸钠。归因于水包油乳状液中油滴因为带异种电荷没有被乳化剂包裹,从而聚集合并成较大的油滴,使得乳化液粒径增大,从而影响乳状液的稳定性[6],添加乳化剂可有效地降低油滴与水之间的界面张力,乳化后的油滴分布更为均匀,保持了乳状液的物理稳定性,从而保证了货架期内的稳定性。
2.4 乳化剂的量对水包核桃油乳状液稳定性的影响
按照1.3.4 进行试验,选择十二烷基磺酸钠作为乳化剂,得出水包核桃油的稳定性系数随乳化剂用量的变化规律如图6所示,油浓度随乳化剂种类的变化规律如图7所示。
由图6可见,随着乳化剂浓度的越大,水包核桃油乳状液稳定性系数增大,放置时间增长,乳状液稳定性系数缓慢降低,乳化剂浓度为0.10%的时乳化液较稳定。由图7可见,油浓度随浓度变化较慢的乳化剂浓度为0.10%,且在货架期内较为稳定。综合来说,乳化剂浓度为0.10%时,乳状液较为稳定。
2.5 水相pH值对水包核桃油乳状液稳定性的影响
按照1.3.4 进行试验,得出水包核桃油的稳定性系数随乳化剂用量的变化规律如图8所示,油浓度随乳化剂种类的变化规律如图9所示。
由图8,图9可知,乳状液的稳定性、油浓度都随pH 值变化显著,pH=7时,稳定性系数最大,油浓度也最大,综合上述两个因素,调节水相pH=7,有助于更好地保持乳状液货架期的物理稳定性。
2.6 影响乳状液稳定性的因素正交试验
结合上述单因素试验结论,对影响水包核桃油乳状液货架期物理稳定性的因素进行正交试验。数据分析如表2所示。
由表2试验结果可知,对水包核桃油乳状液货架期内物理稳定性影响大小顺序为B>C>A,即乳化剂浓度是显著性影响因素,其次为水相pH值,温度对其影响最小。保持水包核桃油乳状液稳定性的最佳试验方案为A1C2B3,即当乳化剂浓度为0.50%,水相pH为7.0,温度为0 ℃时,水包核桃油乳状液物理稳定性最好。
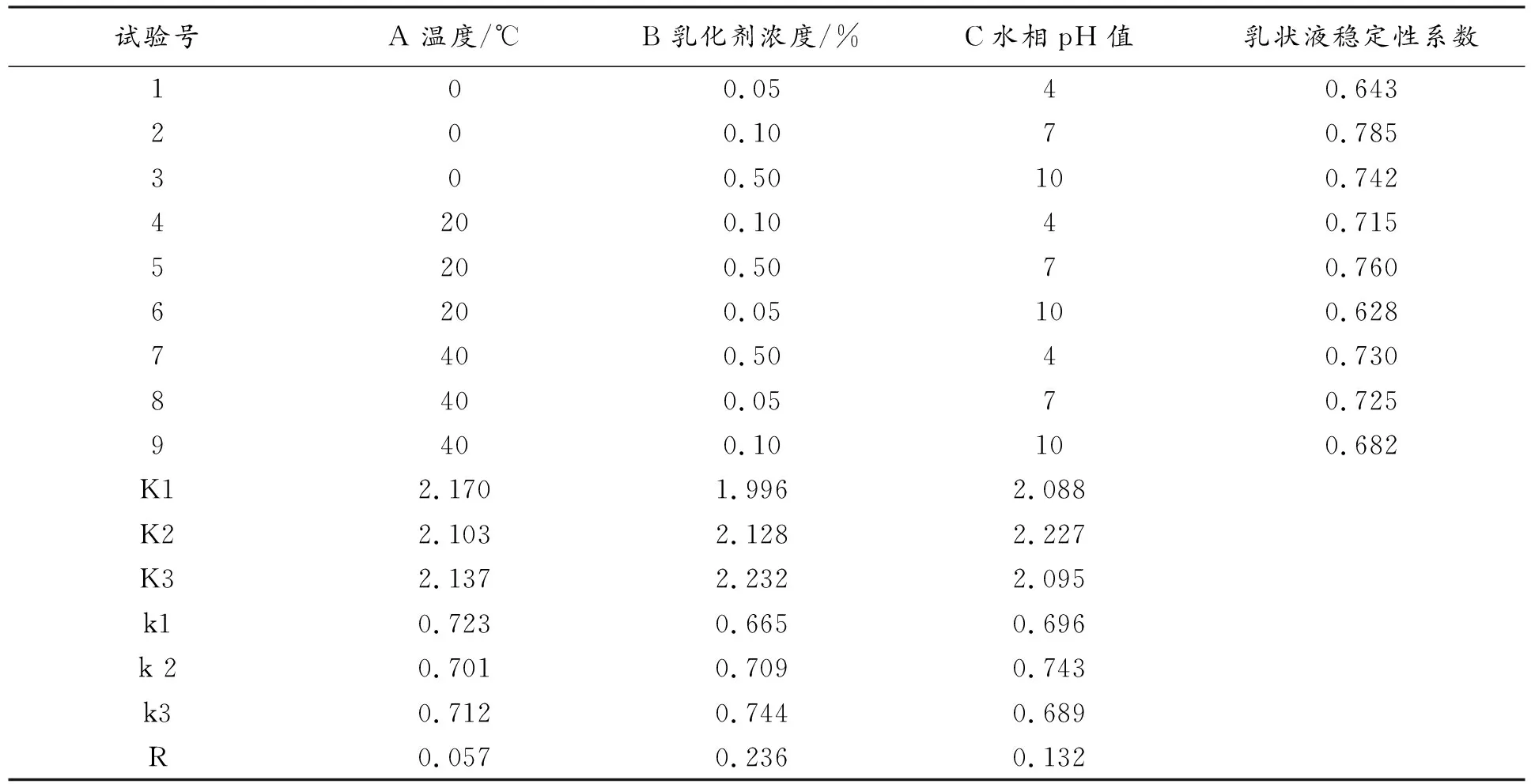
表2 正交试验
3 结论
研究通过单因素试验和正交试验发现,决定水包核桃油物理稳定性的多个因素中,乳化剂的种类及其用量是起决定性作用的,笔者研究选择十二烷基磺酸钠作为乳化剂,当储存温度为0 ℃,十二烷基苯磺酸钠乳化剂的浓度为0.50%,水相pH为7.0时,水包核桃油乳状液表现最为稳定。这些因素的控制有效降低了冷榨核桃油工艺的局限性,保证了冷榨核桃油的物理稳定性,延长了其货架期。

