薏苡仁油软胶囊对移植于裸鼠的人体肝癌HepG2的抑制作用
李翔 李大鹏 潘绵立 沈龙海 李炳生
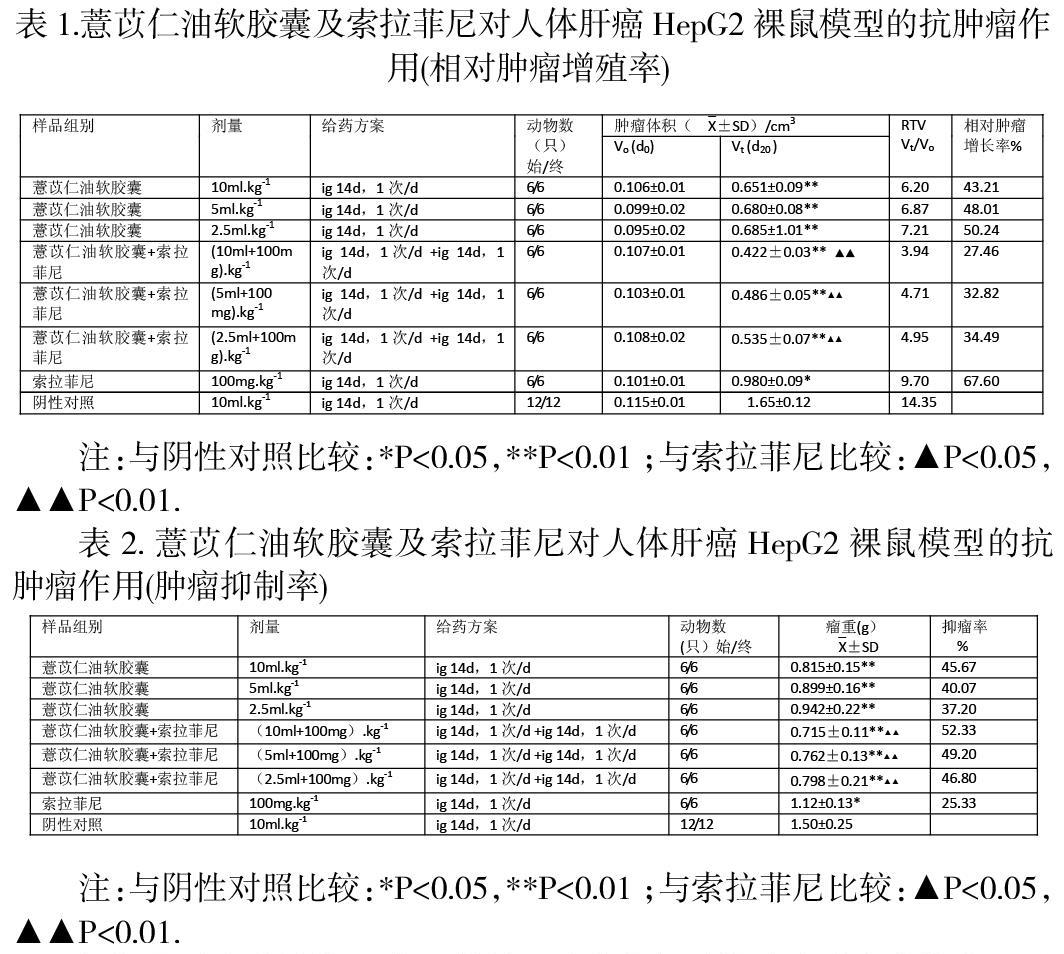
摘要:目的研究薏苡仁油软胶囊单用及合并索拉菲尼对移植于裸鼠的人体肝癌HepG2的抑制作用。方法制备移植于裸鼠的人体肝癌HepG2模型,分别按计划方案给药,动态观察和测量肿瘤大小及荷瘤鼠体重,按金氏公式计算肿瘤抑制率及相对肿瘤增长率。结果单用薏苡仁油软胶囊三个剂量组对移植于裸鼠的人体肝癌HepG2抑瘤率分别为45.67%、40.07%、37.20%,薏苡仁油软胶囊(三个剂量)合并索拉菲尼对应抑瘤率分别为52.33%、49.20%、46.80%。结论在本实验条件下,单用薏苡仁油软胶囊三个剂量组对移植于裸鼠的人体肝癌肿瘤细胞具有很好的抑制作用,合并索拉菲尼具有明显相加作用。
关键词:薏苡仁油软胶囊;裸鼠;肝癌HepG2;金氏公式
薏苡仁油注射液(商品名:康莱特注射液)是中国工程院院士李大鹏教授研制开发的中药二类抗肿瘤药物,是从禾本科植物薏苡仁中提取天然有效抗癌活性物质薏苡仁油制备而成的脂肪乳剂,大量临床研究已证实其具有明显的广谱抗肿瘤作用[1-3]。薏苡仁油软胶囊是在该注射液产品基础上对剂型进行改进后开发而成的口服制剂,相对于注射剂型,更方便患者服用,主要用于原发性非小细胞肺癌的治疗。索拉菲尼(如多吉美)为当前临床广泛应用的用于治疗无法手术或远端转移肝细胞癌(HCC)的一线靶向药物,然而该药在肝癌治疗中存在的原发性或获得性耐药情况愈发突出,影响了肝癌的疗效[4],如何有效应对此类疾病一线药物耐药后的治疗选择,逐渐成为热点问题。鉴于前述薏苡仁油乳剂的广谱抗癌作用,笔者进行了薏苡仁油软胶囊单用及合并索拉菲尼对移植于裸鼠的人体肝癌HepG2的抑制作用实验,初步探索薏苡仁油软胶囊单用及联合索拉非尼治疗肝癌的效果,为缓解索拉菲尼耐药问题提供新的思路与依据。
1. 实验材料
1.1 实验药物
薏苡仁油软胶囊(含薏苡仁油99.5%,维生素E0.5%)(浙江康莱特药业有限公司,薏苡仁油软胶囊原液直接灌胃使用);多吉美(甲苯磺酸索拉菲尼,拜耳医药);生理盐水。
1.2 实验动物
BALB/C裸鼠(SPF级),上海斯莱克实验动物有限责任公司提供,动物合格证号:SCXK(沪)20121-0002。
1.3 瘤源
人体肿瘤肝癌HepG2由上海医药工业研究院药理室传代。
2. 实验方法
取液氮冻人体肿瘤肝癌HepG2细胞株,复苏后,置37℃、5%CO2条件下培养。经传代培养后,取对数生长期的细胞,用生理盐水制备成(1-2)×106细胞·mL·1浓度的细胞悬液,接种于裸鼠右腋皮下。待肿瘤生长至1g以上时,无菌条件下取体内生长旺盛的人体肿瘤肝癌HepG2第 2代异种移植模型的肿瘤组织,切割成1~2mm3大小的均匀小块,用套管针于每只裸小鼠右腋皮下接种一块。待接种肿瘤被触及后,随机分组,按实验设计方案给药,见表1。
所应用的饲料、垫料、笼具及接触的器械等均应高压消毒后使用,裸鼠置于层流架中SPF条件饲养,动态观察和测量肿瘤大小及荷瘤鼠体重,每 5d用卡尺测量各裸鼠肿瘤的短径(a)及长径(b),按(a2×b)/2公式计算肿瘤体积。根据测量计算的肿瘤体积计算出相对肿瘤体积(RTV),RTV=Vt/V0。其中V0为随机分组(即d0)时的肿瘤体积,Vt为每一次测量(即dn)时的肿瘤体积。四周左右处死各组动物,剖取肿瘤称重,按下列公式计算肿瘤抑制率及相对肿瘤增长率。
肿瘤抑制率%=[(对照组平均瘤重- 给药组平均瘤重)/对照组平均瘤重]×100%
相对肿瘤增殖率%=(给药组RTV/对照组RTV)×100%
合并用药的效应根据金氏公式计算Q值:
Q=Ea+b/(Ea+Eb-Ea×Eb)
Ea+b为合并用药的抑瘤率,Ea和Eb分别为A药和B药的抑瘤率。如Q值0.85-1.15为相加(+),﹥1.15为增强(++)。
3. 实验结果:
按照实验方法操作,实验结果见表1 及表2。
根据金氏公式计算Q值,结果显示薏苡仁油软胶囊联合索拉菲尼具有相加作用:
薏苡仁油软胶囊10mL·kg-1合并索拉菲尼100mg·kg-1,Q值0.8805(+)。
薏苡仁油软胶囊5mL·kg-1合并索拉菲尼100mg·kg-1,Q值0.8905(+)。
薏苡仁油软胶囊2.5mL·kg-1合并索拉菲尼100mg·kg-1,Q值0.8812(+)。
4. 实验结论
薏苡仁油软胶囊剂量10,5,2.5mL·kg-1, 按照连续灌胃给药14d,1次·d-1的方案单独给药,对移植于裸鼠的人体肝癌HepG2的生长有明显抑制作用。
薏苡仁油软胶囊剂量10,5,2.5mL·kg-1,分别合并索拉菲尼100mg·kg-1,对移植于裸鼠的人体肝癌HepG2的抑瘤作用明显强于薏苡仁油软胶囊或索拉菲尼单独给药,两药合并有明显的相加作用。
5. 讨论
肝癌是我国最常见的恶性肿瘤之一,据国家癌症中心2015年恶性肿瘤流行病学估算结果显示,肝癌当年新发病例约37万,居恶性肿瘤第4 位,死亡约32.6万,居恶性肿瘤第2 位。2015年肝癌发病率位居男性第3 位,女性第7 位;死亡率居男性第2 位,女性第3 位[5]。而据全球癌症负担估计结果显示,在全球185个国家或地区中,中国的恶性肿瘤发病、死亡位居中等偏上水平,其中如食管癌、胃癌、肝癌等惡性肿瘤的发病和死亡约占全球的一半[6],整体防控形势严峻。
对于晚期肝癌病人,有效的系统治疗可减轻肿瘤负荷,改善肿瘤相关症状,提高生活质量,延长生存时间。多激酶抑制剂索拉非尼是被美国食品药品监督管理局批准的用于治疗晚期肝癌的一线分子靶向药物。国家卫健委颁布的原发性肝癌诊疗规范(2019年版)及CSCO发布的原发性肝癌治疗指南(2018年版)均将索拉非尼推荐为晚期HCC的一线治疗药物[7,8]。多项临床研究表明,索拉非尼对不同国家地区、不同肝病背景的晚期肝癌病人都具有一定的生存获益[9]。而相对于肝功能Child-Pugh B級,Child-Pugh A级的病人生存获益更明显[10]。然而,部分HCC对其耐药性的出现影响了总体疗效,耐药分为原发性(HCC原本就对索拉非尼缺乏敏感性)和获得性(开始敏感,治疗过程中出现耐药)两类,相关机制研究尚未达成统一认识[11]。如何有效应对此类疾病一线疗法耐药后的治疗方式选择,成为一线临床医生所面临的新问题,形成了新的临床需求。
HepG2是肝癌药效学实验中常用瘤株。从本次实验结果看,薏苡仁油软胶囊不仅单用可明显抑制其生长,合并索拉非尼更具有明显相加作用。此外,薏苡仁油软胶囊还具有增强免疫、降低化疗药物不良反应的效果,其原料薏苡仁属药食同源,在中国已有上千年应用历史,多年临床经验亦证实其安全性良好。综上所述,薏苡仁油软胶囊对于提高晚期HCC的治疗水平具有较大潜力,有望成为晚期HCC患者另一治疗用药选择,值得进一步临床研究与探讨。
参考文献:
[1] 李大鹏.康莱特抗肿瘤研究论文集[M].杭州:浙江大学出版社,1998.
[2] 李炳生,陈秀华,任文龙等.康莱特注射液的抗肿瘤作用[J].中国医药工业杂志,1998,29(10):456-458.
[3] 周萌,王瑞,米田.康莱特注射液在恶性肿瘤综合治疗中的应用效果[J].临床医学研究与实践,2019(26):43-44.
[4] 高彦君,姚颐,宋启斌等.原发性肝癌索拉非尼耐药机制的研究进展[J].肿瘤学杂志,2019(09):836-840.
[5] 郑荣寿,孙可欣,赫捷等.2015年中国恶性肿瘤流行情况分析[J].中华肿瘤杂志,2019,41(1):19-28.
[6] Bray F,Ferlay J,,et al.Global cancer statistics,2018:GLOBOCAN esti-mates of incidence and mortality worldwide for36cancers in185countries[J].CA Cancer J Clin,2018,68(6):394-424.
[7] 中华人民共和国卫生健康委员会.原发性肝癌诊疗规范(2019年版),中国实用外科杂志,2020(02):11-138.
[8] CSCO指南工作委员会.原发性肝癌诊疗指南(2018.V1)[M].北京:人民卫生出社,2018.
[9] Llovet JM,Ricci S,et al.Sorafenib in advanced hepatocellular carcinoma[J].N Engl J Med,2008,359(4):378-90.
[10] Pressiani T,Boni C,et al.Sorafenib in patients with Child-Pugh class A and B advanced hepatocellular carcinoma:a prospective feasibility analysis[J].Ann Oncol,2013,24(2):406-11.
[11] 胡倍源,覃伟,董琼珠,钦伦秀.肝细胞癌(HCC)对索拉非尼耐药相关机制的研究进展[J].复旦学报(医学版),2018(06):884-888.

