非晶态合金纳米管催化苯酚加氢性能研究*
莫 敏,郭晓娟,关红儒,寻友益
(1 湖南第一师范学院,湖南 长沙 410205;2 南京大学化学化工学院,江苏 南京 210093)
环己醇是重要化工产品的中间原料,在涂料、合成洗涤剂、纺织等工业有着重要的用途[1]。目前,人们主要利用液相法将苯酚在镍催化剂作用下催化加氢制得环己醇,但此方法存在活性高,选择性低的特点[2]。非晶态合金在苯酚加氢反应中也表现出优异的催化活性,催化活性和选择性都比较高,得到广泛研究[3-5]。
传统液相化学合成的非晶态合金,得到的基本是实心的纳米颗粒状催化剂,这种催化剂不容易获得很高的表面积,而且在催化加氢反应中稳定性很差,容易结块。把非晶态合金制备成管状结构,在结构稳定性上更有优势[6-9]。本文利用层状液晶模板法成功合成出二元Ni-B、三元Ni-P-B和四元Ni-Co-P-B非晶态纳米管催化剂,研究其催化苯酚液相加氢制取环己醇的催化性能。
1 实 验
四元非晶态合金Ni-Co-P-B纳米管的制备:将0.005 mol (6.4 g) Tween 40和0.0025 mol (0.58 g)樟脑磺酸溶于5.8 mL去离子水中,然后加入x mol NiCl2·6H2O和y mol CoCl2·6H2O (x+y=0.0025 mol,x:y=1:0.3),以及适量的NaH2PO2,在50 ℃水浴下充分混合搅匀,N2气氛下缓慢地冷至25 ℃,再泵入3.5 mol·L-1NaBH4和0.1 mol·L-1的NaOH混合溶液,在N2中老化24 h后,用去离子水和无水乙醇分别洗涤,最后保存N2氛中备用。非晶态Ni-P-B和Ni-B纳米管采用相同的制备方法获得。
非晶态合金Ni-Co-P-B纳米颗粒的制备:0.0025 mol (0.58 g)樟脑磺酸,x mol NiCl2·6H2O和y mol CoCl2·6H2O (x+y=0.0025 mol,x:y=1:0.3),以及适量的NaH2PO2溶于50 mL水中,再在N2氛下泵入3.5 mol·L-1NaBH4和0.1 mol·L-1的NaOH混合溶液,在N2氛中老化24后,用去离子水和无水乙醇分别洗涤,最后保存N2氛中备用。
催化剂活性评价:在100 mL的高压釜中依次加入2.5 mmol 催化剂,1.0 g苯酚,和60 mL的无水乙醇,反复通入H2赶走体系中的空气。将高压釜加热到358 K,并开启搅拌器,搅拌速度800 r/min,将高压釜的压力设置到1.0 MPa(此时被设置成反应时间为0),在反应过程中,定时放出釜内少量溶液。用GC-2014 SHIMADZU 型气相色谱仪分析加氢产物各组分的含量,分析条件为:SGE SE230 毛细管色谱柱(0125 mm×30 m),FID 检测器,载气为N2,柱温250 ℃,峰面积归一法确定含量。
2 结果与讨论
2.1 液晶前体和催化剂物相分析
图1(b)为Ni-B、Ni-P-B、Ni-Co-P-B纳米管和Ni-Co-P-B纳米颗粒的XRD谱图。从图1可知,在2θ=45°处有一个鼓包,表明样品为非晶态结构。

图1 覆盖在玻璃片上的液晶前体小角XRD图(a)和非晶态纳米管、纳米颗粒的广角XRD图(b)
2.2 催化剂形貌表征
图2为Ni-Co-P-B、Ni-P-B、Ni-B纳米管和Ni-Co-P-B纳米颗粒的TEM图,从图2可以看出,纳米管直径比较均匀,约60~65 nm,长度约为几个微米;纳米颗粒粒径约10~15 nm。纳米管和纳米颗粒的SAED图进一步证实了非晶态结构。

图2 非晶态合金纳米管、纳米颗粒的TEM图
2.3 催化剂组成与比表面积
ICP分析了样品中各元素的原子比,各个样品的成分在表1中给出。图3分别为非晶态合金Ni-Co-P-B NTs,Ni-P-B NTs,Ni-B NTs和Ni-Co-P-B NPs的N2吸附-脱附等温线,可以看出,该等温线为IUPAC规定的第IV类等温线,即中孔材料的特征等温线。在P/Po=0.4~1.0之间有细长的滞后环。非晶态合金纳米催化剂的比表面积、孔容和孔分布数据在表1中给出,利用BJH脱附枝计算所得的孔径与TEM测出的孔径基本一致。

表1 催化剂组成、比表面积、孔径、孔容
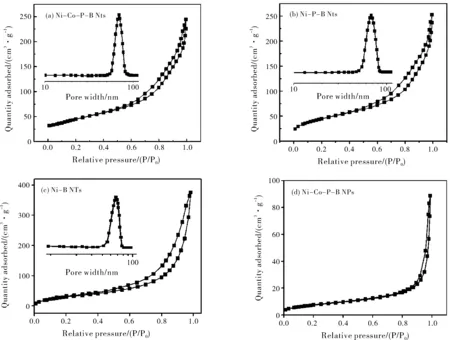
图3 N2吸附-脱附等温线和孔径分布曲线
2.4 催化剂表面结构XPS分析
Ni-B NTs、Ni-P-B NTs和Ni-Co-P-B NTs的XPS谱图如图4所示。从Ni 2p结合能谱可见,催化剂中存在两种镍物种,一种为Ni的氧化物,在~856.0 eV附近,另一种为金属Ni,在~852.8 eV附近(图4a)[10]。对于B 1s结合能谱来说,在~188.2 eV附近的峰为B单质峰,在~192.4 eV附近的为B的氧化物的峰(图4b)[11]。图4c为P 2p能级,在~129.1 eV附件,对应单质P[12-15]。图4d为Co 2p能级,在~777.5和~780.7 eV附近,分别对应于单质Co和Co的氧化物[4,16]。因为氧化物状态非常稳定,对组分间的电子相互作用影响不大,电子转移仅仅发生在金属单质Ni、Co与B、P之间。相对于Ni-B NTs,在催化剂中掺杂P,Ni-P-B NTs和Ni-Co-P-B NTs中单质Ni的能级向低能级移动,说明Ni上富集电子。

图4 Ni-B NTs, Ni-P-B NTs和Ni-Co-P-B NTs的XPS谱图
2.5 苯酚催化加氢性能
图5为Ni-B NTs,Ni-P-B NTs,Ni-Co-P-B NTs和Ni-Co-P-B NPs催化苯酚加氢反应转化率随时间变化曲线图。Ni-B NTs在反应400 min后,转化率为71%,产物中环己醇选择性为82%,其余为环己烷;Ni-P-B NTs在反应400 min后转化率相对于Ni-B纳米管来说有所提高,达到87%,对环己醇的选择性可达96%,其余为环己烷;四元非晶态合金纳米管Ni-Co-P-B NTs在反应完300 min后,转化率可达到100%;产物中环己醇选择性可达99%,其余为环己烷;四元非晶态合金Ni-Co-P-B NPs催化性能较低,在反应完成400 min时,转化率仅23%,产物中环己醇选择性高达85%。可见,将非晶态合金催化剂制备成管状结构,苯酚加氢催化性能得到比较大的提高。在Ni-B NTs中引入P,可使得反应催化活性提高,对环己醇的选择性也大大提高;在Ni-P-B纳米管中引入第二种金属(Co),形成四元非晶态Ni-Co-P-B纳米管,可使得催化性能得到提高。
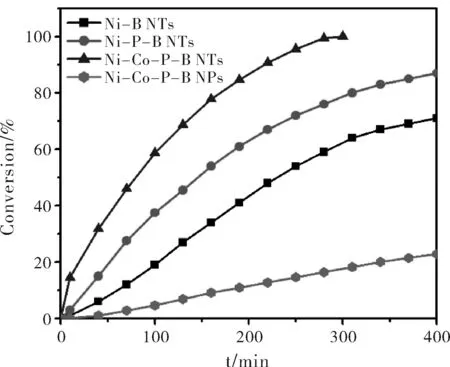
图5 催化苯酚加氢转化率与时间关系曲线图
3 结 论
运用层状液晶模板法制备了形貌均一的非晶态合金纳米管。利用XRD、TEM、ICP、低温N2吸附以及XPS等表征了纳米管的结构、组成、比表面积、孔分布及表面状态。将四元非晶态合金Ni-Co-P-B纳米管用于催化苯酚加氢制取环己醇,并与二元非晶态合金Ni-B、三元非晶态合金Ni-P-B纳米管催化性能进行比较,发现:在Ni-B中加入P元素,形成三元非晶态合金Ni-P-B纳米管,催化性能得到提高;在三元非晶态合金Ni-P-B纳米管中加入第二种金属Co,形成四元非晶态合金Ni-Co-P-B纳米管,发现催化苯酚制取环己醇性能进一步得到提高,这可能是由于金属Ni和Co的协同作用以及B、P对催化剂表面金属Ni的电子状态起到调节作用导致的。Ni-Co-P-B 纳米管的催化活性高于同组分的Ni-Co-P-B 纳米颗粒,可能是因为纳米管的比表面积远远高于纳米颗粒的比表面积,以及纳米管特殊的管状结构更有利于催化苯酚催化加氢反应。

