瑞舒伐他汀和阿托伐他汀治疗冠心病的疗效及安全性研究
于水江


【摘要】目的:探索瑞舒伐他汀和阿托伐他汀治疗冠心病的疗效及安全性。方法:择取80例冠心病患者作为实验研究对象,摸球法随机分组,两组中各有40例,对照组给予阿托伐他汀治疗方案,对观察组给予瑞舒伐他汀治疗方案,分析两组的治疗前后血脂水平、治疗效果、不良反应发生率。结果:观察组血脂水平优于对照组且临床疗效更高,不良反应发生率更低,差异有统计学意义(P<0.05)。结论:瑞舒伐他汀对改善患者血脂水平具有非常明显的作用,临床疗效好,安全性高,值得推广使用。
【关键词】瑞舒伐他汀;阿托伐他汀;冠心病患者;临床疗效;安全性
【中图分类号】R541.4 【文献标识码】A 【DOI】10.12332/j.issn.2095-6525.2020.12.220
冠心病是一类临床常见疾病,具有较高的致死率和致残率,是目前影响患者生活质量,威胁其生命安全的主要疾病之一[1],阿托伐他汀与瑞舒伐他汀均为冠心病治疗方案,而基于冠心病的特点和危害,瑞舒伐他汀更加科学有效[2],更能改善患者血脂水平。本文将为验证这一结论进行如下分析。
1资料和方法
1.1基本资料
病例挑选年段:2018年1月-2019年1月。
病例一般资料:冠心病患者共80例,摸球法随机分组。对照组:奇数号,共40例,男21,女19;年龄59-69(64.18±3.22)岁。观察组:偶数号,共40例,男20,女20;年龄60-68(64.16±3.19)岁。组间资料对比,P>0.05。
1.2操作方法
对对照组实施阿托伐他汀治疗方案:药物由北京嘉林药业有限公司提供,国药准字为H19990258,10mg/次,1次/天。
对观察组实施瑞舒伐他汀治疗方案:药物由南京先声东元药业有限公司提供,国药准字为H20113265,10mg/次,1次/天。
两组患者均连续治疗6个月,期间对两组患者进行其他基础治疗,如服用抗血小板聚集、扩血管、β受体阻滞剂等药物,同时进行心理疏导、饮食干预等基础护理,观察记录治疗数据,团队分析数据的准确性和可靠性。
1.3观察指标
(1)统计治疗前后血脂水平,包括总胆固醇、甘油三酯、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇几个指标。(2)统计治疗效果,分为显效、有效、无效,总有效率=显效率+有效率。疗效标准:①临床症状消失,判定为显效;②临床症状明显缓解,判定为有效;③临床症状未缓解,判定为无效。(3)统计不良反应发生率,包括胃肠道不适、乏力、便秘几个指标,不良反应发生率=(胃肠道不适例数+乏力例数+便秘)/例数x100%。
1.4统计学处理
文中计数(x2检验)、计量(t检验)资料用SPSS20.0软件处理,P<0.05表示数据差异有统计学意义。
2结果分析
2.1治疗前后血脂水平
结果:治疗前对比无差异(P<0.05)治疗后观察组总胆固醇、甘油三酯、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇水平均优于对照组(P<0.05)。见表1。
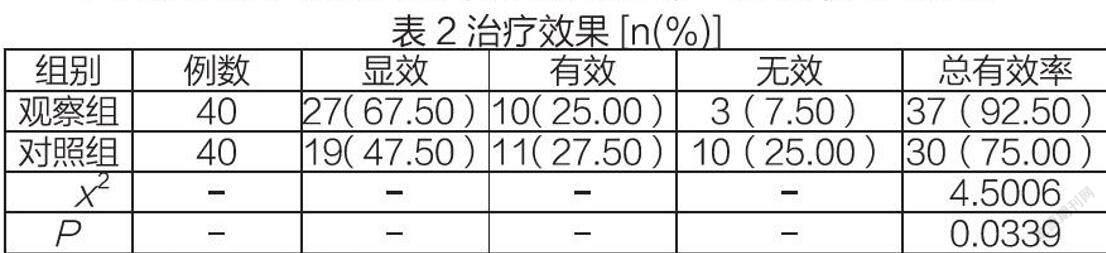
2.2治疗效果
结果:观察组治疗总有效率高于对照组(P<0.05)。见表2。
2.3不良反应发生率
结果:观察组不良反应(胃肠道不适、乏力、便秘)发生率低于对照组(P<0.05)。见表3。
3讨论
冠心病作为一种病因复杂、病情严重的疾病,严重困扰患者的日常生活,更危及患者的生命健康安全[3]。临床研究表明,冠心病发作的高危因素为高血脂,故降血脂是冠心病治疗的重要思路,基于此,阿托伐他汀和瑞舒伐他汀均在临床中得以应用。
阿托伐他汀可有效抑制胆固醇、HMG-CoA还原酶的生物合成,从而有效降低脂蛋白和胆固醇水平,并恢复血管内皮功能;瑞舒伐他汀主要作用于肝脏,可有效提高LDL细胞表面受体数目并促进其分解和吸收,从而有效降低极低密度脂蛋白(VLDL)和LDL微粒总数[4]。上述结果中,观察组血脂水平优于对照组且临床疗效更高,不良反应发生率更低,由此可佐证瑞舒伐他汀相较阿托伐他汀在冠心病治疗中的有效性和安全性,更能改善患者血脂水平[5]。
综上所述,以降血脂为核心开展治疗工作,瑞舒伐他汀治疗方案可发挥巨大作用,临床疗效好,安全性高,值得在临床中推广使用。
参考文献:
[1]封和.瑞舒伐他汀与阿托伐他汀治疗冠心病的对比及对TNF-α,IL-6,CRP的影响[J].现代医学与健康研究电子杂志,2019,v.3;No.48(17):61-63.
[2]夏杨,张惠军,陈宇强,等.瑞舒伐他汀与阿托伐他汀对冠心病的疗效及不良反应分析[J].中西医结合心血管病电子杂志,2018,6(36):51-52.
[3]业居聪.瑞舒伐他汀与阿托伐他汀在治疗冠心病患者中的疗效与安全性分析[J].人人健康,2020,No.523(14):652-653.
[4]陈守芳.瑞舒伐他汀与阿托伐他汀治療冠心病的疗效对比研究[J].世界最新医学信息文摘(电子版),2020,020(005):145-146.
[5]徐晓.比较瑞舒伐他汀和阿托伐他汀对冠心病的治疗效果[J].医学信息,2018,031(0z2):167-168.

