探讨老年非瓣膜性房颤左心房内径与左心房/左心耳血栓的关系
梁丽明,白树堂,符洪犊,羊家慧
(海口市人民医院心脏外科,海南 海口 570208)
心房纤维性颤动(atrial fibrillation,AF)作为临床常见的心律失常,因其易引发血栓事件严重影响公众生命健康,其中非瓣膜性房颤(non-valvular atrial fibrillation,NVAF)患者出现脑卒中的风险较常人高出5倍余,所以NVAF血栓事件的预防及治疗是临床的重中之重,目前华法林或新型口服抗凝药治疗日益广泛[1-2]。NVAF的血栓来源为左心耳(left atrial appendage,LAA)或(及)左心房(left atrium,LA),其中LAA来源血栓较为常见。研究指出,NVAF造成心房无效收缩、排血受阻,左房压力增大,此时LAA发挥调节心房压力作用,引起自身结构及收缩能力改变,进而造成LAA血流速度缓慢、血液淤积,形成血栓[3-5];而心房内附壁血栓机制则与内皮细胞功能损伤、炎症及血流动力学改变等有关[5]。早期预测及识别血栓可极大减少血栓事件的风险。因而评估老年NVAF患者LA形态及重构在识别及预测LA/LAA血栓方面的价值较大。本文通过分析2015年3月至2018年11月本院收治的存在LA/LAA血栓的NVAF患者心脏彩色超声变化特点明晰LAD与此类患者LA/LAA血栓的相关性。
1 资料与方法
1.1 一般资料
回顾性分析2015年3月至2018年11月269例年龄超过60岁的老年NVAF患者临床资料及经胸或食道心脏彩超结果,其中51例患者存在LA/LAA血栓,为血栓组,另选择51例无血栓患者为对照组。所选病例中男性63例,女性39例,年龄60~82岁,平均(68.23±6.92)岁。NVAF的诊断标准依据2019年AHA《2019心房颤动(房颤)患者管理指南更新》制定[6]。纳入标准(同时满足以下两项):(1)年龄≥60岁;(2)回顾临床资料及心脏彩超资料完整无缺失。排除标准(具备任一项即排除):(1)既往存在大面积陈旧性心肌梗死;(2)服用抗凝药物治疗;(3)存在肝肾疾病终末期等其它不适合入组的疾病;(4)病史记录存在心脏瓣膜病或施行心脏瓣膜置换术或瓣膜成形术。
1.2 临床特征指标
通过分析入组患者临床电子病例,收集受试者临床特征,包括高血压、糖尿病、吸烟史、房颤持续时间(根据病程记录)及类型(阵发性或持续性)、高脂血症、年龄及性别等资料。
1.3 实验室指标
检索检验系统,收集受试者入院后首次实验室检测指标,包括D-二聚体(D-Dimer)、血小板计数(platelet count,Plt)、纤维蛋白原(fibrinogen,FIB)、肌酐(creatinine,Cr)、血小板平均体积(mean platelet volume,MPV)、凝血酶学时间(prothrombin time,PT)、部分凝血活酶时间(activated partial thromboplastin time,APTT)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)、总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG))等指标。
1.4 LA/LAA血栓
心脏彩超可见LA/LAA自发显影和/或LAA血栓即为LA/LAA血栓形成。具体定义:LA/LAA自发显影:心脏彩超可见相应部分出现旋涡状运动的烟雾状回声;血栓:至少两个切面均可探及LAA内团块状回声,边缘清晰[7]。
1.5 心脏彩色超声
心脏彩色超声检测仪为Philips EPIQ 7C彩色超声诊断仪,超声测量探头型号选择X5-1,频率为1.0~5.0 MHz,扫描角度设定为60°~90°。择胸骨旁长轴平面测量LAD,收集心脏彩超相关数据包括左室舒张末期内径(left ventricular end diastolic diameter,LVEDD)、左室收缩末期内径(left ventricular end systolic diameter,LVESD)、左心房内径(left atrial diameter,LAD)、左心耳开口宽度(left atrial appendage opening width,LAAW)、左心室射血分数(left ventricular ejection fraction,LVEF)及左心室短轴缩短率(fraction shortening,FS)。
1.6 统计学方法
数据统计采用SPSS 13.0软件。连续变量采用均数±标准差形式表示,两组间比较采用两个独立样本t检验;计数资料采用构成比形式表示,两组间比较采用非参数秩和检验;影响LA/LAA血栓的临床因素通过二元及多元Logistic回归分析;LAD预测LA/LAA血栓的临床价值通过受试者工作特征(ROC)曲线评估。P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者临床特征资料及实验室检查指标比较
血栓组患者年龄、房颤病程、持续性房颤及D-Dimer显著高于对照组(P<0.05),见表1。
2.2 两组患者心脏彩超指标
与对照组相比,血栓组患者LAD显著升高,LVEF及LAAW显著降低,差异均有显著性,但其它指标两组间比较,差异无显著性。见表2。
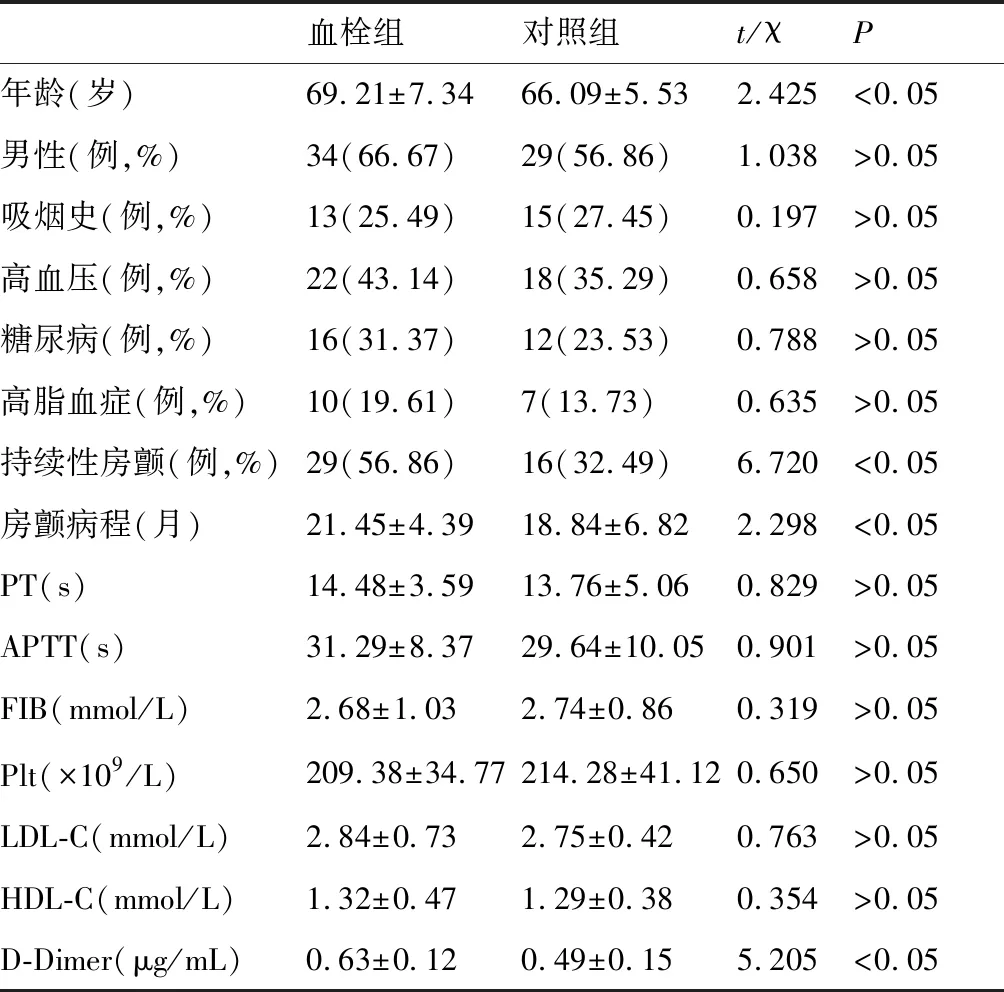
表1 两组患者临床特征资料及实验室检查指标比较
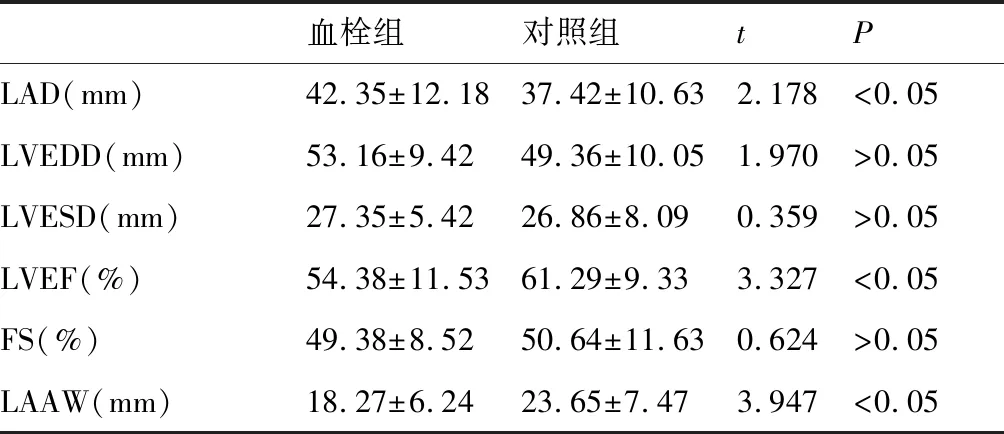
表2 两组患者心超指标比较
2.3 二元Logistic回归分析影响LA/LAA血栓的临床因素
由表1表2得出D-Dimer、年龄、LVEF、房颤病程、持续性房颤、LAD及LAAW在两组间的差异均有显著性。以上述指标为自变量,以LA/LAA血栓形成为因变量进行二元Logistic回归分析,房颤病程、持续性房颤、LAD及LAAW是LA/LAA血栓的危险因素,其优势比(Odds ratio,OR)(95%CI)见表3。
2.4 多元Logistic回归分析影响LA/LAA血栓的因素
多元Logistic回归分析影响LA/LAA血栓的因素可知,房颤病程、LAD及LAAW是LA/LAA血栓的危险因素,其优势比(Odds ratio,OR)(95%CI)见表4。
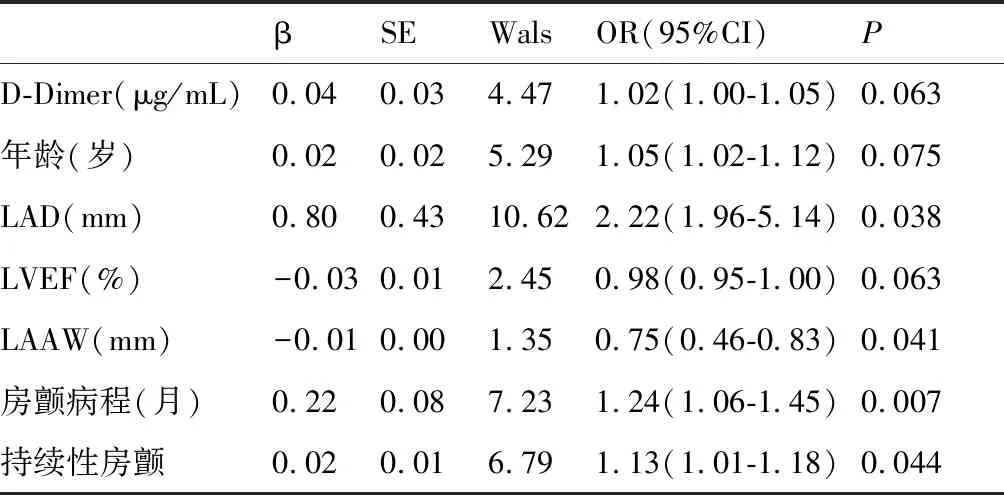
表3 二元Logistic回归分析影响LA/LAA血栓的为临床因素
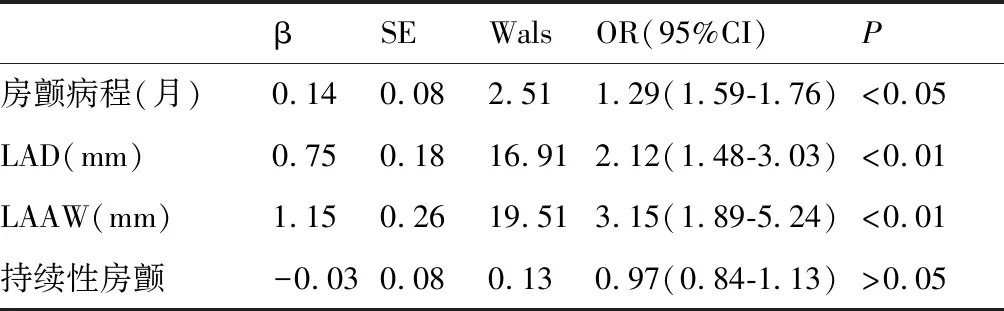
表4 多元Logistic回归分析影响LA/LAA血栓的因素
2.5 受试者工作特征(ROC)曲线分析LAD预测LA/LAA血栓的临床价值
由ROC曲线可知,LAD预测LA/LAA血栓的曲线下面积(AUC)(95%CI)为0.83(0.74-0.91),见图1所示。
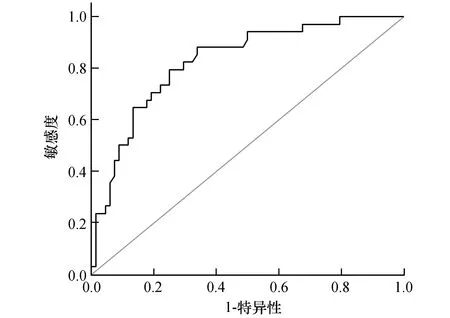
图1 ROC曲线分析LAD预测LA/LAA血栓的临床价值
3 讨 论
随着年龄增加,AF患者血栓栓塞风险也明显升高,给老年患者带来了高死亡及高致残率,影响患者预后和生存质量,造成家庭及社会的沉重负担[7]。本课题组发现,LA/LAA血栓患者年龄更大;B型利钠肽(B-type natriuretic peptide,BNP)由结构及功能受损的心房及心室释放入血,其水平在合并血栓的AF患者中增加,被证实为影响左心耳血栓形成的独立危险因素[8],提示AF患者左心房结构和功能改变与LAA血栓有关。
血栓组患者房颤病程及持续性房颤显著高于对照组,同时,二元Logistic回归分析发现房颤病程及持续性房颤是LA/LAA血栓形成的危险因素,这表示随着房颤病程的延长LA/LAA血栓形成的风险增加。这是由于长时间AF状态引起LA结构重塑和功能改变的程度更甚。LA结构重塑表现在心房扩大及形状改变,杨廷杰等[9]学者发现AF患者因心房压力增加等原因,LA更易出现非对称性的球形改变以抵消心房扩张过程中的房壁张力,维持结构的稳定,而非对称性的结构引起心房内血流动力学,引起心房内血液淤滞,增加血栓形成风险[10],体外构造心房球形模型也验证了上述结论[11],更重要的是,慢性炎症反应参与LA重塑,加重心房细胞损伤、激活血小板,参与血栓形成[9]。进一步的分析发现,LAD作为反应LA扩大程度的指标,其高水平增加了LA/LAA血栓形成的风险,同时也是预估LA/LAA血栓的临床指标,其优势比(OR)(95%CI)为2.22(1.96-5.14),ROC曲线下面积(AUC)(95%CI)为0.83(0.74-0.91)。
此外,本文结果显示心功能减退增加了血栓事件的风险,这与AF所致心功能受损有关。LAAW也是LA/LAA血栓形成的危险因素,这与LAA特殊的解剖结构密切相关,AF引起左心耳开口明显增宽,造成其形状改变,如球形改变等,最终阻碍左心耳血流的排出,导致血液淤积形成血栓[12]。
综上所述,LAD是NVAF患者LA/LAA血栓形成的危险因素,也具备潜在的预测价值,对于临床医师及时识别LA/LAA血栓高危患者有重要意义。

