Fe3O4-MnO2复合材料催化降解水中有机污染物的研究进展
张 磊
(中国石化 石油工程设计有限公司山东省油田采出水处理及环境污染治理重点实验室,山东 东营 257026)
随着工业的发展,大量的污染物排放到水环境中,对人类健康造成很大的威胁。目前水中有机污染物的降解技术包括光催化[1-2]、基于活化过硫酸盐(PS)的新型高级氧化[3-4]和光电催化等[5-6]。利用金属氧化物催化降解水中有机污染物具有原料易得、操作简单、成本低廉等优势。MnO2具有较高的氧化电位,可以高效活化PS产生硫酸根自由基(SO4⁻·)来氧化水中有机污染物[7-8],也能负载其他物质活化H2O2产生羟基自由基(·OH)来氧化水中有机污染物[9],且对环境十分友好。但MnO2催化降解水中有机污染物后,易形成细小的颗粒,难以固液分离,较难循环利用。
Fe3O4-MnO2复合材料在降解水中有机污染物方面具有明显的优势[10]。由于Fe3O4具有磁性强、结构均一、比表面积小、活性高、重复利用性好的优点[11-13],Fe3O4-MnO2复合材料即解决了MnO2难以固液分离的缺点,又能提高水中有机污染物的降解速率,在水污染治理方面具有广泛的应用前景。本文总结了Fe3O4-MnO2复合材料催化降解水中有机污染物的研究进展,为Fe3O4-MnO2复合材料的设计和催化降解过程的研究提供参考。
1 Fe3O4-MnO2复合材料的主要合成方法
1.1 液相沉积法
张姝等[14]利用FeCl3、FeCl2·4H2O、NaOH、聚乙二醇(PEG)、KMnO4、四水合乙酸锰、柠檬酸、NH3·H2O、无水乙醇等,将MnO2包裹在纳米磁性Fe3O4颗粒上,液相沉积合成了磁性Fe3O4-MnO2复合材料。
1.2 溶胶-凝胶法
溶胶-凝胶法是利用马弗炉高温煅烧制得磁性Fe3O4-MnO2复合材料[14]。将四水合乙酸锰、去离子水、柠檬酸溶液、Fe3O4、PEG溶液、NH3·H2O等在60 ℃下搅拌2 h,将产物置于真空干燥箱中制得干凝胶,再将干凝胶置于马弗炉中在280 ℃下煅烧10 h,制得Fe3O4-MnO2复合材料。
液相沉积法和溶胶-凝胶法都可以将MnO2包裹在Fe3O4颗粒上制成复合材料,液相沉积法制备的Fe3O4-MnO2复合材料颗粒粒径更大,颗粒近似球状且表面光滑,而溶胶-凝胶法制备的Fe3O4-MnO2复合材料颗表面粗糙呈絮状结构,且液相沉积法制备的Fe3O4-MnO2复合材料的饱和磁化强度更高。
1.3 水热法
水热法是将两种或多种金属氧化物结合在一起的常见方法。将有机配体、金属盐、溶剂混合,密封到反应釜中,加热后溶剂逐渐挥发,达到超临界状态并析出晶体。该方法很好地解决了反应物在室温下难溶的问题,且升降温可控,易于实现工业化。
董正玉等[15]采用两步水热法,先用FeSO4·7H2O、聚乙烯比咯烷酮、NaOH溶液制得Fe3O4粉末,再将Fe3O4粉末加入到KMnO4、HCl、去离子水混合溶液中,在110 ℃下烘烤10 h制得磁性纳米核壳结构Fe3O4@α-MnO2。
1.4 共沉淀法
NAWAZ等[16]采用共沉淀方法制备了介孔结构的Fe3O4-MnO2复合材料。将MnSO4·H2O加入到丙三醇水溶液中,混匀,再加入Fe3O4纳米颗粒。将NH4HCO3加入到丙三醇水溶液中,混匀。将上述两种溶液混合后在50 ℃下搅拌,Fe3O4和已形成的MnCO3微球结合,形成Fe3O4-MnCO3复合材料。分别用无水乙醇和去离子水清洗Fe3O4-MnCO3复合材料,置于真空干燥箱中90 ℃干燥6 h,再放入马弗炉中400 ℃下煅烧5 h,得到Fe3O4-MnO2复合材料。
2 Fe3O4-MnO2复合材料的应用
2.1 Fe3O4-MnO2复合材料催化降解水中染料类污染物
Fe3O4-MnO2复合材料催化降解水中染料类污染物的应用较为广泛,可处理的染料主要有偶氮染料RBK5[15]、亚甲基蓝[17-19]、酸性橙7[20]、罗丹明B[21]。董正玉等[15]采用核壳结构Fe3O4@α-MnO2催化降解偶氮染料RBK5,在体系pH为7、Fe3O4@α-MnO2投加量为1.2 g/L、过一硫酸盐(PMS)投加量为4 mmol/L、RBK5投加量为30 mg/L的最佳条件下,RBK5降解率达91%。
FANG等[20]采用Fe3O4-MnO2催化剂活化水中H2O2降解酸性橙7,在体系pH为5.5、温度为303 K、酸性橙7质量浓度为50 mg/L、Fe3O4-MnO2投加量为0.6 g/L、H2O2投加量为0.12 mL/mL的条件下,Fe3O4-MnO2-H2O2体系的酸性橙7降解率为96.8%,大于Fe3O4-H2O2体系(18.4%)和MnO2-H2O2体系(79.2%)的酸性橙7降解率。
此外,研究者还发现,随着MnO2负载量的提高,酸性橙7降解率也提高,这是因为,在中性溶液中,MnO2对H2O2的催化活性高于Fe3O4对H2O2的催化活性。当MnO2负载量(w)从10%增加到20%时,酸性橙7降解率从59.2%提高至96.8%。体系pH为3.5~7.5时,该催化剂均具有较高的催化活性。该催化剂连续使用7次后酸性橙7降解率无明显下降。
ZHANG等[17]采用水热法将柠檬酸钠分别合成可溶于水的Fe3O4纳米片和Fe3O4空心纳米球,然后加入KMnO4溶液,采用共沉淀法分别合成Fe3O4-MnO2纳米复合光催化剂。采用该催化剂在紫外光照射下降解水中亚甲基蓝,催化活性高,稳定性高,耐酸性强,可循环利用。
2.2 Fe3O4-MnO2复合材料催化降解水中苯酚类污染物及其衍生物
水中的苯酚类污染物及其衍生物毒性大,难降解。刘杰等[22]将Fe3O4-MnO2复合材料作为Fenton催化剂用于去除水中的对氯酚,与Fe3O4-H2O2和MnO2-H2O2体系相比,Fe3O4-MnO2-H2O2体系具有更高的催化活性,对氯酚降解率达96.8%,但Fe3O4-MnO2-H2O2体系在较低pH条件下才具有较高的催化降解效果。通过外加磁场的方法可以实现Fe3O4-MnO2催化剂的回收。
Fe3O4-MnO2催化剂也可活化水中的O3和PS。NAWAZ等[16]研究了介孔Fe3O4-MnO2复合材料催化O3降解水中酚类混合物的情况,在体系pH为9、催化剂加入量为0.2 g/L、O3流量为2.5 mg/min的条件下,Fe3O4-Mn2O3、Fe3O4-MnO2、Fe3O4-MnCO3、Fe3O4和MnO2催化O3降解水中Ph-CH3(1 mmol/L)的降解率分别为64.2%、99.5%、73.1%、75.8%和89.4;催化O3降解水中Ph-Cl(1 mmol/L)的降解率分别为56.6%、93.9%、59.8%、66.9%和79.1%。Fe3O4-MnO2展现出较强的催化性能。
DONG[23]采用水热法合成了Fe3O4-α-MnO2复合材料,活化PS降解水中双酚A。在体系pH为中性、室温、双酚A加入量30 mg/L、PS加入量3.0 mmol/L、Fe3O4-α-MnO2加入量1.2 g/L的条件下,反应90 min,水中双酚A降解完全,Fe3O4-α-MnO2催化剂可重复利用。
3 Fe3O4-MnO2复合材料催化降解水中有机污染物的机理研究
3.1 活化H2O2催化降解水中有机污染物的机理研究
Fe3O4-MnO2复合材料中的Fe2+和Mn4+可活化H2O2产生·OH降解水中有机污染物。刘杰等[22]研究发现,Fe3O4-MnO2核壳结构催化剂活化H2O2降解水中四氯酚(4-CP)的降解率接近100%,而单独的Fe3O4和MnO2催化H2O2降解水中4-CP的降解率只有44.2%和33.2%。表明Fe3O4-MnO2催化剂中的Fe3O4和MnO2存在协同催化效应。
FANG等[20]采用Fe3O4-MnO2活化水中H2O2降解水中酸性橙7,机理主要涉及H2O2被催化后产生HO2·、O2-·、HO·等自由基,具体降解机理如下:
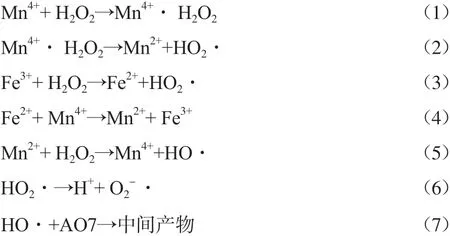
3.2 活化PS催化降解水中有机污染物的机理研究
PS被催化剂活化后产生强氧化性的SO4⁻·,SO4⁻·在水溶液中存在的时间长,在酸性条件下SO4⁻·也可以稳定存在。此外,SO4⁻·和·OH相比,接触有机污染物的时间更长,因此,SO4⁻·比·OH降解有机污染物更彻底。
MnO2本身可以高效活化PS催化降解水中有机污染物[24],引入Fe3O4不但可以使活化效率提高,也解决了MnO2难以固液分离的缺点,使Fe3O4-MnO2催化剂可循环利用。LIU等[25]利用Fe3O4-MnO2催化剂活化水中PMS降解水中4-CP的机理主要是Fe3O4-MnO2催化剂中的Mn4+起到活化水中PMS的重要作用,Fe2+在一定程度上也可以起到活化PMS产生SO4⁻·的作用,PMS被活化后产生SO4⁻·、SO5⁻·等自由基,具体降解机理如下:
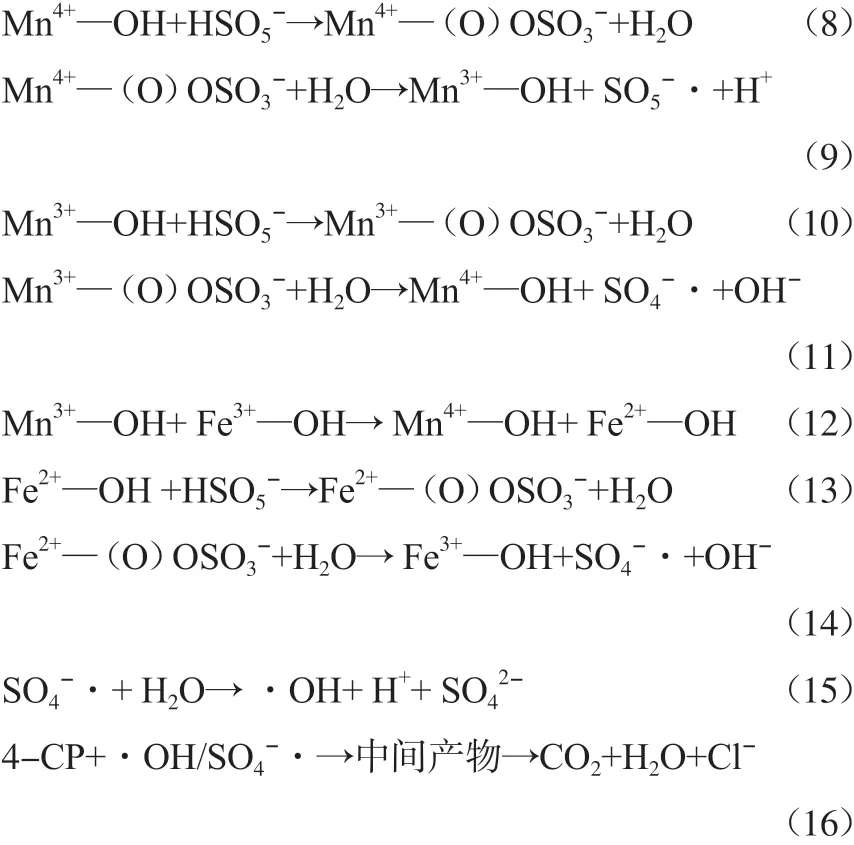
3.3 活化O3催化降解水中有机污染物的机理研究
O3分子具有强氧化性,容易降解含有双键基团的有机物,而对小分子的醛酸类有机污染物降解效果不明显,单独的O3直接氧化水中有机污染物效率不高[26]。Fe3O4-MnO2复合材料催化O3氧化水中有机污染物具有催化能力强、易于分离循环利用、稳定性好、原料易得的优势。
气态的O3在催化剂表面分解主要包括两个步骤:催化剂对水中O3的吸附和催化剂吸附的降解中间产物对水中O3的解吸附。LÜ等[27]发现,O3分子在催化剂表面吸附与水分子存在竞争关系,O3在水中转化为·OH后降解水中有机污染物。NAWAZ等[16]研究发现:Fe3O4-MnO2复合材料的表面不但吸附水中O3,还吸附水分子,吸附的O3与氢氧根离子反应生成·OH,·OH分散在溶液中降解水中有机污染物,Mn4+的存在增加了催化剂表面的路易斯酸性基团的数量,进而增加对O3的吸附量,所以Fe3O4-MnO2复合材料可以吸附更多的O3,产生更多的·OH。
3.4 光催化降解水中有机污染物的机理研究
Fe3O4-MnO2复合材料在光催化领域也有应用,其机理主要是利用光照的条件,在光催化降解过程中发生电子的转移以及价带、导带和空穴的形成。ZHANG等[17]制备的以MnO2为核,外部涂以Fe3O4的纳米复合材料,在紫外光照射下对水中亚甲基蓝具有优良的降解性能。
溶液pH可以影响光催化剂的表面电荷特性,从而影响光催化剂吸附水中有机污染物的行为[28]。研究者提出了MnO2-Fe3O4复合材料在高pH和低pH条件下光催化降解水中亚甲基蓝的机理。在酸性溶液中,带正电荷的MnO2-Fe3O4复合材料光催化产生·OH降解水中的亚甲基蓝,但是水中的亚甲基蓝发生电离后带有正电荷,同性相斥造成MnO2-Fe3O4复合材料吸附水中亚甲基蓝的速率减弱。另一方面,在高pH环境下,带负电荷的MnO2-Fe3O4复合材料会减少MnO2-Fe3O4复合材料和亚甲基蓝分子之间的静电排斥,加快吸附水中亚甲基蓝的速率。但MnO2-Fe3O4复合材料的光催化效率取决于水中·OH的多少,这也是亚甲基蓝的降解速率在弱酸性条件下高于在强碱性条件下的原因。经过实验得知:MnO2-Fe3O4复合材料光催化剂降解水中亚甲基蓝最佳的pH为7.5,这是静电吸引和在MnO2-Fe3O4复合材料光催化剂表面产生·OH的分散作用的综合效应。
4 进一步提高Fe3O4-MnO2复合材料催化性能的研究
研究者为了更高效地降解水中有机污染物,对Fe3O4-MnO2复合材料进行了一系列的拓展研究。
1)在Fe3O4-MnO2复合材料上再负载活性基团。这些活性基团主要包括一些金属氧化物、活性炭(AC)、石墨烯、凹凸棒等。黄晓东[29]将Fe3O4-MnO2复合材料负载到AC上合成Fe3O4-MnO2-AC复合催化剂,通过活化过硫酸盐降解染料效果良好。王艳等[30]将Al2O3负载到Fe3O4-MnO2复合材料上,用其催化H2O2降解水中偶氮染料活性黑5,去除效率比Fe3O4-MnO2复合材料显著提高。贾若琨等[31]合成的Fe3O4-MnO2-MgO复合催化剂可以高效催化H2O2降解水中亚甲基蓝。夏文君等[32]将铁锰氧化物负载到石墨烯上合成rG-Fe2MnO4催化剂可高效活化PMS降解水中金橙G。MEI等[33]合成的Fe3O4-MnO2@石墨烯催化剂可活化H2O2降解水中亚甲基蓝。吕杭杰等[34]在凹凸棒上负载Fe3O4-MnO2,可协同O3氧化处理甲基橙废水。
2)多种催化方式并用。李彤等[35]采用微电解法辅助铁-锰-碳复合材料处理对苯二酚废水,对苯二酚降解率可达95.55%,效果显著。
5 结语与展望
a)Fe3O4-MnO2复合材料在催化降解水中有机污染物方面具有很广阔的应用潜力。关于Fe3O4-MnO2复合材料活化PS降解水中有机污染物的研究较多,将过渡金属氧化物负载到Fe3O4-MnO2复合材料上,两者协同作用可增强其催化降解能力。目前,关于Fe3O4-MnO2复合材料用于光催化的研究较少,将光催化剂负载到Fe3O4-MnO2复合材料上,可制备新型光催化剂,提高光催化剂的回收性能。
b)Fe3O4-MnO2复合材料未来的研发方向是实现负载方式的多样性和提高复合材料的热稳定性,制备出形貌多样、结晶性能好、稳定性高、经济性好、功能多样的Fe3O4-MnO2复合材料。

