妊娠期糖尿病合并子痫前期患者临床特点分析
刘素新,罗梦梦,胡小月,霍 琰
(1.河北省人民医院产科,河北 石家庄 050051;2.金华市中心医院产科,浙江 金华 321000)
据世界卫生组织(WHO)最新研究发现妊娠期肥胖发生率高达25.3%[1],其可导致妊娠期糖尿病(gestational diabetes mellitus,GDM)、妊娠期高血压、子痫前期(preeclampsia,PE)、早产、巨大儿、产后出血等不良妊娠结局[2]。GDM及PE均是妊娠期常见并发症,可增加孕妇及新生儿远期代谢综合征风险[3-4]。孕前肥胖、妊娠期超重均可增加GDM、PE等不良妊娠结局的发生[5],但GDM患者中仅部分同时并发PE。本研究通过回顾性分析GDM合并PE妇女的临床特点、妊娠结局及其与孕前体质量的关系,探讨GDM合并PE的高危因素,以便早期识别,改善母儿结局。
1资料与方法
1.1资料来源
收集2016年9月至2018年10月在河北省人民医院定期进行产前检查并分娩的单胎妊娠孕妇共3 264例,其中单纯GDM患者480例,同时合并PE者70例。所有孕妇既往无肝肾功能不全、胃肠道疾病、肺部疾病、感染性疾病或甲状腺疾病、糖尿病等内分泌及代谢性疾病史,均未服用影响血脂、血糖代谢的药物,自愿加入调查并签署知情同意书。
1.2方法
采取回顾性研究,记录孕妇的年龄、孕前身体质量指数(body mass index,BMI)、分娩次数及方式、孕期是否患有并发症或合并症(如羊水过多、羊水过少、胎膜早破、产后出血、甲状腺疾病等);记录新生儿出生体质量、新生儿并发症(如新生儿呼吸窘迫综合征、新生儿高胆红素血症、新生儿咽下综合征等)。
GDM和PE疾病均参照《妇产科学》[6]进行诊断,孕前BMI分类参照中国成人分类标准[7]。本研究将甘油三酯(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)、极低密度脂蛋白胆固醇(VLDL-C)水平高于同孕期健康孕妇第95百分位数(P95)及高密度脂蛋白胆固醇(HDL-C)水平低于同孕期健康孕妇第5百分位数(P5)定义为妊娠期脂代谢异常(dyslipidemia,DLP)[8]。本组临床资料TG>4.73mmol/L,TC>7.91mmol/L,HDL-C<1.33mmol/L,LDL-C>4.74mmol/L,VLDL-C>1.08mmol/L,超过各值即诊断为DLP。
1.3统计学方法

2结果
2.1两组临床资料和生化指标的比较
GDM+PE组的孕前BMI、孕早期FPG、TG和VLDL-C水平均高于GDM组,而OGTT 2h血糖、HDL-C值则均低于GDM组,且GDM+PE组初产妇比率高于GDM组,两组比较差异均有统计学意义(均P<0.05);经Spearman相关性分析结果表明,孕早期FPG水平与OGTT 0h(r=0.310)、OGTT 2h(r=0.277)血糖值呈正相关(均P<0.05),而与OGTT 1h无相关性(r=0.130,P>0.05),见表1、表2。
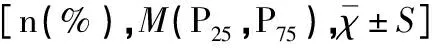
表1 两组临床资料的比较结果
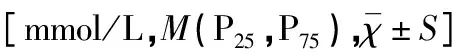
表2 两组生化指标的比较结果
2.2 GDM+PE相关因素的分析
2.2.1单因素分析情况
以是否发生GDM+PE疾病为因变量,以孕前BMI、孕早期FPG、TG、HDL-C、VLDL-C水平及产次为自变量,行单因素分析,结果显示孕前BMI≥24kg/m2及初产妇与GDM+PE疾病发生有关,见表3。
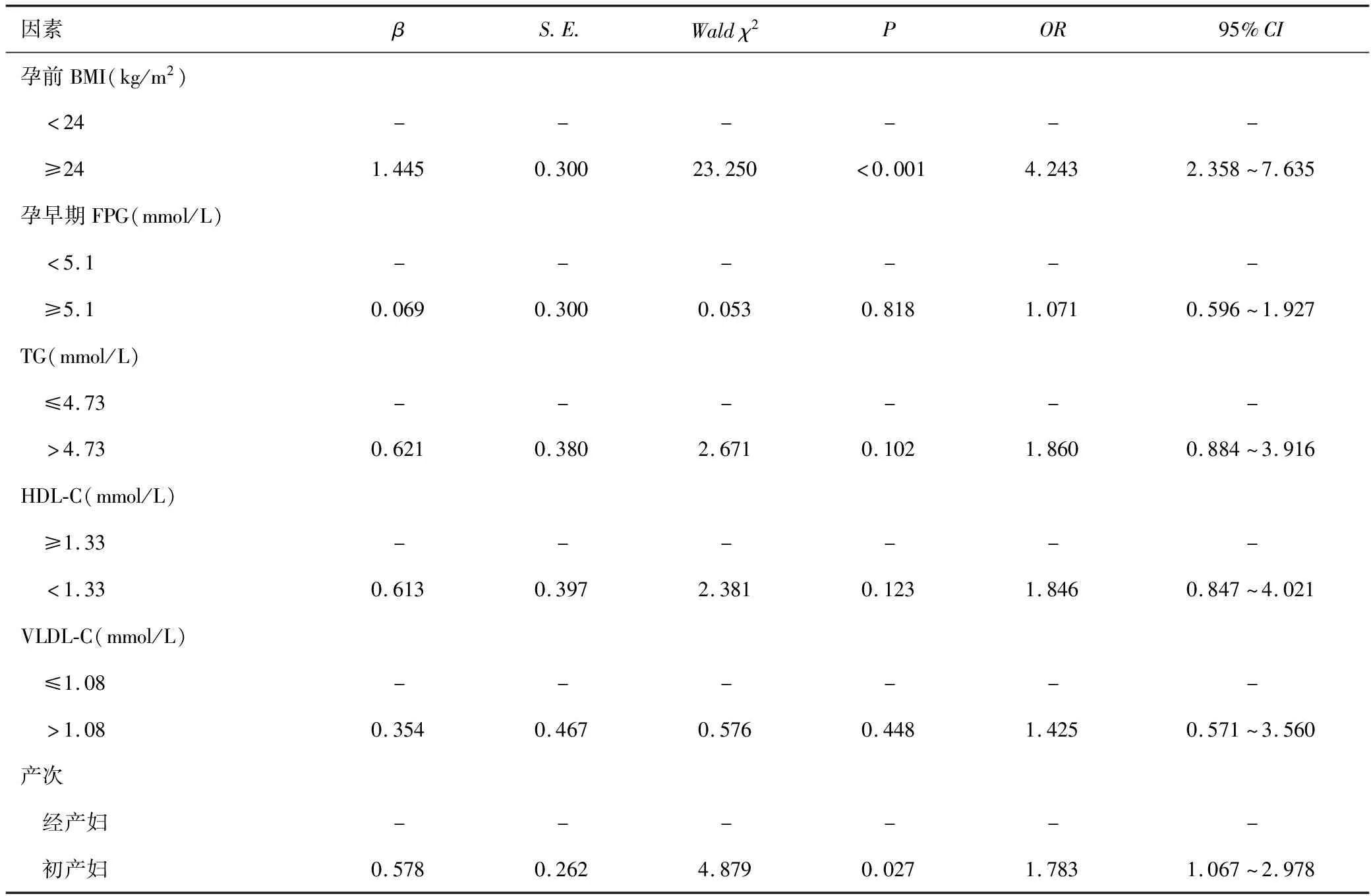
表3 影响GDM+PE疾病的单因素分析结果
2.2.2多因素分析情况
进一步行多因素Logistic回归分析,Logistic回归模型PGDM+PE=1/{1+exp[-(-3.177+1.496×孕前BMI≥24kg/m2+0.629×初产妇)]};结果显示孕前BMI≥24kg/m2发生GDM+PE疾病的风险是BMI<24kg/m2的4.463倍;初产妇发生GDM+PE疾病的风险是经产妇的1.876倍,可见孕前BMI≥24kg/m2及初产妇是发生GDM+PE疾病的高危因素,见表4。
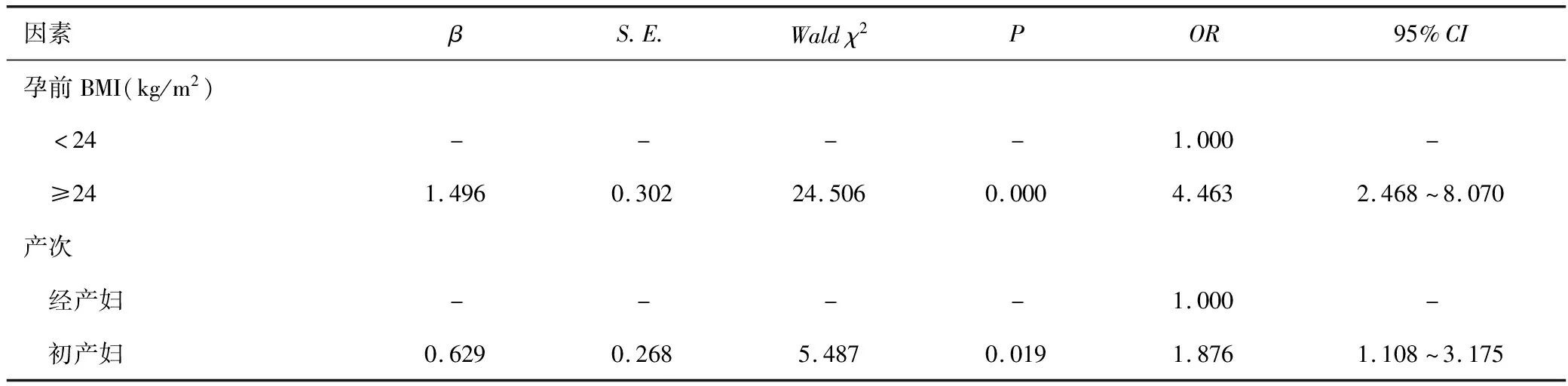
表4 GDM+PE疾病危险因素的多因素Logistic回归分析
2.3两组妊娠结局的比较
GDM+PE组发生羊水过多、早产儿、转NICU、低出生体质量儿及产后出血的发生率均明显高于GDM组,两组比较差异均有统计学意义(均P<0.05),见表5。
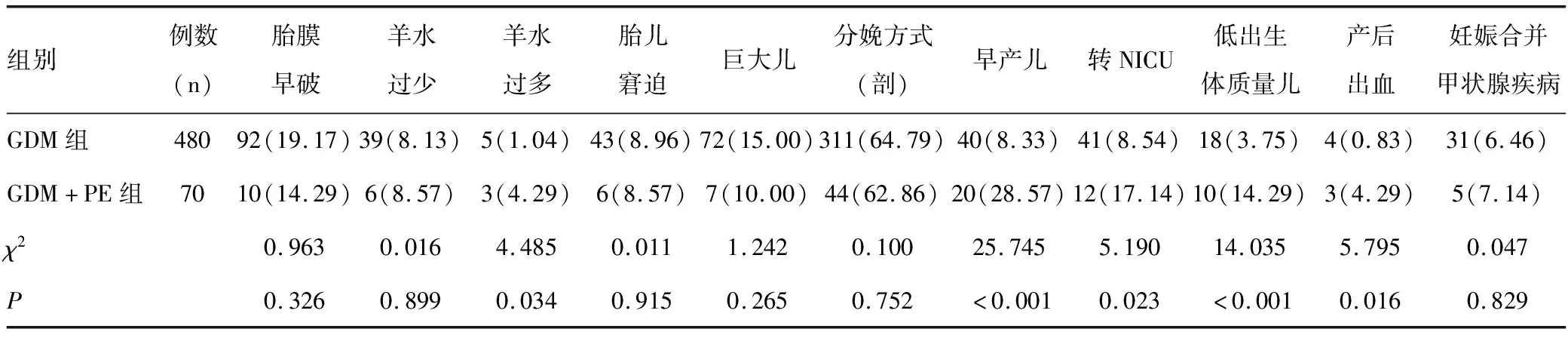
表5 两组妊娠结局的比较结果[n(%)]
3讨论
3.1孕前超重与肥胖是GDM并发PE的高危因素
GDM和PE是导致妊娠期母婴不良结局的主要原因,GDM合并PE的发生率较低[9],尚无充足证据明确两者间的具体机制。Vieira等[10]发现GDM和PE发病机制不同,且早孕期的胰岛素抵抗和炎症与PE发病无关[11]。陈鹏等[12]研究显示,孕前超重和肥胖的孕妇使妊娠期高血压疾病的风险明显增加,而GDM并非是PE的相关危险因素,其他相关因素在影响PE疾病的同时也对GDM产生了一定的影响。近来有研究发现两者发病机制相似,GDM是PE发病的独立危险因素,而孕前BMI的增加是两者发病最重要的预测指标[9]。GDM可继发血流动力学改变致动脉硬化和血压升高[13-14]。GDM患者良好的血糖控制可显著降低远期心血管疾病的风险[15]。
本研究将GDM组与GDM+PE组孕妇进行比较发现,GDM+PE的孕前BMI、孕早期FPG、TG、VLDL-C水平及初孕妇比率均高于GDM组,而HDL-C则低于GDM组(均P<0.05)。经多因素Logistic回归分析发现,仅孕前BMI≥24kg/m2及初产妇是GDM+PE的危险因素(均P<0.05),表明超重及肥胖是GDM合并PE的高危因素,这与以往研究结果[5,9,16]一致。分析原因可能是由于肥胖可致脂质水平异常,氧化血脂可直接或间接损伤内皮;另外,肥胖可诱发炎症因子的过度表达[17],多种炎性细胞因子分泌水平异常,如白介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)及c-反应蛋白(CRP)等进一步介导了炎症和胰岛素抵抗,从而影响妊娠期代谢过程,造成GDM和PE等不良妊娠结局[18-20]。Montoro等[21]研究显示,GDM发生PE组的初产妇率高于GDM组未发生PE组,GDM是PE发生的高危因素。胰岛素抵抗和细胞缺损是GDM的特征,很难排除其在妊娠期高血压疾病发病中的作用。GDM与妊娠期高血压疾病之间还可通过交感神经、CRP、TNF-α及内皮细胞之间相互作用,因此影响GDM发生的相关因素有可能直接或间接进一步促使并发妊娠期高血压疾病的发生[18]。同时,初产妇更容易精神紧张、焦虑,促进了病情的进展。本研究发现,GDM合并PE组中初产妇比率明显增高,初产妇也是GDM合并PE疾病的高危因素,与Montoro等[21]研究结果相似。
本研究中影响GDM发生的年龄、孕早期FPG、TG水平等均不是GDM合并PE疾病的危险因素,分析原因可能为:①与本研究中患有GDM合并PE疾病的孕妇孕期规范产前检查、孕期干预(调整饮食,控制血糖及血脂、血压等)、及时住院治疗有关;②两组样本量均较少,尤其是GDM合并PE疾病的患者病例数仅70例,故还需增加样本量进一步研究。
3.2 GDM合并PE增加不良妊娠结局的发生
与GDM组相比,GDM合并PE组的产后出血、羊水过多、早产儿、低出生体质量儿及转NICU发生率均明显增高(均P<0.05)。有研究显示,孕前超重及肥胖是产后出血的危险因素,考虑可能与肥胖孕妇脂肪堆积,腹肌、肛提肌乏力,出现原发性子宫收缩乏力、导致第二产程产力延长等产力因素有关[22-23]。肥胖可通过多条途径参与子宫收缩力的调节[24-25]。一项纳入了24 634名妊娠妇女的研究表明,肥胖与巨大儿、多胎妊娠等因素共同增加了产后出血发生率,结果证实肥胖并非产后出血的重要危险因素[26]。Butwick等[27]发现GDM、PE等可直接导致产后出血的发生,与GDM和PE发病有关的脂肪细胞因子,如瘦素、内脂素、生长素等细胞因子参与了子宫收缩的调节[28]。因此考虑GDM合并PE疾病发生产后出血的可能与两者发病的病理机制有关。有研究发现初产妇可能因子宫自身张力高、精神心理等因素易增加PE、GDM的发生,也增加胎膜早破和胎儿窘迫的发生,可能直接或间接地增加了早产、低出生体质量儿、转NICU的风险[29]。有研究显示,GDM、PE是导致早产的主要原因,因GDM孕妇易发生羊水过多,增加了胎膜早破、自发性早产的发生,若同时并发PE疾病,可影响胎盘血管结构及功能变化导致胎儿低体质量,胎儿长期缺血缺氧可致胎儿窘迫,往往需提早结束妊娠,使早产儿、低出生体质量儿及转NICU的风险均有所增加[30-31]。
总之,本研究表明GDM合并PE妊娠妇女孕前BMI、孕早期FPG、TG、VLDL-C水平及初孕妇比率均高于GDM妇女,孕前BMI≥24kg/m2、初产妇是GDM合并PE疾病发生的高危因素。GDM合并PE疾病的患者羊水过多、早产儿、低出生体质量儿、转NICU及产后出血等母儿并发症明显增多。因此,应做好孕前宣教,超重及肥胖妇女应控制体质量后再妊娠,孕期通过宣教、饮食调节及适量运动等方法控制体质量增长,减少GDM、PE疾病的发生,改善母儿预后。

