应用CBCT评价CGF促进颌骨囊肿术后骨缺损修复的临床研究
李欣,刘学,王杨,徐明
(华中科技大学协和深圳医院 口腔科,广东 深圳 518052)
0 引言
颌骨囊肿是口腔颌面外科的常见病与多发病,目前最常用的治疗方法为手术摘除。但是,术后颌骨内遗留的骨腔易导致继发感染、病理性骨折、种植牙骨量不足等并发症的发生。为了促进骨缺损区的愈合,骨移植是目前治疗颌骨囊肿术后骨缺损的主要方法。本研究应用锥体束CT(Cone Beam Computed Tomography,CBCT)评估浓缩生长因子(concentrated growth factors,CGF)联合羟基磷灰石生物陶瓷及口腔修复膜应用于颌骨囊肿手术,促进骨缺损的愈合,取得了满意的效果。
1 资料与方法
1.1 一般资料。病例收集2016年10月至2017年9月,于深圳市南山医院口腔科就诊,诊断颌骨囊肿并完成手术治疗的病人60例,受试者年龄18-60岁,男女性别比近1:1。以相似年龄、性别分布平均分为3组(每组病患数20例),均采用彻底刮治的方法切除囊肿,所有手术均由第一作者主刀完成。纳入标准:无不良烟酒嗜好及药物过敏史;患者身体健康,无严重的全身系统性疾病;有较好的依从性。排除标准:不符合颌骨囊肿纳入标准者;资料欠缺或不能配合手术者;骨质疏松患者;口腔卫生条件差者。
1.2 材料与设备。南山医院口腔科手术患者自体血液;离心机(Silfradent 塞法登特公司,意大利);真空采血管;羟基磷灰石生物陶瓷(北京市意华健科贸有限责任公司,中国);口腔修复膜(烟台正海生物技术有限公司,中国);CBCT Planmeca(Planmeca公司,芬兰);手术器械(南山医院口腔科)。
1.3 方法
1.3.1 CGF的制作:首先采集20-40 mL(2-4管)患者的静脉血,注入试 管中,注满后勿摇动,立即放入离心机的转筒中。设定制备 CGF 程序,制备完成后,可见试管中分为三层,最上层为血清,中间为纤维蛋白层(CGF的主要载体),底层为红细胞及血小板,留取纤维蛋白层及少部分底层的红细胞层,并存储在稀释的抗菌溶液中备用。
1.3.2 手术方式:术前采用相同视野及拍摄参数拍摄CBCT,完善常规检查,排除手术禁忌证,受累牙由同一位医生行完善的根管治疗或予以拔除。实验组,手术采用口内角形或梯形切口,翻瓣、去骨,充分暴露囊腔并完整刮除囊肿;行根尖切除术,彻底搔刮根尖周围及囊腔骨壁,球钻修整骨创缘,生理盐水冲洗;彻底止血后,将制备好的适量CGF剪碎至约1 mm大小颗粒,及羟基磷灰石生物陶瓷彻底混合,混合物填塞入缺损骨腔,适当加压,平齐原骨创缘。后覆盖海奥口腔修复膜,并将剩余的CGF材料压制成膜,再以CGF膜覆盖于海奥口腔修复膜之上表面,组织瓣对位缝合,关闭创口。术后应用抗生素3 d,复方氯己定含漱液漱口1周,7-10 d拆线。对照组,手术方式相同,只是未植入cgf。空白对照组,手术方式一样,缺损骨腔内未植入任何材料。
1.3.3 术后随访:患者术后每隔3个月定期复诊,临床检查创口愈合情况,相同视野及参数下拍摄CBCT。
1.4 测量方法。HU值:可反应出单位区域的平均骨矿物质含量,可作为骨缺损修复的重要指标。在植骨区和正常骨组织区截取相同面积的区域,分别测量HU值。HU差值=植骨区域平均HU值-正常区域平均HU值。HU差值越小说明植骨区与正常骨组织骨密度差距越小,骨愈合越快越好。选取骨缺损最长直径对应的失状面、冠状面和轴面为测量平面,测量平面平均Hu值。同时测量颌骨对应正常位置相同面积平面的平均HU值。术后3个月、6个月分别测量。所有病例测量均由一人完成,且每个位置重复测量三次取平均值。
1.5 统计学分析。实验数据采用SPSS 23.0统计软件进行单因素方差分析,α=0.05。
2 结果
2.1 临床检查。术后观察随访3-6个月。60例患者全身情况良好,口腔内术后伤口均达到一期甲级愈合,无感染、裂开,无膜暴露及骨粉溢漏,对应黏膜颜色、质地正常。
2.2 影像学观察、测量数据分析。3个月、6个月时,组一(CGF+GBR)从失状面、冠状面及轴面三个面HU差值均优于组二(GBR)及组三(空白)。提示颌骨囊肿骨缺损区的愈合效果及愈合时间组一(CGF+GBR)最佳,并有显著差异(P<0.05)。三组都可见到,术后6个月相比3个月骨缺损区域的愈合情况更好,详情见表1、表2、表3。
表1 各时间段各组冠状面HU差值及统计学分析(±s)
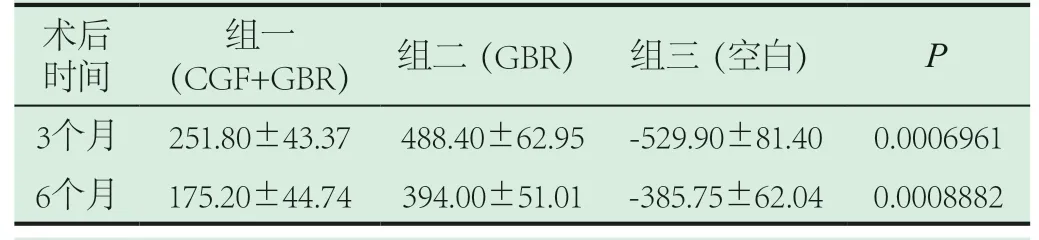
表1 各时间段各组冠状面HU差值及统计学分析(±s)
?
表2 各时间段各组失状面HU差值及统计学分析(±s)

表2 各时间段各组失状面HU差值及统计学分析(±s)
?
表3 各时间段各组轴面HU差值及统计学分析(±s)

表3 各时间段各组轴面HU差值及统计学分析(±s)
?
3 讨论
Buser等在1993年提出了引导骨再生(GBR)的概念。现在,GBR技术已被广泛应用在牙槽外科、牙周科和口腔种植领域[1]。在GBR技术中各种骨替代材料与血浆提取物的混合使用在目前的临床应用中被广泛使用。
浓缩生长因子(CGF)是Sacco首次开发出来的,由静脉血分离制作而成[2]。是继富血小板血浆(plateletrich plasma,PRP)和富血小板纤维蛋白(platelet-rich fibrin,PRF)之后的第三代血浆提取物,促进骨缺损修复和软组织愈合[3-5]。
CGF技术是以患者自身静脉血为原料,通过梯度密度离心的方法获得,再单独或联合其他生物材料注入硬组织缺损或软组织创伤处,从而修补缺损,诱导生长,加速局部创伤的愈合并提高愈合质量。其中的浓缩生长因子包含:骨形成蛋白(BMPs)、血管内皮生长因子(VEGF)、表皮生长因子(EGF)、转移生长因子-β(TGF-β)、血小板衍生生长因子(PDGF)、类胰岛素生长因子(IGF)、以及成纤维细胞生长因子(FGF)等,它们有促进细胞增殖、促进血管生成、移植物存活及诱导骨组织再生的作用[6],并具有修复促进和促进创口愈合的功能[7]。
有实验表明,CGF与羟基磷灰石生物陶瓷联合使用后,二者在骨再生方面表现为相互促进,发挥协同作用的效果,并加快了骨组织再生,比单独应用羟基磷灰石生物陶瓷效果更佳[8]。
羟基磷灰石生物陶瓷,在骨增量手术中应用较广泛。其结构呈多孔状,对成骨细胞有支架作用,可维持或增加成骨空间。但HA无骨诱导性,仅起骨引导作用。本研究结果表明,采用CGF联合HA骨粉、口腔生物膜进行GBR手术,完成颌骨缺损修复的治疗,取得了满意的效果。国内外部分研究也同样支持CGF联合骨替代用品,在修复颌骨缺损方面具有良好的效果。
CGF来源于自体本身,无毒性和免疫原性,操作提取简单而费用低廉,临床应用安全,因此其应用前景应十分广阔。本研究通过测量比较组一(CGF+HA+修复膜)、组二(HA+修复膜)和组三(空白对照)术后3-6个月,经CBCT测量植骨区和正常骨组织密度的变化,对比说明不同方式对颌骨缺损修复的不同影响。结果显示不同时间段组一和组二相对组三都取得了良好的骨愈合结果,而组一相比组二,在相同时间点上取得了更好的颌骨愈合情况。说明CGF同羟基磷灰石生物陶瓷以及口腔修复膜的联合应用,对颌骨骨缺损的再生修复有明显的促进作用,且再生所需时间短。
骨组织再生是一个极其复杂的过程,生长因子相互作用的机制还未完全明确。以及骨粉和CGF的混合比例、两种混合物植入骨缺损区的松紧度等因素是否存在影响亦有待进一步研究。相信随着相关基础性研究和临床试验的不断深入,CGF的应用前景必将更为广阔。

