多相流海底管道内腐蚀模型研究
(重庆工商大学融智学院,重庆 401320)
调研发现,作为海上油气田的主动脉和生命线[1]的海底管道49%为混输管道[2],其输送的介质为油、气、水多相介质,其流动形态复杂且气相介质中含有CO2/H2S,水相介质中存在Cl-,比单相输送的腐蚀更严重,同时增加了管道腐蚀速率预测的难度。
崔钺等[3]基于流场作用和De Waard 95腐蚀预测模型,改进了CO2腐蚀模型,为天然气管线腐蚀预测体系的建立提供一种新思路。张清等[4]首次将分压比pCO2/pH2S引入油管钢腐蚀速率预测模型,在不同分压比下,视一种气体腐蚀为主导,另一种气体腐蚀为影响因素来建立两个分模型,进而将两个分模型叠加,得到总的腐蚀速率预测模型。该预测模型与已有预测模型完全兼容,且与试验数据吻合较好。姚彬等[5]研究油管腐蚀是由H2S-CO2-Cl--H2O体系引起的电化学腐蚀,以CO2腐蚀为主,同时存在H2S腐蚀,Cl-对腐蚀穿孔有一定的促进作用。建议添加缓蚀剂或对油管添加表面涂层、镀层和油管衬里,提高油管服役寿命。
通过调研发现,针对CO2/H2S/Cl-共存条件下的腐蚀机理有专家在进行研究,但是对于多种因素下的协同腐蚀模型研究较少。因此,为了更好地掌握海底管道在CO2/H2S/Cl-多因素协同作用下的腐蚀速率,亟需研究海底管道在CO2/H2S/Cl-共存条件下的腐蚀模型。
1 腐蚀机理
1.1 CO2腐蚀机理
碳钢的CO2腐蚀被称为甜腐蚀,是石油和天然气工业中的主要问题。干燥的CO2气体本身不具有腐蚀性,遇水生成碳酸,与金属表面接触产生腐蚀。CO2的反应式[6]为:

(1)
(2)
(3)

(4)
因此,CO2腐蚀形成的腐蚀产物FeCO3,根据腐蚀环境的不同,具有不同的表现形式,在某些环境中对钢铁具有一定的保护性。
1.2 H2S腐蚀机理
碳钢的H2S腐蚀被称为酸腐蚀。近年来,海底管道输送中含有大量的H2S,因此解决此问题变得更加重要。尽管对H2S与低碳钢的相互作用的机理已经进行了研究,但由于其复杂性和H2S的毒性,所以关于H2S的腐蚀机理研究的成果较少[7-8]。

(5)

(6)



(7)
1.3 CO2/H2S共存条件下的腐蚀机理
尽管H2S气体的溶解度比CO2气体高(约3倍),但由H2S的离解产生的酸比碳酸弱,因此,H2S气体对降低溶液pH值的影响与CO2气体大致相同。与溶解的CO2不同,气态的H2S需要一个溶解的步骤,形成H2Sad,才能形成酸。如果是溶解后的H2S,则不需要水合的步骤。
一般来说,CO2/H2S系统中的三种腐蚀机理可以根据H2S的浓度进行分类[9],见图1。

图1 CO2/H2S系统腐蚀机理
研究表明:在CO2/H2S同时存在的金属腐蚀环境中,H2S的存在既能通过阴极反应加速金属的腐蚀,也能通过腐蚀产生的FeS沉淀产物,形成保护膜来减缓金属腐蚀。因此,在如何判断是加速腐蚀还是减缓腐蚀问题上,需要进一步研究。在两者共存的情况下,金属的腐蚀速率受到两者相对含量的影响,但是试验结果具有很大的离散性。据文献[10]报道:当H2S分压小于690 Pa时,反应会形成FeS沉淀,在金属表面形成致密的保护膜而减缓腐蚀。当H2S分压大于或等于690 Pa时,生成的产物不具有保护性。因此,腐蚀产物膜生成情况对H2S的腐蚀严重程度产生影响。同时,温度和流动状态都会影响到H2S腐蚀的严重程度。
1.3.1 H2S主导(酸状态)
溶解的H2S是弱酸,因此,通过提供额外的阴极反应,H2S不仅降低了溶液的pH值,而且还可以通过提供阴极反应,加速管道的腐蚀:

(8)
如果H2S的量足够高,此时的H2S可以直接还原,这表明此时是由H2S主导的系统。此外,元素硫通常与高浓度的H2S相关。H2S也能导致酸性水环境钢的氢鼓泡和硫化物应力腐蚀开裂。
1.3.2 CO2主导(甜状态)
除了“酸状态”相关的腐蚀开裂之外,少量的H2S可以以各种方式影响CO2腐蚀。Ioffe A V[11]研究发现少量的H2S会降低腐蚀速率。另一方面,H2S的存在也可根据反应式(9)形成FeS薄膜。

(9)
根据各种环境因素,可以形成不同形态的FeS。在某些情况下,FeS薄膜可能是非保护性的,易导致钢的局部腐蚀。
当H2S在以CO2为主的体系中以低浓度存在时,FeS膜会干扰FeCO3的形成[12]。这是因为FeS薄膜比FeCO3膜更容易从管壁上除去。在湍流条件下,产物易脱落,会导致腐蚀速率增大。
CO2/H2S体系结垢的热力学过程十分复杂,至今仍未得到很好的理解。在一些条件下,表面垢的组成不仅取决于介质的化学性质、FeCO3和FeS的溶解度,而且还取决于两种结垢机制的动力学。
(1)Fe3C
Fe3C是碳钢的一种相组织,在低碳钢被腐蚀后留下的腐蚀产物。碳化铁薄膜具有导电性、多孔性,不具有保护性[13]。这种多孔性薄膜的形成可能会导致其与金属基体形成腐蚀电池,从而加速腐蚀。
(2)FeCO3
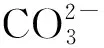
(3)FeS
FeS保护膜的结构和组成在很大程度上取决于体系中H2S浓度。薄膜的保护性能主要取决于溶液的pH值[15]。当溶液pH值为3~5,H2S浓度较低时,FeS的保护膜抑制了基体的腐蚀[16]。
1.4 Cl-对腐蚀速率的影响
在Cl-存在环境中,碳钢的腐蚀反应式为[17-18]:

(10)

(11)

(12)
总反应为:

(13)

(14)

(15)
当Cl-浓度较低时,腐蚀产物膜与外界离子交换速率较慢,随着反应的进行,Cl-浓度逐渐减少,进而对β-FeOOH 的转化产生了影响,加速了管道的腐蚀。
2 腐蚀模型
2.1 CO2腐蚀模型
由挪威石油公司开发的Norsok模型是基于实验室数据和油田数据而建立的经验模型。腐蚀速率(Vcorr)预测模型的核心公式为:
(16)
式中:Kt——与温度以及腐蚀产物膜相关的常数;
S——与流速有关的管壁切应力,Pa;
fCO2——CO2的逸度;
f(pH)t——溶液的pH值对腐蚀速率的影响因子。
Norsok模型只考虑了流速对腐蚀速率的影响,没有考虑流型与流态的作用。
除了Norsok模型外,常见的模型还有Corpos模型、De Waard 95模型[19]、Casandra模型、Predict模型、ECE模型、IFE模型、Nesic模型和Gray模型[20],部分腐蚀预测模型对比分析见表1。

表1 腐蚀预测模型对比分析
2.2 H2S腐蚀模型
学者们对于CO2的腐蚀模型研究较多,且不同的学者根据自己的研究成果和理论分别建立了不同的腐蚀预测模型,针对单一条件下H2S的腐蚀预测模型研究较少。根据反应动力学理论可知,在一定条件下,腐蚀反应速率与反应物浓度有一定的关系,而实际腐蚀情况更为复杂,包括温度、压力、pH值和介质浓度等对腐蚀速率的影响,无法用简单的理论计算得到,若发生应力腐蚀则需要考虑力的大小、方向和变化的因素[21]。若不考虑其他因素的影响,H2S单独腐蚀时,其数学模型为:
ln(Vcorr)=C1+C2ln(pH2S)
(17)
式中:Vcorr——硫化氢的腐蚀速率,mm/a;
pH2S——硫化氢的分压,MPa;
C1,C2——常数。
2.3 CO2/H2S共存条件下的腐蚀模型

通常采用叠加的方法来建立腐蚀模型:
ln(VCorr-Total)=ln(VCorr-CO2)+ln(VCorr-H2S)+C
(18)
ln(VCorr-CO2)=C1+0.67ln(pCO2)
(19)
ln(VCorr-H2S)=k[ln(pCO2)+ln(pH2S)]+
2aln(pH2S)+bln(pH2S)+C2
(20)
式中:VCorr-Total,VCorr-CO2,VCorr-H2S——总的腐蚀速率、CO2的腐蚀速率、H2S的腐蚀速率,mm/a;
pCO2,pH2S——CO2的分压、H2S的分压,MPa;
C,C1,C2,k,a,b——常数。
2.4 腐蚀预测模型的修正
调研发现,腐蚀模型只考虑了CO2的分压、H2S的分压和流速的影响,但是在海底管道实际运行中,溶液中Cl-的存在会加速管道的腐蚀。Cl-对于腐蚀的影响主要分为两个方面:一方面是由于Cl-的存在使钝化膜不易形成,即使形成了腐蚀产物膜也有可能会遭到破坏,从而形成大阴极小阳极的情况,造成局部腐蚀;另一方面Cl-在浓度较高的情况下,由于Cl-和氧的吸附竞争,会导致金属表面膜中的氧的位置被Cl-替代,膜被溶解,从而导致腐蚀加剧。
由于氯离子的半径较小、活性较高,故能够吸附在钢铁表面,替代掉腐蚀产物膜中的氧原子,并与腐蚀产物膜中的阳离子结合形成可溶性氯化物。因此,为了精确预测海底管道的腐蚀速率,除了考虑CO2的分压、H2S的分压和流速的影响之外,还必须考虑Cl-的影响。在原有腐蚀预测模型的基础上,提出一个适用于海底管道多相流的腐蚀模型:
ln(VCorr-Total)=0.67ln(pCO2)+k[ln(pCO2)+ln(pH2S)]+2aln(pH2S)+bln(pH2S)+dln(v)+eln(CCl-)+C
(21)
式中:pCO2和pH2S——CO2的分压、H2S的分压,MPa;
C,k,a,b,d,e——常数;
v——介质流速,m/s;
CCl-——氯离子质量浓度,g/L。
某海底混输管道全长13.3 km;管段管材是X65管,直径为304.8 mm,壁厚为12.7 mm。入口压力1.28 MPa,入口温度60.6 ℃,出口压力0.75 MPa,出口温度54.3 ℃,CO2分压为4~7 kPa,H2S分压为0.064~0.128 kPa,Cl-质量浓度为10.135 g/L。
采用多相流专业软件模拟海底管道的流动状态,得到沿线的温度、压力、流速、CO2分压和H2S分压,见图2至图4。管道的真实腐蚀速率如图5所示。

图2 沿线的温度、压力分布
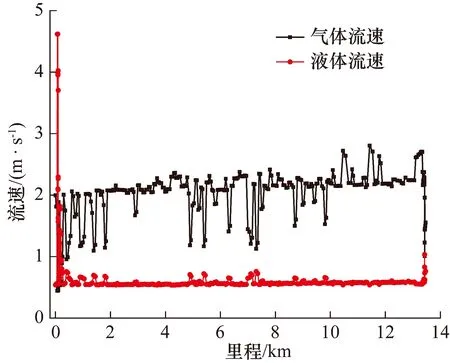
图3 沿线的流速分布

图4 沿线的CO2和H2S分压分布
由图2至图4可知,海底管道的温度、CO2和H2S分压随着管道的里程逐渐降低,根据修正的腐蚀模型判断出海底管道的腐蚀速率是逐渐降低的,且与实际管道腐蚀速率相符合。由图3可知,海底管道气体流速骤降的原因是:海底管道中存在立管,导致液体流速增加,同时也造成管道前段腐蚀速率增大。
根据公式(21)计算沿线的腐蚀速率,选取管线上的80个点作为训练数据,11个点作为预测数据(见表2),并将预测的腐蚀速率与海底管道的内腐蚀检测数据(见图5)进行对比分析。
通过误差分析发现,管线预测的腐蚀速率最大误差为15.198%,Norsok预测腐蚀模型的最大误差高达150.465%。因此,在含CO2/H2S/Cl-多相流海底管道中采用修正的预测腐蚀模型,能够准确地预测管道的腐蚀速率。

图5 海底管道的真实腐蚀速率

表2 预测点腐蚀速率
3 结 论
(1)通过对多因素协同腐蚀(CO2,H2S和Cl-)的机理分析,结合流动参数的模拟分析,建立了一个适用于海底输油管道多相流的腐蚀速率预测模型。
(2)常用的Norsok腐蚀预测模型预测误差达到150.465%,而修正的腐蚀速率预测模型的最高误差为15.198%,提高了腐蚀速率预测精度。

