基于CiteSpace的新型冠状病毒肺炎治疗研究现状及热点的可视化分析
王 艳,夏国光,程 洋,戴 丽
(北京积水潭医院呼吸与危重症医学科,北京 100035)
严重急性呼吸综合征冠状病毒2型(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)引起的新型冠状病毒肺炎(COVID-19)目前已构成全球大流行[1]。鉴于科学发现的速度之快以及大量人群感染SARS-CoV-2所产生的临床数据,临床医师及研究人员需要迅速了解COVID-19治疗相关研究的准确信息。CiteSpace软件是在科学计量学、数据可视化背景下逐渐发展起来的文献可视化分析软件,可通过可视化的手段来呈现某一研究领域的文献的基础知识、研究热点,预测研究特征及演变趋势[2]。本研究以PubMed数据库和Web of Science核心合集数据库作为数据来源,通过CiteSpace软件进行文献计量和可视化分析,快速、客观地提供COVID-19治疗领域的研究现状及热点信息。
1 资料与方法
1.1 数据来源及获取方法
检索PubMed数据库和Web of Science核心合集数据库,获取COVID-19治疗相关研究的文献,检索时间限定为2019年12月1日至2020年5月23,语言限定为英文。具体检索策略为:((SARS-CoV-2[Title/Abstract] OR 2019-nCoV[Title/Abstract] OR “2019 novel coronavirus”[Title/Abstract])OR(COVID-19[Title/Abstract] OR “2019 novel coronavirus infection”[Title/Abstract]))AND((Therapeutics[Mesh])OR(Treatment*[Title/Abstract] OR Therap*[Title/Abstract]))。
1.2 数据分析方法及指标解读
本研究使用CiteSpace 5.6.R3软件,设置时区分割中年份为2019—2020年,时间跨度分段长度为1年。分别选取作者、机构、国家、关键词、文献共被引和期刊共被引6个不同节点类型生成可视化图谱。节点大小与节点类型内容出现频次成正比;各节点之间的连线粗细及连线数量代表各节点之间的联系程度,联系越近,连线越粗越多。CiteSpace中使用中介中心性来量化节点在网络中地位的重要性,中介中心性越高,表示网络中越多的联系需要通过该节点,该节点在网络中常发挥桥梁作用,中介中心性≥0.1的节点常用紫色圈进行重点标注。
2 结果
根据以上检索策略,在PubMed数据库中初步检索出3 699篇文献,在Web of Science核心合集数据库中初步检索出995篇文献,共计4 694篇文献。将所有文献导入Endnote X9.2软件进行去重,发现643篇重复文献,最终纳入4 051篇文献进行分析。
2.1 合作网络分析
2.1.1 作者合作网络分析:依据普赖斯定律[3]可以计算核心作者的数量,计算公式为N=0.749×(ηmax)×1/2,其中ηmax代表发文量最多的作者所发的论文数量,发文量>N篇的作者称为核心作者。CiteSpace统计结果显示,发文量最多的作者为“LIU LEI”,共发文9篇,由上述公式可得出N=3.37,故COVID-19治疗相关研究的核心作者须满足发文量≥4篇。经CiteSpace统计,共有106名作者符合上述要求,限于篇幅所限,列出发文量≥7篇的主要核心作者,见表1。COVID-19治疗领域目前主要包括3个团队,“LIU LEI”“LINDSEY R BADEN”和“BÉLA FÜLESDI”分别为3个团队的核心;3个团队内部合作较为密切,但团队之间合作较少,见图1。

表1 COVID-19治疗领域的主要核心作者(频次≥7次)Tab 1 Main core authors in the field of COVID-19 treatment (frequency≥7 times)
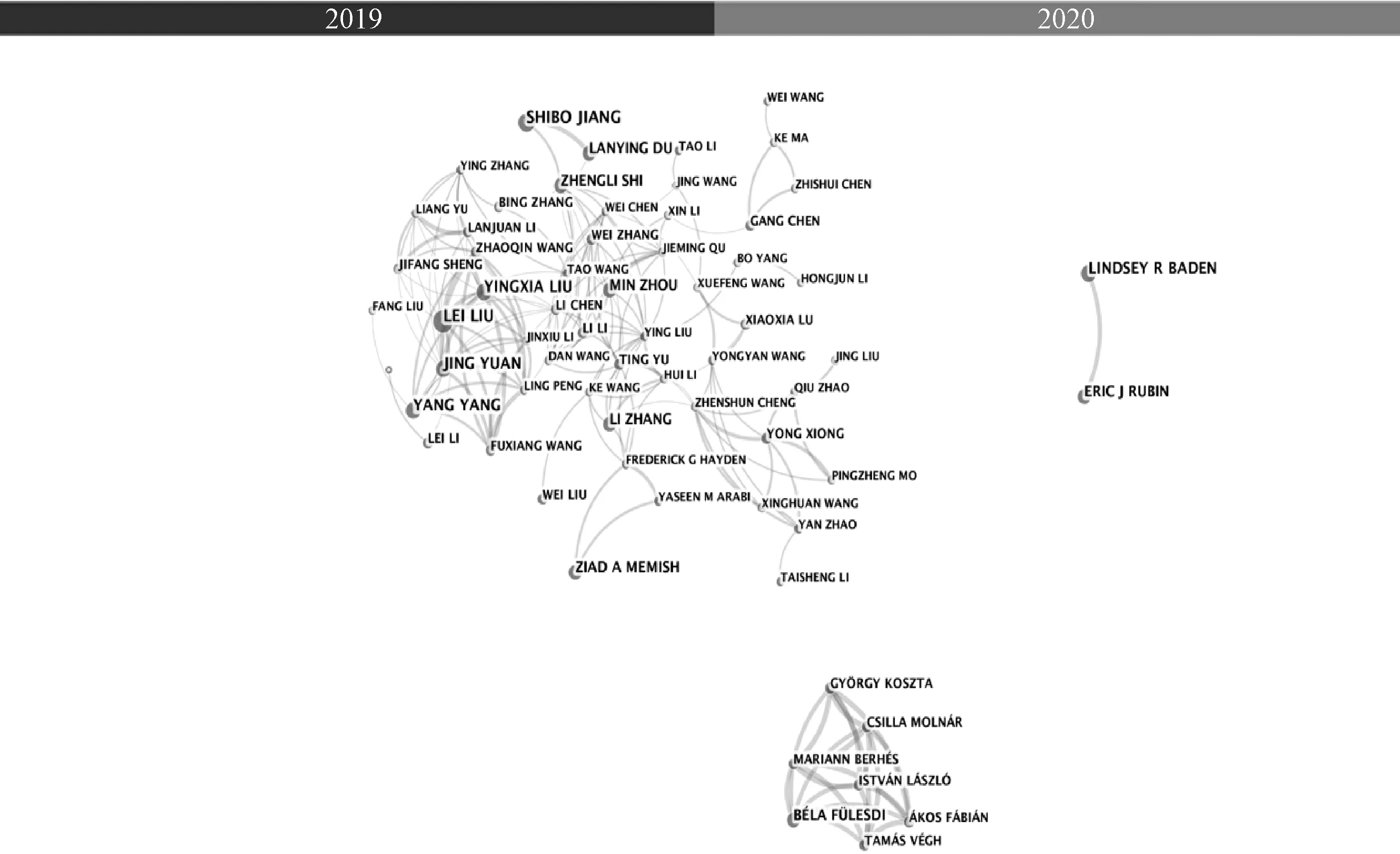
图1 COVID-19治疗领域的作者合作网络的可视化图谱Fig 1 Visualization map of co-author analysis in the field of COVID-19 treatment
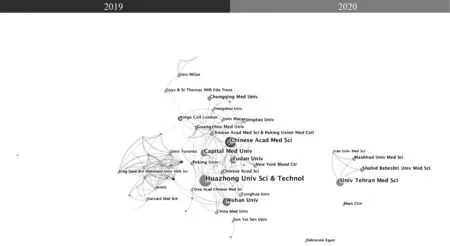
图2 COVID-19治疗领域的机构合作网络的可视化图谱Fig 2 Visualization map of co-institutions analysis in the field of COVID-19 treatment
2.1.2 机构合作网络分析:COVID-19治疗领域的机构合作网络的可视化图谱见图2。由图2可见,发表文献较多的机构依次为华中科技大学(Huazhong University of Science & Technology)(64篇)、中国科学院(The Academy of Sciences of China)(58篇)、德黑兰医科大学(Univ Tehran Med Sci)(42篇)、首都医科大学(Capital Medical College)(41篇)、复旦大学(Fudan University)(38篇)和武汉大学(Wuhan University)(35篇)等;所有机构之中,中国科学院、北京协和医院(Peking Union Medical College Hospital)、武汉大学、伦敦国王学院(King’s College London)和麦克马斯特大学(McMaster University)的中介中心性>0.1,说明上述机构是促进国内外相关研究机构之间合作的关键枢纽;COVID-19治疗领域目前主要包括3个主要研究团队,其中华中科技大学和中国科学院、多伦多大学(Univ toronto)、德黑兰医科大学分别为3个团队的核心。
2.1.3 国家合作网络分析:全球共有52个国家和地区发表了COVID-19治疗相关文献,发文量排序居前10位的国家为中国(536次)、美国(463次)、意大利(240次)、法国(79次)、印度(71次)、德国(65次)、加拿大(61次)、澳大利亚(58次)、伊朗(42次)和英国(29次)。中国、美国和意大利3个国家发文量多,且中介中心性高,说明在其本身投入大量人力物力资源进行COVID-19治疗的同时亦注重国际间合作,见图3。

图3 COVID-19治疗领域的国家合作网络的可视化图谱Fig 3 Visualization map of co-countries analysis in the field of COVID-19 treatment
2.2 关键词共现分析

图4 COVID-19治疗领域关键词共现可视化图谱Fig 4 Visualization map of co-occurrence network analysis of keywords in the field of COVID-19 treatment
关键词是文献内容重要信息的体现,一定时期内出现频次高的关键词可能是当时领域内的研究热点或研究重点[4]。COVID-19治疗领域关键词共现可视化图谱见图4,前30位的高频关键词见表2。可见,目前COVID-19治疗的热点主要集中在抗病毒药(包括洛匹那韦/利托那韦、瑞德西韦等)、免疫调节(包括托西珠单抗、恢复期血浆等)和中医药(包括莲花清瘟制剂等)3个方面。

表2 COVID-19治疗领域的高频关键词(前30位)Tab 2 High frequency keywords in the field of COVID-19 treatment (top 30)
2.3 共被引分析

图5 COVID-19治疗领域文献共被引分析的可视化图谱Fig 5 Visualization map of literature co-citation analysis in the field of COVID-19 treatment
2.3.1 文献共被引分析:通过对被引文献进行共被引分析可发现被引频次较高的文献。通常,被引频次高低可在一定程度上反映文献的学术影响力和经典程度。对Web of Science核心合集数据库检索出的341篇文献进行文献共被引分析,结果见图5。被引频次排序居前2位的论文分别为:(1)Huang CL(2020年)[5](共被引频次130次)。该研究详细介绍了我国武汉市COVID-19患者的流行病学、临床表现、实验室检查结果、放射学特征、治疗和临床结局。该研究涉及41例COVID-19患者,所有患者均接受了经验性抗菌药物治疗,其中38例患者接受了抗病毒治疗(奥司他韦);此外,有9例患者接受了糖皮质激素治疗。(2)Chen NS(2020年)[6](共被引频次89次)。该文献中详解介绍了99例COVID-19患者的流行病学和临床特征,提示SARS-CoV-2感染呈聚集性,更可能影响患有合并症的老年男性,并可能导致严重甚至致命的呼吸系统并发症。99例患者中,75例接受了抗病毒治疗,包括奥司他韦、更昔洛韦以及洛匹那韦/利托那韦,大多数患者接受了单一(25/99)或联合(45/99)的抗菌药物治疗,19例患者还接受了糖皮质激素治疗。中介中心性可发现和衡量节点内容的重要性。在所有共被引文献中,中介中心性排序居前2位的文献为:(1)Arabi YM(2020年)[7](中介中心性为0.17)。这是一项回顾性队列研究,目的是评估利巴韦林和重组干扰素(RBV/rIFN)治疗对重症中东呼吸综合征(Middle East respiratory syndrome,MERS)患者预后的影响。结果提示,RBV/rIFN疗法通常用于重症MERS患者,但与降低90 d死亡率或更快的MERS病毒 RNA清除无关。(2)Wang M(2020年)[8](中介中心性为0.12)。该研究评估了5种现有的经过美国食品药品管理局批准的药物(利巴韦林、喷昔洛韦、硝唑尼特、萘莫司他和氯喹)和2种广谱抗病毒药(瑞德昔韦、法匹拉韦)对临床分离的SARS-CoV-2的体外抗病毒效力,结果显示,瑞德昔韦和氯喹在体外控制SARS-CoV-2感染方面非常有效。
2.3.2 期刊共被引分析:对Web of Science核心合集数据库检索出的341篇文献进行期刊共被引分析,结果见图6。共被引频次排序居前10位的期刊依次为《Lancet》(233次)、《New England Journal of Medicine》(208次)、《Nature》(106次)、《Jama-journal Of The American Medical Association》(93次)、《Journal of Medical Virology》(86次)、《Journal of Virology》(76次)、《The Journal of the American Medical Association》(65次)、《The Lancet Infectious Diseases》(62次)、《PLoS ONE》(59次)和《Science》(59次),涉及医学综合、病毒学、传染病学和免疫学等多个学科。

图6 COVID-19治疗领域期刊共被引分析的可视化图谱Fig 6 Visualization map of journal co-citation analysis in the field of COVID-19 treatment
3 讨论
SARS-CoV-2是一种单链RNA包膜病毒,通过与血管紧张素转换酶2(angiotensin converting enzyme 2,ACE2)受体结合的S蛋白(刺突糖蛋白)入侵细胞。与受体结合后,病毒颗粒利用宿主细胞受体和核内体进入细胞。宿主2型跨膜丝氨酸蛋白酶(TMPRSS2)有助于病毒通过S蛋白进入。一旦病毒进入细胞,就可以合成编码复制酶-转录酶复合物的病毒多聚蛋白。然后,病毒通过其依赖于RNA的RNA聚合酶合成RNA,合成结构蛋白导致病毒颗粒装配和释放[9]。上述病毒的生命周期步骤提供了治疗的潜在靶点。
本研究进行作者、机构和国家合作网路分析,结果提示,各国学者、机构广泛关注COVID-19治疗领域并展开密切合作,即使在COVID-19大流行期间,为研究COVID-19的可能的治疗方法,在短时间内启动了为数众多的临床试验以寻求高质量证据。我国学者、研究机构为COVID-19治疗领域的研究主力。
通过对关键词的共现分析,揭示了COVID-19治疗的研究热点主要集中于抗病毒药、免疫调节和中医药3个方面。
抗病毒药方面:在当前全球紧急情况下,正常药物开发途径的速度无法满足医疗需求。因此,在上述SARS-CoV-2生命周期的基础上,已知对其他RNA病毒(包括人类免疫缺陷病毒、流行性感冒病毒、严重急性呼吸综合征冠状病毒和MERS冠状病毒等)有效的药物的重新利用和加速抗病毒治疗的发展引起了研究者们的广泛关注。有希望的药物靶标包括:(1)与其他冠状病毒具有同源性的非结构蛋白。①3-胰凝乳样蛋白酶和类木瓜蛋白酶。其负责将病毒肽裂解成功能单位,用于病毒在宿主细胞内的复制和包装。洛匹那韦/利托那韦是美国食品药品管理局批准的治疗人类免疫缺陷病毒的口服组合剂,通过体外抑制3-胰凝乳样蛋白酶证明了对其他冠状病毒的活性[10]。我国曹彬教授牵头的一项随机开放性研究结果提示,与对照组相比,洛匹那韦/利托那韦组的199例COVID-19患者在总体死亡率、病毒载量的降低方面均没有显著的获益[11]。目前的数据表明,洛匹那韦/利托那韦在COVID-19治疗中的作用有限。②RNA依赖的RNA聚合酶。其负责病毒RNA合成,可能被现有的抗病毒药阻断。如瑞德西韦,其最初是为治疗埃博拉病毒而开发的核苷类似物,在体内和体外模型中,其对包括严重急性呼吸综合征冠状病毒和MERS冠状病毒在内的一系列致病病毒都有疗效[12]。该药正在进行Ⅲ期临床试验,是目前最有希望的药物之一。我国重症COVID-19患者的随机、双盲、安慰剂对照研究结果显示,瑞德西韦对重症COVID-19患者的临床症状没有明显改善,其有效性仍有待研究[13]。(2)2型跨膜丝氨酸蛋白酶(TMPRSS2)抑制剂。宿主细胞产生的TMPRSS2在S蛋白的蛋白水解过程中起着重要作用,启动了SARS-CoV-2与ACE2受体的结合,TMPRSS2抑制剂甲磺酸卡莫司他有可能成为治疗COVID-19的药物[9]。(3)氯喹和羟氯喹。其可影响ACE2糖基化、蛋白水解过程,阻止病毒进入细胞,且具有免疫调节作用,体外可有效抑制SARS-CoV-2[8]。近期,一项检验羟氯喹疗效的非随机、开放研究报告了36例患者的队列研究,结果提示,与对照组相比,羟氯喹组患者在纳入6 d后鼻咽拭子病毒阳性率显著降低,但由于缺乏随机化和盲法以及样本量小,其结果的可靠性受到限制[14]。
免疫调节方面:肺部和其他器官严重损伤的潜在病理生理学是增强的免疫反应和细胞因子释放“细胞因子风暴”[15]。因此,除了直接针对病毒的方法外,针对关键炎症细胞因子或免疫反应的其他方面的治疗已成为另一个研究热点,主要涉及糖皮质激素、干扰素、托西珠单抗、间充质干细胞、恢复期血浆或免疫球蛋白。一项对714例严重急性呼吸综合征或严重流行性感冒患者的8项观察研究进行的荟萃分析结果提示,恢复期血浆和免疫球蛋白的应用与死亡率的降低有关(OR=0.25,95%CI=0.14~0.45,I2=0%),但其用于COVID-19的治疗需进一步的安全性和有效性试验[16]。
中医药方面:我国防治COVID-19过程中,中医药受到高度重视,其在国家卫生健康委员会发布的各版COVID-19诊疗指南中均有推荐。其中,莲花清瘟制剂已被证实可在体外显著抑制SARS-COV-2复制,影响病毒形态并发挥抗炎活性[17]。
本研究有一定局限性:一方面,关于COVID-19治疗的文献数量庞大且增长速度很快,这意味着随着新证据的出现,研究结果和建议也在不断演变;另一方面,部分相关研究在bioRxiv、medRxiv、chemRxiv等预印版平台发表,本研究未纳入此部分文献,研究结果可能存在偏倚。
综上所述,COVID-19大流行是严重的全球公共卫生危机。本研究应用CiteSpace软件,快速、客观地对COVID-19治疗领域的研究现状和热点进行了可视化呈现,提示各国学者、机构间密切合作,在抗病毒药、免疫调节和中医药3个方面展开了深入研究,但迄今为止,尚无来自随机对照试验的证据表明存在对COVID-19疗效显著的治疗措施,临床上主要以对症支持治疗为主。期待各国学者、机构间继续紧密合作,将国际资源投入到高质量的临床试验中,早日得到指导临床实践的高质量证据。

