住院老年2型糖尿病合并痛性神经病变患病率及危险因素
孙艳 吴智勇 徐永霞 王芬 孔晓明
(安徽医科大学 1第一附属医院老年内分泌科,安徽 合肥 230022;2附属心理医院 合肥市第四人民医院老年心理科)
糖尿病是一种严重危害人体健康的慢性疾病,在慢性并发症中糖尿病周围神经病变患病率最高,国外报道30%~90%糖尿病患者合并周围神经病变〔1〕。糖尿病痛性神经病变(PDN)是糖尿病周围神经病变的一种类型,表现为远端肢体对称性的自发性疼痛、痛觉过敏、异常接触性疼痛。PDN的神经痛症状多在夜间明显,常导致患者睡眠障碍,超过一半的患者合并焦虑、抑郁的症状,严重影响患者的生活质量〔2〕。研究报道〔3〕16%~34%的糖尿病患者合并下肢疼痛症状,也有报道示糖尿病周围神经病变的患者中50%合并PDN〔4〕。在老年2型糖尿病患者中,由于年龄及全身衰老状况,PDN患者的临床疼痛症状更为明显,对生活质量的影响更大。目前针对老年糖尿病患者PDN的相关研究并不多,本研究探讨老年2型糖尿病患者PDN的患病率及其危险因素。
1 对象与方法
1.1对象 选取2018年4月至2019年2月安徽医科大学第一附属医院老年2型糖尿病住院患者127例,男86例,女41例,平均年龄(70.07±8.12)岁,平均糖尿病病程(13.41±8.69)年,平均收缩压(131.55±16.64)mmHg,平均舒张压(72.73±10.55)mmHg,平均空腹血糖〔FBG,(7.44±2.46)〕mmol/L,平均糖基化血红蛋白〔GHB,(7.93±1.94)〕%。
1.2方法
1.2.1一般资料的收集 所有患者由专门人员详细询问病史及一般资料,包括性别、年龄、糖尿病病程、是否吸烟,并测量血压。
1.2.2糖尿病周围神经病变及PDN 的筛查 糖尿病周围神经病变诊断标准依据2017年中国2型糖尿病防治指南的周围神经病变诊断标准:①确诊2型糖尿病;②诊断糖尿病时或之后出现的神经病变;③临床症状和体征与糖尿病周围神经病变的表现相符;④有临床症状(疼痛、麻木、感觉异常等)者,5项神经检查(踝反射、针刺痛觉、震动觉、压力觉、温度觉)任1 项异常;无临床症状者,5项检查中任2项异常,临床诊断为糖尿病周围神经病变;⑤排除以下情况:其他病因引起的神经病变,如颈腰椎病变(神经根压迫、椎管狭窄、颈腰椎退行性变)、脑梗死、急性炎症性脱髓鞘性多发性神经症;严重动静脉血管性病变(静脉栓塞、淋巴管炎)等;药物尤其是化疗药物引起的神经毒性作用及肾功能不全引起的代谢毒物对神经的损伤。
糖尿病周围神经病变的患者如存在对称性下肢疼痛、痛觉过敏或异常接触性疼痛的患者,诊断为PDN〔5〕。所有入组对象由专人利用糖尿病周围神经筛查包进行踝反射、针刺痛觉、震动觉、压力觉、温度觉的检查,进行糖尿病周围神经病变的筛查。对于诊断为PDN的患者由专人利用疼痛数字量表(NRS)对疼痛程度进行评分。
1.2.3实验室数据收集 所有患者行一般生化检查,包括FBG、GHB、白蛋白(ALB)、肌酐(Cr)、肾小球滤过率、总胆固醇(TC)、三酰甘油(TG)、低密度脂蛋白胆固醇(LDL-C)、24 h尿蛋白、尿白蛋白/肌酐(A/C)。由于标本留取及患者依从性的原因,肾小球滤过率、TC、TG、LDL-C完成126例,24 h尿蛋白完成119例,尿A/C完成123例。
1.2.4下肢血管彩色多普勒检查 采用美国GE公司彩色多普勒仪进行下肢血管的检查,了解患者下肢动脉病变程度,共124例完成。
1.2.5PDN患病率分析的分组标准 由于老年人血压特点表现为收缩压增高明显,脉压增大,因此血压分组采用收缩压<140 mmHg为分组标准,舒张压<80 mmHg为分组标准;FBG<7 mmol/L为分组标准;GHB以2型糖尿病控制目标<7%为分组标准;ALB、Cr、24 h尿蛋白、尿A/C均按正常范围分组。TC、TG、LDL-C按2017年中国糖尿病防治指南中血脂控制目标进行分组;下肢血管彩超结果根据下肢动脉病变程度进行分组:正常(0)、动脉硬化(1)、动脉硬化伴斑块形成(2)、动脉硬化伴斑块形成伴血管狭窄(3)。
1.3统计学方法 采用SPSS19.0软件进行χ2检验、二元Logistic回归分析。
2 结 果
2.1住院老年2型糖尿病PDN的患病率 127例住院老年2型糖尿病患者,98例诊断为2型糖尿病周围神经病变,患病率77.3%;30例诊断PDN,患病率23.6%。PDN患者NRS平均(5.87±1.61)分。GHB、ALB、Cr、肾小球滤过率、下肢动脉病变程度是2型糖尿病合并PDN的影响因素。见表1。
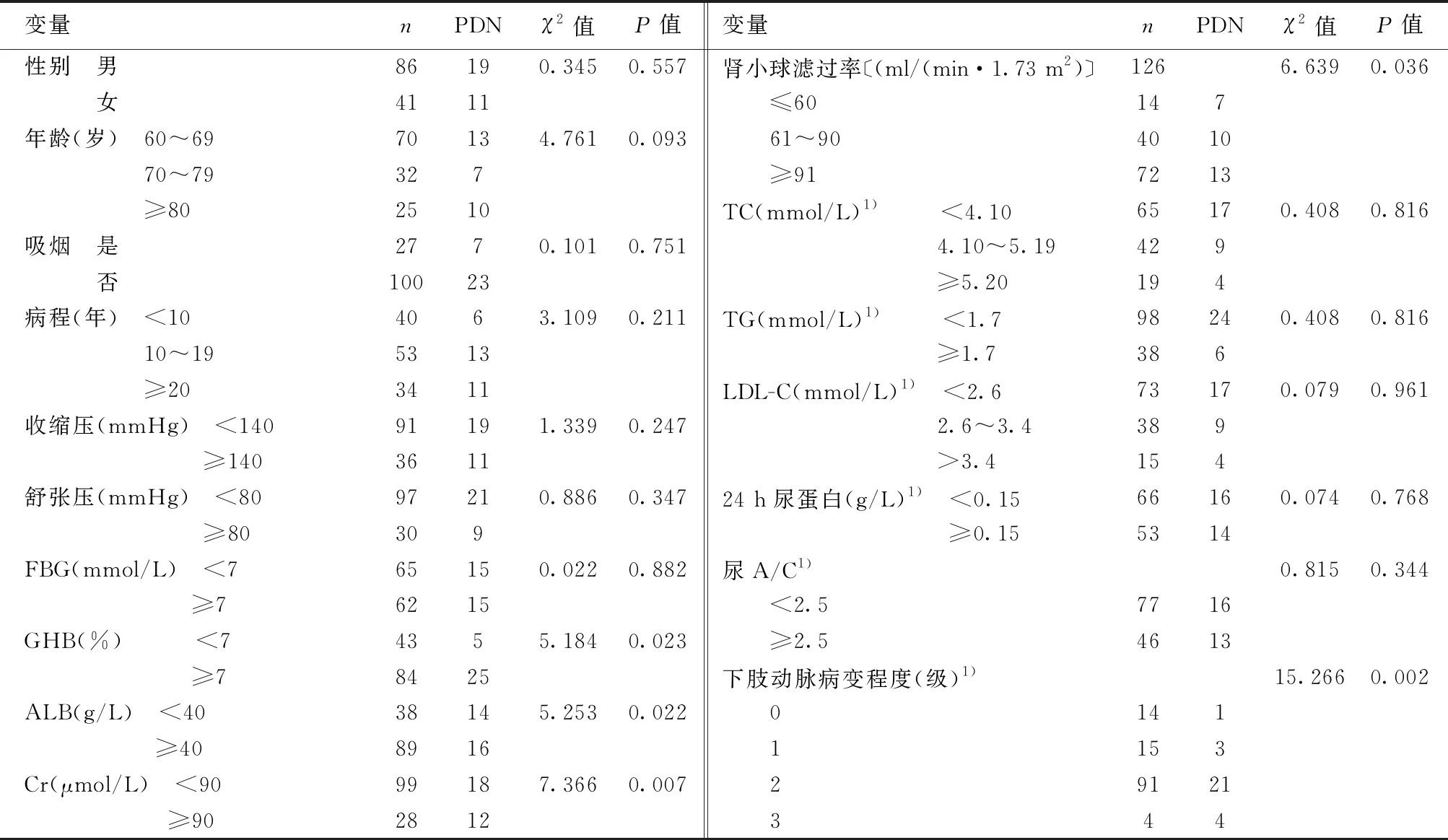
表1 不同临床特征患者PDN患病率比较(n=127,n)
2.2老年2型糖尿病合并PDN的二元Logistic回归分析 以是否为PDN作为因变量(Y=0,1),将患病率存在显著差异的临床指标GHB、ALB、Cr、肾小球滤过率、下肢动脉病变程度及可能与PDN相关的糖尿病病程作为协变量,进行二元Logistic回归分析。ALB为2型糖尿病合并PDN的保护性因素,而糖尿病病程、下肢动脉病变程度为老年2型糖尿病合并PDN的危险因素。见表2。

表2 住院老年2型糖尿病合并PDN的Logistic回归分析
3 讨 论
PDN作为糖尿病周围神经病变的一种特殊类型,由于其存在针刺、刀割、火烧样异常痛觉及痛觉过敏,且常在夜间症状明显,严重影响患者的生存质量。目前对于老年2型糖尿病患者PDN患病率的研究尚不多,因此对于老年PDN的患病率尚无明确结论。国外研究〔6〕发现12.5%的糖尿病患者认为存在疼痛是很正常的现象或是疾病进展的正常过程,从未向医生主诉或诊断,因此PDN存在着较大的漏诊率。本研究发现住院老年2型糖尿病合并PDN患病率为23.6%,与国外报道的PDN患病率类似〔2,7〕。PDN患者NRS平均(5.87±1.61)分,反映了老年PDN患者疼痛程度状况。
PDN的发病机制目前尚不明确,治疗效果总体欠佳。目前对PDN主要的处理原则包括严格的血糖控制、针对神经病变发病机制的治疗及疼痛症状的控制〔8〕。国外报道约39%的PDN患者未得到有效处理〔6〕,而在治疗的患者中也只有1/3减轻了50%的疼痛〔9〕,可见PDN的治疗现状仍不乐观。糖尿病周围神经病变认为与高糖及胰岛素抵抗导致的氧化应激、山梨醇旁路代谢异常、线粒体功能受损、神经营养因子耗竭等多种致病因素互相作用导致神经细胞损伤相关〔10〕。而PDN的发病可能还与导致疼痛的中枢机制有关〔11〕。目前研究发现PDN的危险因素包括年龄、糖尿病病程、肥胖、女性,另外高血压、高脂血症、吸烟等也可能与PDN有关〔12,13〕。本研究未发现血压、血脂、吸烟状况与PDN患病率的相关性,原因与住院老年2型糖尿病患者多数合并高血压、高脂血症病史明确,已进行降压、降脂治疗且本研究吸烟患者的例数相对较少有关。
本研究结果提示持续的血糖稳定状况较单次血糖的波动与PDN的关系更密切。严格控制血糖对于降低糖尿病周围神经病变的获益是明确的,在临床中长期稳定控糖仍是延缓并发症进展的强有力证据〔14〕。
神经滋养血管的病变导致的血管低灌注和神经内膜缺氧与糖尿病周围神经病变相关〔15〕,本研究发现下肢动脉病变严重程度与PDN的患病率相关。老年患者由于年龄因素及相对较长的糖尿病病程,合并下肢血管病变的程度较重,导致神经供血障碍从而引发PDN。且由于血管病变引起的肢体缺血性疼痛混杂在神经痛中无法完全区分也可能是老年PDN患病率较高的原因。老年糖尿病患者由于长期饮食控制,可能出现营养不良、ALB水平较低的现象。老年人中由于营养状况下降易合并如肌少症、贫血、骨质疏松等疾病,这些疾病可加快衰弱的过程〔16〕。低蛋白血症导致肌肉力量及支撑能力的下降及老年人合并的骨质疏松导致的骨密度下降,均可能与PDN的疼痛发生有关。
糖尿病导致的肾病和神经病变,均属于糖尿病微血管病变,因此在发病机制上有一定的同源性〔17,18〕。此外肾功能水平下降与不宁腿综合征的发生相关,而不宁腿综合征表现为小腿深部于休息时出现难以忍受的不适感觉〔19〕,与PDN的疼痛不适有一定的类似,在临床上两者很难完全鉴别,且两种疾病是否有一定关联目前尚不清楚。
综上,老年患者PDN的发生可能是多因素、多疾病综合导致,如下肢血管病变、低蛋白血症、肾功能下降可能合并的不宁腿综合征等,这些疾病均与下肢的疼痛、不适症状相关,因此对于老年PDN患者应多角度考虑疼痛产生的原因,综合对因处理。并且在老年长病程糖尿病患者的诊治过程中,要注意饮食控制的程度,防止饮食过度控制导致的低蛋白血症、营养不良的出现,同时需重视下肢血管病变的常规筛查及正规治疗。

