粗盐中难溶性杂质的去除
赵培龙




粗盐中难溶性杂质的去除实验是初中化学的一个基础实验。实验目的旨在引导同学们体验固体混合物初步提纯的实验过程,巩固溶解、过滤操作技能,学习蒸发操作技能。
夯实基础
1. 实验用品:酒精灯、烧杯、玻璃棒、蒸发皿、坩埚钳、漏斗、药匙、量筒、铁架台(带铁圈)、托盘天平、滤纸、火柴、粗盐、蒸馏水。
2. 实验步骤:
(1)溶解:用量筒量取10 mL水倒入烧杯中。用托盘天平称取5.0 g粗盐,用药匙将该粗盐逐渐加入盛有10 mL水的烧杯里,边加边用玻璃棒搅拌,一直加到粗盐不再溶解为止,称量剩余的粗盐。
注意事项:①粗盐具有吸湿性,为防止天平的托盘受污染,在称量时必须在左、右托盘上各放一张相同的纸张,或在小烧杯中进行称量;②量取10 mL蒸馏水,应选用10 mL规格的量筒。
(2)过滤:用滤纸和漏斗制作一个过滤器。将烧杯中的液体沿玻璃棒倒入过滤器,进行过滤。若滤液仍浑浊,应再过滤一次。
注意事项:①过滤时须遵循“一贴、二低、三靠”的原则;②过滤时应先过滤上层澄清液体,然后再将混有大量沉淀的液体倒入漏斗,并用蒸馏水洗净烧杯,洗涤液须倒入漏斗中,最后用少量蒸馏水洗涤滤渣2~3次;③如果两次过滤仍然浑浊,应检查实验装置并找出原因,改正后再次过滤。
(3)蒸发:将蒸发皿放到铁架台的铁圈上,把滤液倒入蒸发皿中,用酒精灯加热,并用玻璃棒不断搅拌液体,待出现较多固体时停止加热。
注意事项:①加热过程中要用玻璃棒不断搅拌滤液,防止因局部温度过高造成液滴飞溅;②不要立即把热的蒸发皿直接放在实验台上,以免烫坏实验台。
(4)计算产率:待蒸发皿中的固体冷却至室温后,用玻璃棒把蒸发皿中的食盐转移到滤纸上,称量其质量,把称量后的食盐回收到指定的容器中,然后计算精盐的产率。精盐的产率=×100%。
1. (2019·江苏·苏州)在“粗盐的初步提纯”实验中,下列操作正确的是( )。
A. 取用粗盐 B. 溶解粗鹽 C. 过滤粗盐水 D. 蒸干滤液
解析:取用药品时,瓶塞要倒放,A选项瓶塞没有倒放,操作错误;溶解操作应在烧杯中进行,不能用量筒溶解固体,B选项操作错误;过滤液体时,要注意“一贴、二低、三靠”的原则,C选项操作正确;蒸发操作应在蒸发皿中进行,D选项操作错误。故选C。
答案:C
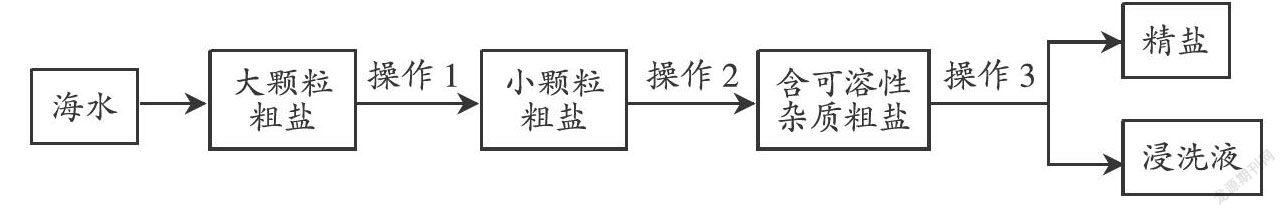
2. (2019·江苏·盐城)从海水中可以提取粗盐(含CaCl2、MgSO4等可溶性杂质和少量泥沙)。小明利用如图流程进行除杂,得到精盐,回答下列问题。
(1)操作1需要在 (填字母序号)中进行。
A. 研钵 B. 量筒 C. 烧杯 D. 广口瓶
(2)操作2的步骤为溶解、过滤、 、结晶,过滤操作中玻璃棒的作用是 。
(3)操作3的步骤为“盐洗”(即用NaCl溶液浸洗粗盐,以溶解除去其中可溶性杂质),过滤、烘干,则“盐洗”溶液应选用NaCl的 (填“饱和”或“不饱和”)溶液。
(4)在农业生产上,常用质量分数为16%的NaCl溶液来选种。小明称取实验制得的精盐16 g,加入盛有84 mL蒸馏水的烧杯里(实验条件下,水的密度为1 g·mL-1),完全溶解。配制所得的NaCl溶液的浓度低于16%,原因是 。
(5)若利用化学方法除去粗盐中CaCl2、MgSO4两种杂质,可在粗盐溶液中依次加入稍过量的三种溶液:BaCl2溶液、 (填化学式)溶液、Na2CO3溶液。充分反应后过滤,加入过量稀盐酸,搅拌、煮沸。
解析:(1)将大颗粒的粗盐磨制成小颗粒的粗盐需要在研钵中进行,故选A。
(2)粗盐的提纯分为溶解、过滤、蒸发、结晶四步;过滤操作中玻璃棒的作用是引流。
(3)“盐洗”的目的是洗去其他可溶性杂质,留下氯化钠固体,则“盐洗”溶液应选用NaCl的饱和溶液,这样氯化钠固体才不会溶解,而只溶解其他可溶性杂质。
(4)配制所得的NaCl溶液的浓度低于16%,原因是精盐不纯(有杂质)或未完全烘干。
(5)若利用化学方法除去粗盐中CaCl2、MgSO4两种杂质,先加入稍过量的BaCl2溶液除去硫酸根离子;再加入稍过量的氢氧化钠溶液除去镁离子;再加入稍过量的碳酸钠溶液除去溶液中钙离子和钡离子;充分反应后过滤,最后加入过量稀盐酸,搅拌、煮沸。
答案:(1)A (2)蒸发 引流 (3)饱和 (4)精盐不纯(有杂质)或未完全烘干 (5)NaOH

