纳米氧化铝的合成方法及其对As的吸附研究进展*
海 傲,李露露,步延鹏,马诗院,张成琳,曾 瑞,袁近秋,张云庚,陈丹云
(1.河南大学化学化工学院,河南 开封 475004;2.济源市环境科学研究所,河南 济源 459000;3.河南大学民生学院,河南 开封 475004)
0 引 言
As在自然界中广泛存在,是一类重要的环境污染物,As污染现象在全世界范围内普遍存在[1-5]。近年来,As污染事件在我国多个地区发生,给人们的生产生活带来了很大危害[6-8]。据相关调查,我国有大约1470万人生活的地区地下水As含量超出WHO的饮用水标准限定值(10 μg·L-1),其中600万人处于饮用水As含量严重超标的威胁中[9-10]。

目前常见除As方法主要包括化学沉淀法[19-22]、吸附法[23- 26]、离子交换法[27-30]、氧化法[31-33]、生物法[34-37]、膜分离法[38- 41]、电化学法[42-44]等。在具体应用场景中由于污染的复杂性,往往需要多种修复方法联合使用[45]。在众多的除As方法中,吸附法因其便捷、经济、绿色无二次污染的特点拥有广阔的应用前景。常见的吸附剂有活性炭[46-48]、氧化铝[49-52]、二氧化锰[53-55]、铁基氧化物[56-58]以及高分子化合物[59-60]。其中纳米氧化铝因其具有低成本、高选择性以及优良的稳定性能等方面的优势[49],是一种优良的除As材料。早在1971年Bellack[61]发现活化的γ-Al2O3可以有效去除水中的As;Han等[62]利用异丙醇铝作为原料,以三嵌段共聚物 Pluronic P123为模板,制备出比表面积高达312 m2·g-1的介孔纳米氧化铝,对As (Ⅴ)的最大吸附容量为36.6 mg·g-1;Saha等[63]利用反相微乳液法合成氧化铝纳米管,并采用原位分散法将其固定在壳聚糖接枝的聚丙烯酰胺基体上,结果显示与高分子复合之后的纳米氧化铝对As (Ⅴ)的负载能力为6.56 mg·g-1,比单一的纳米氧化铝(4.23 mg·g-1)具有更好的吸附效果。
1 纳米氧化铝的合成方法
随着纳米科技的发展,纳米氧化铝的合成方法也日趋丰富,主要分为固相法、液相法和气相法[64](见图1)。

图1 纳米氧化铝合成方法分类图Fig 1 Classification diagram of nano-alumina synthesis method
1.1 固相合成法
固相合成法是将铝盐等一些含铝化合物经研磨后进行煅烧,通过发生固相反应制得纳米氧化铝[65]。作为合成纳米氧化铝的重要途径之一,该方法具有操作简便,成本低廉的优点[66]。具体又包括机械研磨法和高温热解,两种合成方法所涉及的反应物均为固相。
1.1.1 机械研磨法
机械研磨法是指将一些含铝(如氢氧化铝、粉煤灰、高岭土等)的材料通过物理机械研磨的方式,将尺寸较大的颗粒转化为粒径在纳米尺度的微粒,然后通过机械分离将其中的杂质去除,最终得到纳米氧化铝[67-69]。吴光进等[70]以工业氢氧化铝为原料,经机械球磨并热分解自粉化后,制得纯度高达99.95%,粒径在1 μm左右的高纯超细球形氧化铝,并且粉体高度分散。该方法操作便捷,但是得到的纳米氧化铝粒径不均一、易团聚且形貌不可控。
1.1.2 高温热解法
高温热解法是利用硫酸铝铵或碳酸铝铵等热不稳定的含铝铵盐在高温条件下分解,获得纳米氧化铝[71-75]。Ma等[76]以硫酸铝铵和碳酸氢铵为原料,在pH=9,37℃条件下合成出NH4[Al(OOH)HCO3],并以此作为前驱体在500℃下热分解,获得了网状γ-Al2O3,平均粒径51.9 nm,比表面积190 m2·g-1。Yong等[77]保持NH4HCO3溶液pH=10,并向其中滴加NH4Al(SO4)2溶液,在8℃条件下合成了前驱体,之后在1 150 ℃煅烧3 h,得到了直径70 nm的多孔α-Al2O3。
1.2 气相合成法
气相法是直接利用气体或者通过等离子体、激光蒸发、电子束加热、电弧加热等方式将物质变成气体,使之在气体状态下发生物理或化学反应,最后在冷却过程中凝聚长大形成超细微粉[78]。气相法可分为化学气相沉积法、激光诱导气相沉积法和等离子气体合成法[79]。
1.2.1 化学气相沉积法
化学气相沉积法以无机铝盐(如AlCl3)或有机金属铝化合物为原料,将其溶于有机溶剂中,然后以一定的流速通入火焰中,高温下生成Al2O3粒子并附着在反应器壁[80-81]。Sokolowski等[82]将乙酰丙酮铝喷入碳氢化合物火焰中,通过快速燃烧氧化反应,在喷雾器频率为ν=1 MHz时,制备出了Al2O3气溶胶,获得了直径为30 Å的Al2O3球形颗粒。Kelekanjeri等[83]以0.0015 mol·L-1乙酰丙酮铝的异丙醇溶液为沉积液,在沉积温度为1 050~1 125°C时制备了α-氧化铝薄膜。该合成方法可通过控制原料气体流速控制纳米氧化铝的粒度,并且可以解决纳米氧化铝在合成过程中的团聚问题。
1.2.2 激光诱导气相沉积法[84]
激光诱导气相沉积法是利用激光在小范围内产生高温环境,使得反应物在极短的时间内气化,并在气态完成一系列物理化学变化,生成氧化铝晶核,随着气体离开高温区域,晶核迅速长大成为一定大小的纳米氧化铝颗粒。此方法制备的氧化铝粒度均一,且可利用激光进行精准操控。但生产成本高,难以实现工业化规模合成应用。
1.2.3 等离子气体合成法
在等离子体氛围下,铝或含铝化合物与空气发生氧化反应,生成氧化铝并迅速冷却得到产物粒子[85]。Johnston等[86]在O2气氛中激光烧蚀Al靶,所得纳米氧化铝粉末的比表面积为135~250 m2·g-1,粒径在3~7 nm。并且发现随着氧气压力和激光流量的增加,粉末比表面积减小(粒径增大)。用X射线衍射研究发现粉体在约1 200 ℃时,直接从γ- Al2O3转变为α-Al2O3,同时保持较小的粒径(30 nm)。Borsella等[87]以三甲基铝(Al(CH3)3)和氧化亚氮(N2O)为气相反应物,加入乙烯(C2H4)作为增感气体,合成的粉末颗粒经1 200~1 400 ℃热处理后得到碳污染极低的六方α-Al2O3粉末,粉末由粒径为15~20 nm的球形单晶纳米粒子组成。Kumar等[88]利用直流电弧等离子体反应器在等时氧气流动条件下合成出了球形δ- Al2O3粒子,直径约为50 nm。相较于工业Al2O3,该δ-Al2O3粒子在pH=7时具有更高的Zeta电位(+42.7 mV)。
1.3 液相合成法
液相合成法是目前实验室和工业上广泛采用的制备超微粉的方法,其过程是把铝盐配制成一定浓度的溶液[89],再选择一种合适的沉淀剂或用蒸发、升华、水解等操作将金属离子均匀沉淀或结晶出来,最后将沉淀或结晶物脱水或者加热分解制得超微粉。液相合成法是目前纳米氧化铝合成最为广泛的方法,按照具体制备方法和条件不同又可以分为沉淀法、微乳液法、水/溶剂热法、溶胶-凝胶法。
1.3.1 沉淀法
以硝酸铝或硫酸铝等水溶性铝盐为原料,采用沉淀剂与铝离子发生水解反应生成氢氧化铝、羟基氧化铝等氧化铝水合物,后经干燥、高温煅烧脱水得到氧化铝纳米粒子。常用的沉淀剂包括氨水、碳酸氢铵、碳酸钠等。Parida等[90]以硝酸铝为前驱体,碳酸铵为沉淀剂,采用控制沉淀法制备了γ-Al2O3多孔球形纳米颗粒,粒径4.7~5.7 nm,比表面积190 m2·g-1,孔容0.467 cm3·g-1。Zhao等[91]以硝酸铝和硫酸铝为原料,采用碳酸铵作沉淀剂合成了介孔氧化铝。获得了有序的蠕虫状孔,比表面积高达250~300 m2·g-1,孔径分布窄,约为6 nm。实验结果表明,介孔氧化铝的结构与前驱体有关,前驱体主要由铝源和pH值决定。Zhou等[92]采用直接沉淀法,以Al2(SO4)3·18H2O和NaOH为原料,十二烷基苯磺酸盐为表面活性剂,控制反应温度60~70 ℃,Al2(SO4)3的初始浓度约为0.5 mol·L-1,合成了纳米纤维状前驱体。随后前驱体在1 000 ℃下煅烧3 h,得到宽5~10 nm,长60~100 nm的氧化铝纳米纤维。
1.3.2 微乳液法
微乳液法在合成纳米粒子方面具有较为广泛的应用,其具体做法是选择两种互不相溶的水相和油相,然后在表面活性剂和助表面活性剂的作用下形成油包水型的反相微乳液,以微乳液滴作为纳米氧化铝的微反应器,而外层的油膜则阻止了氧化铝(前体)颗粒的进一步长大,进而使产物粒子尺寸控制在纳米量级。Piao等[93]以环己烷-水作为油水体系,采用聚乙二醇辛基苯基醚(TritonX-100)作为表面活性剂,正丁醇为助表面活性剂,采用反相微乳液法制备了γ-Al2O3纳米粒子,比表面积为450 m2·g-1,粒径小于10 nm,且非常均一。Ghosh等[94]以Al(NO3)3·9H2O为原料,采用含丁二酸(-2-乙基)己酯磺酸钠(AOT)和失水山梨醇油酸酯(Span80)两种表面活性剂的反相微乳液体系,制备了介孔γ-Al2O3纳米柱(见图2),BET比表面积59.3 m2·g-1,孔隙体积0.040 cm3·g-1,平均孔径2.65 nm。Wang等[95]采用反相微乳液法制备了热稳定性强的氧化铝材料。得到的氧化铝1 100℃煅烧10 h后仍以γ过渡相存在,比表面积为52 m2·g-1。

图2 介孔γ-Al2O3纳米柱SEM图Fig 2 SEM images of mesoporous-Al2O3 nano-rods
1.3.3 水/溶剂热法
水/溶剂热法是将反应原料密封于带有聚四氟乙烯内衬的高压反应釜中,以水或有机溶剂作为溶剂,在较高的温度(100~400 ℃)和压力下合成纳米粒子,然后经过滤、洗涤、干燥等后处理得到产物粒子。Li等[96]以硫酸铝铵水合物(NH4Al(SO4)2·9H2O)、尿素和聚乙二醇-2000(PEG-2000)为原料,通过水热法制备了具有分级结构的花状γ-AlOOH颗粒。后经800 ℃煅烧,转变为具有层状结构的立方γ-Al2O3,比表面积为101 m2·g-1,微球直径3~5 μm,介孔尺寸约为13 nm。Zhu等[97]以硝酸铝为铝源,聚乙二醇为模板剂,采用简单的水热法合成了新型类茎状氧化铝。合成的氧化铝由均匀的纳米棒组成,长度约1~1.5 μm,表面附着大量的六角纳米片,厚度约10 nm。Xue等[98]以Al(NO3)3·9H2O为铝源,葡萄糖为碳源,在160 ℃水热反应6 h后得到含有碳核的AlOOH微球,然后在不同温度下煅烧获得了均匀的氧化铝空心球(图3)。
1.3.4 溶胶-凝胶法
溶胶-凝胶法常被应用于氧化物纳米粉体的制备,具体过程是以铝醇盐或者无机铝盐为原料,在碱性条件下(pH>9)进行水解并聚合后得到氢氧化铝胶体溶液,然后经过干燥浓缩后得到透明凝胶,最后经过干燥、研磨、煅烧后得到超细纳米氧化铝微粉。Deng等[99]采用溶胶-凝胶造粒法制备了多孔γ- Al2O3纳米颗粒,制备的γ-Al2O3颗粒粒径1~3 nm,具有大的比表面积(380 m2·g-1)和孔体积(0.5 cm3·g-1),孔径分布均匀(20~60 Å)。张旭光等[100]以硝酸铝为铝源,十六烷基三甲基溴化铵和尿素为复合模板剂,采用溶胶-凝胶法制备了介孔氧化铝,比表面积为400 m2·g-1,孔径分布在3~5 nm之间,形成的蠕虫状孔道具有短程有序性。Tan等[101]以硝酸铝和苹果酸为原料,采用溶胶-凝胶法制备氧化铝前驱体溶胶。探讨了苹果酸和聚乙烯吡咯烷酮(PVP)含量对溶胶可纺性的影响。当硝酸铝、苹果酸和PVP的质量比为10∶3∶1.5时,制得的凝胶纤维长度80 cm以上。在1 200 ℃烧结得到了表面光滑、直径约20 μm的氧化铝纤维。
2 纳米氧化铝在As吸附过程中的影响因素
纳米氧化铝在吸附除As的过程中受到多种因素的影响,这些影响纳米氧化铝吸附性能的因素归纳起来主要包括比表面积、pH以及共存离子。
2.1 比表面积的影响
在纳米氧化铝吸附As的过程中,氧化铝的比表面积对As的去除率具有重要影响,大的比表面积意味着可以提供更多的吸附位点,从而提高吸附率,因此比表面积是衡量氧化铝吸附能力的重要因素[62]。为此科研人员采用了多种合成手段提高Al2O3的比表面积。Darban等人[25]利用高岭土通过沉淀法制备出了多孔γ-Al2O3,比表面积可达201.53 m2·g-1,粒径仅为22~36 nm。通过对As(Ⅲ)的吸附实验显示,其对于As(Ⅲ)的去除率可达97.65%。李荣辉等人[50]通过简单的水热和高温煅烧法自组装形成三维层级花状活性氧化铝,比表面积为 231.7 m2·g-1,这种纳米结构为As的吸附提供了丰富的活性位点。Kim[51]等人通过水解法制备了海绵状多孔氧化铝,比表面积为307 m2·g-1,对于As(Ⅲ) 和As(Ⅴ)的最大吸附容量分别为121 mg·g-1和47 mg·g-1。Han等[62]采用三嵌段共聚物 Pluronic P123作为模板,通过与氢氧化铝溶胶进行化合反应,然后通过煅烧制备介孔氧化铝。该介孔氧化铝材料对As(Ⅴ) 具有极好的吸附效果。在近中性(pH=6.6±0.1)水溶液中吸附量可达36.6 mg·g-1。Patra 等[102]报道了一种高效的自组装介孔α-Al2O3材料,该介孔α-Al2O3材料由2~10 nm的球形纳米颗粒组成,拥有较大的比表面积(231~497 m2·g-1),对水溶液中的砷酸根具有极强的吸附能力。
2.2 pH的影响
无论是对As(Ⅲ)还是As(Ⅴ)的去除,体系的pH都具有显著的影响,有时甚至是决定性的[49,105]。pH可以影响Al2O3表面的电位[103],而对于以含氧酸根离子形式存在的As来说,显然更容易因静电吸引而被表面带有正电荷的Al2O3所吸附,而氧化铝的等电点(PI)处于8~8.5之间[104],当pH低于PI时,Al2O3表面呈现正电位,从而对于As的吸附起到积极作用;相反则不利于As的吸附。然而值得注意的是,当吸附环境的pH过高或过低时均不利于As的吸附,这应该归因于Al2O3系两性氧化物,过高或过低的pH环境会使得Al2O3表面发生部分溶解,从而影响As的吸附。Li等[26]探究了pH对于As在Al2O3表面吸附的影响,发现pH在4~9时,可以对As具有良好的去除效果,而当pH>10或pH<3时,Al2O3对于As的去除率急剧下降(图4)。Lin等[49]的研究发现,在多数pH条件下,氧化铝对于As(Ⅲ)的吸附效果远不如As(Ⅴ),且pH对于As(Ⅲ)的影响呈现吸附效果随pH的升高先升高后下降的趋势,在pH≈7时效果最好;而对于As(Ⅴ)的吸附,pH在3~6的范围内均可以呈现出较好的吸附效果。
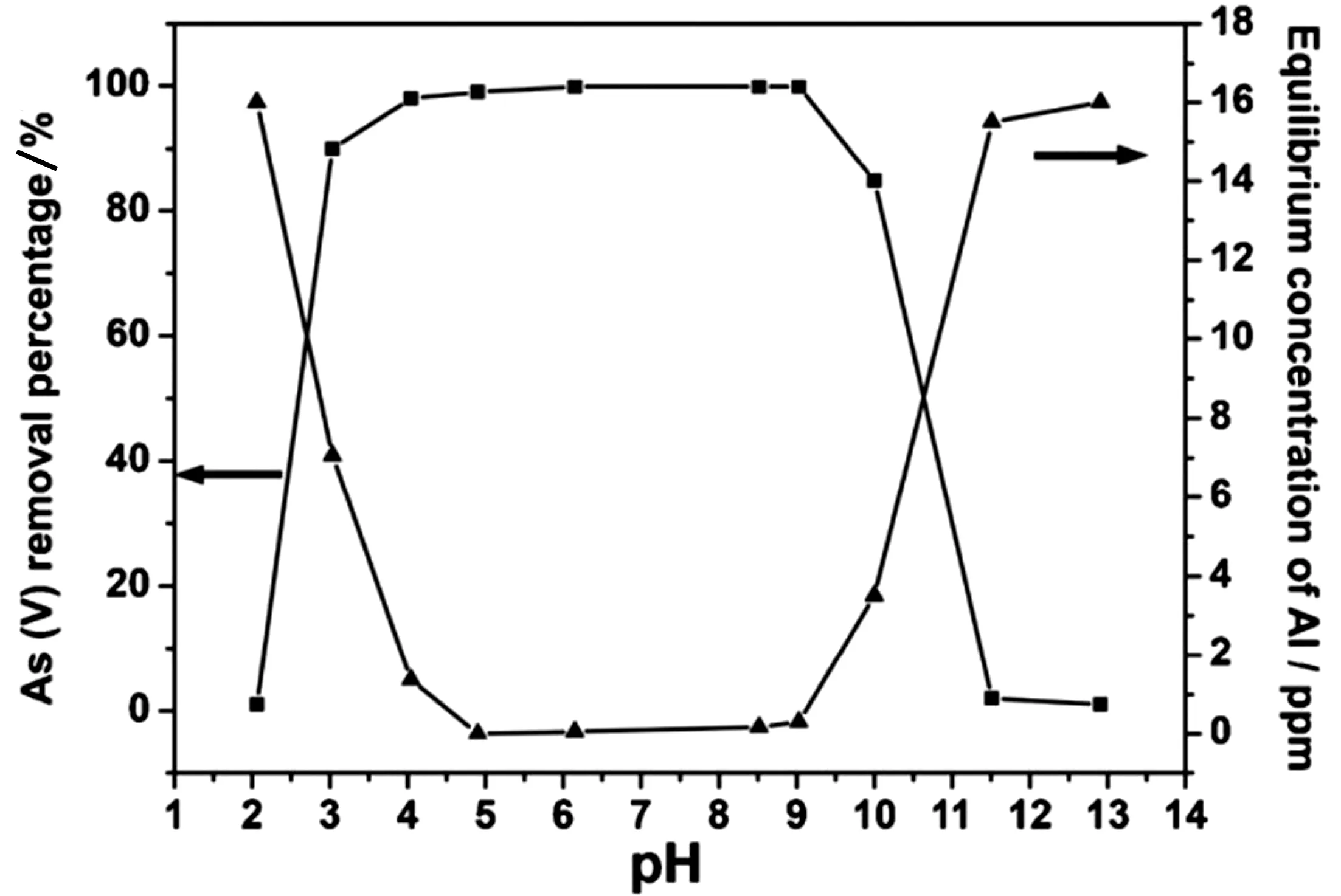
图4 As去除率与溶液pH关系曲线Fig 4 Relation curve between As removal rate and solution pH
2.3 共存离子的影响
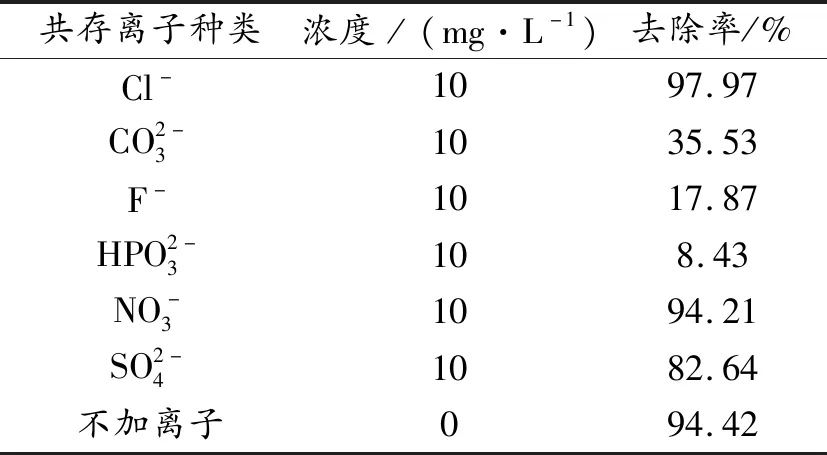
表1 共存离子对As去除率的影响Table 1 Influence of co-existing ions on As removal rate
3 结 语
总结了纳米Al2O3的合成方法及其在吸附除As方面的应用现状,尽管目前纳米Al2O3的制备方法种类繁多,合成出的Al2O3形貌层出不穷,但是大比表面积纳米Al2O3的合成方法还不是很成熟,而大的比表面积恰恰是纳米Al2O3高效除As的重要影响因素,因此,采用简便、绿色的方法合成大比表面积的纳米Al2O3仍是一大难题。此外,当前吸附As的纳米Al2O3多数表面没有功能化,对于多种离子共存的复合污染的治理效率仍待提高,因此我们可以从表面改性、与其它修复剂复配、掺杂稀土元素等方面加大研究,以提高纳米Al2O3对复合污染体系的治理效率。

