医院药品不良反应监测分析服务系统研究
王羡欠,龚震宇,龚文涛,袁玉妹,喻建勇,田 波
(1. 江西省人民医院信息处,330006,南昌;2. 江西省人民医院药剂科,330006,南昌)
0 引言
随着科学技术的不断发展和创新,许多新型的药物被研制成功并应用于各种疾病。但是不仅新型药物的不良反应尚未完全研究透彻,甚至一些已经临床应用多年的药物,对其不良反应的了解仍有一些空白部分。但是药品的不良反应(ADR)确实已经严重影响到老百姓的生活质量,程度较轻的药品不良反应会带来过敏症状或者降低药品疗效,程度较重的药品不良反应甚至会直接威胁到民众的生命健康[1]。世界卫生组织(WHO)通过统计调查,得出了一份报告,该报告指出全球每年死亡的人口中,有较大比例的死亡人口并不是由于疾病或者衰老所导致的,而是由于错误地使用了药品而产生了一系列不良反应[2]。甚至科技和医疗水平都相对发达的中国,每年因药物不良反应而不得不住院治疗的都有超过200万人。这其中甚至还有约19万人因此死亡[3]。如“齐二药事件”“欣弗事件”“巴基斯坦109人因药物不良反应死亡事件”等今年来发生在国内外的一系列因ADR而造成严重后果的事件,对当事人和其家属都造成了无法挽回的痛苦,同时也导致了严重的社会问题[4]。近年来国家食品药品监督管理局开始重视起ADR的监测并实行集中分类管理,同时从法律法规、技术提升、系统性管理等多方面不断进行完善[5-6]。法规建设方面,有《药品不良反应监测管理办法(试行)》《中华人民共和国药品管理法》《药品不良反应报告和监测管理办法》。并在信息化建设方面,建立了国家药品不良反应监测信息网络体系。自主上报式和院级单位集中管控式是我国目前对ADR进行系统管理的两大体系。自主上报式有较大的覆盖范围,可以监测到医药领域的各个细枝末节,但是其上报内容质量较低、可信度不足、需要专业医师花费大量的人力物力进行验证。院级单位集中管控式有着较为权威的临床病例为佐证,其上报内容可信度较高,但是存在着覆盖范围小、涉及工作环节极为繁杂,并且涉及到的验证存储环节成本颇高[7]。本文针对以上现状,开发了一种医院药品不良反应监测分析服务系统。该系统以与院级电子病历系统和院级患者信息管理系统(HIS)集成为方式,可以有效地达成患者根据医嘱进行用药的基本情况与患者个人基本信息和疾病病程变化情况的有效综合性采集;同时与更高级的ADR系统的数据信息接口进行数据交换。通过以上操作流程,可基本实现在院级单位下,基本药物使用情况的采集。除此之外,数据交换接口子系统将以院级药物集中管理与监测的方式,实现院级单位对药品使用的归档管理和信息共享功能。
1 国内外医院药品不良反应监测分析服务系统研究现状
搜集单一的药品不良反应监测报告很容易,但是如何对所有药品的不良反应都进行统一地搜集并管理,就成了该研究方向的核心。近年来,仅仅是在国内的研究领域就有许多将药品不良反应监测分析进行整体化、统一化的研究成果。周克雄[8]提出了将医院集中监测、处方事件监测与自发呈报监测等多上报途径相结合的思路,进行药品不良反应监测分析服务系统的设计。王玲[9]也提出将药品不良反应监测分析服务系统与HIS相结合的思路,将药品不良反应检测结果进行统一监督管理。徐冠[10]等人已经提出了在基层医院进行宣传、促进开展药品不良反应监测和报告的工作基础上,更要及时统一地收集和分析、警戒临床中存在的不安全因素。姜继娟[11]探讨了使用PDCA循环管理模式对促进医院药品不良反应监测上报及其效果的影响。然而国内关于医院药品不良反应监测分析服务系统的研究多数停留在对某一环节的详细探讨,而缺乏一个能够上升到省级平台且具有较高整体性和系统性的结果。
基于医院药品不良反应监测分析服务系统的研究不仅在国内处于研究的起步阶段,甚至在国际研究领域中,取得有效成果的研究也并不多见。B A Adenuga[12]等人探讨了偏远地区进行药品不良反应系统化检测的重要性。R Pauline[13]等人提出了使用时间编码的方式,对新发现的药品不良反应监测报告进行统一编码和集中管理。但是在国际研究领域中,关于医院药品不良反应监测分析服务系统也存在较多空白区域。因此将传统ADR检测模式与现有的HIS等医疗机构管理系统进行信息集成就显得迫在眉睫,这一研究可以实现对院级单位开出的处方中,所发生的ADE事件以及重点监测的药品各方面信息进行自动收集整理、归纳分析、专家评价、处方预警、患者反馈及后续服务等功能,具有较好的研究潜力和效应预期。
2 医院药品不良反应监测分析服务系统的技术背景
2.1 基于ACCESS的ADR数据库搭建技术
ADR是按照药品说明或者医嘱所进行正常药物使用时所产生的一系列与药品本身存在关系的不良反应。因此ADR数据本身就涉及了整个医学界所有的分支领域,甚至可以说所有药品都存在不同程度的ADR。因此,如果将大量的ADR报告进行汇总整理,并按疾病类别进行分类再进行统一的管理,将是一个极为庞大的工程。我国已经建立了国家药品不良反应监测系统,并每年一次发布监测报告,而该监测系统已经是囊获了国内外医学领域许多专家的权威意见,具有较高的参考价值和应用价值[14]。但是由于国家药品不良反应监测系统针对的对象是全国的医学领域,不管是新增一条ADR病例报告还是对已经存在于系统中的报告进行修改或者删除,都要历经很长时间的审核流程。并且每年发布一次监测报告的周期也很长,不利于实时更新[15]。而我国幅员辽阔,不同地区的多发疾病种类也不尽相同。如川渝地区多发肛肠类疾病、新藏蒙地区多发高反类疾病、沿海地区多发暑热疾病等[16]。由于某些疾病具有地区多发性,因而在大量临床用药的案例下,针对某一药品或某一类药品的ADR报告也往往更加丰富和全面。结合以上分析,设计自主的ADR中间数据库是十分有必要的。
本研究采用OFFICE ACCESS软件进行ADR数据库的搭建[17-18]。针对ADR报告的具体情况,如图1所示,先将数据库字段按如下定义:顺序号、性别、年龄、疾病类别、过敏史、药物使用情况(含剂量和频率)、使用药物类型、使用配液浓度、使用配液用量、给药途径、联合用药情况、ADR发现情况、临床症状、预后情况、原药品生产厂家、案例报告单位、参考文献来源。然后,在数据库表中以双份案例的形式,录入ADR报告案例,并由药学部专人核查;随后,由专人将数据库的界面进行美化,并给出集成模块的思路构建;最后,将语句化操作进行包装,实现语句化到图形化操作的转变[19]。如此可以建立院属或者市省级的ADR数据库。
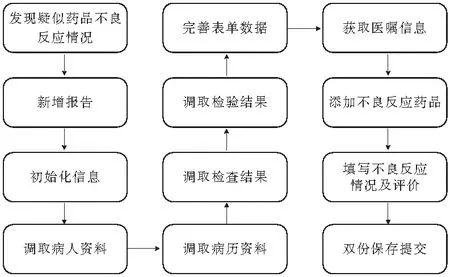
图1 中间数据库上报新案例流程
2.2 基于HIS等系统的医院药物警戒系统(CHPS)对接技术
中国医院药物警戒系统(CHPS)是国家食品药品监督管理总局药品评价中心组织开发的辅助监测哨点发现、报告、评价药械不良反应事件的,并开展药品重点监测、上市后研究,同时获取药械警戒信息的信息化系统[20-21]。但是如何将国家级的CHPS系统与上述中建立的中间数据库以及院级HIS等系统进行对接,就成为了设计该服务系统的核心技术[22-23]。
图2所示为基于HIS等系统的医院药物警戒系统(CHPS)对接技术。首先将诸多医院业务信息系统如HIS、电子病历(EMR)、实验室信息系统(LIS)、影像归档和通信系统(PACS)等系统的数据进行数据清洗、数据整合、数据过滤,筛选并整理出信息真实且完整度较高的ADR案例,然后导入上述设计的中间数据库。其中中间数据库的内容由对应管理员进行格式审查,例如对数据库内容的字段唯一性、关联性等进行技术核查。再由对应科室的医生和护士进行医学真实性核查,遇到难以判断的案例可以组织专家组会进行讨论研究。然后再通过互联网的形式,与国家级CHPS进行数据交换,由更高级的专家组和技术人员再进行核查。如此一来,可以实现中间数据库实时更新,保证了数据更新的效率;同时辅助国家级CHPS一年一更新,保证了数据的权威性。
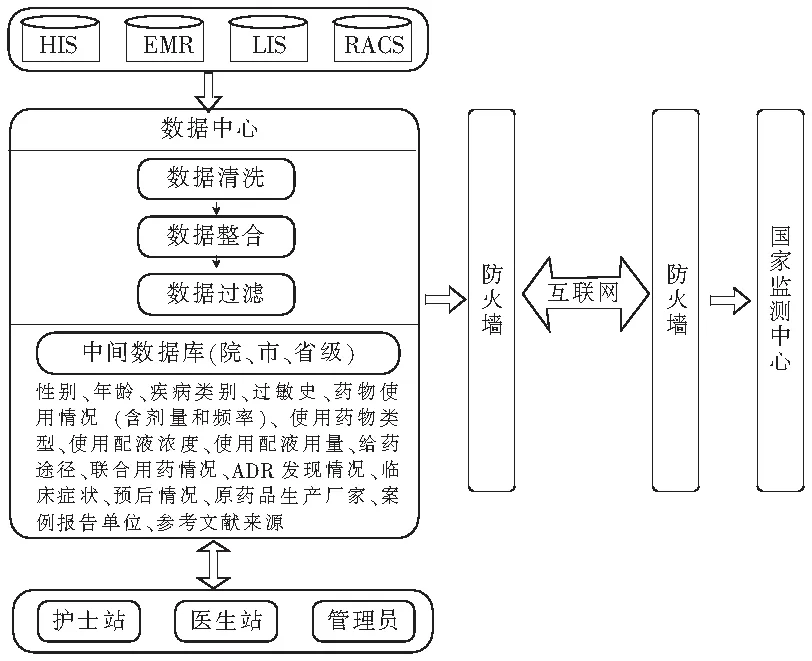
图2 CHPS与HIS等系统对接流程
3 医院药品不良反应监测分析服务系统的设计流程
3.1 关键技术组合分析
对医院药品不良反应监测分析服务系统设计的关键技术在于3个方面:数据采集的关键技术分析研究、数据同步的关键技术分析研究、报告上传的关键技术分析研究。
3.1.1 数据采集的关键技术分析研究 院级单位的诸多系统,例如重点药物评价系统都需要与电子病历系统、HIS等进行对接以保证正常的数据交换和实时更新,如此一来各个科室可以掌握最新的药物信息。使用链式服务实现以上需求是目前较为常用的一种技术手段,链式服务将多种系统有规律地进行连接、保证了数据的实时更新与共享。链式服务同时还可以在总控制台实时调用各个子端的数据,并由此为据建立更加直观的视图。
3.1.2 数据同步的关键技术分析研究 在使用链式服务将数据全部采集完毕后,需要保证至少在院级单位、各个科室可以实时共享数据,同时还需要与院级单位的各系统保证实时数据更新。
3.1.3 报告上传的关键技术分析研究 ADR报告与审核报告最终都需要统一整理后,再上传至上一级中心平台,因此存在着跨平台的问题。解决的方案主要有2种,一种是将报告转换成Excel格式的数据,然后登录省平台,利用省平台提供的Excel导入报告的功能实现上报;另一种方案是利用WebService的技术自动将报告转换成xml格式的数据,然后调用省平台提供的上传服务程序直接将报告上传至省中心。
3.2 系统结构
系统结构如图3所示:本系统划分为系统管理、基础数据管理、监测系统、再评价系统以及处方事件监测系统4个子模块。
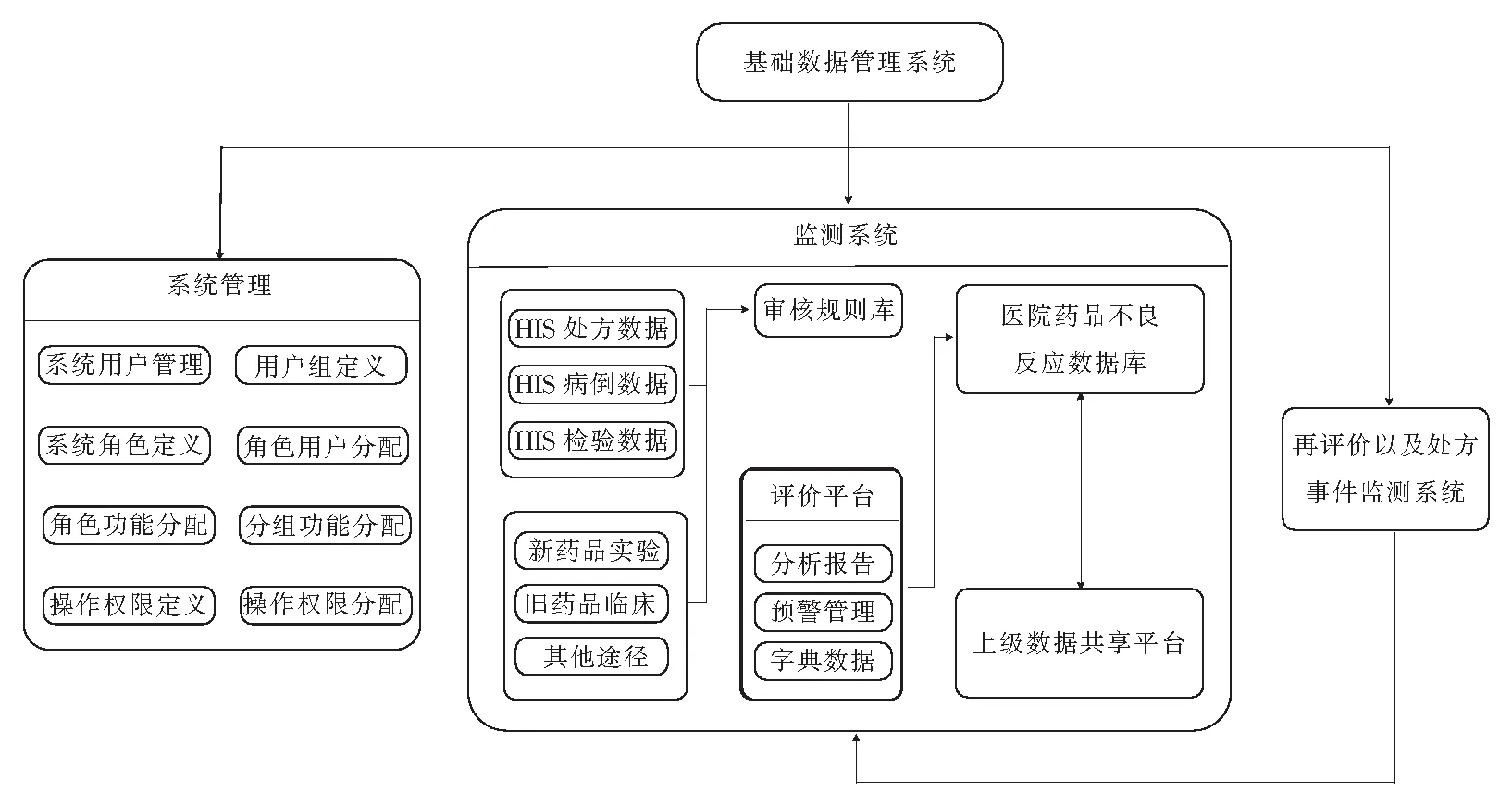
图3 医院药品不良反应监测分析服务系统结构
3.2.1 系统管理 系统管理的主要功能是定义用户组的信息,分配系统功能和各组分权限,这也是实现系统用户化和功能化的基本前提。系统管理中实现了:系统用户管理、用户组定义、系统角色定义、角色用户分配、角色功能分配、分组功能分配、操作权限定义、操作权限分配共计8个功能分支,可以有效地实现对用户的功能划分。
3.2.2 基础数据管理系统 基础数据管理系统存储着各个子系统的基础数据,为各个子系统进行数据更新和交换提供基础保障。可以说,基础数据管理系统是整个医院药品不良反应监测分析服务系统的基石。
3.2.3 监测系统 监测系统的信息来源分为2个部分,一部分是来自内部的:根据HIS提供的患者个人信息、病例信息以及用药情况;另一部分是来自外部的:医药公司提供的新药品实验结果、其他医疗机构发现的旧药品不良反应临床报告和其他一些信息来源。将2种来源的信息按照一定规则进行审核,然后进行第一次评价,给出具体的评价结果并上传数据库。在完成院ADR报告的上报、评价、审核的流程后,最后上传至上级数据共享平台。
3.2.4 再评价系统以及处方事件监测系统 药品品种再评价系统通过来源于HIS的病人多方面信息进行更进一步地论证、再评价,这些信息包括但不限于病历、用药情况等。完成再评价后上传到上一级评价中心,同时监测各级医疗单位发生的处方事件,与上级数据平台保持实时更新,作为整个系统的第2份保障。
3.3 业务流程
系统的业务流程主要体现在院级检测平台数据采集和生成过程。由3个部分组成:1)根据医生开出的处方,对进入监管范围的药品进行数据标记并记录;2)对接已经存在ADR的药品,着重进行不良反应记录;3)已经入库的记录进行预警等级分配,并设置预警系统。
4 结果与分析
如图4所示该系统可以通过角色功能进行分组管理,也可以通过药理分组对ADR案例进行管理。该分组管理模式主要是对药品评价数据收集过程中所涉及的药品、诊断、体征、检验检查项目等相关信息进行标准库与同义词库的构建,主要涉及的标准数据管理内容有药品生产厂家、药理作用分类、给药途径、药品剂量单位、医学主题词库、检查检验项目名称、单位转换、诊断类型、生命体征等。构建标准数据库与同义词库的主要目的是在医院构建与标准词所对应的同义词库,可用于清洗、标准化医院所输出的数据。
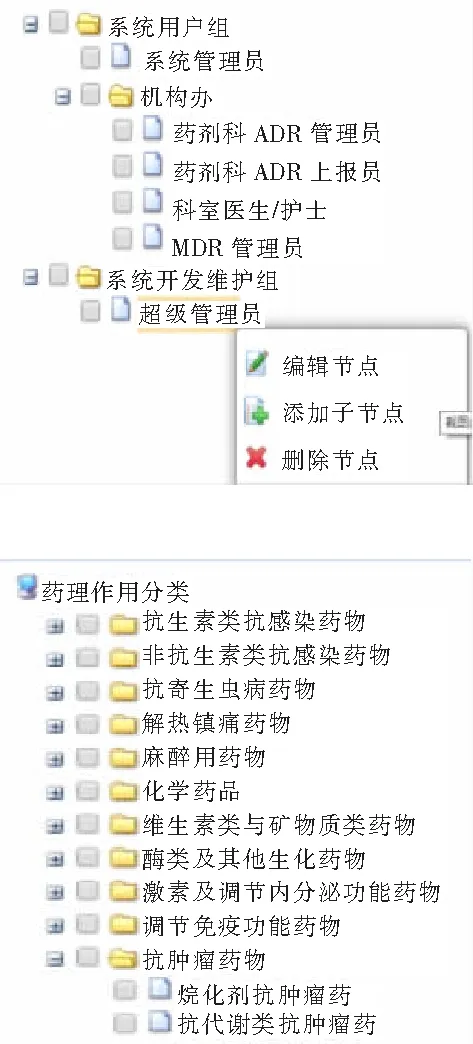
图4 用户角色功能分组和药理分组管理效果图
如图5所示,系统也可以用诸多医院业务信息系统读取病人医嘱用药、病历、检验等信息,也可自行按规范新增。在填写内容过程中,如果某必填项没有填写内容,该报告保存以后,当需要提交该报告时,则会触发校验,不能提交。与现有的其他ADR监测系统不同的是,本文所研究的系统具有良好的与院内其他系统对接的能力。如图6所示,现有的ADR监测系统便捷性较差,医师在开药时,系统无法通过医生开出的处方直接提示相关药物的ADR报告,而需要医师手动进入ADR监测系统进行查询。
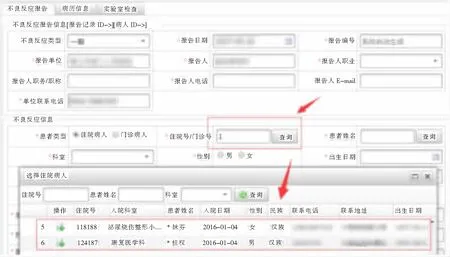
图5 不良反应数据上报(来源于CHPS)
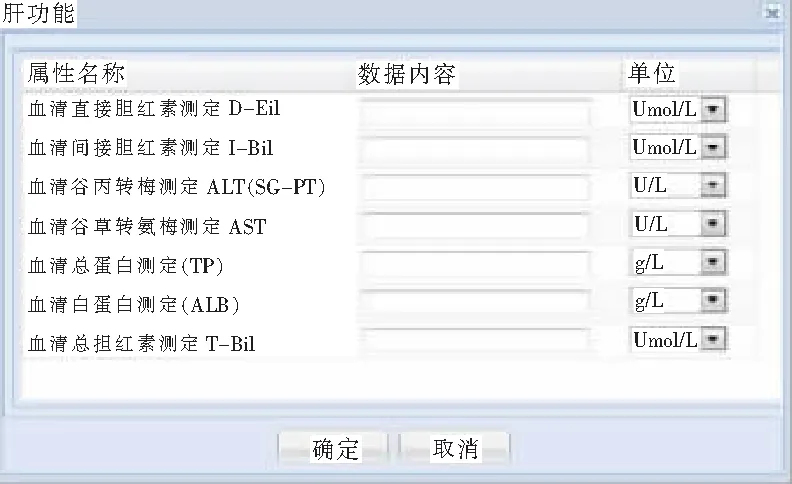
图6 现有ADR监测系统
图7展示了来源于CHPS的数据导出功能,可导出列表中所有药品不良反应报告数据,也可筛选后导出。系统既可以在医院内Intranet环境下用excel表格形式上传药品不良反应报告至省平台,同时,也在Internet环境下一键上传至省平台。该系统确实能够实现HIS等系统、中间级数据库、国家级CHPS之间的数据互换。
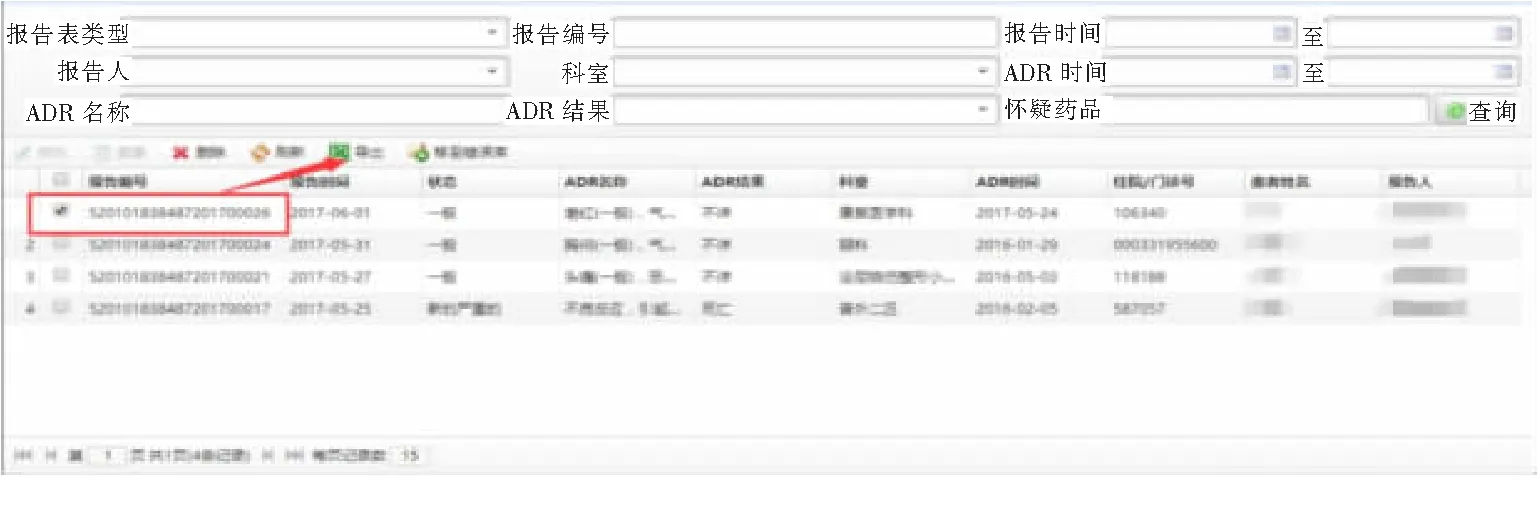
图7 数据导出功能(来源于CHPS)
5 结束语
本文针对药品不良反应的危害和我国医院药品不良反应管理模式的现状,提出以一种新型的医院药品不良反应监测分析服务系统。该系统可以满足国家对平台统一的对接要求,保证病人用药安全,降低药品不良反应对人民生命健康所构成的危害。并实现院级单位对于ADR相关事件和报告的综合管理策略,有效地探索了ADR系统性监测、处方事件预警性管理等先进方法与较为传统的呈报监测方法有机结合的创新模式。通过药品不良反应监测网络和为各科室提供一站式在线服务的形式,实现不良反应信息资源共享和综合开发利用,具有良好的经济和社会效益预期。

