发酵香肠源抗氧化肽的稳定性
栾晓旭,冯美琴,孙 健,*
(1. 南京农业大学食品科技学院,国家肉品质量安全控制工程技术研究中心,江苏 南京 210095;2.金陵科技学院动物科学与技术学院,江苏 南京 210038)
近年来,随着合成抗氧化剂的逐渐淘汰,具有抗氧化活性的天然物质被广泛应用于抑制肉制品的氧化酸败[1-4]。据报道,从肉制品中获得的肽具有良好的抗氧化活性[5-7],为发酵香肠通过内源性抗氧化肽抑制自身氧化进程、延长保质期提供了可能。这一猜想在诸多学者的研究中得到证实[8-11]。并且,抗氧化肽具有安全性高、易吸收、活性强等优点,但作为蛋白质的降解产物,抗氧化肽的稳定性较弱,活性容易受环境因素影响。
抗氧化肽在生产加工、贮藏期间不可避免地会发生水解、氧化、脱酰胺、环化等生化反应,破坏肽链结构,从而导致其活性降低甚至完全丧失[12-13]。另外,消化道中的蛋白酶会一定程度上降解抗氧化肽,生成更低分子质量的短肽和游离氨基酸,影响其稳定性。姚轶俊等[14]分析了菜籽抗氧化肽WDHHAPQLR的稳定性,发现高温、强酸强碱、NaCl、蔗糖等不利于多肽活性的保持,苯甲酸钠和山梨酸钾对其稳定性影响不明显。刘晶晶等[15]认为温度、食盐、蔗糖对河蚬抗氧化肽的羟自由基清除活性影响不大。据郑志强等[16]报道,小麦抗氧化肽的稳定性与温度、pH值、食品原辅料、金属离子和模拟胃肠道消化密切相关。另外,多肽的氨基酸组成多样、排列方式千变万化,多肽的结构和活性各异,对各影响因素的响应程度也有所不同。唐宁等[17]研究发现玉米抗氧化肽Leu-Pro-Phe的抗氧化活性随NaCl和糖类添加量的增加显著增强,与葡萄糖相比,Leu-Pro-Phe对蔗糖更为敏感。Liu Dongmei等[18]则发现高NaCl浓度会导致鸭肉源抗氧化肽部分析出,肽活性降低。胡小军等[19]认为葡萄糖可与肽发生美拉德反应,生成的还原性产物可增强肽液的抗氧化活性,因此葡萄糖的增效作用比蔗糖更强。
本实验从接种植物乳杆菌CD101的发酵香肠中提取到了具有较强抗氧化活性的粗肽粉,但其稳定性尚不明确,生产和应用受到一定限制。因此,本实验以体外1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)自由基清除活性、Fe2+螯合活性和2,2’-联氮双(3-乙基苯并噻唑啉-6-磺酸)(2,2’-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid),ABTS)总抗氧化能力为指标,探究温度、pH值、食品配料、金属离子和模拟胃肠道酶系对发酵香抗氧化肽稳定性的影响,旨在为发酵香肠抗氧化肽作为功能性抗氧化剂的生产、贮藏和应用提供一定的理论和实验依据。
1 材料与方法
1.1 材料与试剂
发酵香肠为实验室自制;胃蛋白酶、胰蛋白酶、DPPH(分析纯)、1-苯胺基萘-8-磺酸(1-aniline naphthalene-8-sulfonic acid,ANS)(分析纯) 美国Sigma公司;ABTS总抗氧化能力检测试剂盒 上海碧云天生物技术有限公司;菲啰嗪、NaNO2(分析纯)上海阿拉丁生化科技股份有限公司;磷酸盐缓冲液(phosphate buffered saline,PBS)、氯化亚铁、蔗糖、葡萄糖、NaCl(均为分析纯) 国药集团化学试剂有限公司。
1.2 仪器与设备
Ultra Turrax T25高速匀浆机 德国IKA公司;RE-52AA旋转蒸发仪 上海亚荣生化仪器厂;ES2030冷冻干燥机、L-8900A氨基酸自动分析仪 日本Hitachi公司;Spectral Max M2e多功能酶标仪 美国伯腾仪器有限公司。
1.3 方法
1.3.1 发酵香肠源抗氧化肽的制备[20]
发酵香肠→去肠衣、肥肉、筋膜→绞成肉糜→冰浴匀浆(0.1 mol/L pH 7.2 PBS;15 000 r/min,4×15 s)→静置2 h→12 000 r/min离心20 min→取上清液,纱布过滤→加入3 倍体积40%乙醇溶液→静置过夜→12 000 r/min离心20 min→取上清液,抽滤→旋转蒸发→冷冻干燥→发酵香肠抗氧化肽。
1.3.2 DPPH自由基清除活性测定
参考Najafian等[21]方法,测定粗肽液的DPPH自由基清除率。
1.3.3 螯合Fe2+能力的测定
根据Yu Di等[22]的方法,测定粗肽液螯合Fe2+能力。
1.3.4 ABTS总抗氧化能力测定
参照Mejri等[23]的方法,使用ABTS总抗氧化能力检测试剂盒进行测定。
1.3.5 疏水性测定[24]
用超纯水配制粗肽液,梯度稀释,采用ANS荧光探针法测定荧光强度。以粗肽液浓度为横坐标、荧光强度为纵坐标作图,直线斜率即为粗肽液的表面疏水性指数H0。
1.3.6 游离氨基酸含量测定
将肽液与10%的磺基水杨酸溶液按4∶1混合,2~8 ℃静置1 h,1 000 r/min离心15 min,取上清液,经0.45 μm的尼龙滤膜过滤,取20 μL,用自动氨基酸分析仪测定。
1.3.7 发酵香肠肽体外抗氧化能力的稳定性分析
1.3.7.1 温度对发酵香肠抗氧化肽活性的影响
配制质量浓度为1 mg/mL的发酵香肠抗氧化肽溶液,分别在25(室温)、40、60、80、100 ℃水浴中保温2 h,保温完成后急速冷却,测定DPPH自由基清除率、Fe2+螯合率和总抗氧化能力。
1.3.7.2 pH值对发酵香肠抗氧化肽活性的影响
配制质量浓度为1 mg/mL的粗肽液,用1 mol/L盐酸和氢氧化钠调整溶液pH值分别为3.0、5.0、7.0、9.0、11.0,室温振荡反应2 h,结束后调节样品的pH值为7.0,测定DPPH自由基清除率、Fe2+螯合率和总抗氧化能力。
1.3.7.3 食品原料对发酵香肠抗氧化肽活性的影响
配制质量浓度为1 mg/mL的粗肽液,分别添加质量分数2%、4%、6%、8%、10%的蔗糖、葡萄糖和氯化钠,室温振荡2 h后,测定DPPH自由基清除率、Fe2+螯合率和总抗氧化能力。
1.3.7.4 金属离子对发酵香肠抗氧化肽活性的影响
配制质量浓度为1 mg/mL的粗肽液,分别添加50、100、150、200、250 μg/mL的CuCl2和KCl,室温振荡反应2 h,测定DPPH自由基清除率、Fe2+螯合率和总抗氧化能力。
1.3.7.5 NaNO2对发酵香肠抗氧化肽活性的影响
配制质量浓度为1 mg/mL的粗肽液,分别添加质量分数0.005%、0.010%、0.015%、0.020%、0.025%的NaNO2,室温振荡反应2 h后,测定DPPH自由基清除率、Fe2+螯合率和总抗氧化能力。
1.3.7.6 体外模拟胃肠道消化对发酵香肠抗氧化肽活性的影响
3.1.1 医学图书馆管理人员的软实力要提高。医学院校图书馆管理人员在一定程度上存在差异,包括知识水平的不同,相关专业不一,所以对图书资料专业知识了解不足,计算机信息技术,英语水平普遍底,导致医学图书馆管理素质参差不齐。图书馆学家阮冈纳赞说过:“不管图书馆坐落在什么地方,开馆时间和设备怎样,也不管管理图书馆的方法怎样,一个图书馆成败的关键还是在于图书馆工作者”[19]。因此,医学图书馆的发展与馆员的素质密切相关。大数据时代医学图书馆如何应对面临的挑战,如何更好的开展图书馆的工作,就要不断学习图书馆相关知识,和医学相关知识。具备卓越的洞察力,有对信息组织和检索能力。
配制1 mg/mL的粗肽液,用1 mol/L盐酸调节粗肽液pH值至2.0,加入质量分数4%的胃蛋白酶,在37 ℃消化2 h,每30 min取一次样,消化完成后分成两部分,一部分沸水浴15 min终止反应,为胃蛋白酶消化样品。剩余部分继续反应,用0.9 mol/L碳酸氢钠溶液调节粗肽液pH值至5.3,再用1 mol/L氢氧化钠溶液调节粗肽液pH值至7.5,加入质量分数4%的胰蛋白酶,在37 ℃环境中孵育2 h,每30 min取一次样,反应完成后沸水浴15 min,为胰蛋白酶消化样品。分别测定消化前、胃蛋白酶酶解、胰蛋白酶酶解后的粗肽液的表面疏水性、游离氨基酸含量和抗氧化活性。
1.4 数据分析
2 结果与分析
2.1 温度对发酵香肠抗氧化肽活性的影响
如图1所示,粗肽液的DPPH自由基清除率与温度呈负相关。与室温相比,60 ℃孵育2 h,DPPH自由基清除率下降约16%。当温度继续升高,DPPH自由基清除率急剧下降(P<0.05),100 ℃时活性仅为16.87%。ABTS阳离子自由基清除率变化趋势与此类似,但下降幅度较小。与25 ℃时相比,100 ℃时ABTS阳离子自由基清除力下降5%左右。据Asaduzzaman等[25]报道,长时间暴露于高温中会导致抗氧化肽变性聚集,使得粗肽液的自由基清除活性下降。与此相反,加热温度在25~80 ℃时,Fe2+螯合率逐渐增大,100 ℃时略有下降,但螯合率仍比25 ℃时高出3%左右。这可能是因为高温处理改变了抗氧化肽的构象,使得组氨酸更容易与Fe2+结合,体系中Fe2+含量减少,粗肽液的Fe2+螯合率增加[26]。完整的二级结构对维持肽类的生物活性十分重要,处理温度过高、加热时间长不可避免地会改变抗氧化肽的二级结构[27-28],影响其稳定性。因此,发酵香肠和抗氧化肽宜在中低温环境中加工。
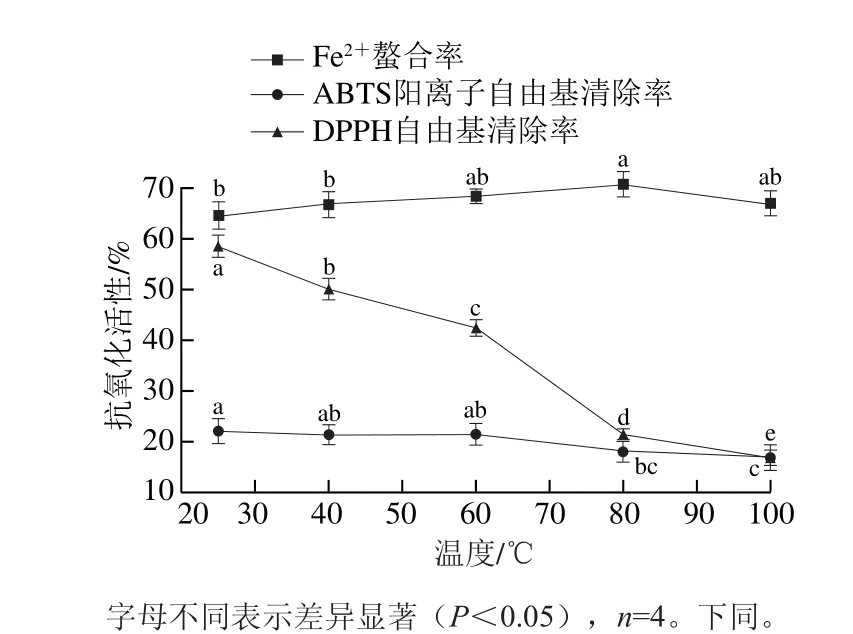
图1 温度对发酵香肠抗氧化肽活性的影响Fig. 1 Changes in antioxidant activities of peptides extracted from fermented sausages at different temperatures
2.2 pH值对发酵香肠抗氧化肽活性的影响
pH值可通过影响肽的电离势和电子转移能力影响肽的抗氧化活性[29]。如图2所示,pH 7.0时粗肽液的DPPH自由基清除活性最高,偏酸或碱性环境都会导致DPPH自由基清除活性显著下降(P<0.05)。其中,在pH 3.0环境中孵育2 h,粗肽液的DPPH自由基清除率下降10%,而在pH 11.0环境中反应2 h,活性下降22%。因此,粗肽液的DPPH自由基清除活性对碱性环境更敏感。碱性环境会促进肽类物质发生外消旋或脱酰胺反应,从而导致多肽的活性下降[30-31]。而酸性或低酸介质则会降低分子溶解度,影响肽分子羟基的有效性,这有可能促进氢原子的捐赠,减弱DPPH自由基清除活性[32]。pH 7.0时粗肽液的Fe2+螯合率最低,随着碱性或酸性的增强螯合率显著增强(P<0.05),但增加幅度较小。碱性环境中氧合酰胺基上的氮原子会携带负电荷,增强抗氧化肽对Fe2+的吸引力,从而提高Fe2+螯合率[28]。姚轶俊等[14]研究发现菜籽抗氧化肽Fe2+螯合活性随pH值递增呈先增高后降低的趋势,与本实验趋势相反。这可能是因为发酵香肠抗氧化肽和菜籽抗氧化肽的结构、氨基酸组成和最适pH范围等有所不同,导致在相同条件下2 种抗氧化肽的活性存在一定差异。粗肽液的ABTS阳离子自由基清除活性对pH值不敏感,清除率上下波动,变化不显著(P>0.05)。发酵香肠抗氧化肽耐酸、碱性较弱,为了保持较好的抗氧化活性,宜在中性、弱酸性环境中加工制备、保藏发酵香肠及其抗氧化肽。

图2 pH值对发酵香肠抗氧化肽活性的影响Fig. 2 Changes in antioxidant activities of peptides extracted from fermented sausages under different pH conditions
2.3 食品配料对发酵香肠抗氧化肽活性的影响
2.3.1 NaCl的影响

图3 NaCl对发酵香肠抗氧化肽活性的影响Fig. 3 Changes in antioxidant activities of peptides extracted from fermented sausages at different NaCl contents
如图3所示,加入NaCl后,粗肽液的DPPH自由基和ABTS阳离子自由基清除率分别增强18%和6%左右。Pereira等[32]认为,肽与含有NaCl的食品基质之间的相互作用有利于肽生物活性的维持。相反地,随着NaCl添加量的提高,粗肽液的螯合Fe2+活性急剧下降(P<0.05),添加量达10%时,螯合率仅为22.23%。这可能是因为NaCl对肽分子结构造成一定程度破坏,加速氨基酸侧链的裂解,导致其螯合Fe2+能力下降[33]。结果表明,NaCl有利于抗氧化肽清除自由基活性的提高,对螯合Fe2+活性保持有不良影响。为保证抗氧化肽较高的活性,在加工和应用过程中应适量添加食盐,或者对产品进行脱盐等处理。

图4 葡萄糖对发酵香肠抗氧化肽活性的影响Fig. 4 Changes in antioxidant activities of peptides extracted from fermented sausages at different glucose contents
图4 中,粗肽液的DPPH自由基清除活性与葡萄糖添加量呈显著正相关(P<0.05),添加量为10%时,DPPH自由基清除活性增加至未添加组的1.23 倍。研究表明,多肽和氨基酸可以与还原糖类发生美拉德反应,促进醛、酮等还原性物质的生成,提高肽液的供质子能力,从而促进抗氧化活性的提高[19,34]。粗肽液的Fe2+螯合活性与葡萄糖添加量呈负相关,添加量从2%提高至10%时,Fe2+螯合率从52.56%下降到42.36%。添加糖类将提高溶液黏稠度,阻碍肽段与Fe2+螯合。粗肽液的ABTS阳离子自由基清除活性对葡萄糖的抑制作用敏感度较低,活性稳定在19%左右。

图5 蔗糖对发酵香肠抗氧化肽活性的影响Fig. 5 Changes in antioxidant activities of peptides extracted from fermented sausages at different sucrose contents
图5 中,蔗糖组的变化趋势与葡萄糖组类似,但当添加量相同时,蔗糖组的活性保持率高于葡萄糖组。另外,蔗糖质量分数升高时,DPPH自由基清除活性稍有升高,但无显著差异(P>0.05)。胡晓等[35]研究结果与本研究结果类似。原因可能在于蔗糖为非还原糖性多糖,常温下水解不完全,美拉德反应受到一定抑制[36-37]。唐宁[17]和Guérard[38]等的研究表明,糖类是玉米抗氧化肽和鱼肉源抗氧化肽的增效剂,但每种糖的作用效果略有不同。
2.3.3 NaNO2的影响

图6 NNaaNNOO2对发酵香肠抗氧化肽活性影响Fig. 6 Changes in antioxidant activities of peptides extracted from fermented sausages at different NaNO2 contents
图6 中,NaNO2添加量在0.005%~0.025%范围内时,粗肽液的DPPH自由基清除率先降低后升高,在0.020%时取得最小值,清除率约为45%。Fe2+螯合活性则先升高后降低,在0.020%时螯合率为63.35%,仅比未添加组低4%左右。NaNO2添加量递增时,粗肽液的ABTS阳离子自由基清除率上下波动,无显著差异(P>0.05)。结果表明,发酵香肠加工中常用的发色剂、防腐剂NaNO2对发酵香肠抗氧化肽的活性影响较小。因此,在国家标准规定的添加范围内NaNO2对发酵香肠抗氧化肽稳定性影响不大。
2.4 金属离子的影响

图7 CCuu22+对发酵香肠抗氧化肽活性的影响Fig. 7 Changes in antioxidant activities of peptides extracted from fermented sausages at different Cu2+ contents

图8 K+对发酵香肠抗氧化肽活性影响Fig. 8 Changes in antioxidant activities of peptides extracted from fermented sausages at different K+ contents
由图7、8可知,Cu2+和K+显著抑制了粗肽液清除自由基活性(P<0.05),其中Cu2+的抑制作用更明显。当离子质量浓度达到250 μg/mL时,粗肽液分别保持30.89%和48.18%的DPPH自由基清除率。过渡金属Cu2+更容易与多肽形成配合物[39],阻碍DPPH自由基清除过程。Thanonkaew等[40]发现Cu2+对乌贼肌肉肽的稳定性无显著影响。这可能是因为多肽的组成不同,对金属离子的响应机制和程度也有所不同。金属离子质量浓度从5 μg/mL递增至250 μg/mL过程中,K+对ABTS阳离子自由基清除活性影响不显著(P>0.05),Cu2+可增强其清除活性,Cu2+质量浓度为250 μg/mL时,清除率可达16.66%,比50 μg/mL时高出10%左右。Cu2+和K+对Fe2+螯合活性影响不一,其中,Cu2+可显著增强其活性(P<0.05),离子质量浓度为250 μg/mL时取得最大值94.77%,为未添加金属离子时的1.4 倍。随K+浓度升高,粗肽液的Fe2+螯合率的变化趋势为降低-升高-降低,离子质量浓度为200 μg/mL时螯合率为64.67%,约比未添加组低3%,250 μg/mL时螯合率取得最小值57.87%。于丽娜等[26]发现加入Cu2+后,样品的Fe2+螯合率增大为对照样品的2.3 倍,与本实验结果类似。原因在于氯化铜的水溶液为弱酸性,导致肽链上组氨酸残基中的咪唑基接受质子,容易与Fe2+形成六元环和七元环,提高粗肽液对Fe2+的螯合活性。结果表明,在加工、贮藏发酵香肠及其抗氧化肽时应尽量避免与铜制器具接触,同时尽量不与富含Cu2+的原辅料混合加工。
2.5 模拟胃肠消化道酶系对发酵香肠抗氧化肽活性的影响
2.5.1 模拟胃肠消化道酶系对游离氨基酸组成的影响

表1 模拟胃肠道消化中发酵香肠粗肽液游离氨基酸组成的变化Table 1 Changes in free amino acid contents of peptides extracted from fermented sausages during simulated GI digestion with pepsin followed by typsin μg/mL
如表1所示,胃蛋白酶消化2 h后,粗肽液中游离氨基酸总量从77.620 μg/mL显著增加到84.326 μg/mL(P<0.05),再经过2 h的模拟胰蛋白酶消化,游离氨基酸总量进一步增加到98.474 μg/mL,是消化前的1.27 倍。这可能是因为胃蛋白酶的主要作用是破坏多肽的二级结构,将其水解成更小分子的肽。而胰蛋白酶则可以将多肽进一步水解,同时伴随着大量游离氨基酸生成[18]。另外,经过胃酶和胰酶的水解,粗肽液中疏水氨基酸Val、Leu、Pro、Ala、Met含量显著增高(P<0.05),Lys、Arg等具有金属离子螯合能力的氨基酸也显著增多(P<0.05)。
2.5.2 模拟胃肠消化道酶系对表面疏水性的影响

图9 模拟胃肠消化中发酵香肠粗肽液表面疏水性的变化Fig. 9 Effect of simulated GI digestion on surface hydrophobicity of antioxidant peptides extracted from fermented sausages
图9 表明,胃酶消化后,粗肽液的表面疏水性可达441.16,显著高于消化前(P<0.05)。这进一步验证了在胃蛋白酶的作用下,发酵香肠抗氧化肽的结构遭到破坏,使其多肽内部的疏水基团的得以暴露,表面疏水性增加[24]。而胰蛋白酶酶解后,粗肽液的表面疏水性锐减至6.63(P<0.05)。结合表1可知,胰蛋白酶水解导致游离氨基酸特别是Asp、Glu、Lys、Arg、Thr等亲水性游离氨基酸显著增多,会导致粗肽液的亲水性增强,表面疏水性降低。
2.5.3 模拟胃肠消化道酶系对发酵香肠粗肽液抗氧化活性的影响

图10 模拟胃肠消化对发酵香肠抗氧化肽活性的影响Fig. 10 Effect of simulated GI digestion on antioxidant activities of peptides extracted from fermented sausages
如图10所示,0~120 min为模拟胃蛋白酶消化,120~240 min为模拟胰蛋白酶消化。经过120 min的模拟胃蛋白酶消化后,粗肽液的DPPH自由基清除率显著(P<0.05)下降至45.8%,与消化前相比,活性保持率约77%,这可能是因为消化酶的最适温度(37 ℃)不利于粗肽液DPPH自由基清除活性的保持(图1)。在胰蛋白酶的作用下,粗肽液的DPPH自由基清除活性完全丧失。Zhu Chaozhi等[24]报道,模拟胃肠道消化会导致粗肽液的DPPH自由基清除活性显著降低。胃蛋白酶消化显著(P<0.05)降低了粗肽液的Fe2+螯合活性,消化120 min后活性仅为26%。模拟胃蛋白酶消化改变了多肽结构,破坏了螯合金属离子的基团或氨基酸。而120 min的胰蛋白酶消化结束后,粗肽液的Fe2+螯合率显著增加(P<0.05)至95.94%,是消化前的1.41 倍左右。这与酶解液中显著增多的中性和酸性氨基酸有关[41]。蛋白酶解可显著增强粗肽液的ABTS阳离子自由基清除活性,但ABTS阳离子自由基清除率与消化时间、酶系种类无显著相关性(P>0.05),在实验时间内一直维持在40%左右。
3 结 论
本实验探究了不同因素及体外模拟胃肠道酶系消化对发酵香肠抗氧化肽稳定性的影响。结果表明,中高温、酸碱性环境不利于抗氧化肽活性保持;食盐和糖类可促进体系中自由基的清除,抑制抗氧化肽的Fe2+螯合活性;在国标规定范围内使用NaNO2对抗氧化肽稳定性影响不大;与K+相比,Cu2+对抗氧化肽稳定性的影响更为显著;模拟胃肠道酶系消化后,DPPH自由基清除活性完全丧失,Fe2+螯合率显著升高,这与蛋白酶改变了肽链结构和氨基酸组成有关。

