双黄连口服液质量分析
吴雪琴,王胜义,王磊,王富河,吴亮红,崔东安,孙研
(中国农业科学院兰州畜牧与兽药研究所,甘肃省中兽药工程技术研究中心,兰州 730050)
中兽医药作为我国兽医医疗系统的重要组成部分,在疾病预防和治疗方面发挥着重要作用。在全球高度重视细菌耐药性和抗生素慎重使用背景下,中兽药逐步成为保障动物源食品安全的重要战略工具[2]。另一方面,绿色、无抗的中兽药亦成假兽药盛行的重灾区。由农业农村部组织的兽药质量监督抽检和风险监测报告结果显示,中药类产品不合格率偏高,不合格项目主要集中在产品性状、鉴别、检查项和含量等,并有些中兽药产品中检出非法添加物[3-4]。因此,监测中兽药产品质量总体水平和状态,发现可能影响药品质量与安全的因素及隐患,为进一步强化对中兽药产品质量的监管、不断提高中兽药产品安全有效和质量水平的可控、保障动物用药安全和动物源食品安全提供有力的技术支撑。
双黄连口服液由金银花、黄芩和连翘三味中药提取精制而成,具有辛凉解表、清热解毒的功效[1]。现代药理学研究表明,双黄连口服液具有广谱抑菌[5]、抗病毒[6]、解热抗炎[7]、免疫调节[8]等作用。在治疗畜禽感冒、炎症、病菌感染等疾病的临床效果好,而且其毒副作用小,因此在兽医临床的应用广泛。同时,双黄连制剂,组方精简,疗效确切,因此是兽药企业青睐的产品,目前有1245个兽药企业具有双黄连制剂的生产批准文号,其中有569个企业生产双黄连口服液。
研究以双黄连口服液产品为研究对象,依据2015版《中国兽药典》二部双黄连口服液质量标准,采用薄层色谱法和高效液相色谱法,分析双黄连口服液中黄芩苷、绿原酸和连翘苷的色谱特征和含量,对市售双黄连口服液进行质量考察,为进一步提升双黄连口服液质量控制提供技术依据。
1 材料与方法
1.1 材料
1.1.1 药品和对照品 在市面上随机购买18个不同厂家的药品,将其进行编号1-18。绿原酸对照品(110753-201817)、黄芩苷对照品(110715-201821)、连翘苷对照品(110821-201816)。
1.1.2 仪器与试剂 高效液相色谱U-3000(赛默飞世尔科技(中国)有限公司);SP-20E全自动点样仪(上海科哲生化科技有限公司);GoodLook-1000型全自动薄层色谱成像系统(上海科哲生化科技有限公司);SGel型电动喷雾器(德国DESAGA公司);ME235S型微量分析天平(赛多利斯公司);AL104电子天平(梅特勒-托利多有限公司);KH5200型超声波清洗器(昆山禾创超声仪器有限公司);硅胶G板200 mm×100 mm(青岛海洋化工厂生产);聚酰胺薄膜(国药集团化学试剂有限公司);中性氧化铝柱(Agela Techologies);精密鼓风干燥箱(上海一恒科学仪器有限公司)
甲醇、乙腈为色谱纯;乙醇、醋酸、三氯甲烷、硫酸等为分析纯。
1.2 方法
1.2.1 定性鉴别[1]
1.2.1.1 黄芩苷、绿原酸的定性鉴别方法[1]供试品溶液的制备:分别量取18个厂家的双黄连口服液1 mL,分别加75%乙醇溶液5 mL,摇匀,既得。
对照品溶液的制备:精密称取黄芩苷对照品11.49 mg、绿原酸对照品1.14 mg,加入75%乙醇分别定容在10 mL量瓶中,浓度为1.122和0.114 mg/mL。
方法测定:照薄层色谱法试验,吸取上述三种溶液各2 μL,分别点于同一聚酰胺薄膜上,以36%乙酸为展开剂,展开,取出,晾干,置紫外光灯365 nm下检视。检查供试品色谱中,在与黄芩苷对照品、绿原酸对照品色谱相应的位置上,是否显相同颜色的荧光斑点。
1.2.1.2 连翘苷的薄层鉴别方法[1]供试品溶液的制备:分别量取18个厂家的双黄连口服液1 mL,分别加甲醇5 mL,摇匀,静置,取上清液,既得。
对照品溶液的制备:精密称取连翘苷对照品5.13 mg,加甲醇定容在10 mL量瓶中,浓度为0.513 mg/mL。
方法测定:照薄层色谱法试验,吸取上述两种溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇(5∶1)为展开剂,展开,取出,晾干,喷以10%的硫酸乙醇溶液,在105 ℃加热至斑点显色清晰。检查供试品色谱中,在与连翘对照品色谱色谱相应的位置上,是否显相同颜色的斑点。
1.2.2 含量测定
1.2.2.1 黄芩苷、绿原酸含量测定[1]色谱条件:Waters Symmetry© C18色谱柱(250 mm×4.6 mm,5 μm);流动相∶乙腈为A、0.4%磷酸溶液为B如表1梯度洗脱;体积流量1.0 mL/min;柱温:30℃;检测波长324 nm;在上述色谱条件下,理论塔板数按绿原酸峰计算不应低于6000。

表1 黄芩苷、绿原酸洗脱梯度表Tab 1 Gradient table of Baicalin and chlorogenicacid elution
供试品溶液的制备:分别精密量取18个厂家的双黄连口服液1 mL,置50 mL量瓶中,加50%甲醇适量,超声处理20 min,放置至室温,加50%甲醇稀释至刻度,摇匀,经微孔滤膜过滤,即得。每个样品平行3次。
对照品溶液的制备:精密称取黄芩苷对照品20.20 mg,绿原酸对照品1.53 mg,分别置100 mL量瓶中,加50%甲醇定量使溶解并稀释至刻度,摇匀,经微孔滤膜过滤,即得。
样品含量测定:在上述色谱条件下,分别精密吸取对照品溶液和不同厂家供试品溶液各10 μL,注入液相色谱仪。
结果分析:根据对照品、供试品的峰面积,以外标法计算样品中黄芩苷、绿原酸的含量,用SPSS21.0进行分析,结果以平均值±标准偏差表示。
1.2.2.2 连翘苷含量测定[1]色谱条件:Waters Symmetry© C18色谱柱(250 mm×4.6 mm,5 μm);流动相∶乙腈∶水(25∶75);检测波长278 nm;体积流量1.0 mL/min;柱温:30 ℃;在上述色谱条件下,理论塔板数按连翘苷峰计算不应低于6000。
供试品溶液的制备:分别精密量取18个厂家的双黄连口服液1 mL,分别加在中性氧化铝柱(100~12目,6 g,内径为1 cm)上,用70%乙醇40 mL洗脱,收集洗脱液,浓缩至干,残渣加50%甲醇适量,温热使溶解,转移至5 mL量瓶中,并稀释至刻度,摇匀,经微孔滤膜过滤,即得。每个样品平行3次。
对照品溶液的制备:精密称取连翘苷对照品6.46 mg,置100 mL量瓶中,加50%甲醇定量使溶解并稀释至刻度,摇匀,经微孔滤膜过滤,即得。
样品含量测定:在上述色谱条件下,分别精密吸取对照品溶液和不同厂家供试品溶液各10 μL,注入液相色谱仪,检测。
结果分析:同1.2.2.1黄芩苷、绿原酸含量测定分析方法。
2 结 果
2.1 定性鉴别结果
2.1.1 黄芩苷、绿原酸定性鉴别结果 黄芩苷、绿原酸薄层色谱鉴别结果见图1~图7,供试品色谱中,样品1、2、3、4、5、6、7、8、10、11、12、13、14、15、18中的黄芩苷,样品1、2、3、4、5、6、7、8、10、11、12、13、15、16、18中的绿原酸在与对照品色谱相应的位置上有相应的斑点,而样品8、9、14、15、17中的黄芩苷,样品9、14、16、17中的绿原酸在与对照品色谱相应的位置上无相应的斑点。
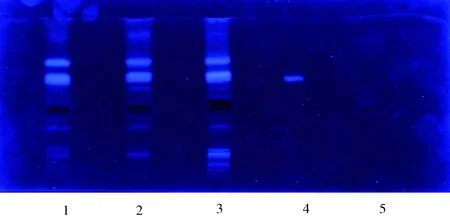
图1 1-3:双黄连口服液样品3.2.1;4:绿原酸对照品;5:黄芩苷对照品Fig 1 1-3: Shuanghuanglian oral liquid sample 3.2.1;4: Chlorogenic Acid reference substance;5: Baicalin reference substance

图2 1-3:双黄连口服液样品6.5.4;4:绿原酸对照品;5:黄芩苷对照品Fig 2 1-3:Shuanghuanglian oral liquid sample 6.5.4;4:Chlorogenic Acid reference substance;5:Baicalin reference substance
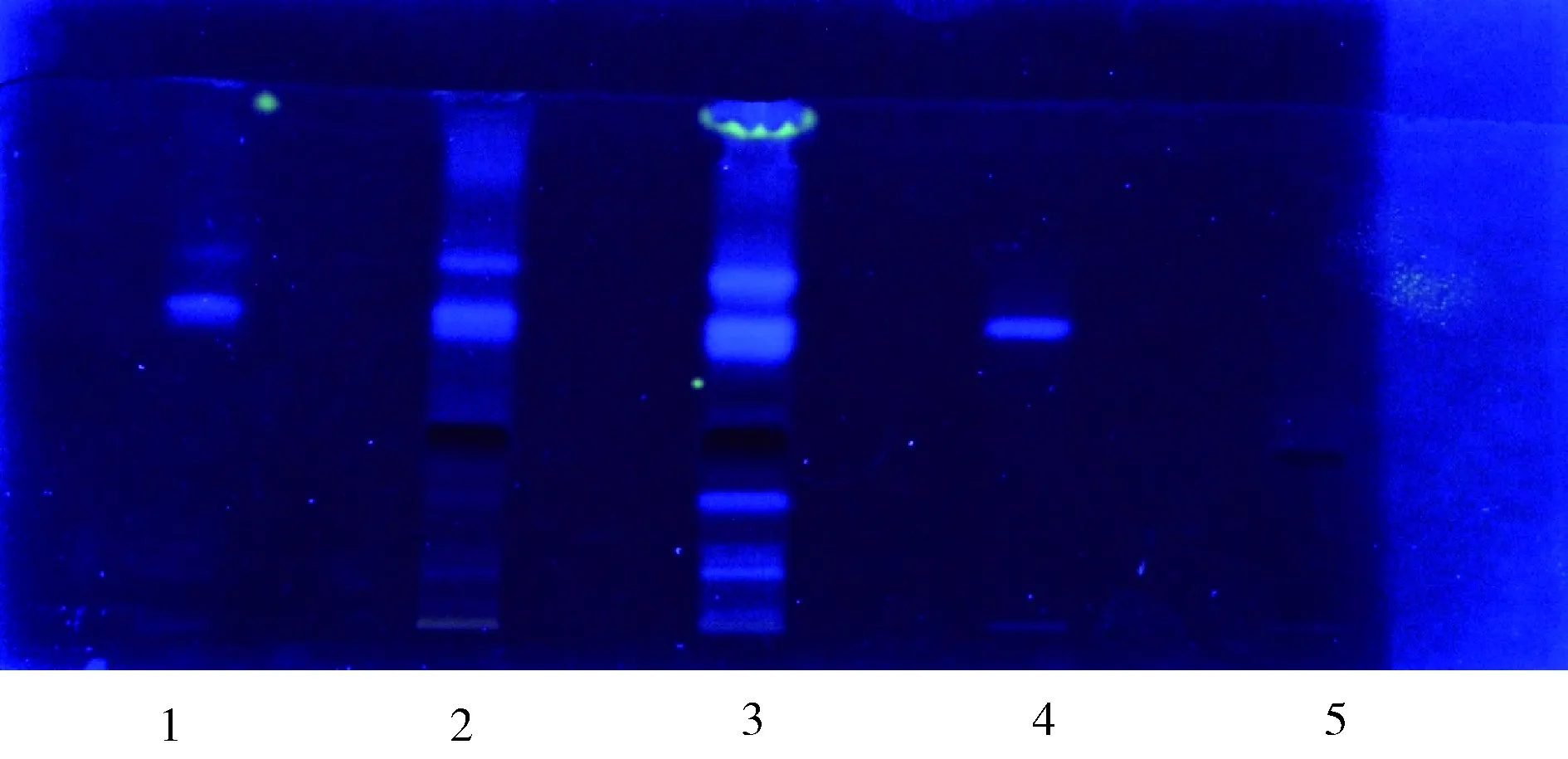
图3 1-3:双黄连口服液样品8.7.6;4:绿原酸对照品;5:黄芩苷对照品Fig 3 1-3: Shuanghuanglian oral liquid sample 8.7.6;4: Chlorogenic Acid reference substance;5: Baicalin reference substance

图4 1-2:双黄连口服液样品10.9;3:绿原酸对照品;4:黄芩苷对照品Fig 4 1-2:Shuanghuanglian oral liquid sample 10.9;3:Chlorogenic Acid reference substance;4:Baicalinreference substance
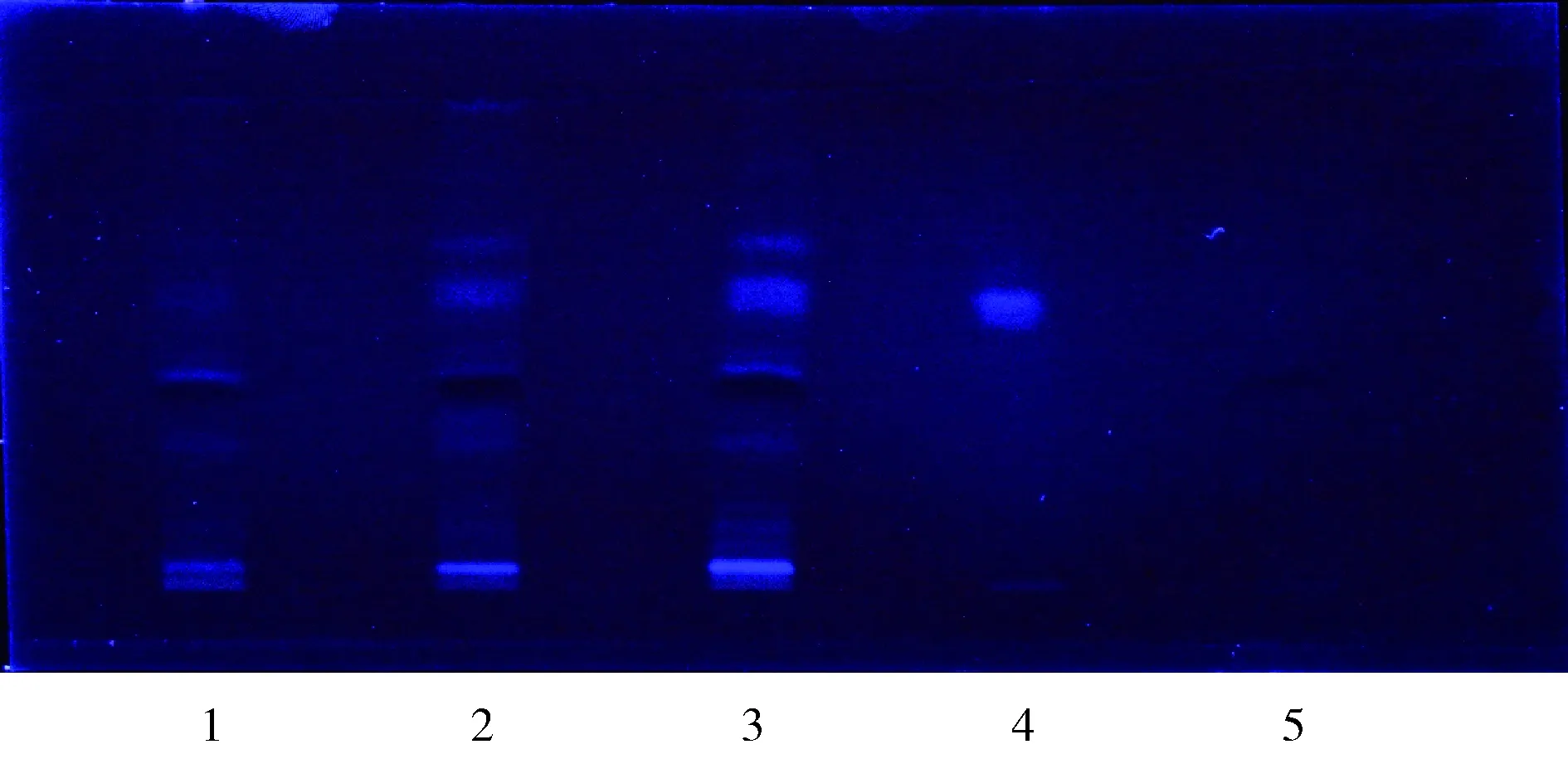
图5 1-3:双黄连口服液样品13.12.11;4:绿原酸对照品;5:黄芩苷对照品Fig 5 1-3:Shuanghuanglian oral liquid sample 13.12.11;4:Chlorogenic Acid reference substance;5:Baicalinreference substance

图6 1-3:双黄连口服液样品16.15.14;4:绿原酸对照品;5:黄芩苷对照品Fig 6 1-3:Shuanghuanglian oral liquid sample 16.15.14;4: Chlorogenic Acid reference substance;5: Baicalinreference substance

图7 1-2:双黄连口服液样品18.17;3:绿原酸对照品;4:黄芩苷对照品Fig 7 1-2:Shuanghuanglian oral liquid sample 18.17;4:Chlorogenic Acid reference substance;5:Baicalinreference substance
2.1.2 连翘苷定性鉴别结果 连翘苷薄层色谱鉴别结果见图8~图12,供试品色谱中,样品1、2、3、4、5、6、7、8、10、11、12、13中的连翘苷在与对照品色谱相应的位置上有相应的斑点,而样品9、14、15、16、17、18中的连翘苷在与对照品色谱相应的位置上无相应的斑点。

图8 1-4:双黄连口服液样品4.3.2.1;5:连翘苷对照品Fig 8 1-4:Shuanghuanglian oral liquid sample 4.3.2.1;5:Phillyrin reference substance

图9 1-4:双黄连口服液样品8.7.6.5;5:连翘苷对照品Fig 9 1-4:Shuanghuanglian oral liquid sample 8.7.6.5;5:Phillyrin reference substance

图10 1-2:双黄连口服液样品10.9;3:连翘苷对照品Fig 10 1-2:Shuanghuanglian oral liquid sample 10.9;3:Phillyrin reference substance

图11 1-4:双黄连口服液样品14.13.12.11;5:连翘苷对照品Fig 11 1-4:Shuanghuanglian oral liquid sample14.13.12.11;5:Phillyrin reference substance
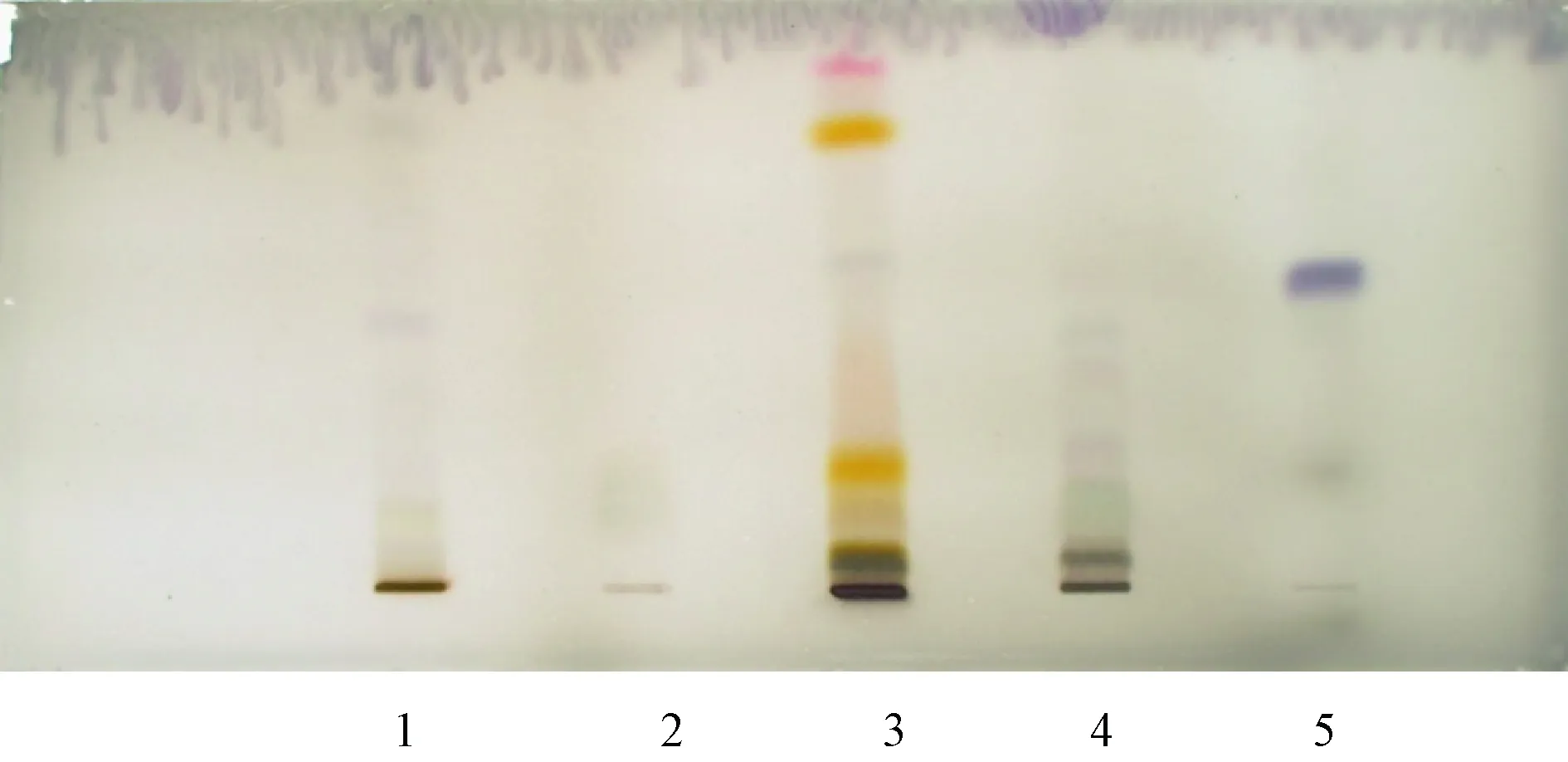
图12 1-4:双黄连口服液样品18.17.16.15;5:连翘苷对照品Fig 12 1-4:Shuanghuanglian oral liquid sample18.17.16.15;5:Phillyrin reference substance
2.2 含量测定结果
2.2.1 黄芩苷、绿原酸含量测定结果 《中国兽药典》二部规定:双黄连口服液每1 mL含黄芩以黄芩苷计不得少于10.0 mg[1]。
双黄连口服液黄芩苷含量测定结果见表2,样品1、2、3、4、5、6、7、11、12、13、18中的黄芩苷含量均高于10.0 mg/mL,而样品8、9、10、14、15、16、17中的黄芩苷含量均低于10.0 mg/mL。
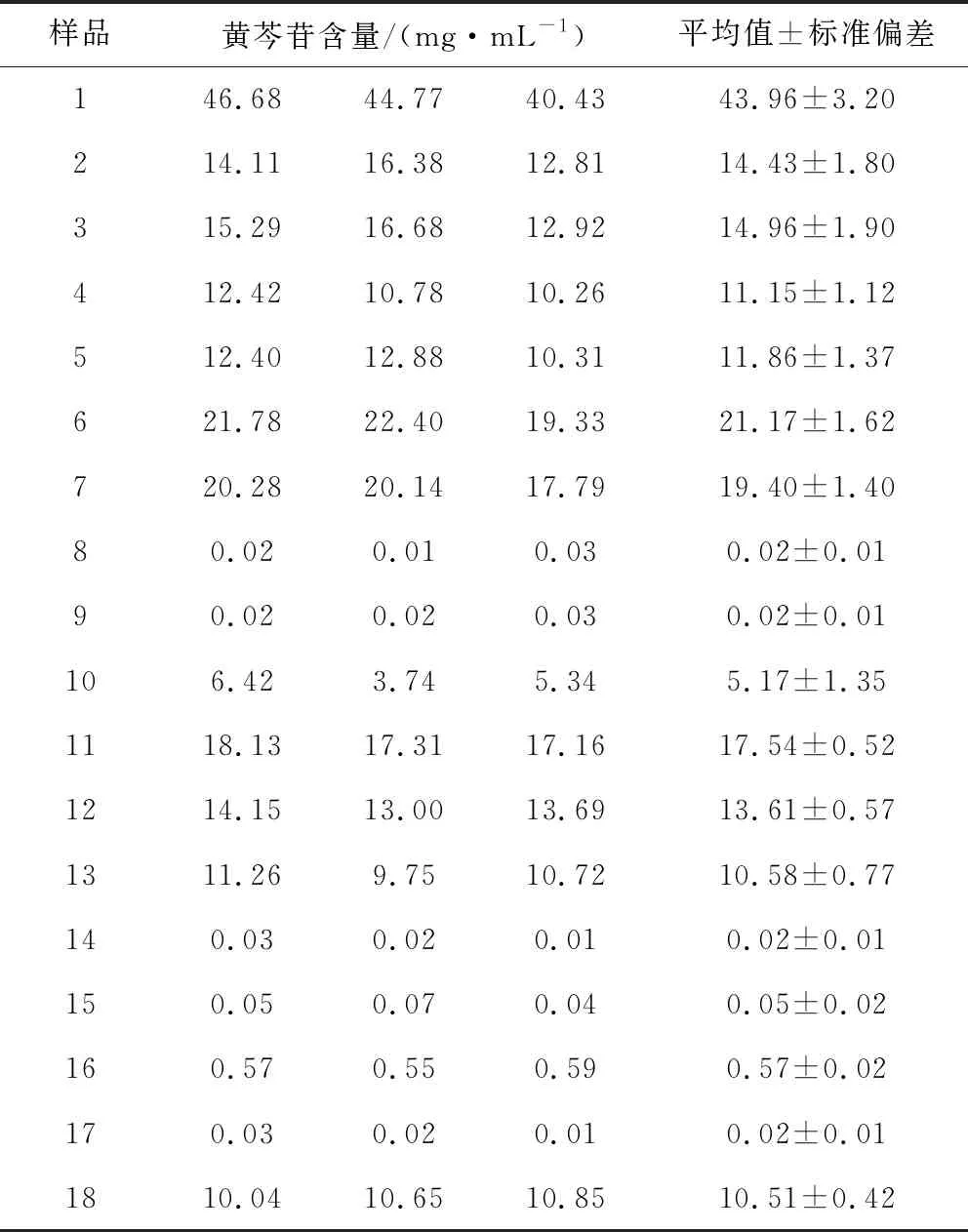
表2 双黄连口服液黄芩苷含量测定结果Tab 2 Determination of Baicalin in Shuanghuanglianoral liquid
《中国兽药典》二部规定:双黄连口服液每1 mL含金银花以绿原酸计不得少0.60 mg[1]。
双黄连口服液绿原酸含量测定结果见表3,样品1、2、3、4、6、11中的绿原酸含量均高于0.60 mg/mL,而样品5、7、8、9、10、12、13、14、15、16、17、18中的绿原酸含量均低于0.60 mg/mL。
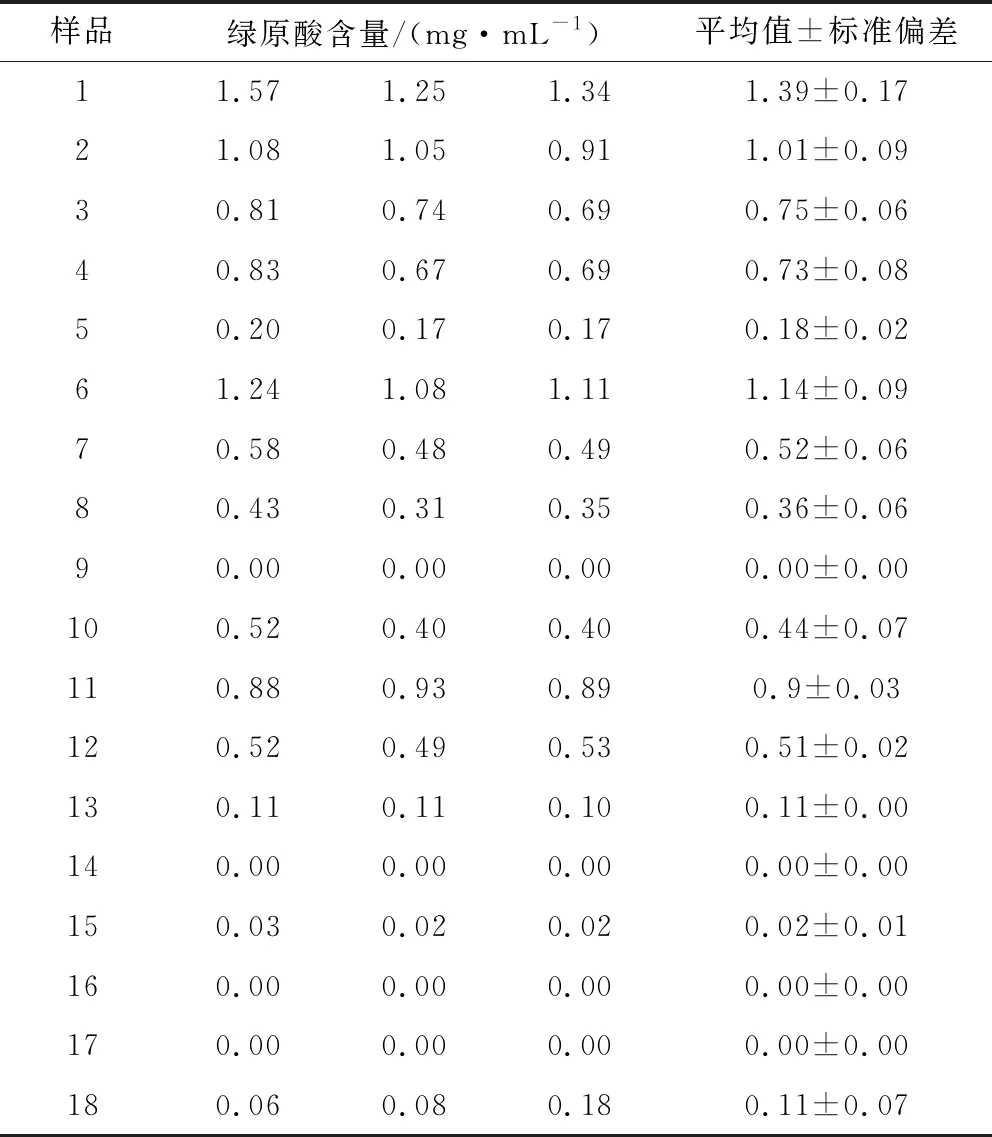
表3 双黄连口服液绿原酸含量测定结果Tab 3 Determination of Chlorogenic Acid inShuanghuanglian oral liquid
2.2.2 连翘苷含量测定结果 《中国兽药典》二部规定:双黄连口服液每1 mL含连翘以连翘苷计不得少于0.30 mg[1]。
双黄连口服液连翘苷含量测定结果见表4,样品1、2、3、4、6、7、11中的连翘苷含量高于0.30 mg/mL,而样品5、8、9、10、12、13、14、15、16、17、18中的连翘苷含量低于0.30 mg/mL.

表4 双黄连口服液连翘苷含量测定结果Tab 4 Determination of Phillyrin in Shuanghuanglianoral liquid
计算双黄连口服液黄芩苷、绿原酸及连翘苷含量与含量限度的百分比见表5,黄芩苷含量与含量限度的百分比≥150%比例为22.22%、≤100%比例为38.89%。黄芩苷含量与含量限度的百分比最高为439.61%,而最低的为0.17%,相差很大。绿原酸含量与含量限度的百分比≥150%比例为16.67%、≤100%比例为66.67%。绿原酸含量与含量限度百分比最高为231.48%,而最低的为0.02%,相差较大。连翘苷含量与含量限度的百分比≥150%比例为38.89%、≤100%比例为61.11%,连翘苷含量与含量限度的百分比最高为341.87%,而最低的为0.46%,相差较大。
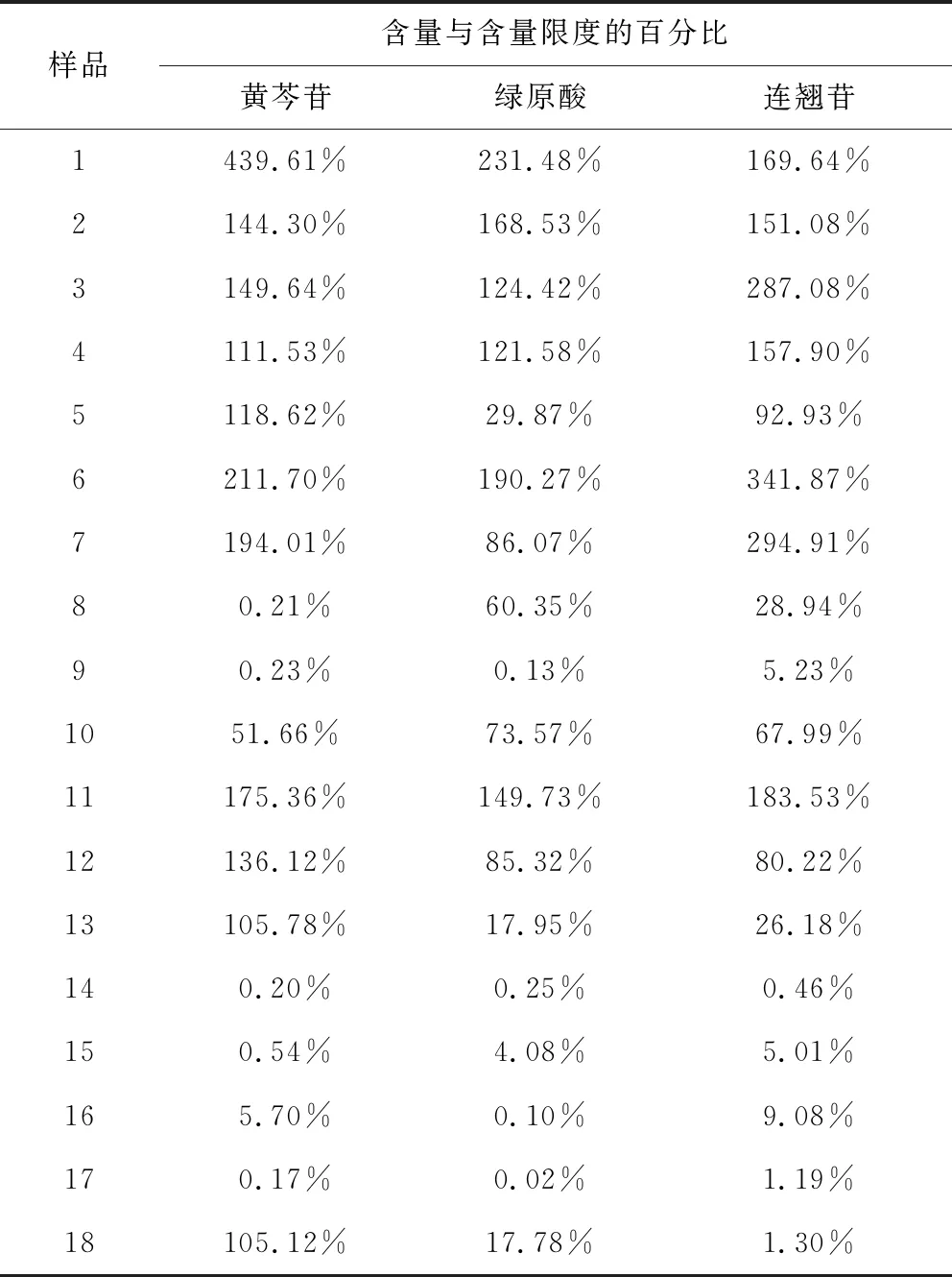
表5 双黄连口服液黄芩苷、绿原酸及连翘苷含量与含量限度的百分比Tab 5 Content and limit of Baicalin, chlorogenicacid and Phillyrin in Shuanghuanglian oral liquid
3 讨 论
在双黄连口服液中,黄芩苷含量范围为0.17%~439.61%、绿原酸含量范围为0.02%~231.48%、连翘苷含量范围为0.46%-341.87%,黄芩苷含量差别尤为突出。绿原酸、连翘苷含量与含量限度的百分比<100%比例分别为为66.67%、61.11%,绿原酸含量不合格是造成双黄连口服液质量问题的主要因素。各厂家药材产地、来源不同对双黄连口服液主要成分含量差异有很大影响。黄芩中黄芩苷含量一般在范围7.95%~32.5%[9-10],但大多在14. 1% ~32. 5%[11],一些道地药材中黄芩苷的含量略低于药典中的9%;金银花中绿原酸含量一般在范围1.5%~4.60%[12-14];连翘中连翘苷含量一般在0.15%~0.90%[15-16],一般青翘中的连翘苷含量高于老翘。因此在选用药材时,各厂家应严格控制药材质量,不能只局限于道地药材,应从供给稳定性和质量稳定性选择优质的药材。在生产质量控制时,应以临床疗效为导向,确定药材来源,遵循“药材好,药才好”原理,从中药材源头全过程质量控制。
中药不同于化学药,不仅其成分复杂,生产工艺也较难控制,并容易出现漏洞。各厂家生产工艺有所不同,也会造成制剂主要成分含量存在差异。因此各厂家不仅要加强生产过程监管,在中药制剂中更应严格控制好工艺环节操作。从药材的提取、萃取、干燥、混合制剂等过程中都会影响产品最终质量。中药制剂不是质量标准规定出来的,也不是按照质量标准检验出来的,而是生产出来的。生产工艺作为中药制剂成为最终产品的一道工序, 对其质量有着决定性的作用。基于“质量源于设计”理念,优化建立双黄连口服液的生产工艺,并对生产工艺过程中的各个环节进行调控,确保中药制剂质量控制稳定性和有效成分的均一性,提升产品市场竞争力。
黄芩苷是一种相对不稳定的化合物,遇光、热易分解变化[10];绿原酸是一种不稳定的化合物,在室温下或遇光易分解变化,尤其是在溶液状态下稳定性更差。双黄连口服液在保存过程中绿原酸含量下降明显[17],导致尚处于有效期内的产品经常出现质量不合格的问题。氧化强度和酸碱度对连翘苷稳定性影响较大[15]。因此严格控制双黄连口服液的pH值,建议用棕色瓶保存生产后的双黄连口服液,良好保存和使用,防止产品质量下降。
4 建 议
在黄芩苷的薄层鉴别中,兽药典要求双黄连口服液含量不低于10.0 mg/mL[1],但薄层鉴别中黄芩苷对照品浓度为0.1 mg/mL,结果中样品斑点明显大于对照品斑点,且对照品斑点较淡,建议薄层鉴别黄芩苷对照品浓度应为1.0 mg/mL。建议展开剂用36%的醋酸,能使黄芩苷与绿原酸斑点良好的分离,方便鉴别。展开剂展开时,温度不宜过高,不利于样品中黄芩苷与绿原酸分离。制备黄芩苷标品溶液时,因其不易溶解,本试验采用超声的方法使其较快溶于甲醇。
pH值是影响绿原酸含量的敏感因素[17],pH值越大,绿原酸含量下降越快。因此在生产过程中严格控制pH值,防止绿原酸含量下降。建议将双黄连口服液的pH值范围适当降低。
2015版《中国兽药典》(二部)未规定含量上限,黄芩苷含量范围为0.17%~439.61%、绿原酸含量范围为0.02%~439.61%、连翘苷含量范围为0.46%~341.87%,双黄连口服液主要成分的含量存在较大的差异,黄芩苷尤为突出,临床实际给药量会影响临床疗效。这一结果提示临床,主要成分含量差异可能会造成各产品临床疗效存在显著性差异,应选用质量稳定、信誉度高的厂家生产的药品。因此,建议药典质量标准规定含量上限,以此进一步完善和提高质量标准,同时加强质量标准的研究和控制。

