构建“四重表征”思维模型,发展学生学科核心素养
庄业明 赵伟华

通过构建思维模型认识事物是一种重要的科学思维方法和认知手段,《普通高中化学课程标准(2017年版)》(以下简称2017版课标)凝练了“证据推理与模型认知”等五个方面的化学学科核心素养体系,要求教师积极开展“素养为本”的课堂教学实践,主动探索“素养为本”的有效课堂教学模式和策略。本文以人教版高中化学必修1“离子反应”教学为例,谈谈如何通过构建“四重表征”思维模型发展学生的化学学科核心素养。
学生在学习人教版必修1“离子反应”的有关内容时,对离子反应的实质不能做出准确、完整的陈述,主要表现为化学基本概念模糊、化学实验过程描述不完整、化学用语使用错误、化学原理理解偏差等。比如,学生比较容易判断NaCl在水中电离出Na+和Cl-,AgNO3在水中电离出Ag+和NO3-,也可以准确预测出以上反应会生成白色沉淀,但对于Ag+和Cl-结合生成AgCl沉淀的微观过程表述不清,无法解释反应的实质,以至于很难进行有效的知识迁移。若不对学生的能力进行有效的评价与诊断,给出有针对性的指导,学生在以后学习人教版选修4“水溶液中的离子平衡”这一内容时,就有可能会因为以上知识缺漏,在解答“离子平衡”的综合问题时出现认知困难。
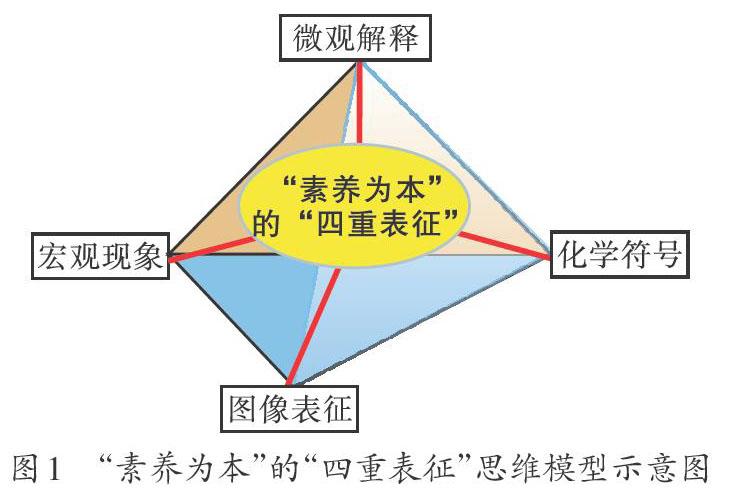
学生之所以出现上述陈述性表征问题,是因为他们还没有建立完善的微粒观,对相关基本概念理解不深,实验学习只注重实验结果、不注重实验过程,不能将相关知识储备转化为有利于解决问题的工具。本文拟利用化学学习的四个层面表征——宏观现象、微观解释、化学符号、图像表征,通过“四重表征”融合(如图1),启发学生学习构建思维模型,促进其学科思维的形成与发展,从中发展解决相关问题的化学学科核心素养。
一、用开放性问题导入,触发学生的深层思考
课堂教学中,教师要善于指导学生运用现有知识和学习经验解决新问题,可以把学生提出的实验方案作为课堂的素材或主线,为“四重表征”思维模型的构建做铺垫。教师可设置开放性问题,发散学生思维,诊断、评价、解决学生学习化学基本概念、化学原理、化学实验等知识时遇到的问题,引导其进入深度学习。
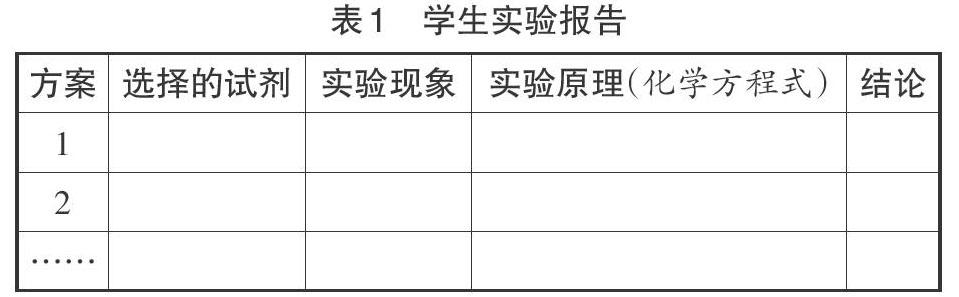
【实验设计】请鉴别用同样试剂瓶盛装的NaOH溶液和稀硫酸,完成实验报告(如表1)。供选试剂:KCl溶液、CuSO4溶液、Na2CO3溶液、Ba(OH)2溶液、石蕊溶液、酚酞溶液。
学生活动:分组讨论→提出不同的实验方案→动手实验验证→观察实验现象→得出结论。
学生可能提出的实验方案(如表2):
二、多角度分析,构建“四重表征”思维模型
首先,学生实际操作自己设计的实验并观察实验现象;其次,分析溶液混合前后微粒的变化,掌握离子反应的判断和离子方程式的书写等内容;最后,借助图像表征更直观地认识并掌握离子反应的实质。通过构建“四重表征”思维模型,培养学生构建微观抽象理论模型的能力。
教师引导,分析建模:以学生提出的实验方案4(选择的试剂:CuSO4溶液)为例,分析离子反应的实质,研究溶液混合前后试管中微粒的变化情况(如图2)。
教师启发设问:①溶液混合后出现的实验现象是什么?②反应的实质是什么?③如何用化学语言表达?
学生讨论,得出如下结论。①宏观现象:产生蓝色沉淀;②微观解释:Cu2+和OH-之间按照个数比1∶2相互结合生成Cu(OH)2沉淀,Na+、SO42-未参与反应,像这种在离子之间进行的反应称为离子反应;③化学符号:可以用Cu2++2OH-=Cu(OH)2↓表示CuSO4和NaOH发生反应的实质,像这种用实际参加反应的离子的符号来表示反应的式子叫作离子方程式。
师生讨论,共同建模:运用规范的化学用语,对反应进行微观解释(如图3)。
教师设疑:该离子反应会引起溶液中离子总浓度发生怎样的变化?请设计实验加以证明。
师生共研,得出如下实验方案:通过导电性实验,将离子浓度变化可视化,观察灯泡亮度、电导率曲线变化趋势,判断离子浓度大小。
演示实验:用装有0.5mol/L CuSO4溶液的烧杯连接带有灯泡的导电装置,同时并联电导率传感器(连接电脑),将0.5mol/L NaOH溶液缓慢加入CuSO4溶液中,直至过量。
学生活动:做实验之前,先由学生预测实验现象,并尝试用笔绘制混合液导电能力的图像(如图4)。(提示:溶液中离子浓度越大,导电能力越强,电导率越大)
学生汇报预测结果:灯泡由亮变暗,后又逐渐变亮;电导率变化曲线呈现先逐渐降低后又逐渐升高的趋势。灯泡由亮变暗、曲线逐渐降低,原因是NaOH与CuSO4发生反应使溶液中离子总浓度减少;灯泡又逐渐变亮、曲線逐渐升高,原因是NaOH溶液过量,发生电离,使混合液中的离子总浓度增大。
实验演示,完善模型:展示学生预测结果,并进行实验演示,观察电导率变化曲线(如图5)。“四重表征”逐层进阶,加深学生对离子反应实质的理解和掌握,进行知识内化和迁移。
“四重表征”思维导图:在构建“四重表征”思维模型(如图6)的过程中,教会学生构建和运用思维模型的方法,归纳形成同类型知识的思维导图,以达到培养学生化学学科核心素养和科学探究能力的目的。
三、学以致用,强化模型,解决问题
通过构建思维模型,深化课堂主题,深入挖掘离子反应的实质,学生的离子观得以建立。接下来,教师应将本节重点知识升华,提高学生应用理论知识解决实际问题的能力,培养学生掌握“观察思考→信息加工→总结归纳→提炼方法”的科学探究方法。
【模型巩固训练】请利用本节所学离子反应原理、离子方程式等知识,运用“四重表征”法解题。
【例题】(2016年北京卷)在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图7所示。下列分析不正确的是( )。
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH-
C.a、d两点对应的溶液均显中性
D.c点,两溶液中含有相同物质的量的OH-
模型分析(如图8):通过两组实验的反应原理(微观解释),写出反应的离子方程式(化学用语),找到两组实验所对应的图像中的曲线(图像表征),进而判断选项正误。
选项解析:通过模型透析可知,曲线①代表滴加H2SO4溶液的变化曲线,A选项正确;曲线②中,从反应开始到b点,未参加反应的离子有Na+、OH-,B选项正确;H2SO4溶液在a点已消耗完原溶液中的OH-,NaHSO4溶液到d点才能消耗完全部的OH-,D选项不正确。因此,本题选D。
离子反应是高中化学最重要的基本理论之一,它与工业生产、社会生活以及生命活动都密切相关,我们面临的诸如环境污染等社会问题,均可以用离子反应知识来解决。本教学设计意在引导学生在实验探究中完成“四重表征”思维模型的构建,既能帮助学生深刻理解离子反应的实质,又能帮助学生解决高考中很多类似的问题,同时还能培养学生用模型认知思想解决身边化学问题的能力。(题图左为庄业明,右为赵伟华)
注:本文为2017年度广西教育科学“十三五”规划A类重点课题“基于学科核心素养培养的高中化学教学单元设计的研究”(课题编号2017A003)的阶段研究成果。
(责编 龙 飞)

