含Sm3+、Y3+聚合物的制备及转光性能
肖尊宏,谭冠华
(贵州师范大学 化学与材料科学学院,贵州 贵阳 550025)
0 引言
随着煤、石油、天然气不可再生能源面临着日益枯竭,寻找新的能源已成为一个国家长远发展的当务之急。太阳能是一种取之不尽的廉价环保能源,太阳能的充分利用是解决当前人类面临的能源短缺和环境污染等问题的根本途径[1]。太阳能是植物光合作用的能量来源,植物通过光合作用合成的生物质能源,通过转换成乙醇等为人类提供了新的能源[2]。但植物光合作用吸收日光具有选择性,其中主要吸收日光的蓝紫光(400~480 nm)和红橙光(600~680 nm)[3]。光生态学研究表明[4]:蓝紫光和红橙光能够促进植物的光合作用,并且蓝光能促进植物的营养器官如茎、叶的生长,红光有利于植物的花朵、果实等方面的生长;黄绿光(510~580 nm)大多被反射而不吸收,紫外光(290~400 nm)能促进枝干老化和病菌繁殖,对植物的生长有不良影响,把日光中的紫外光、黄绿光和近红外光的一种或几种转换为作物所需要的红光或蓝光,有利于太阳能的充分利用,提高作物产量和反季节生产,因此转光技术研究不断取得新的进展[5-8]。转光技术的关键在于转光剂。
目前,转光剂可分为稀土无机、稀土有机配合物和有机荧光染料转光剂[6,9]。稀土无机转光剂和稀土有机配合物小分子转光剂与高分子基质容易发生相分离,造成薄膜力学性能变差,光转换性能下降[10],而Eu(III)的稀土配合物红光转光剂,其最大发射波长在612 nm左右,而叶绿素a和叶绿素b对红光的最大吸收分别在660 nm和643 nm处,显然,Eu(III)配合物的发射光谱与叶绿素的吸收光谱并不一致,转光效率不高[11],Sm(III)配合物最大荧光发射峰位于645 nm左右,与叶绿素的最大吸收吻合。Sm(III)配合物作为转光离子,Y(III)作为敏化离子,合成聚合物转光剂,这方面的研究报道较少。本文首先合成Sm、Y离子配合物,然后与丙烯酸甲酯共聚,制备了Sm(Y)(aa)(acac)2phen与丙烯酸甲酯共聚物[12],合成路线如下:
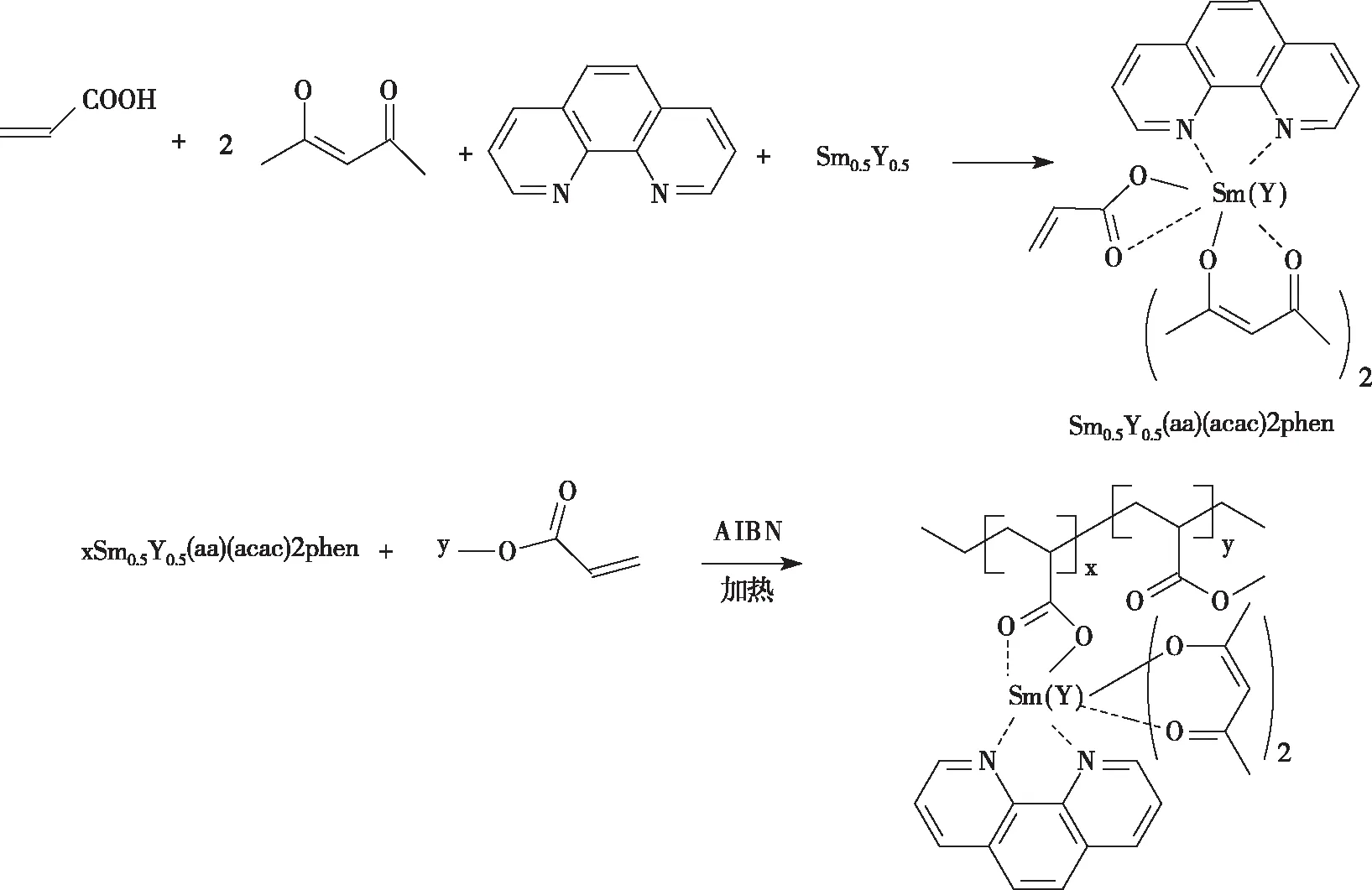
图1 Sm(Y)(aa)(acac)2phen与丙烯酸甲酯共聚物的合成路线Fig.1 Synthetic route of Sm(Y)(aa)(acac)2phen-co-MA polymer
1 实验部分
1.1 试剂与仪器
Sm2O3、Y2O3纯度99.99%,国药集团化学试剂有限公司;丙烯酸(aa):CP试剂,天津市科密欧化学试剂开发中心;乙酰丙酮(acac):AR试剂,天津市大茂化学试剂厂;1,10-邻菲啰啉(phen):AR试剂,天津市科密欧化学试剂开发中心;丙烯酸甲酯:AR试剂,天津市科密欧化学试剂开发中心;偶氮二异丁腈(AIBN), 国药集团化学试剂有限公司,二甲基亚砜(DMSO)为AR试剂,并经脱水后重蒸使用。
红外光谱采用美国PE Spectrum One型傅里叶红外光谱仪测定,KBr压片法或薄膜法;紫外光谱采用Shimadzu UV-265型紫外与可见分光光度计测定,以二甲基亚砜作溶剂;元素分析用美国PE 2400型元素分析仪测试;荧光光谱采用日本日立公司产F 4600荧光光谱仪测试,选择参数为:光电倍增管电压为700V,扫描狭缝宽度激发(Ex)和发射(Em)都是5 nm,扫描速度为1 200 nm/min。试样的测试方法为粉末压片,或以DMF作溶剂,溶液测定;热重分析采用德国NETZSCH公司产STA 409 PC型热分析仪测定,气氛为N2,升温速度为10 ℃/min。扫描电镜采用JSM-6490LV和INCA-350 X射线能谱仪观察;熔点由Olympus BH-2 型偏光显微镜观察;分子量以及分子量分布用Waters2414凝胶渗透色谱仪测量,分离柱为Waters styragel column,流动相THF的流速为1.0 mL/min,用单分散的聚苯乙烯作标定,Breeze为数据处理软件。
1.2 Sm(acac)2(aa)phen和Sm0.5Y0.5(acac)2(aa)phen的合成[13]
准确称取0.352 0 g Sm2O3(1.0 mmol)溶于5 mL浓盐酸中,加热蒸发除去多余的盐酸,配成3 mL SmCl3水溶液;将2 mmol aa溶于20 mL乙醇中,磁力搅拌溶解,加入上述已配好的SmCl3水溶液,用4 mol/L的NaOH溶液调节其pH值到7.0,然后水浴恒温60 ℃反应1.5 h;然后加入4 mmol乙酰丙酮(acac)溶于5 mL乙醇的溶液,再加入溶有2 mmol邻菲罗啉(phen)的乙醇溶液10 mL,继续反应2 h,去除大部分水及乙醇,沉淀物经减压抽滤后,用水和乙醇各洗涤3次,在40 ℃下真空干燥,得到Sm(acac)2(aa)白色固体粉末,产率82.0%,无熔点。以同样的方法合成Sm0.5Y0.5(acac)2(aa),产率为82.5%,无熔点。
1.3 Sm(Y)(aa)(acac)2phen、Sm0.5Y0.5(acac)2(aa)与丙烯酸甲酯共聚物的合成[12]
在氮气气氛保护下,往聚合管中加入Sm(acac)2(aa)(phen)单体、丙烯酸甲酯、AIBN和溶剂二甲基亚砜(DMSO),摇匀,反应过程中氮气保护。将聚合管放入50 ℃的恒温水浴中聚合48 h时间,然后升温到110 ℃反应3 h,取出聚合物固体,减压抽干溶剂,将固体放在45 ℃真空烘箱中干燥24 h,得Sm(Y)(aa)(acac)2phen与丙烯酸甲酯淡黄色共聚物(P1),以同样的方法合成了Sm0.5Y0.5(acac)2(aa)phen与丙烯酸甲酯共聚物(P2)。
2 结果与讨论
2.1 聚合物的红外光谱分析[14]
单体Sm0.5Y0.5(acac)2(aa) phen和聚合物P2的红外吸收光谱图如图2,图2中的左图是单体Sm0.5Y0.5(acac)2(aa)的红外光谱,红外谱图新出现1 517.4 cm-1、1 432.5 cm-1、1 143.4 cm-1和1 103.1 cm-1、850.3 cm-1和732.2 cm-1等吸收峰,均是对应于phen的ν(C=N)、ν(phen)(骨架)、β(CH)、γ(CH)特征峰,这些谱峰与自由配体phen相比,ν(C=N)红移65.6 cm-1,γ(CH)两个吸收峰分别红移3.4 cm-1和6.4 cm-1,而ν(phen)(骨架)则蓝移11.3 cm-1,β(CH)两个吸收峰分别蓝移4.7 cm-1和11.6 cm-1,表明了phen的两个氮原子参与配位。图2中的右图是P2的红外光谱,主要反映的是丙烯酸甲酯结构的特征吸收峰,1 733.6 cm-1处的吸收峰是由ν(C=O)的伸缩振动产生的,在1 196.8 cm-1左右出现强而宽的吸收峰,这是由C-O-C的伸缩振动产生的,在1 059.4 cm-1处存在一个弱的对应于C-C伸缩振动与C-H变形振动吸收峰。同时,从谱图中还观察到关于phen环的γ(CH)特征峰(828 cm-1和758.4 cm-1处),以及在421.6 cm-1处出现较弱的Sm-O伸缩振动吸收峰,均表明稀土配合物单体参与聚合。

图2 单体Sm0.5Y0.5(acac)2(aa)(左)和聚合物P2(右)的红外光谱图Fig.2 IR of Sm0.5Y0.5(acac)2(aa) phen (L) and P2(R)
2.2 聚合物的紫外光谱分析[14]
聚合物(P2)和单体Sm0.5Y0.5(acac)2(aa)的紫外吸收光谱如图3所示,由图3可知,与单体相比,聚合物的紫外吸收主峰发生红移且吸收强度增强,其在256 nm附近的吸收峰是对应于丙烯酸甲酯链段中C=O的n→π*跃迁吸收,而中心在286 nm附近的吸收峰,与单体Sm(acac)2(aa)(phen)的吸收峰相近,可认为主要是单体中配体的紫外吸收峰。可见,只要引入少量的稀土配合物单体,共聚物就表现出配合物配体的强紫外吸收特性,表明稀土配合物参与共聚合。
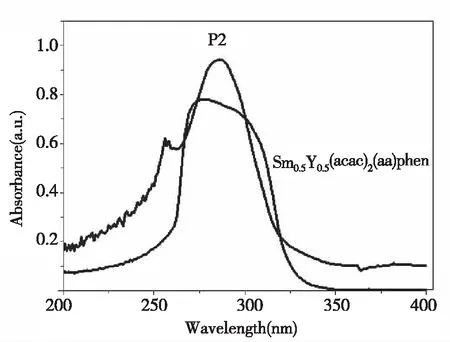
图3 聚合物P2和Sm0.5Y0.5(acac)2(aa)的紫外光谱Fig.3 UV of Sm0.5Y0.5(acac)2(aa) and P2
2.3 聚合物P2的分子量分布
由GPC谱图4看出,共聚物P2的GPC只出现单峰,由此可推断聚合物里只有一种结构的分子链,结合前面的分析,我们认为共聚体系中只发生共聚合反应而不发生自聚反应。共聚物的平均分子量(MW)为4.1万,分子量分布为2.1~2.5,分布较窄,分子量较大对材料能形成高质量的薄膜有利。
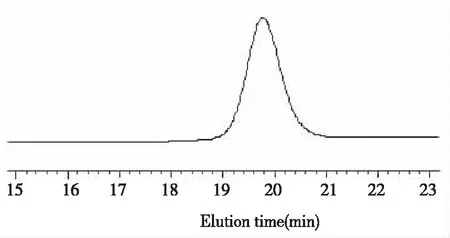
图4 P2的GPC谱图Fig.4 GPC curve of P2
2.4 P2与聚乙烯相容性分析
P2与聚乙烯固体颗粒按1∶50质量比混合均匀,加热压成薄膜,扫描电镜采用JSM-6490LV观察SEM,如图5。从图5上看出,P2与聚乙烯固体相容性较好,没有相分离,P2在聚乙烯薄膜中分散比较均匀。

图5 P2与聚乙烯固体共混成膜的扫描电镜(SEM)Fig.5 SEM of P2 and PE blend film
2.5 热稳定性分析
图6为Sm0.5Y0.5(acac)2(aa) phen的TG曲线。由图6可知,配合物起始分解温度在256 ℃,而配体aa、acac、phen的熔点均小于256 ℃,说明配合物中无自由配体存在;一般配体水或结晶水的分解温度也低于256 ℃,这表明配合物中不含水[15]。温度升到280~420 ℃之间,配合物剧烈分解,失重显著,达43.37%,630 ℃以后重量趋于恒定。在250~630 ℃之间,大部分配合物失重曲线都有比较明显的折点,表明稀土多元配合物是分步分解的。此外,稀土配合物在其分解前都观察不到熔融效应的吸热峰,说明稀土配合物没有熔点。配合物的分解温度达到250 ℃以上,适合做转光剂。

图6 Sm0.5Y0.5(acac)2(aa)phen的热失重曲线(TG)Fig.6 TG of Sm0.5Y0.5(acac)2(aa)phen
2.6 荧光光谱分析
在发射波长645 nm下测定出其最佳激发波长,聚合物P1的激发波长为330 nm,P2的激发波长是350 nm。图7是聚合物P1和P2的激发光谱(Ex)和发射光谱(Em)图。可看到对应于4G5/2→6H5/2、4G5/2→6H7/2和4G5/2→6H9/2跃迁的565 nm、600 nm和645 nm 3种波长的荧光,其中4G5/2→6H9/2跃迁发出的645 nm红光较强。P2的激发波长比P1红移20 nm且在645 nm的荧光也比P1强,说明Y3+离子对Sm3+发光有敏化作用,敏化机理[15]如图8所示,由于Y3+离子的f0轨道上没有电子,不存在能发生辐射的电子跃迁,Y3+离子不发光,Y3+配合物把吸收的光能转移给了Sm3+离子,有助于Sm3+离子发光,所以P2的荧光强度比P1大。钐氧化物比钇氧化物价格贵,用Y3+离子取代了部分Sm3+离子,节约了成本,有利于稀土转光农膜的推广应用。
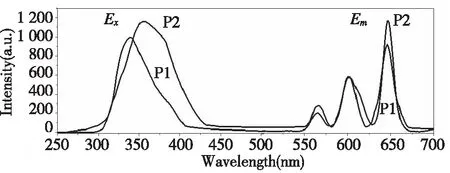
图7 P1和P2的激发(Ex)和发射光谱(Em)Fig.7 Excitation and emission spectra of P1 and P2
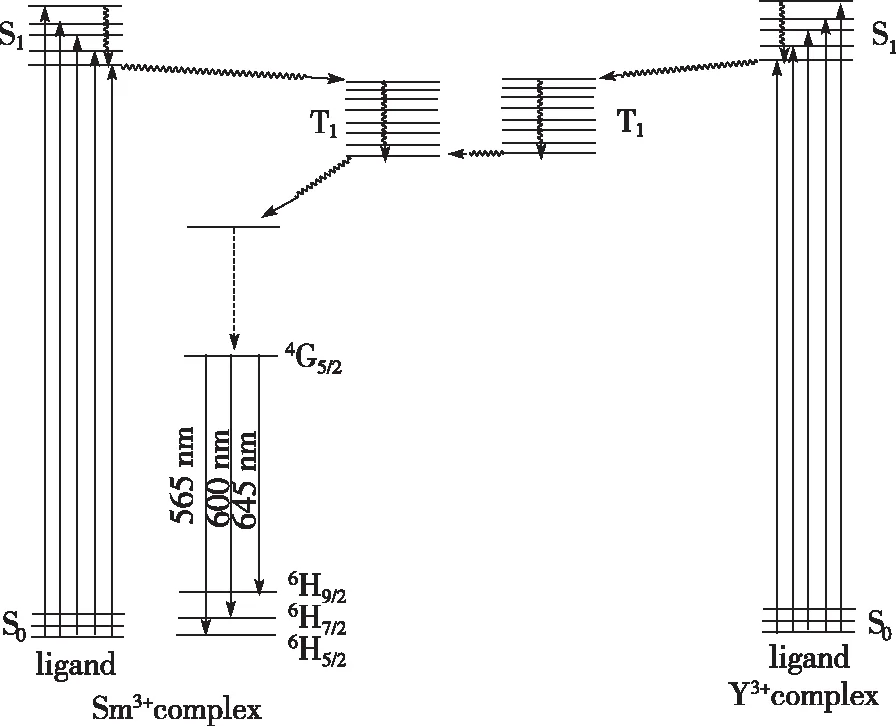
图8 Y3+敏化Sm配合物的能量转移图Fig.8 Energy transfer in Y3+ sensitizing Sm complex process
3 结论
用丙烯酸、乙酰丙酮做第一配体,邻菲罗啉做第二配体,合成了多元可聚合的单体Sm(Y)(aa)(acac)2phen和Sm0.5Y0.5(acac)2(aa),然后分别以这两种单体分别与丙烯酸甲酯共聚,得到聚合物P1和P2。配合物热失重分析(TG)分解温度250 ℃以上,表明配合物较为稳定,在350 nm紫外光激发下,发出645 nm的红光,与作物光合作用所需要的643 nm红光非常吻合,满足了光合作用所需光质的“天线效应”;用Y3+离子取代了部分Sm3+离子,增强了Sm3+离子荧光强度,节约了成本,有利于稀土转光农膜的推广应用,P2与聚乙烯固体相容性较好,没有相分离,P2在聚乙烯薄膜中分散比较均匀,因此,Sm0.5Y0.5(acac)2(aa)与丙烯酸甲酯或甲基丙酸甲酯共聚物,有望成为一种潜在的农膜转光剂。

