电化学氟化提高TiO2 薄膜光电催化性能
李 想, 张 林, 杨 波, 吴雅琴
(1. 浙江大学 化学工程与生物工程学院, 浙江 杭州 310027;2. 杭州水处理技术研究开发中心有限公司, 浙江 杭州 310012)
1 引 言
砷普遍存在于自然界的岩石和土壤中,也广泛用于农业杀虫和森林防护,最终进入水体造成污染。饮用水中含有砷增加膀胱、肝、肾、皮肤癌的发病率[1]。砷污染主要有As(III)和As(V)两种价态,As(III)因流动性好,难以富集而危害性较大,因此As(III)氧化成As(V)尤为重要,对 As(III)常见的氧化方法有O2/O3,H2O2,MnO2,UV/Fe(II),TiO2/UV 等[2-5]。这些方法中,TiO2光催化以价格低廉,性能优异,无污染而受到广泛关注,液态体系中,TiO2能有效催化 As(III)生成 As(V),其争论在于催化机理不明确,主要为羟基自由基、空穴、超氧自由基3 种机理[5]。
而TiO2光催化研究中,主要以粉末形态催化剂使用较为普遍,但催化剂回收仍然是个问题[6-7]。TiO2光催化最主要不足在于禁带宽度为3.0~3.2 eV,吸收波长小于387 nm 的紫外光,且光生载流子复合快,催化效率低[1,3,8-11]。对 TiO2掺杂是拓展光吸收范围,抑制载流子复合,提高光催化性能的重要手段,掺杂能在一定程度上提高催化效率,拓展吸收光谱范围,但是掺杂影响TiO2的晶型,改变能带结构,对催化剂的稳定性造成影响(如 N[3,12]、C[13]、F[13-20]等)。特别是对于氟化 TiO2的研究,主要是采用表面吸附的方法,尽管能提高催化效率,但是氟离子在TiO2表面易脱附流失[21-23]。也有报道,在水热体系中加入HF,制备表面氟化TiO2,但是此方法制备的催化剂,不经过高温焙烧影响催化剂的活性[24-25]。本文采用电化学表面氟化方法,不改变催化剂本体结构,提高TiO2光电催化性能,以As(III)作为目标污染物评价催化剂性能,并催化弱吸附的目标污染物苯酚进行比较。研究TiO2薄膜光电催化,以期克服粉末态光催化催化剂回收的问题。
2 实验部分
2.1 实验材料和仪器
试剂:工业钛板(纯度 > 99.7%);丙酮、乙醇、甲醇、浓硝酸(65%~68%)、浓硫酸(98%)、双氧水(30%)、氢氟酸( > 40%)、氨水、钼酸铵、孔雀绿、聚乙烯醇(PVA)、氯化铵、铁氰化钾、四氨基安替吡啉、硫酸钠、高氯酸纳、氟化纳、苯酚、亚砷酸纳(As(III)来源)均为分析纯。
主要溶液:混酸(HF:HNO3= 1:3)用于工业钛板刻蚀;0.5 mol·L-1Na2SO4+ 5% CH3OH;0.5 mol·L-1H2SO4+ 0.5% NaF;As(V)系列标准液,苯酚系列标准液;50 和100 µmol·L-1的As(III)和苯酚溶液,电解质为 0.1 mol·L-1NaClO4,用 NaOH 或 HClO4调节 pH 约为 3.0 值。
主要仪器设备:石英窗口的三电极体系,饱和甘汞电极(SCE),箔片;大面积石英窗口的降解池;CHI660A;500W Xe 灯,752 紫外光栅分光光度计。
2.2 薄膜电极的制备
工业钛板经砂纸打磨后,混酸处理,依次经过丙酮和去离子水超声波清洗15 min,自然干燥后,外加40 V 电压,在1 mol·L-1H2SO4溶液中阳极氧化30 min,去离子水洗净后自然干燥,在马弗炉中500 ℃焙烧1 h,自然降温,制备成TiO2薄膜电极(文中标明为TiO2)。
TiO2在含NaF 的酸性溶液中进行电化学氟化制备成氟化二氧化钛电极,即为F-TiO2,并优化时间、电位、NaF 含量等因素的影响。F-TiO2薄膜在马弗炉中400 ℃ 焙烧1 h,得到去氟化TiO2(文中标明为De F-TiO2)。用于光电性能测试的薄膜电极用硫化硅胶封出面积为0.36 cm2,用于降解实验的薄膜电极面积为39 cm2。
2.3 光电化学测试
光电化学测试使用带有石英玻璃窗口的三电极体系,TiO2薄膜电极、铂片、饱和甘汞电极(SCE)分别为工作电极、对电极和参比电极。500 W Xe 灯模拟光源,正面照射工作电极。除特别说明外,光电测试外加偏压为 +0.8 V,电解质为0.1 mol·L-1NaClO4水溶液,pH 约为3.0。
采用双槽降解或氧化,量筒量取50 mL 苯酚或As(III)溶液于阳极槽中,阴极为电解质,盐桥连接,暗态吸附平衡20 min,外加偏压0.8 V,500 W Xe 灯为激发光源,三电极体系(TiO2电极,箔片,饱和甘汞电极分别为工作电极,对电极,参比电极),每隔0.5 h 或10 min 取样,用752 紫外光栅分光光度计分析,苯酚采用4-氨基安替吡啉分光光度发分析,在510 nm 处测吸光度A[26]。As(V)采用钼酸铵分光光度法分析,在630 nm 处测其吸光度A[27]。苯酚和As(V)的标准曲线如图1。

图1 标准曲线Fig.1 Standard curves of related measurements
3 结果与讨论
3.1 氟化条件优化
考察氟化电压、时间、氟化钠含量对TiO2电极光电性能的影响如图2 所示,电化学氟化在0.5 mol·L-1H2SO4中进行。为了提高光电流的响应强度,光电流测试在含有5% 甲醇的0.5 mol·L-1Na2SO4水溶液 (pH= 3.0) 中进行。图2(a)~(c)可以看出,稳态光电流均出现先增加后降低的趋势,在电压10 V,刻蚀时间5 min,NaF 含量0.5% 时,稳态光电流达到最大。过高的刻蚀电压,延长刻蚀时间,及增加NaF 的含量,导致TiO2薄膜过度刻蚀,以至于薄膜完全刻蚀消耗完,使得光电流出现先增加后降低的现象,因此,最优氟化条件为10 V,5 min,0.5% NaF。除特殊说明外,用于性能评价测试的氟化电极均为最优条件下制备而成的电极。

图2 电位,NaF 含量,时间对光电流的影响Fig.2 Effects of potential, NaF% and time on photocurrent
3.2 光电性能测试
暂态扫描测试及稳态测试如图3 所示,图3(a) LSV 曲线可以看出,光激发条件下,与TiO2相比,F-TiO2电极显著提高光电流响应,尤其在 -0.4~0 V 提高更为明显。尽管因电化学氟化后改变了其表面态,有充电电流及电容的影响,但可以看出,F-TiO2提高起始氧化电位,这是由于提高载流子的分离效率,抑制复合所致[26]。在暗态条件下,TiO2的电流与基线电流类似,F-TiO2电极出现阳极电流,表明氟化后,TiO2电极导电性增加,同时也表明氟化改变其表面态。为了避免充电电流的影响,稳态测试如图3(b),在0.8 V,N2条件下,F-TiO2光电流提高了约2.61 倍,进一步表明氟化提高TiO2光电性能。

图3 TiO2 和F-TiO2 电极的电流特性Fig.3 Current curves on TiO2 and F-TiO2 electrodes
3.3 光电催化性能

图4 光电催化氧化苯酚Fig.4 Photodegradation of phenol
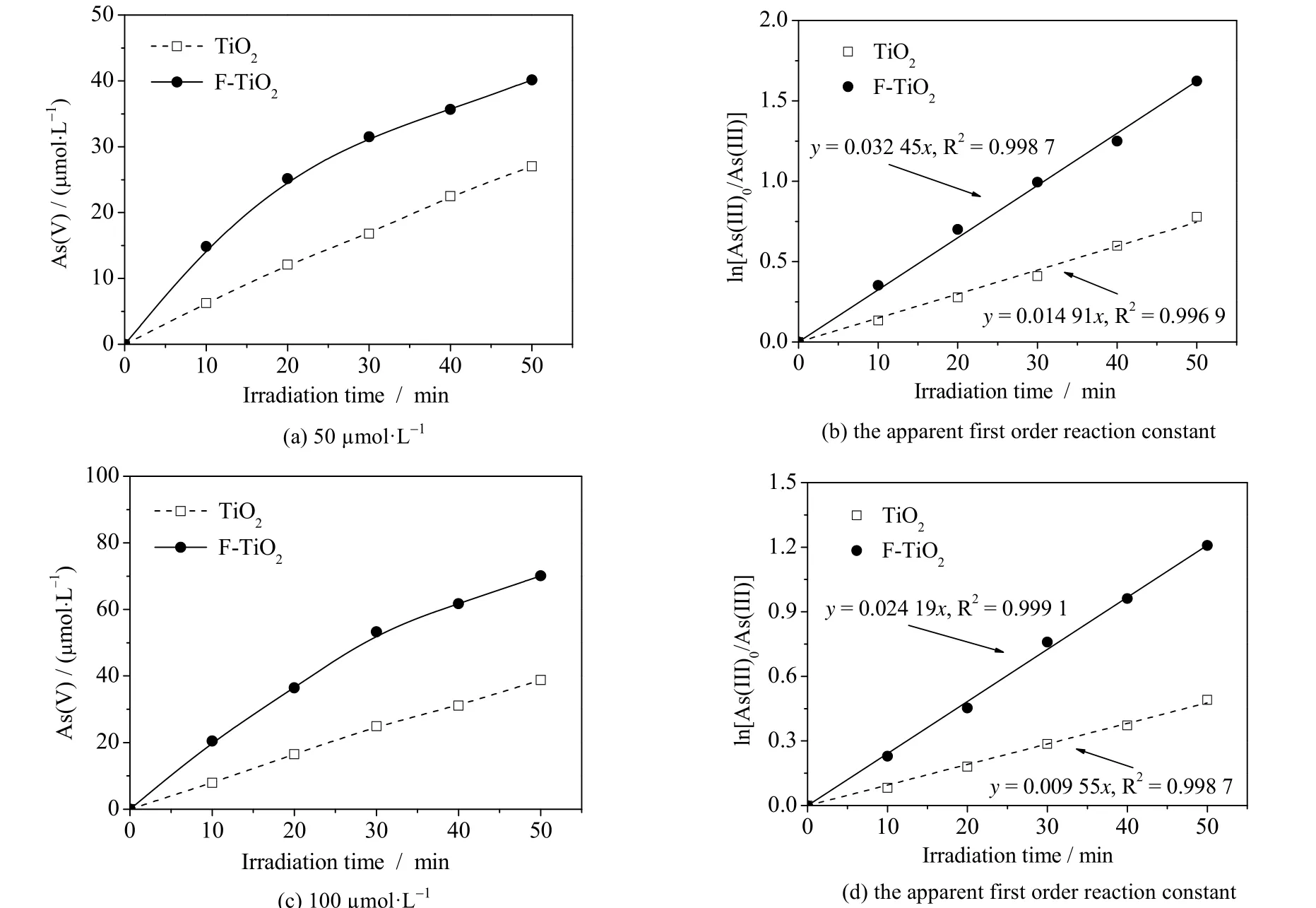
图5 光电催化氧化 As (III)Fig.5 Photoelectrocatalytic oxidation of As(III)
为了测试氟化TiO2薄膜电极的光电催化性能,选取弱吸附的苯酚和吸附较强的As(III)作为目标污染因子研究。图4 是0.8 V,空气氛围中苯酚降解图。图4(a)苯酚起始浓度为50 μmol·L-1,经过2.5 h 光电催化后,苯酚在TiO2上去除率为60.56%,在F-TiO2上去除率87.32%。图4(c)苯酚起始浓度为100 μmol·L-1,经过2.5 h光电催化后,苯酚在TiO2上去除率为44.37%,在F-TiO2上去除率64.79%。相应地,图4(b),4(d)为表观一级动力学反应变化图。图4(b)中,TiO2的表观速率常数为0.385 4 h-1,F-TiO2的表观速率常数为0.779 9 h-1,光电氧化苯酚的速率提高了2.02 倍。图4(d)中,TiO2的表观速率常数为0.243 4 h-1,F-TiO2的表观速率常数为0.412 4 h-1,光电氧化苯酚的速率提高了1.69 倍。从图4 可以看出,苯酚的起始浓度不是限制光电催化氧化速率的因素,还可以看出,F-TiO2更有利于低浓度的苯酚催化降解。图5 为光电催化氧化As(III)生成As(V)曲线,在0.8 V,空气氛围中。图5(a) As(III)起始浓度为 50 μmol·L-1,经过 50 min 光电催化后,TiO2光电催化As(V)的生成率为54.09%,F-TiO2光电催化As(V)的生成率为 80.28%。图 5(c) As(III)起始浓度为 100 μmol·L-1,经过50 min 光电催化后,TiO2光电催化As(V)的生成率为38.82%,F-TiO2光电催化As(V)的生成率为 70.13%。相应地,图5(b)、(d)为表观一级动力学反应变化图。图5(b)中,TiO2的表观速率常数为0.014 91 min-1,F-TiO2的表观速率常数为0.032 45 min-1,光电催化As(V)转化率提高了 2.18 倍。图 5(d)中,TiO2的表观速率常数为0.009 6 min-1,F-TiO2的表观速率常数为0.024 2 min-1,光电催化As(V)的转化率提高了2.53 倍。图5 可以看出As(III)的起始浓度不是限制催化速率提高的因素。由于As(III),As(V)均吸附,尤其As(V)有较强的吸附能力[2,28]。从图6 可以看出,As(V)在F-TiO2表面的平均饱和吸附量大于TiO2。当As(V)达到吸附平衡时,覆盖了催化活性点,抑制了As(III)的催化氧化,因而没有达到100% 转化率。图4,5 还可以看出,相同的条件下,随着浓度的增加,不论是F-TiO2,还是TiO2,光电催化氧化污染物去除率降低,因为在一定的光强激发下,光生载流子的生成量恒定,捕获污染因子的效率也近乎常量,因而,随着初始浓度的升高,光电催化氧化的去除率降低。

图6 As(V)平均饱和吸附量Fig.6 Average saturated adsorption capacity of As(V)
3.4 紫外可见吸收光谱
电化学氟化TiO2显著提高了光电催化性能,为探讨是否因为氟化刻蚀后,光吸收增强引起的性能提高,测定UV-Vis 漫反射吸收光谱如图7,可以清晰地看出,电化学刻蚀后,吸光度降低,表明光电催化性能的提高不是由吸光增大引起的。氟化刻蚀后,降低催化剂的量,因而吸光度降低。氟化后电极表面积增加,从图6 饱和吸附量的变化上,也能间接看出,表面积增加,吸附量增大。氟化前后,TiO2的光谱形状未发生变化,表明电化学氟化不改变TiO2的晶型结构,吸收阈值在385 nm 附近,相应地禁带宽度为3.2 eV,电化学阳极氧化制备的TiO2,经500 ℃ 热处理后,主要为锐钛矿型[29]。
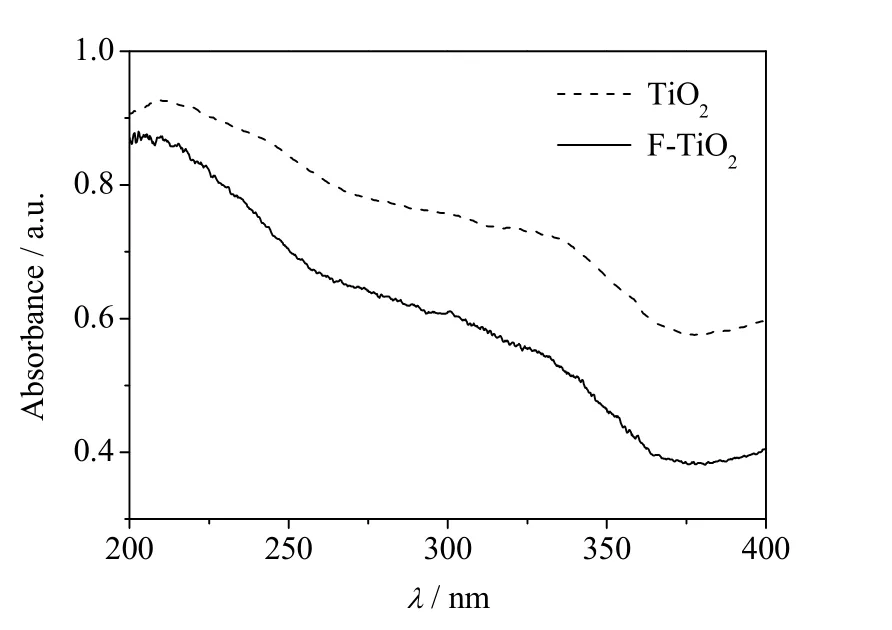
图7 紫外可见漫反射吸收光谱Fig.7 UV-vis diffuse reflectance absorption spectra of TiO2 and F-TiO2
3.5 电化学氟化TiO2 表面氟的形态
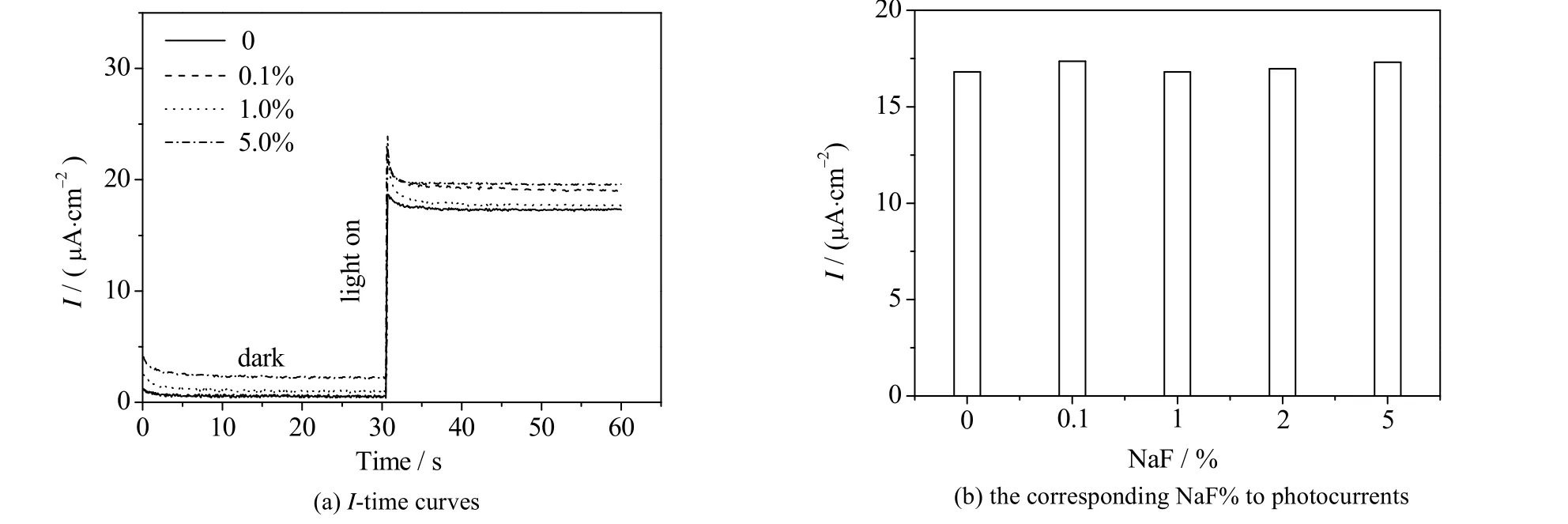
图8 NaF 水溶液对TiO2 电极电流的影响Fig.8 Effects of NaF solution on photocurrent of TiO2 electrodes
为了研究氟离子在电极表面上的形态,也即是氟在TiO2电极表面是游离态还是化学结合态,其关系到氟化电极的稳定性,以及说明电化学氟化提高TiO2光电性能可能的主要原因。验证氟离子是否是吸附在电极表面上或者电化学硫酸氧化所引起的光电性能提高,如图2(d)条件下测试稳态光电流,与TiO2相比,F-TiO2光电流提高了2.89 倍,电化学硫酸氧化提高了1.42 倍,在氟化钠的0.5 mol·L-1硫酸溶液浸泡后测试,电流基本没有变化,表明电化学硫酸氧化能一定程度提高光电流,但不是主要因素,表面吸附氟离子不能提高光电流,表明游离态氟离子不是提高光电催化性能的主要因素。考虑到吸附后测试,表面吸附氟离子浓度太低不能有效提高光电流响应,因而增加电极表面的游离氟离子浓度,做了如图8 实验,在pH 为3.0 的 0.1 mol·L-1NaClO3的水溶液中添加不同含量的NaF 测试光电流,从图8(a)看出,光电流几乎没有提高,相应地,图 8(b)也表明游离氟离子不能提高光电流响应,也就表明电化学氟化后,光电性能的提高不是游离态吸附氟所致。为了进一步评价电化学氟化后,氟在TiO2表面的形态,F-TiO2在400 ℃ 焙烧1 h 后,制备De F-TiO2,测试如图9,LSV 和稳态电流测试可以看出去氟TiO2光电流响应与TiO2几乎一致,表明电化学氟化形成化学键氟可能是TiO2光电催化性质提高的主要因素,同时也可以从图9(a)看出,热处理去氟后,不论是光照条件下,还是暗态条件下,阳极电流现象在 -0.4~0 V 消失,进一步表明表面化学键氟能提高TiO2起始氧化电位,降低载流子复合,提高分离效率。电化学氟化形成化学键氟使得 F-TiO2极其稳定,多次光电催化 As(III)结果表明,性能未见衰减,如图 10所示。电化学结合态氟抑制复合,提高载流子分离效率,可能是电化学氟化提高TiO2光电性能的主要原因。

图9 TiO2 和De F-TiO2 电极的电流特性Fig. 9 Current characteristic curves of TiO2 and F-TiO2 electrodes
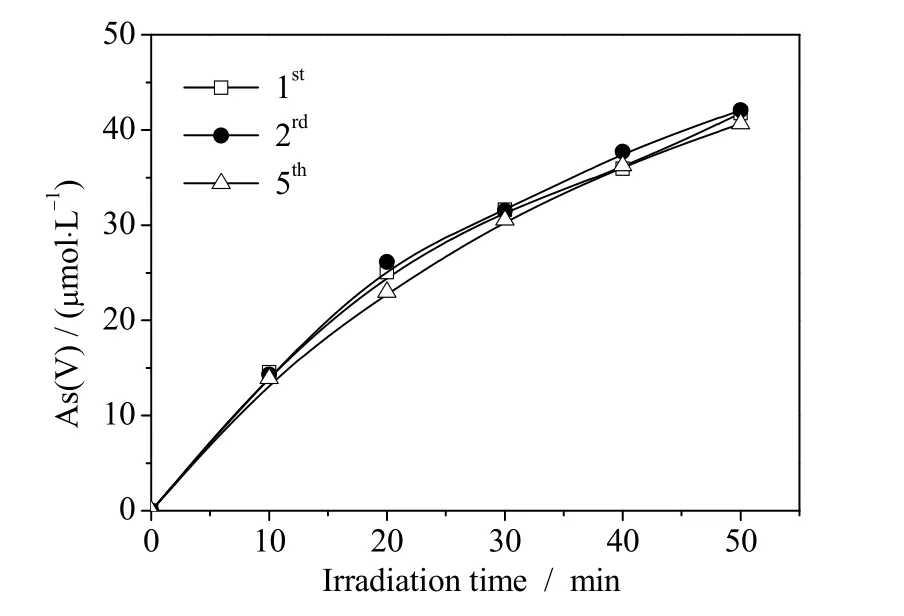
图10 F-TiO2 电极氧化As(III)的稳定性Fig.10 Stability of the F-TiO2 electrode for As(III) oxidation
4 结 论
(1) 电化学氟化TiO2的最优条件为,电位10 V、时间5 min、NaF 含量0.5%。
(2) 在0.8 V,N2条件下,F-TiO2薄膜电极稳态光电流提高了2.61 倍左右。
(3) 在0.8 V,空气条件下,F-TiO2薄膜光电催化氧化50 μmol·L-1As(III)及苯酚的速率分别提高了2.18和2.02 倍,光电催化氧化100 μmol·L-1的As(III)及苯酚的速率分别提高了2.53 和1.69 倍。
(4) 电化学氟化降低TiO2薄膜吸光度,F-TiO2薄膜经过热处理后,光电流提高响应消失,TiO2电极在含氟离子水溶液中测试,不能提高光电流响应,表明表面形成稳定的化学键氟可能是电化学氟化提高TiO2光电催化性能的主要因素。

