经多功能导管化学消融犬左心室前组乳头肌
钱 俊,黄 晶,杨 刚,江永红,朱 悫,刘地川,邓昌明
(重庆医科大学附属第二医院心血管内科,重庆 400010)
左心室乳头肌(papillary muscle, PM)解剖结构复杂,其基底部分布有丰富浦肯野纤维网,在室性心律失常(ventricular arrhythmias, VAS)发生和维持中扮演重要角色[1-2]。经导管射频(radiofrequency, RF)消融是治疗PM起源VAS的有效方式之一,但此类VAS常起源于心肌深部,且消融过程中始终保持电极与PM处于良好贴靠关系并非易事,尤其左心室前组乳头肌(anterior papillary muscle, APM)悬垂于心腔,且基底宽大,相比其他部位心肌(如左心室壁、流出道等)起源VAS,其消融效果差强人意[3-4]。
经导管心肌注射无水乙醇可在靶区域内形成范围可控的消融灶,以减少VAS发生[5-6]。本课题组前期自行研发了一款集心腔内超声(intracardiac echocardiography, ICE)成像和心肌内注射功能于一体的多功能导管,其用于实施室间隔化学消融的可行性已在动物模型中得到验证[7]。本研究尝试利用该导管在ICE图像定位和监控下经心内膜途径向APM基底部注射无水乙醇,评估以之实施APM化学消融的可行性和安全性。
1 材料与方法
1.1 多功能ICE导管系统 系统[8]由以下各部分组成:①32晶阵微型超声探头(频率6.5~10.0 MHz),经同轴电缆连接CTS-5000B型主机(汕头市超声仪器研究所有限公司),装配于导管前端,可提供心腔内二维超声图像;②镍钛合金注射针(29G),自导管尾端进针并从成像探头后方伸出,与成像探头呈30°角,注射针尾端接1.0 ml注射器。
1.2 实验动物 15只健康杂交犬,雌雄不限(体质量15.5~23.5 kg),购于重庆医科大学实验动物中心,随机纳入0.2 ml组、0.4 ml组及0.8 ml组,每组5只。以3%戊巴比妥钠经腹腔注射麻醉动物后保定于手术台上,在无菌条件下暴露左侧颈总动脉,置入9F动脉鞘管,注入肝素(100 IU/kg体质量)抗凝,并经鞘管送入多功能ICE导管直至进入左心室。
1.3 消融过程 利用多功能ICE导管观察心腔内结构,定位到左心室APM后,固定导管及探头朝向,在ICE图像监控下自导管尾端缓慢插入注射针,直至针尖抵达APM基底部。经导管尾端注射器注射少量超声微泡(SonoVue)进一步确定针尖部位,之后对各组缓慢注射相应量无水乙醇。注射完毕后缓退注射针,撤出多功能导管,缝合切口,予青霉素钠(800万IU/天)预防感染。
1.4 安全性评价 消融前及消融5天后通过测定二尖瓣反流面积(mitral regurgitation area, MRA)、射流紧缩口宽度(vena contracta, VC)评估乳头肌功能。消融结束后采用经胸超声(CTS 5000B,汕头市超声仪器研究所)观察有无心腔内附壁血栓、APM断裂及心包压塞等并发症。
1.5 病理学检测 完成上述检查后经静脉注射10%氯化钾20 ml处死动物,取出完整心脏,沿左心室长轴切开,观察有无血栓、赘生物、PM断裂等并发症;随后沿长轴切开APM,观察消融灶大体形态,并计算其体积(公式:4×长度×宽度×深度×π/3)。将组织置于4%多聚甲醛中固定,行HE染色,于光学显微镜下观察消融灶及周边组织病理学改变。
1.6 统计学分析 采用SPSS 15.0统计分析软件。所有数据均以±s表示,使用配对t检验比较各组消融灶体积(cm2)和消融前、消融5天后MRA(cm2)及VC(mm)。P<0.05为差异有统计学意义。
2 结果
左心室APM在ICE长轴切面上呈“卵圆形”(图1A),其尖端可见腱索附着,与左心室壁分界清晰。与周围组织相比,插入心肌组织内的镍钛合金注射针表现为条索状高回声结构(图1B),随心脏搏动而摆动;注射无水乙醇后,肉眼可见局部心肌组织灰度值较前显著增强,呈团块样高回声区域(图1C)。
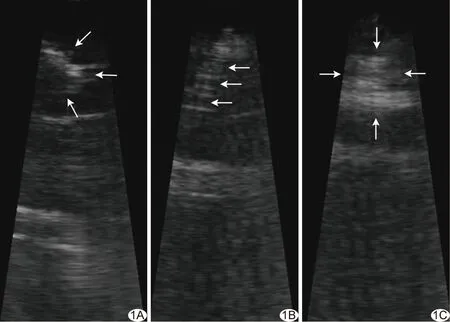
图1 ICE监控下经心内膜面注射无水乙醇消融APM A.左心室APM显示清晰,呈“卵圆形”,头端有腱索附着(箭); B.插入心肌组织中的注射针表现为条索状高回声(箭); C.注射无水乙醇后,局部心肌灰度值较前显著增加,表现为团块状高回声(箭)
2.1 大体观察 取出沿左心室长轴切开心脏发现2只犬心内膜轻微出血,未见附壁血栓、心肌穿孔及PM断裂等并发症。沿长轴切开APM见其基底部存在苍白色、中间夹有暗红区域的消融灶,与周围组织界限分明(图2),0.2 ml、0.4 ml及0.8 ml组 APM基底部消融灶体积分别为(0.37±0.07)cm2、(0.69±0.08)cm2及(0.96±0.19)cm2,较高剂量组消融灶体积大于较低剂量组(P均<0.05)。

图2 0.2 ml组犬左心室APM消融灶大体改变 APM基底部可见苍白色、中间夹有暗红区域的消融灶(箭),未见乳头肌断裂、心内膜血栓及心肌穿孔等 (APM:前组乳头肌;PPM:后组乳头肌) 图3 消融部位心肌病理图 A.消融灶周边组织结构基本完好,横纹清晰,与消融灶界限分明(箭,HE,×40); B.消融中心区域心肌细胞核固缩、碎裂、溶解或消失,可见变形及碎裂的红细胞碎片,伴少量炎性细胞浸润(箭,HE,×100)
2.2 安全性评价 注射针插入心肌瞬间可见室性期前收缩,未见持续性室性心律失常。消融后即刻及消融5天后经胸超声均未发现附壁血栓形成、PM断裂、心肌穿孔及心包压塞等。消融5天后,0.2 ml、0.4 ml组MRA、VC与消融前差异无统计学意义(P均>0.1),0.8 ml组MRA、VC均较前增加(P均<0.05,表1)。
表1 各组消融前后乳头肌功能比较(±s)

表1 各组消融前后乳头肌功能比较(±s)
组别MRA(cm2)消融前消融5天后VC(ml)消融前消融5天后0.2 ml组0.36±0.230.39±0.191.10±0.701.30±0.700.4 ml组0.41±0.210.38±0.191.20±0.501.10±0.500.8 ml组0.36±0.221.16±1.051.40±0.702.50±0.90
2.3 病理学观察 相比正常心肌组织,消融部位心肌纤维排列紊乱,消融中心区域心肌细胞可见出血及凝固性样坏死,细胞核固缩、碎裂,核溶解或消失,消融灶内见大量变形及碎裂的红细胞碎片和少许炎性细胞浸润。消融灶周围组织结构基本完好,横纹清晰,细胞核呈正常卵圆形,与消融灶界限分明(图3)。
3 讨论
本研究利用自制多功能ICE超声导管,采用动物模型验证经心内膜途径实施左心室APM化学消融的可行性和安全性,结果显示利用导管内置ICE探头可对左心室APM定位,以ICE图像进行监控,能够实现注射针进针和注射药物的可视化操作,对左心室APM基底部实现安全消融,且消融灶体积与注射无水乙醇剂量有关,低剂量无水乙醇消融对乳头肌功能无明显影响。
PM解剖结构复杂,室性心律失常起源于此者并不少见。相较于左心室其他部位,乳头肌在心腔内凸起,随心室收缩活动度较大,尤其是左心室APM邻近心室侧壁,腱索、瓣膜等结构影响均可导管贴靠和到位,导致该区域内进行导管相关操作存在一定困难[9-10];为此临床常于右心室放置一条ICE导管,用于观察消融导管与PM之间的空间位置和贴靠关系,但保持导管与剧烈运动的PM之间的稳定性时常遇到困难[10-11];应用多条导管增加血管穿刺频次,且ICE价格相对昂贵,致其使用受到限制[11-12]。
本研究所用导管进入心腔后,ICE图像可清晰显示左心室APM形态,虽探头成像角度与市售商业化ICE导管(如AcuNav©)相比较为狭窄(约20°),但仍可清楚区分APM与左心室壁(图1A);得益于该导管集ICE成像、心肌内注射消融等功能于一体的同轴化设计,无须放置其他导管即可明确消融导管与PM的空间位置,而插入PM的注射针在整个消融过程中亦可起到“锚定”作用,在一定程度上维持导管与PM之间贴靠的稳定性。
PM的特殊结构影响导管消融的稳定性,其解剖学异质性也使心律失常起源点往往位于心肌深部,这是目前消融技术面临的另一个挑战[2]。增加消融能量或利用冷盐水灌注导管可能有助于提升消融效果,但存在可能导致心肌穿孔或心包压塞的潜在风险[13],也可能给能量传递路径上的正常心肌组织带来损伤,甚至影响瓣膜功能[14]。利用心肌内注射导管直接注射化学药物是达成心肌消融、减少室性心律失常发生的另一途径[5],但在无影像学监控条件下进行心肌内注射存在心肌穿孔甚至心包压塞风险[15]。本课题组前期动物实验研究结果已证实了该导管用于实施室间隔化学消融的可行性和安全性[7]。本研究发现,PM内消融灶体积与注射无水乙醇剂量呈显著正相关,提示通过调整注射药量并结合ICE图像对组织内高回声区域扩布范围进行实时监测,可在一定程度内控制性调节消融灶体积,且利用该导管可实现注射针进针和药物注射的可视化操作,降低因进针过深导致心肌穿孔的风险,提高经心内膜注射化学消融PM的安全性;通过比较不同剂量组消融前后MRA、VC,发现较低注射剂量(0.2 ml、0.4 ml)短期内未对乳头肌、二尖瓣功能产生明显影响,提示采取心肌内注射消融策略无需经心内膜面释放能量,通过ICE图像监控注射针进针深度可实现APM基底部相对靶向性消融,而不对其体部及周围组织造成过度损伤,最终实现可控、安全消融左心室APM的目标。
综上所述,本研究利用自制ICE导管成像功能准确识别左心室APM,并实时监测心肌内注射过程,以低剂量无水乙醇在APM基底部形成范围一定程度内可控的消融灶,且对二尖瓣功能无明显影响,可能为消融治疗左心室APM起源的VAS提供新的策略。

