基于网络药理学探讨仙灵骨葆胶囊治疗骨质疏松症的作用机制
綦向军 陈国铭 史佩玉 张兆萍 方彩珊 郑深建 邢万里 黎健敏 周润吉 徐福平
1.广州中医药大学第一临床医学院,广东 广州 5104052.广州中医药大学第二附属医院,广东省中医院治未病中心,广东 广州 510120
骨质疏松症(osteoporosis,OP)是临床常见的全身性骨骼疾病之一,以骨量降低,骨组织微结构破坏,骨脆性增加为特征,以致骨折易于发生[1]。骨质疏松症是一种年龄相关性疾病,随着人口老龄化的进展,OP发病率逐渐升高,早期流行病学调查显示:我国50岁以上女性OP发病率为20.7%,男性为14.4%;60岁以上人群患病率明显增高[2]。据2015年预测,我国在未来20年、40年间用于骨质疏松症的费用分别高达1 320亿元、1 630亿元[3]。因此,OP俨然成为我国严重的公共卫生问题,预防以及早期治疗具有重要的临床意义。
仙灵骨葆胶囊是根据苗族验方研制而成的成方制剂,全方由淫羊藿、续断、补骨脂、地黄、丹参、知母6味中药组成,具有滋补肝肾、强筋壮骨的功效,目前广泛应用于骨质疏松症、骨折、骨关节炎等疾病[4],而在OP的运用方面尤为突出。王桂倩等[5]对仙灵骨葆胶囊治疗原发性OP的随机对照试验进行Meta分析后表明,仙灵骨葆胶囊单用或与其他西药联合使用,在治疗骨质疏松症方面的疗效优于单用西药治疗;安一方等[6]对仙灵骨葆胶囊治疗绝经后OP的随机对照试验进行Meta分析后表明仙灵骨葆胶囊在改善腰椎骨密度、提高临床有效率及改善疼痛方面疗效确切;章秩立等[7]通过对仙灵骨葆胶囊安全性进行系统评价,认为其总体安全性可接受。故宏观上已有大量的循证医学证据表明仙灵骨葆运用于OP具有较好的疗效和安全性,但对于其微观药理作用机制尚缺乏全面、系统的阐述,而传统药理学为证明药物与疾病的关系时,常常通过设置对照实验、控制药物变量,研究其对疾病靶蛋白的亲和力、特异性以揭示药物对疾病的起效机制[8],与中药“多组分、多靶点、多通路”的机制特点不符。网络药理学的概念最初由Hopkins[9]提出,相较于传统药理学相比,网络药理学更加注重多组分、多靶点、多通路的协同作用,与中药的特点相符,目前网络药理学在中药作用机制研究、新药挖掘、老药新用等方面广泛运用[10]。本研究拟运用网络药理学的研究方法进行探究。
1 材料和方法
1.1 数据库与软件
本研究所运用的数据库及软件如下:①中药系统药理学数据库和分析平台(Traditional Chinese Medicine Systems Pharmacology Database and Analysis Platform,TCMSP,http://lsp.nwu.edu.cn/tcmsp.php)[11];②中药综合数据库(Traditional Chinese Medicine Information Database,TCMID,http://www.megabionet.org/tcmid/)[12];③Cytoscape3.7.1软件;④STRING数据分析平台(https://string-db.org/)[13];⑤GeneCards: The Human Gene Database(https://www.genecards.org/)[14];⑥DAVID数据分析平台(https://david.ncifcrf.gov/)[15]。
1.2 仙灵骨葆胶囊活性成分及其靶标的获取
TCMSP中收录了500多种中药以及30 069个中药化合物,TCMID中收录了8 159味中药以及25 210种中药化合物,运用TCMSP、TCMID分别检索淫羊藿、续断、补骨脂、地黄、丹参、知母,获取相应的药效成分。将口服利用度(oral bio-availability,OB)设置为≥30%,类药性(drug likeness,DL)设置为≥0.18进行活性成分筛选,并运用TCMSP查找成分所对应的靶点信息,将所得数据去重后输入STRING数据分析平台获取靶点的标准基因名称。
1.3 仙灵骨葆“活性成分-作用靶标”网络构建
运用Cytoscape 3.7.1软件绘制“活性成分-作用靶标”网络图。将上述活性成分及靶标信息导入软件,根据软件所提供的“network analyzer”功能进行网络拓扑学分析,以靶点度值(degree)和中介中心度(betweenness centrality)评价仙灵骨葆核心成分以及靶点[13]。
1.4 蛋白互作PPI网络构建
将所得靶标信息上传至STRING数据分析平台,数据分析模式设定为“Multiple proteins”,物种限制为“Homo sapiens”,提取靶点所对应的基因信息。对数据进行预读后将置信度设置为≥0.98,并将孤立蛋白进行隐藏,最后输出PPI蛋白网络互作图(protein-protein interaction network,PPI network)。
1.5 骨质疏松症靶标基因的获取
以“osteoporosis”为关键词从GeneCards: The Human Gene Database获取骨质疏松症疾病基因,与仙灵骨葆靶点基因对比后筛选出仙灵骨葆治疗骨质疏松症的关联基因数据。
1.6 KEGG通路富集以及GO生物过程富集分析
将仙灵骨葆治疗骨质疏松症的靶点基因上传至DAVID数据分析平台进行KEGG通路富集以及GO生物过程富集分析,分析时将物种限定为“Homo sapiens”。提取P<0.05的通路以及生物过程,运用Cytoscape 3.7.1软件绘制仙灵骨葆治疗骨质疏松症的“靶点-通路”网络图。
2 结果
2.1 仙灵骨葆活性成分的筛选以及相应作用靶标的获取
以OB≥30%,DL≥0.18为筛选条件,共获得活性成分115种,其中淫羊藿23种,续断8种,熟地黄2种,丹参65种,知母15种,补骨脂2种。详见表1。
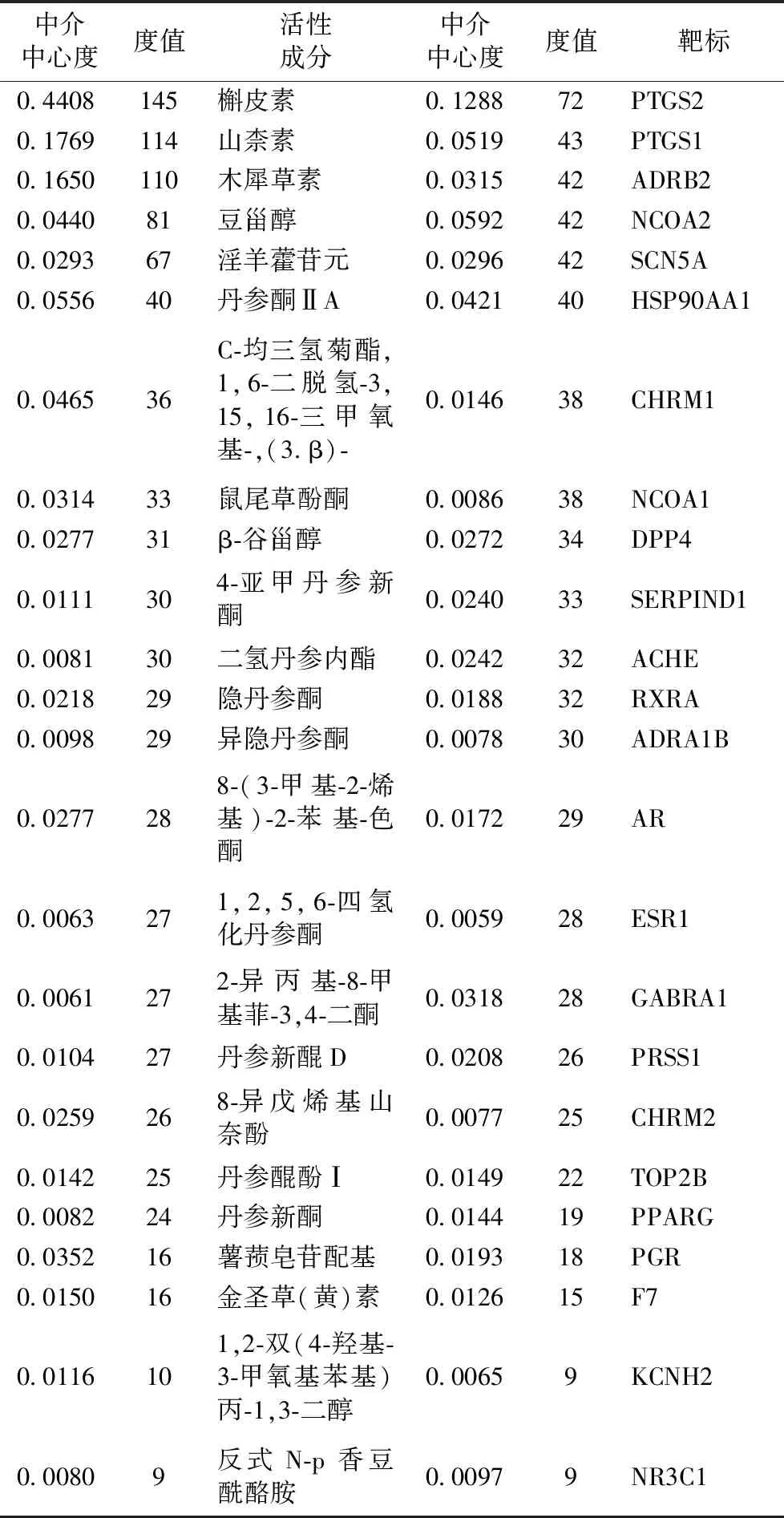
表1 核心活性成分及靶标Table 1 The core active components and targets
2.2 仙灵骨葆“活性成分-作用靶标”网络图
运用Cytoscape 3.7.1软件绘制仙灵骨葆“活性成分-作用靶标”网络图,详见图1。网络图中蓝色圆形节点为作用靶标,黄色多边形节点为活性成分,线条代表活性成分与靶标具有对应关系,共计396个节点,其中活性成分节点95个,靶标节点301个,MOL009317、MOL008188、MOL009322等20个化合物未查询到对应的靶标节点,故未纳入到网络图中。节点的Degree值代表网络中与节点进行连接的线条数。将其网络拓扑学分析结果导出后示:平均节点度值为8.187 817 259,大于该度值的节点共有96个,平均中介中心度为0.005 437 999,大于平均中介中心度的节点有52个。节点所对应的节点度值以及中介中心度越高表明所对应的活性成分或靶点越可能是网络图的核心,可作为对仙灵骨葆治疗骨质疏松症的机制预测依据。Degree值及中介中心度均大于平均值的活性成分及靶标按照Degree进行降序排列后详见表1。

图1 仙灵骨葆“活性成分-作用靶标”网络图Fig.1 The active component-target network of XianlingGubao Capsule
2.3 仙灵骨葆治疗骨质疏松症的交集基因筛选
将活性成分作用靶点转化为基因信息后与骨质疏松症疾病相关基因进行对比后共筛得交集基因143个。详见表2。
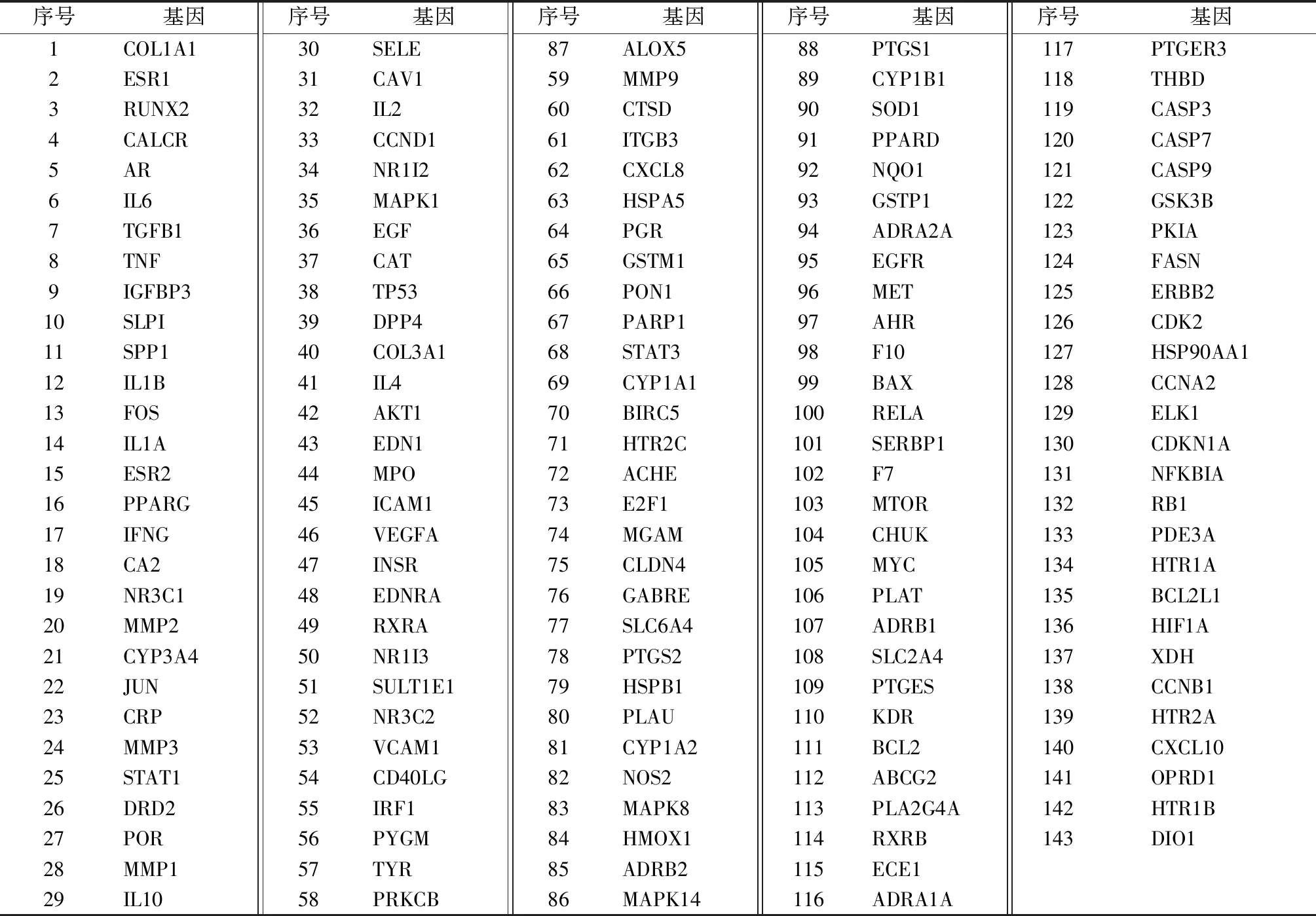
表2 仙灵骨葆治疗骨质疏松症交集基因Table 2 The related genes of XianlingGubao Capsule in treating osteoporosis
2.4 仙灵骨葆PPI网络构建
运用STRING数据平台对仙灵骨葆进行蛋白互作网络分析,设置置信度≥0.98,并且隐藏孤立蛋白后得到仙灵骨葆PPI网络图,共得到111种蛋白之间的互作关系,详见图2,图中圆形节点代表靶蛋白,蛋白之间线条的颜色代表蛋白之间不同的作用关系,详见图3。所得PPI网络图平均节点度值为4.145 454 545,大于该度值的节点共有34个,平均中介中心度为0.022 127 656,大于平均中介中心度的节点有20个。Degree值及中介中心度均大于平均值的活性成分及靶点详见表3。
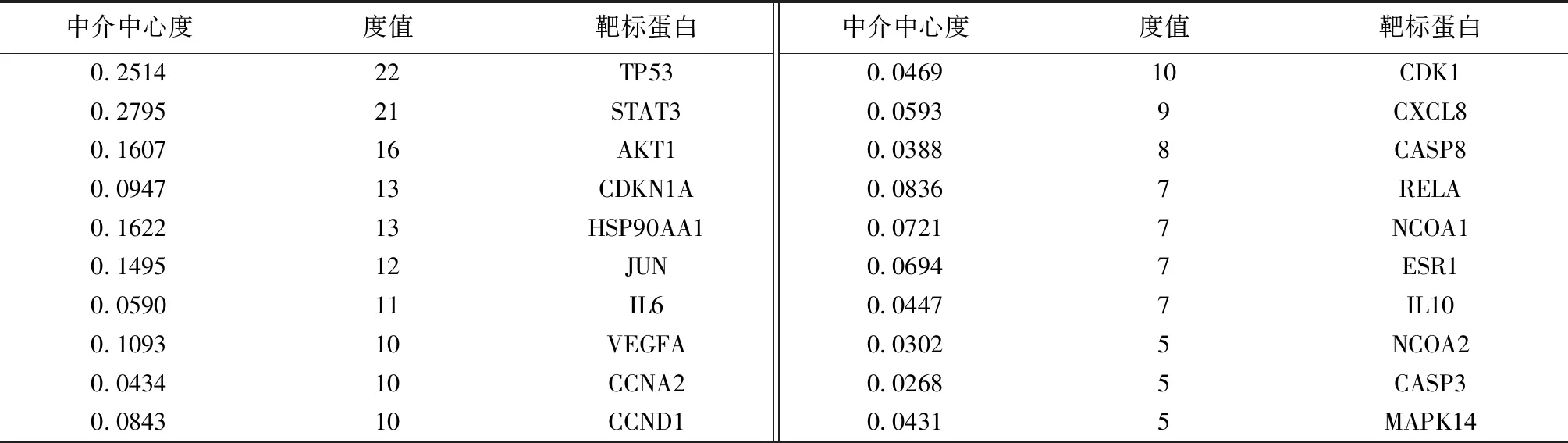
表3 PPI核心靶标蛋白Table 3 The core target proteins in PPI
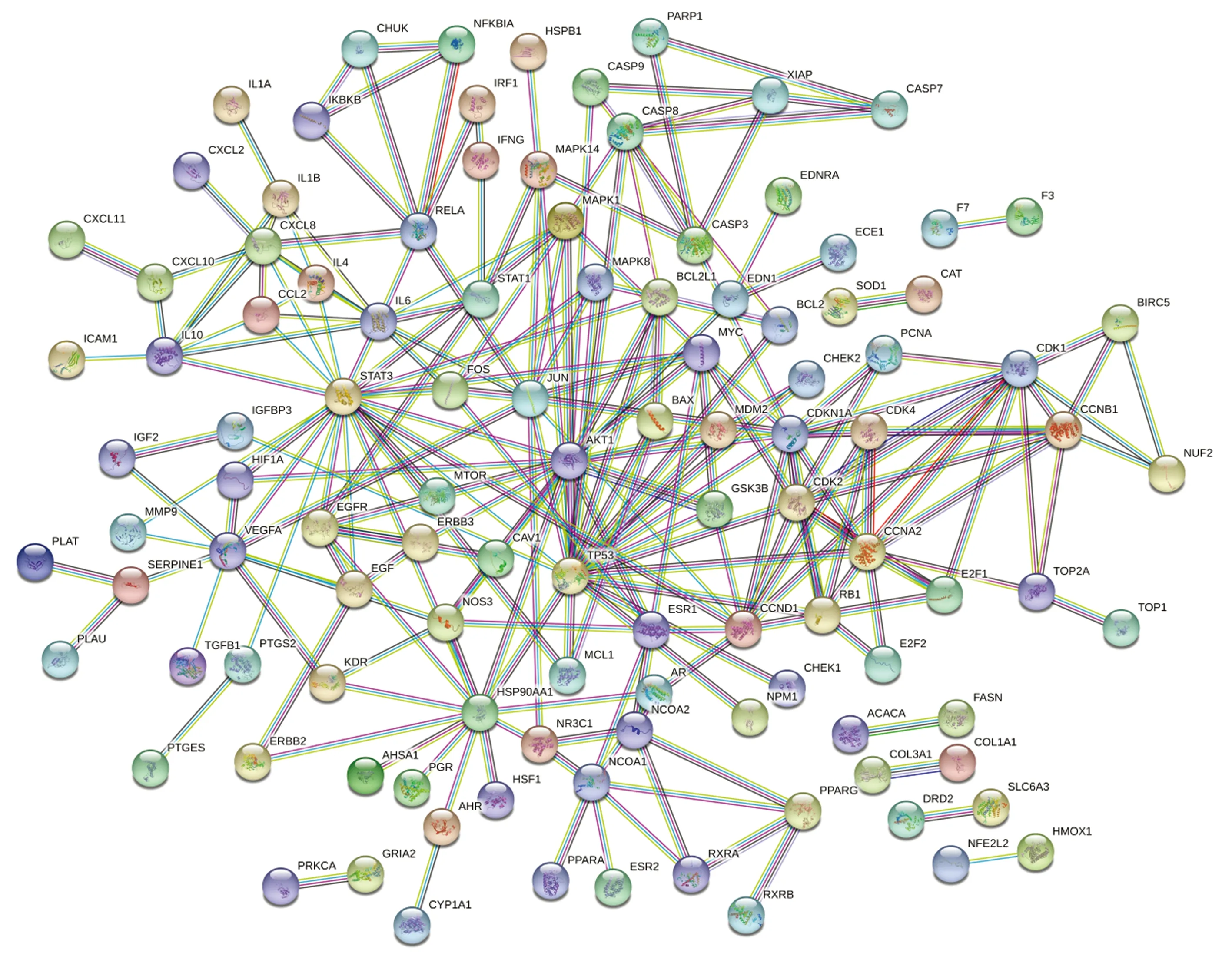
图2 仙灵骨葆PPI网络图Fig.2 The PPI network of XianlingGubao Capsule

图3 蛋白互作关系注释图Fig.3 The annotation of PPI network注:known interactions:已知的相互作用关系;from curated databases:数据库获取;experimentally determined:实验验证;predicted interaction:预测的相互作用关系;gene neighborhood:基因邻域;gene fusions:基因融合;gene co-occurrence:基因共现;others:其他;textmining:文本挖掘;co-expression:共表达;protein homology:同源蛋白
2.5 GO生物过程富集以及KEGG通路富集
运用David数据分析平台对仙灵骨葆治疗骨质疏松症关联基因进行GO生物过程富集以及KEGG通路富集。分别计算相应富集结果的P值(采用Bonferroni法进行校正,P<0.05时富集显著),并提取具有意义的富集结果。GO生物过程富集共获得612项,仅取富集基因数≥10的过程进行展示,详见表4。KEGG通路富集共获得37项,仅TGF-β通路P值大于0.05,详见表5,运用Cytoscape 3.7.1对其进行网络可视化,详见图4,图中粉红色三角形节点代表通路,蓝色圆形节点代表基因,线条代表通路与基因之间的对应关系。

表4 GO生物过程富集展示Table 4 The results of GO biological processes enrichment analysis
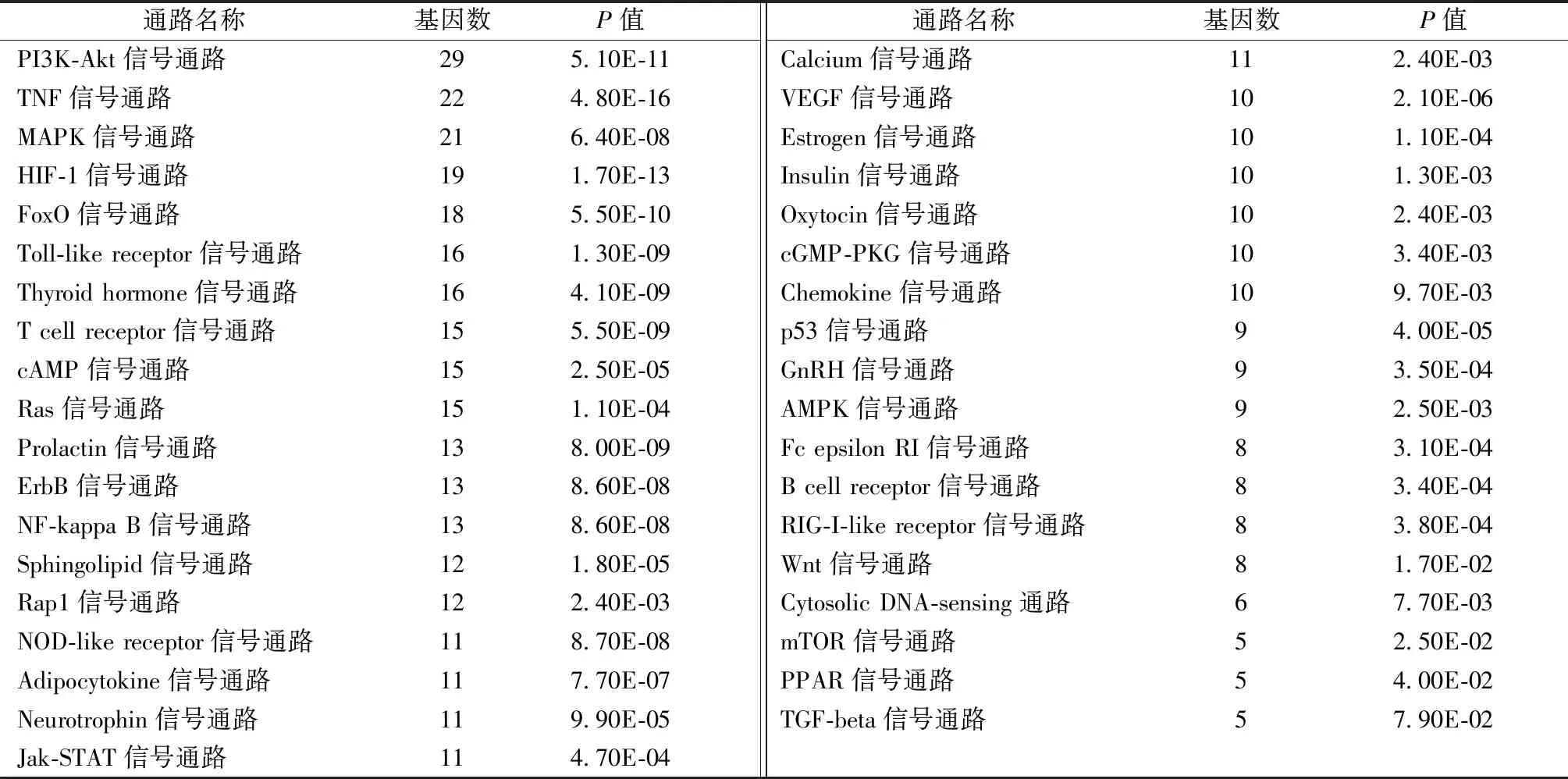
表5 KEGG通路富集图Table 5 The results of KEGG pathways enrichment analysis
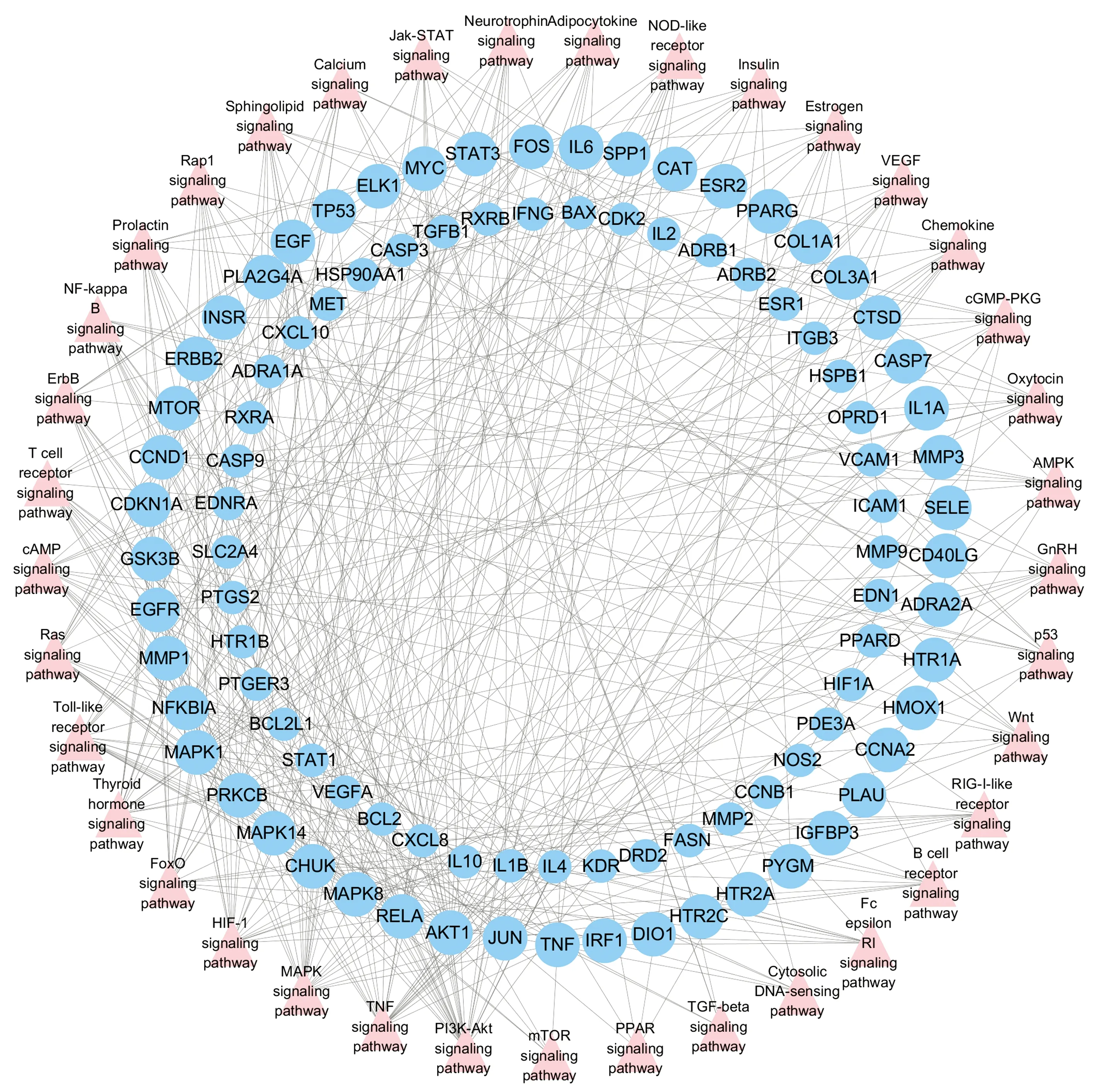
图4 “通路-靶标”网络图Fig.4 The pathway-target network
3 讨论
骨重建失衡,骨吸收/骨形成比例升高是导致骨量丢失的直接原因。成骨细胞以及破细胞在骨重建的过程中扮演着重要的角色,成骨细胞由间充质干细胞分化而来,成骨细胞可分泌骨基质,骨基质经羟基磷灰石沉积后即完成矿化,矿化完成标志骨重建过程结束[16];破骨细胞由单核巨噬细胞前体分化而成,主司骨的吸收[17],因此成骨细胞与破骨细胞的比例是骨质疏松症发生的关键也是治疗的干预重点。OP可分为老年性、绝经后以及特发性,老年性OP成因主要为随着年龄增加,骨重建平衡被打破,造成骨量进行性丢失,绝经后OP除增龄因素外,雌激素水平降低是更为重要的因素[18],而特发性骨质疏松症主要发生于青少年,目前病因尚不明确[19]。OP的发病机制大体如上述,但具体的调节机制受到诸多途径的影响,本研究将从网络药理学分析所得结果对仙灵骨葆治疗OP的潜在机制进行讨论。
3.1 活性成分与靶标
高度值以及高中介中心度活性成分中槲皮素、山奈酚、木犀草素、淫羊藿苷元等均为黄酮类化合物,现有研究表明黄酮类化合物主要通过雌激素受体介导、OPG/RANK/RANKL、酶抑制作用、过氧化物酶增殖子激活受体介导、调节信号转导通路等机制预防OP[20]。槲皮素、山奈酚同属于黄酮醇类,目前对于槲皮素治疗OP较为明确的机制为抑制RANKL的活化[21],OPG/RANK/RANKL机制是破骨细胞生成的关键,RANK与RANKL结合是促进破骨细胞分化的重要环节[22],因此槲皮素可以抑制破骨细胞的生成,减少骨吸收。Kim等[23]发现山奈酚可抑制肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)、白介素-6(interleukin,IL-6)的分泌,而TNF-α、IL-6可诱导巨细胞集落刺激因子(macro-phagecolony-stimulatingfactor,M-CSF)以及RANKL的表达,促进破骨细胞分化,抑制成骨细胞[18]。淫羊藿苷元及其苷类在体内外均有增强成骨细胞活性,抑制破骨细胞活性的作用,而以淫羊藿苷元的作用最强[24]。除黄酮类活性成分外,丹参的活性成分较多,如丹参酮IIA、隐丹参酮等,丹参具有抗氧化、改善微循环,防止血栓等功能,但是近年来许多研究表明丹参及其有效成分具有抗OP或者改善骨代谢的作用[25],如丹参酮IIA可促进间充质干细胞向成骨细胞分化[26]、抑制破骨细胞生成前列腺素E2进而抑制骨吸收[27]。
高度值以及高中介中心度的靶标共有24个,其中PTGS2(COX-2)的度值和中介中心度远高于其他靶标,推测PTGS2是仙灵骨葆的关键靶标。PTGS1(COX-1)是度值排列第2的靶标,与PTCS2均为前列腺素生成的主要限速酶[28],而前列腺素可以诱导M-CSF以及RANKL的表达,促进破骨细胞分化,抑制成骨细胞功能[18]。此外在表1中AR(雄激素受体)至少与29个活性成分相关,现代研究表明雄激素与男性骨骼生长发育,骨量维持有关[29],雄激素可以与成骨细胞表面的雄激素受体结合,促进成骨细胞分化[30]。ESR1(雌激素受体)至少与28个活性成分相关。二者均为仙灵骨葆的靶标核心。整个活性成分-靶标网络图靶标众多,关联复杂,可见仙灵骨葆的起效机制是多成分多靶点的相互作用,并且具有许多潜在的治疗作用。
3.2 PPI网络分析
PPI网络拓扑学特征以细胞周期调节蛋白居多,高度值以及高中介中心度蛋白中TP53、AKT1、CDKN1A、JUN、CCNA2、CCND1、CDK1等蛋白均与细胞生长、分化、凋亡的调节有关,据此推测仙灵骨葆的作用特点在于调节成骨细胞以及破骨细胞的生长周期。值得一提的是表3中IL-6与STATA3之间的相互作用,陈鹏等[31]通过动物实验表明将JAK2/STATA3通路阻断引起IL-6无法表达后,骨质疏松症大鼠骨密度及ALP水平低于未阻断组。此外PPI网络图尚与炎性因子、雌激素等相关。
3.3 GO生物过程富集以及KEGG通路富集
富集基因数较多的GO生物过程所反映的内容与PPI网络规律相似,均与细胞周期有关,炎症反应(IL-6、CXCL8等)、雌二醇反应(ESR1)、血管新生反应(VEGFA)均可与PPI中的蛋白相对应。本研究所展示GO生物过程,正调控NF-kappaB转录活性因子为主要的过程之一,该过程与骨质疏松症的相关机制吻合,即破骨细胞的激活依赖于核因子-κB受体活化配体[receptor activator of nuclear factor-κB (NF-κB) ligand,RANKL]与破骨细胞前体细胞上的RANK结合,从而激活NF-κB,促进破骨细胞分化[22],骨质疏松症基因富集于该过程,上调NF-κB表达,从而引起骨质疏松症。而参与富集的基因均为仙灵骨葆所涉及的基因,说明仙灵骨葆胶囊可以对该过程进行调控,KEGG通路富集结果中NF-kappa B 信号通路富集了13个基因,亦佐证了这一结论。
KEGG通路富集结果中,富集基因数最多的通路为PI3K-Akt信号通路,有研究表明与正常小鼠相比Akt1和Akt2基因均敲除的小鼠骨量明显下降,提示该通路与促进骨形成有关[32]。此外在对淫羊藿苷促进BMSCs分化的研究中发现加入PI3K阻断剂后,淫羊藿苷的促进效果受到显著抑制,提示该通路与BMSCs向成骨细胞分化有关[33]。TNF信号通路是富集基因数排列第2的通路,目前有研究表明,炎性因子TNF-α是绝经后OP发生的主要原因之一,TNF-α可促进RANKL表达,诱导破骨细胞形成[34]。MAPK信号通路是调节成骨细胞生长分化的重要途径,其中具有抗OP作用的主要有ERK通路、p38通路以及JNK通路,ERK通路可以促进骨保护素(osteoprotegerin,OPG)表达[35],而OPG可以与RANK竞争性结合RANKL从而导致破骨细胞的凋亡[36];p38通路则可以促进成骨细胞的矿化过程[37];有研究表明JNK通路缺失后成骨细胞骨钙蛋白以及骨桥蛋白表达明显下降,因此JNK信号通路可能与成骨细胞后期分化有关[38]。KEGG通路结果中部分通路之间表现出协同作用,如HIF-1信号通路与VEGF通路,VEGF可作为HIF-1的下游目的基因,共同参与血管-骨形成的耦联[39];再如TGF-β信号通路、mTOR信号通路、AMPK信号通路,TGF-β1可以募集成骨细胞前体细胞,而成骨细胞可以分泌OPG,OPG可以通过mTOR信号通路以及AMPK信号通路转导信号,抑制破骨细胞分化;朱云艳等[38]发现,Toll样受体通路过表达可引起MAPK以及Akt磷酸化水平的下降。目前有研究表明甲亢是OP的危险因素之一,甲亢可致骨密度下降,由此可以推测,仙灵骨葆或可用于存在甲亢的OP患者。Prolactin(泌乳素)、Estrogen(雌激素)以及GnRH信号通路表明仙灵骨葆具有雌激素调节作用,是仙灵骨葆可运用于绝经后OP的证据。
综上所述,仙灵骨葆主要通过影响成骨细胞以及破骨细胞生长分化,调节骨代谢、雌激素等途径干预OP。仙灵骨葆生物网络复杂庞大,本研究通过构建“活性成分-靶标”网络对仙灵骨葆的核心活性成分以及靶标进行了预测,PPI网络对仙灵骨葆核心蛋白之间相互作用进行分析,运用David数据分析平台进行GO生物富集以及KEGG通路分析,预测仙灵骨葆治疗OP的起效机制,并引证现有研究结果进行对比,所得结果真实可信,为后续的仙灵骨葆药理机制分析和实验设计提供了数据支持。

