多囊卵巢综合征患者血清必需元素水平变化及其与胰岛素抵抗的关系
肖玲 杨颖 雷婷
必需元素是人体代谢过程中必不可少的重要物质,通过参与物质组成、调节催化过程来帮助机体完成各种复杂的代谢过程。不仅如此,必需元素在机体抗炎、抗氧化过程中也发挥重要作用[1]。多囊卵巢综合征(PCOS)的发病机制较复杂,多项研究证实PCOS患者存在氧化应激(OS)损伤,而胰岛素抵抗(IR)在PCOS的病理生理学中也发挥重要作用,二者共同影响女性生殖系统的功能[2]。因此,我们通过对PCOS患者血清必需元素进行分析,探讨PCOS患者血清部分必需元素水平变化及其与IR的关系。
对象与方法
1.对象:2015年6月~2018年12月于湖北省襄阳市中心医院内分泌门诊确诊的PCOS患者85例(PCOS组),年龄20~40岁,平均年龄(31.5±2.3)岁。PCOS诊断标准[3]:临床表现为月经稀发、闭经或不规则子宫出血,并符合下述两项中的1项即可诊断:(1)高雄激素的临床表现或高雄激素血症;(2)超声检查下表现为卵巢多囊样改变,即一侧或双侧卵巢内直径2~9 mm的卵泡数≥12个,或卵巢体积≥10 cm3[卵巢体积(cm3)=0.5×长径(cm)×横径(cm)×前后径(cm)];同时排除其他可能引起高雄激素的疾病和排卵异常的疾病。排除标准:年龄<20岁或>40岁;患有子宫内膜异位、卵巢早衰、合并感染、曾接受卵巢手术或化疗、先天性肾上腺皮质增生症、高泌乳素血症、库欣综合征、甲状腺功能异常、糖尿病或接受任何药物治疗。另选取同期参加体检的健康育龄期妇女90例作为对照组,年龄23~42岁,平均年龄(33.7±3.1)岁。纳入标准:月经规律;盆腔超声检查结果无异常;血糖、血脂及血压均正常;无心、肝、肾脏疾病;近3个月未补充过必需元素。本研究经湖北省襄阳市中心医院伦理委员会批准,所有受试者均知情同意。
2.方法:测量所有受试者的身高、体重,计算BMI。在清晨空腹状态下,抽取所有受试者静脉血6 ml,采用肝素抗凝,于4 ℃冰箱保存待检。采用美国PE公司A7000型原子吸收光谱分析仪和火焰原子吸收法测定血清必需元素(钙、镁、锌、铜、铁)水平;采用葡萄糖氧化酶法测定空腹血糖(FPG);采用电化学发光免疫测定法测定空腹胰岛素(FINS)水平。通过稳态模型评估计算胰岛素抵抗指数(HOMA-IR),HOMA-IR=FINS(μIU/ml)×FPG(mmol/L)/22.5。根据HOMA-IR水平将PCOS患者分为IR组(HOMA-IR≥2.69)40例和非IR组(HOMA-IR<2.69)45例[4],比较两组患者血必需元素水平的差异。
结 果
1.PCOS组与对照组一般资料、内分泌指标及血清必需元素水平比较:两组年龄、BMI和FPG比较差异均无统计学意义(P>0.05)。PCOS组患者的FINS、HOMA-IR及血清铜水平均明显高于对照组(P<0.05),血清锌、镁水平低于对照组(P<0.05),而两组血清钙、铁含量比较差异无统计学意义(P>0.05)。见表1。

表1 PCOS组与对照组一般资料、内分泌指标及血必需元素水平比较
2.IR组与非IR组PCOS患者一般资料、内分泌指标及血清必需元素水平比较:两组患者年龄比较差异无统计学意义(P>0.05)。IR组PCOS患者BMI、FPG、FINS、HOMA-IR及血清铜水平均明显高于非IR组,差异有统计学意义(P<0.05),血清锌水平明显低于非IR组(P<0.05),而两组患者血清钙、铁和镁水平比较差异均无统计学意义(P>0.05)。见表2。

表2 IR组与非IR组PCOS患者一般资料、内分泌指标及血清必需元素水平比较
3.PCOS患者发生IR的影响因素分析:Logistic回归分析结果显示,BMI、FPG和血清铜水平升高及血清锌水平降低均为PCOS患者发生IR的独立危险因素(P<0.05)。见表3。
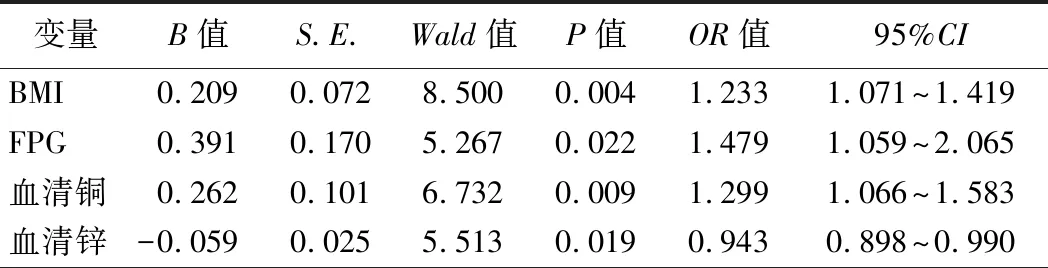
表3 PCOS患者发生IR的影响因素分析
讨 论
PCOS是育龄期女性常见的生殖内分泌疾病,由多种因素造成[5],在育龄期女性中的发病率达5%~10%。PCOS与代谢综合征、IR、肥胖、高血压、血脂异常、心血管疾病及生殖系统异常、不孕症等密切相关,严重影响女性的生育能力、生活质量及远期健康状况[6]。铜、锌、镁、铁等元素是人体必需元素,可通过多种途径调控机体炎症和氧化反应过程。研究表明,PCOS患者发生OS可能会加剧IR,并影响女性生殖系统导致不孕[7]。
锌在维持人体生殖系统的正常功能中发挥重要作用,主要通过调节下丘脑-垂体-性腺轴参与性激素的合成及卵泡的发育。本研究中,PCOS患者血清锌水平低于对照组,且IR组血清锌水平也较非IR组明显降低,与既往研究结果一致[8]。原因可能是PCOS患者的自由基、过氧化物质等氧化负荷上升,而锌组成的铜-锌超氧化物歧化酶具有清除自由基等功能,从而导致血清锌水平降低[9]。另一方面,PCOS是一种慢性炎症反应,锌参与的转运蛋白表达和调控与其密切相关,如锌转运蛋白ZRT/IRT样蛋白(ZIP)14调控慢性炎症的发生,在巨噬细胞中SLC39A8基因编码的锌转运蛋白ZIP8会通过增加锌吸收来抑制炎症信号激活酶的活性,对核因子(NF)-κB通路进行负反馈调节,进一步抑制炎症反应[10]。IR导致PCOS患者炎症加重,而血清锌通过参与调节炎症反应而出现水平下降。
本研究结果显示,PCOS患者血清铜水平呈升高状态,合并IR的PCOS患者血清铜水平进一步升高,原因可能是必需元素之间存在协同和(或)拮抗的作用,铜和锌同为元素周期表第四周期元素,可能在肠黏膜或金属硫蛋白中竞争结合位点,从而相互抑制[11];也有学者认为与铜蓝蛋白的增加有关,后者起到中和自由基抗氧化的作用[12]。而机体内的血清铜含量升高后会结合锌指蛋白(TTP)36,使其不能参与抑制PCOS炎症反应的信号传导通路,造成炎症程度增加[13],从而加重PCOS患者的IR。
镁是葡萄糖代谢过程中重要的辅酶因子,在糖代谢、调节胰岛素分泌等过程中发挥重要作用。国内有研究结果显示,PCOS患者血清镁水平低于正常人群,推测可能与IR及血清钙离子缺乏有关[14]。本研究虽发现PCOS患者血清镁水平明显下降,但未发现血清镁水平与IR之间的相关性,可能需要大样本量研究进一步探讨。此外,本研究未发现PCOS患者血清铁、钙浓度的差异。Hossein等[15]的研究结果显示,PCOS患者血清铁浓度无明显变化,与本研究中结果一致;而Héctor[16]发现PCOS患者血清铁水平升高,尤其是当葡萄糖耐量异常时,提示铁超负荷。Foroozanfard等[17]的研究显示钙和维生素D联合补充可改善PCOS女性的炎症和氧化应激状态。因此,PCOS患者血清铁、钙浓度的变化仍需要更多的研究证实。
综上,人体必需元素铜、锌、镁与PCOS的发生、发展密切相关,对PCOS的诊断和治疗有重要价值,铜和锌元素可能参与PCOS患者IR的发生。如能早期发现机体内必需元素的变化,及早补充所缺少的必需元素,对预防PCOS并发症、提高女性生殖健康有帮助。

