2-甲硫基芳炔化合物的自由基串联环化反应
高 凡 吕琪妍 於 兵
(1. 郑州大学 生命科学学院,河南 郑州450001;2. 郑州大学 化学学院,河南 郑州 450001)
0 引言
自由基串联环化反应(radical cascade cyclization)由于反应条件简单和反应方便可控等特点,在过去十几年里取得了长足发展[1-3]. 人们可以通过化学促进、热促进、光促进、电化学促进等多种手段引发自由基,进而与反应底物发生自由基加成/串联环化反应,合成各种复杂的有机功能分子,如有机杂环化合物、小分子荧光探针、发光材料等. 其中,有机杂环化合物如取代苯并噻吩类和取代黄酮类杂环化合物等,具有良好的生物活性,可用于开发抗菌剂、抗癌药和抗疟疾药等[4-8]. 因此,自由基串联环化反应已经成为有机合成、药物开发、功能材料开发中的重要策略.
近来,2-甲硫基芳炔及其衍生物在自由基串联环化反应中展现出丰富的反应性. 一般地,以2-甲硫基芳炔化合物[9]作为反应底物,可以通过不同手段(热、光、电等)在反应中原位产生自由基(R•),经历自由基串联环化反应历程,实现苯并噻吩类和黄酮类杂环化合物的高效构筑(图1). 本文主要关注2-甲硫基芳炔化合物(包括2-甲硫基芳炔、2-甲硒基芳炔、2-甲硫基芳炔酮、2-甲硒基芳炔酮等)为反应底物的自由基环化反应,合成3-取代苯并呋喃、3-取代苯并噻吩、3-取代苯并硒吩、3-取代黄酮、3-取代硫杂黄酮、3-取代硒杂黄酮等化合物. 这种自由基串联环化反应具有很好的原子经济性和步骤经济性,免去传统合成方法中耗时耗力的中间体分离、保护/脱保护等步骤,是一种简便、绿色的环化策略[10-12]. 根据所构建杂环产物的类型,我们将从两个方面对2-甲硫/硒基芳炔化合物的自由基串联环化反应进行总结:1)五元环的构筑,主要包括3-取代苯并呋喃、3-取代苯并噻吩、3-取代苯并硒吩的合成;2)六元环的构筑,主要包括3-取代黄酮、3-取代硫杂黄酮、3-取代硒杂黄酮的合成.
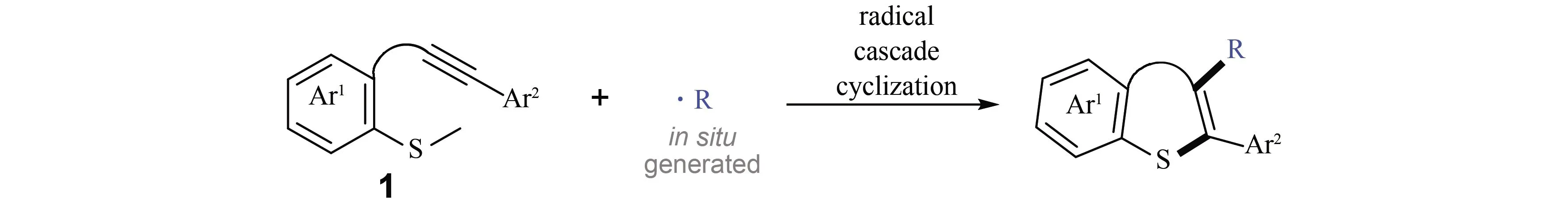
图1 2-甲硫基芳炔化合物的自由基串联环化反应
1 五元环的构筑
2017年,华侨大学宋秋玲课题组[13]以2-甲硫基芳炔[9]和芳基磺酸(2)为反应物,采用叔丁基过氧化氢(TBHP)为氧化剂,在乙腈中100 ℃反应1 h,成功合成了3-磺酰化苯并噻吩(3). 实验研究表明该反应经历自由基历程,可能机理如图2所示,即:芳基磺酸(2)在TBHP的作用下产生磺酰基自由基(4);然后磺酰基自由基(4)选择性地对底物2-甲硫基芳炔[9]的C≡C键进行加成,产生烯基自由基中间体(5);随后中间体(5)发生分子内环化,产生五元环目标产物3-磺酰化苯并噻吩(3),并释放出烷基自由基. 此外,同样的反应条件下,2-甲硒基芳炔[9](X=Se)也能顺利地转化为相应的3-磺酰化苯并硒吩(3). 值得一提的是,该方法的反应底物除了常用的甲基醚,对于苯基醚和苄基醚同样适用. 这种反应条件简单、反应时间短、操作简便的合成路线,为3-磺酰化苯并噻吩、3-磺酰化苯并硒吩的合成提供了高效简便的新方法.
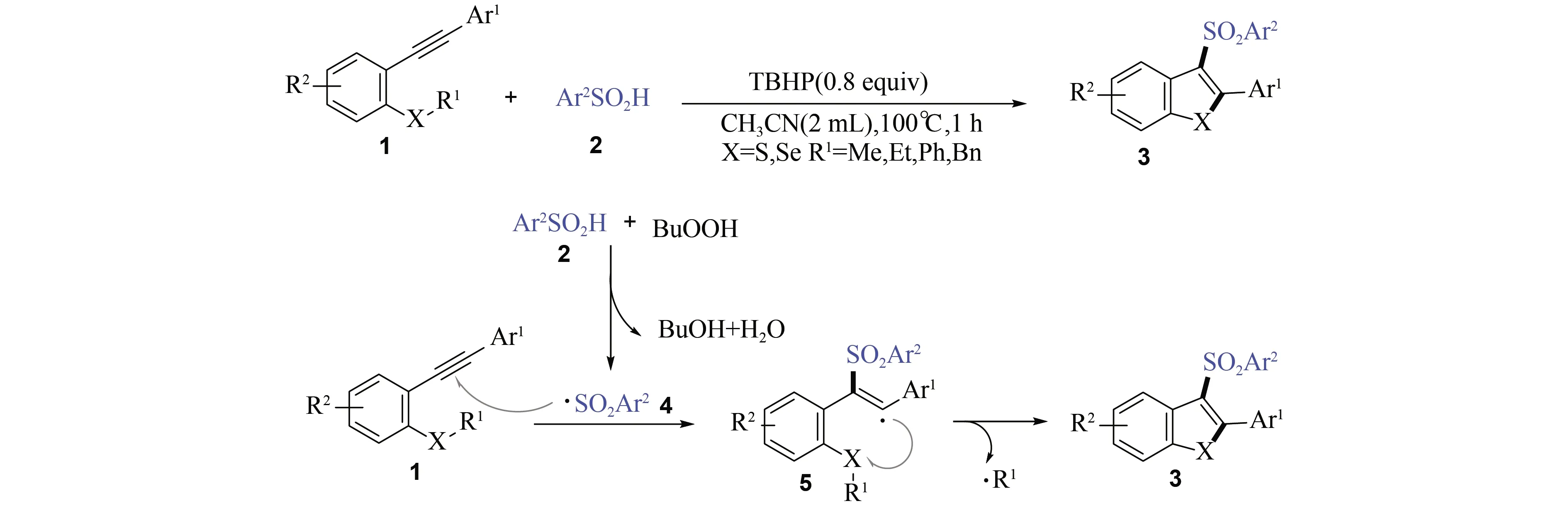
图2 3-苯磺酰取代苯并噻(硒)吩类化合物的合成
在此基础上,温州大学吴华悦等[14]发展了一种银催化的α-酮酸与2-炔基苯甲醚的自由基串联环化反应,实现了3-酰基化苯并呋喃类化合物的合成. 控制实验表明该反应经历自由基历程. 在图3所示的反应机理中,氧化剂过硫酸钾(K2S2O8)首先将Ag+离子氧化为Ag2+离子;然后Ag2+离子促进α-酮酸(6)发生脱羧反应,产生酰基自由基(8). 随后,酰基自由基(8)对反应底物中的炔基加成,得到烯基自由基中间体(9);随后自由基中间体(9)经过分子内环化,释放出烷基自由基,得到产物3-酰基化苯并呋喃(7). 类似地,含有S原子或者Se原子的反应底物参加反应,经历相同的反应历程很容易合成3-酰基化苯并噻吩和3-酰基化苯并硒吩类化合物. 此外,该方法还能用于合成聚合物抑制剂(7a)[15]和雷洛昔芬(raloxifene)前体(7d)[16]. 例如,以甲氧基取代的反应底物1a和6a在标准反应条件下即可生成聚合物抑制剂(7a),产率可达80%.1a和6b在标准反应条件下可以得到中间产物7b,然后在N,N-二甲基甲酰胺(DMF)溶液中加入乙硫醇钠得到去甲基化的酚中间体7c,最后在室温条件下与1-(2-氯乙基)哌啶反应14 h后,最终以63%的总收率得到雷洛昔芬前体7d. 值得一提的是,脂肪链的α-酮酸不适用于该反应,可能是由于脂肪烃酰基自由基容易再次发生脱羰.

图3 3-酰基化苯并呋喃(噻吩、硒吩)类化合物的合成
由于有机硒化物在药物化学,农业化学和催化材料方面的重要作用[17-19],发展新型高效的方法构筑有机硒化物具有巨大的应用价值. 2019年吴华悦等[20]通过银催化的2-炔基苯硫醚与硒粉、芳基硼酸化合物的三组分自由基环化反应,合成了系列3-芳基硒化苯并噻吩类化合物. 该方法的产率最高可达96%. 类似地,2-甲氧基芳炔[9](X=O)为反应底物,在标准条件下也能顺利地转化为相应的3-芳基硒化苯并呋喃类化合物(12)(图4). 由于烷基硒自由基的稳定性较低,相应的烷基硼酸在该反应中不适用. 在该反应中氧气首先将Ag+离子氧化为Ag2+离子,并引发芳基硼酸(11)产生芳基自由基. 随后,芳基自由基与硒粉(10)反应,生成芳基硒自由基(13). 自由基中间体(13)与反应底物[9]发生自由基加成反应,然后经历分子内环化产生最终产物3-芳基硒化苯并噻吩类化合物(12). 该反应表明可以通过芳基自由基实现硒粉的活化,生成活性的芳基硒自由基,为含硒有机化合物的构筑提供了新思路.
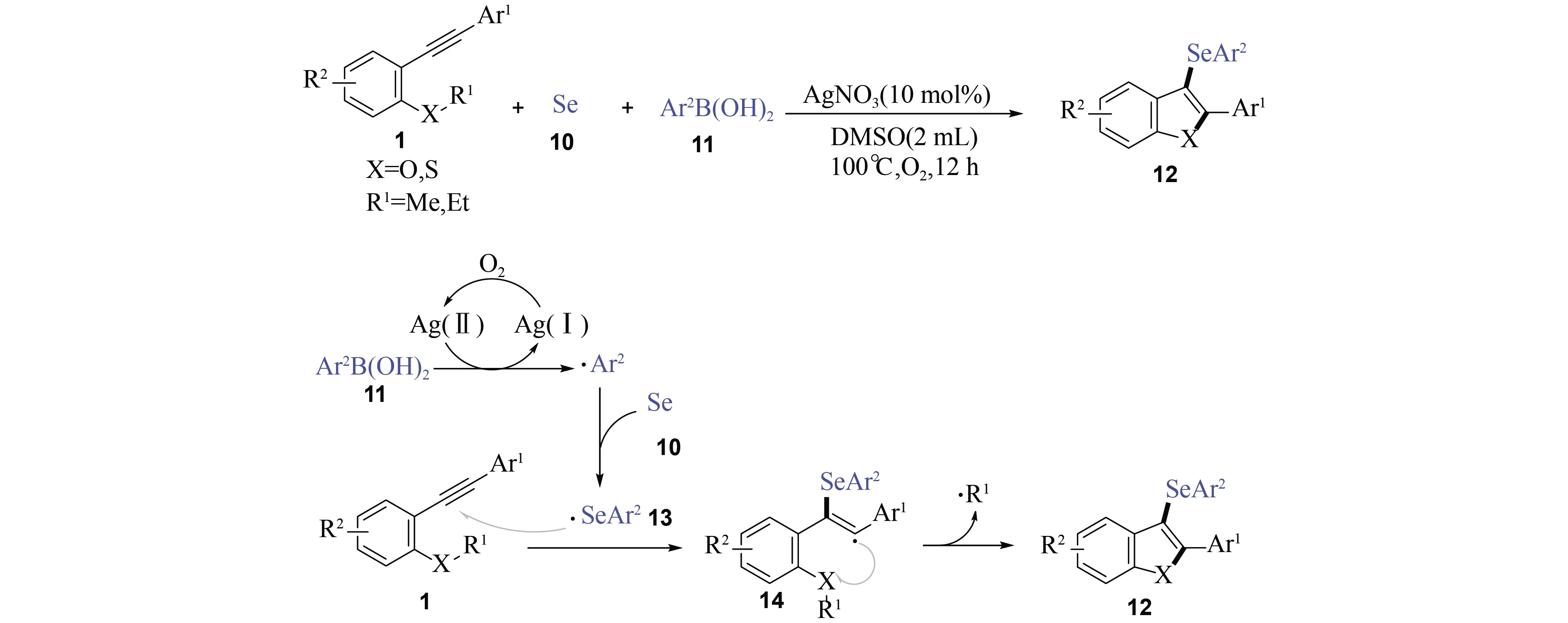
图4 3-芳基硒化苯并呋喃(噻吩)类化合物的合成
同年,厦门大学高玉珍等[21]采用当量Ag2O为氧化剂,实现了2-炔基苯硫(硒)醚与二芳基氧膦(15)的自由基串联环化反应(图5). 该反应同时构建了C-P键和C-S/Se键,以较好的产率和良好的官能团兼容性成功地合成系列3-膦酰化苯并噻(硒)吩类化合物. 对反应机理的研究表明二芳基氧膦(15)首先在Ag2O促进下生成膦酰自由基(17). 类似地,膦酰自由基(17)与2-炔基苯硫(硒)醚[9]发生反应,经历自由基加成、分子内环化等步骤,产生3-膦酰化苯并噻(硒)吩类化合物(16). 虽然该反应为3-膦酰化苯并噻(硒)吩的合成提供了新方法,但是需要使用三氟醋酸(TFA)为反应溶剂,并且消耗当量的银盐,在一定程度上限制了其应用. 针对该催化体系的局限,最近我们课题组[22]发现在可见光照射下以2,4,5,6-四(9-咔唑基)间苯二腈(4CzIPN)为催化剂,过氧化十二酰(LPO)为氧化剂,在水相中可以高效实现该反应,有效地避免了当量Ag2O和TFA的使用.
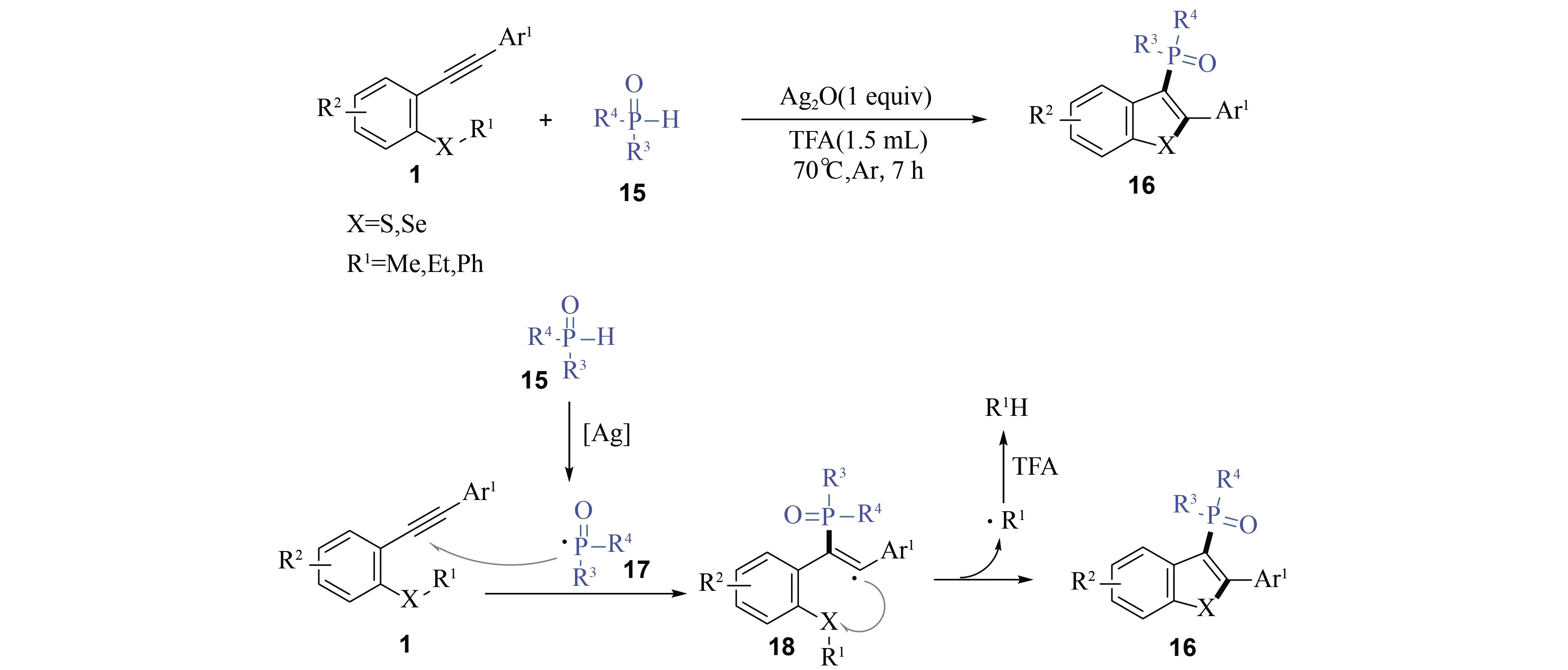
图5 3-膦酰化苯并噻(硒)吩类化合物的合成
最近,黄焰根课题组[23]以2-炔基硫醚[9]与三氟甲基硫醇银(19)为反应物,在过硫酸钾(K2S2O8)为氧化剂的条件下,合成系列3-三氟甲硫化苯并噻吩类化合物(20)(图6). 相较于此前的反应体系,该反应表现出更好的取代基兼容性. 当取代基Ar1为2-噻吩基和3-噻吩基时,该反应也能分别以65%和67%的产率生成相应的含噻吩取代基的3-三氟甲硫化苯并噻吩类化合物.
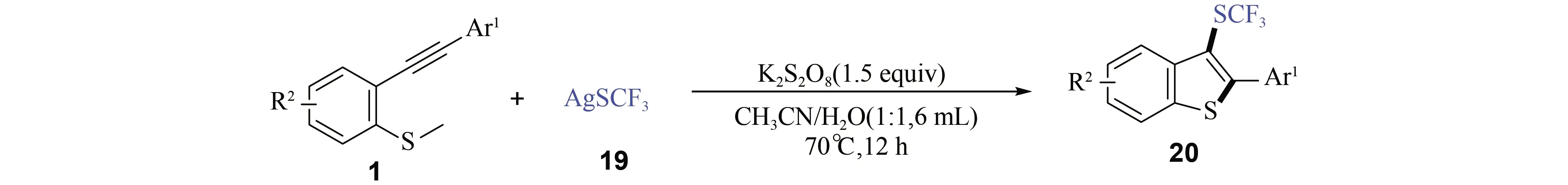
图6 3-三氟甲硫化苯并噻吩类化合物的合成
太阳能是一种理想的绿色能源,因此将相对温和的太阳光(或可见光)直接应用到有机合成中,会使反应更加的绿色与经济[24-27]. 针对2-甲硫基芳炔化合物的自由基串联环化反应,除了上述氧化剂介导、银促进的反应方法之外,近年来人们也发展了可见光诱导的反应方法. 例如,2017年Almendros和Alcaide课题组[28]在可见光诱导下,使用金和钌的双金属催化体系实现了2-炔基硫(硒)醚(21)与氟硼酸重氮盐(22)的串联环化反应,合成2,3-二芳基取代的苯并噻(硒)吩类化合物(23). 在图7所示机理中,在氟硼酸重氮盐(22)与可见光诱导下产生的激发态光敏剂[RuL3]2+*通过单电子转移(SET)作用,释放N2并生成芳基自由基.Ar1(24)和[RuL3]3+. 接着,芳基自由基(24)与Au(I)催化剂(25)发生氧化加成,生成Au(II)自由基中间体(26). 随后[RuL3]3+通过SET作用将中间体(26)氧化为强亲电性的Au(III)中间体(27),自身被还原成光敏剂[RuL3]2+,完成光催化循环. Au(III)中间体(27)与反应底物(21)中的C≡C键配位生成配合物
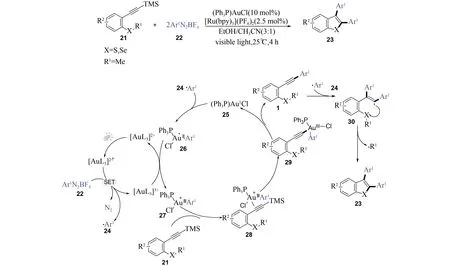
图7 2,3-二芳基取代的苯并噻(硒)吩类化合物的合成
(28),随后经过C-Si键的金属化得到中间体(29). 中间体(29)发生还原消除得到2-甲硫基芳炔中间产物[9]并重生Au(I)催化剂(25). 随后芳基自由基.Ar1(24)进一步与2-甲硫基芳炔中间体[9]经历自由基加成、分子内环化等步骤生成2,3-二芳基取代的苯并噻(硒)吩类化合物(23),并释放出烷基自由基. 该反应通过可见光诱导的Au/Ru双金属催化,在温和条件下为合成2,3-二芳基取代的苯并噻(硒)吩类化合物提供高效的新方法.
2018年,华侨大学宋秋玲课题组[29]采用Ir(Ⅲ)的配合物作为光催化剂,在室温下通过可见光诱导以2-甲硫基芳炔[9]与芳基磺酰氯(31)为反应物,在乙腈中反应24 h,通过自由基串联环化反应实现了3-磺酰化苯并噻吩类化合物(3)的合成(图8). 在可见光下Ir(Ⅲ)光催化剂通过金属-配体电荷转移(MLCT)作用产生相应的激发态Ir(Ⅲ)*. 然后,Ir(Ⅲ)*与苯磺酰氯(31)通过单电子转移(SET)产生磺酰基自由基(4),同时Ir(Ⅲ)被氧化成Ir(Ⅳ). 类似地,磺酰基自由基(4)与2-甲硫基芳炔[9]经历自由基加成、分子内环化等步骤,生成3-磺酰化苯并噻吩(3),并释放出烷基自由基去还原Ir(Ⅳ),重生光催化剂Ir(Ⅲ). 该反应以芳基磺酰氯(31)为磺酰化试剂,在温和的条件下以较高的产率实现3-磺酰化苯并噻吩的合成,最高产率可达95%. 值得注意的是,该方法也同样适用于合成3-磺酰化苯并硒吩.
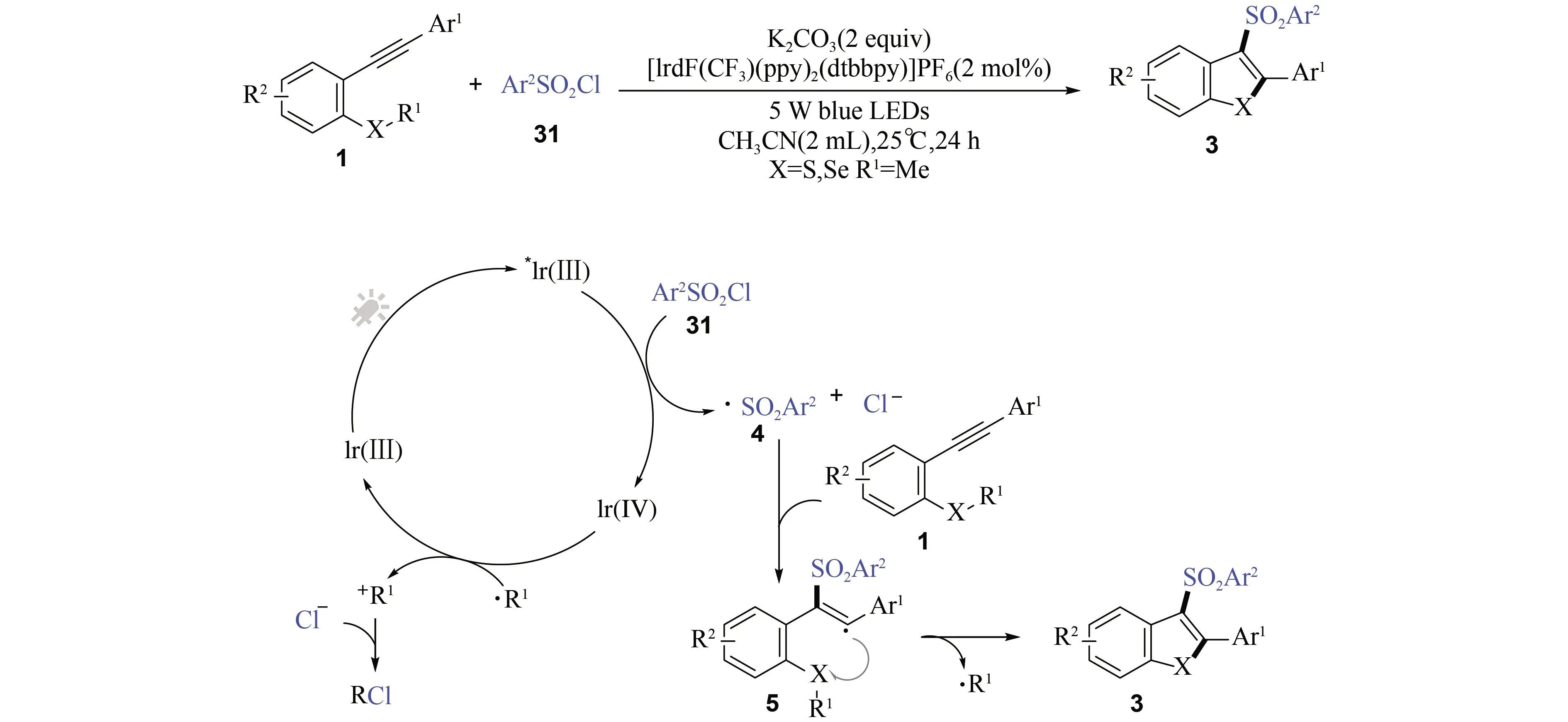
图8 3-磺酰化苯并噻(硒)吩类化合物的合成
值得注意的是,上述研究中反应物2-甲硫基芳炔[9]的甲基在反应中并未得以利用,而是以相应的烷基自由基的形式释放出来生成相应的副产物. 为了充分提升反应的原子利用率,最近台州学院吴劼课题组[30]采用焦亚硫酸钠(Na2S2O5,32)作为烷基自由基的受体,在可见光诱导下以Ru(bpy)3Cl2为光催化剂,MeSO2Na为添加剂,实现了2-甲硫基芳炔[9]的甲磺酰化串联环化反应,合成3-甲磺酰化苯并噻吩类化合物(33)(图9). 其中,光催化剂Ru(bpy)3Cl2在可见光诱导下产生激发态,通过单电子转移(SET)氧化甲基亚磺酸盐,产生甲基磺酰自由基(34). 甲基磺酰自由基(34)直接与2-甲硫基芳炔[9]发生自由基加成、串联环化反应,生成目标产物3-甲磺酰化苯并噻吩类化合物(33),并释放出甲基自由基. 值得关注的是,在环化过程中释放的甲基自由基与焦亚硫酸钠(32)产生的SO2作用,再次生成甲基磺酰自由基(35),可以再次与2-甲硫基芳炔[9]发生自由基加成,经历烯基自由基中间体(36)的分子内环化,生成产物3-甲磺酰化苯并噻吩(33)并释放出甲基自由基. 通过甲基自由基的接力循环过程,逐步消耗反应物完成反应. 该反应不仅以较高产率得到3-甲磺酰化苯并噻吩类化合物(33)(产率最高可达96%),还能将反应物中的烷基转移到到目标产物中,提升了反应的原子经济性. 遗憾的是,当Ar1为吡啶或者烷基时(如叔丁基,三甲基硅基、酯基)时,没有得到预期产物. 主要原因可能是当Ar1为芳基时,烯基自由基中间体(36)近似于苄基自由基,相对较稳定,有助于进一步发生分子内环化.
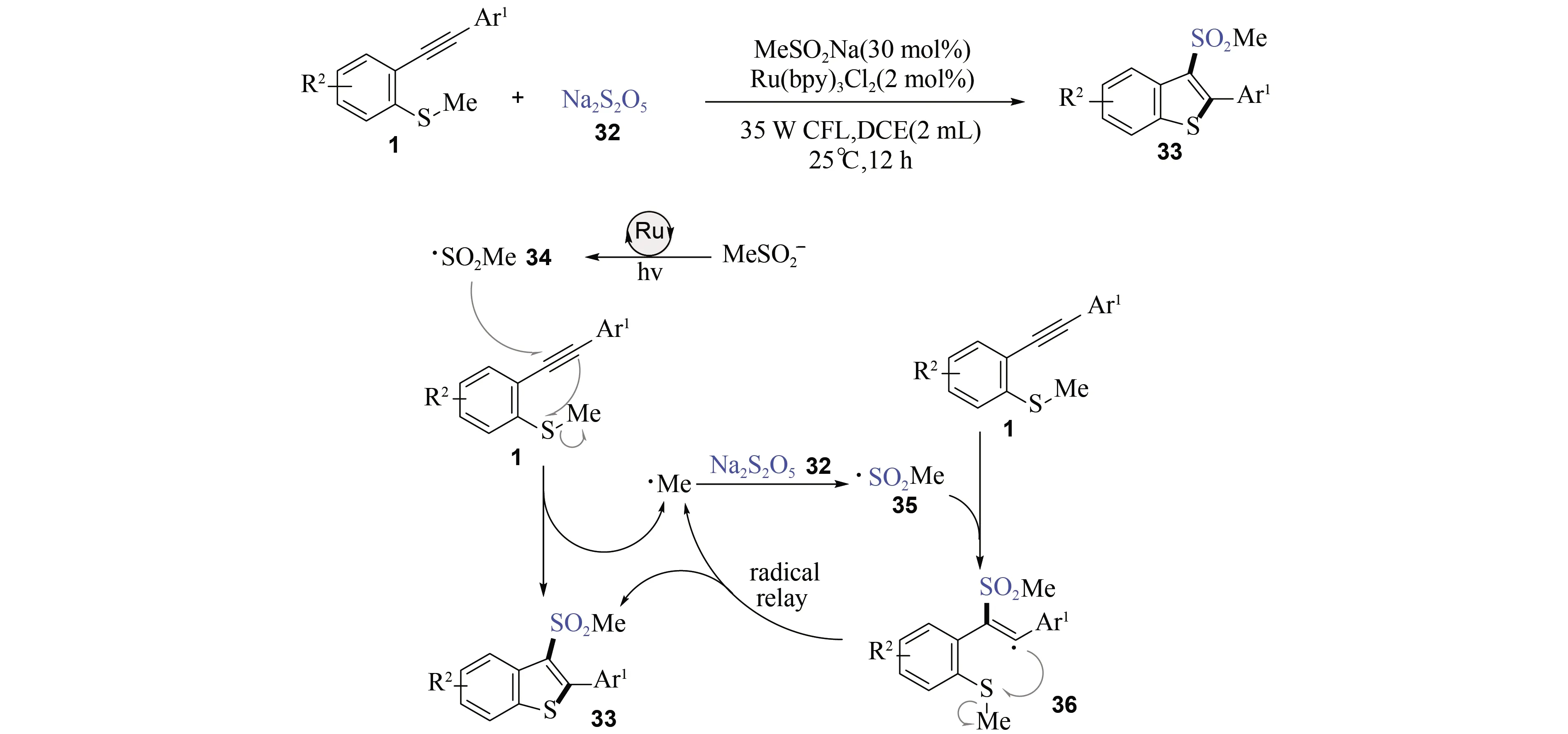
图9 3-甲磺酰化苯并噻吩类化合物的合成
2 六元环的构筑
黄酮类化合物存在于众多天然产物分子中,是一类生物活性分子和极具潜力的药物骨架. 因此,发展黄酮类衍生物的合成新方法具有重要的应用价值. 上述提及的反应中,采用2-甲硫基芳炔[9]为反应物,通过自由基串联环化反应可以很容易地构建五元杂环. 如果在反应物中再增加一个碳原子,则有可能通过类似的自由基串联环化反应一步实现六元杂环的构筑. 因此,以2-甲硫基芳炔酮(37)为反应物有望合成3-取代硫(硒)杂黄酮类化合物. 例如,2017年,Alcaide和Almendros等[28]率先采用2-甲硫基芳炔酮(37)为反应底物,在可见光诱导下采用金和钌的双金属催化体系,实现了其与氟硼酸重氮盐(22)的串联环化反应,合成2,3-二芳基(硫杂)黄酮类化合物(38)(图10).
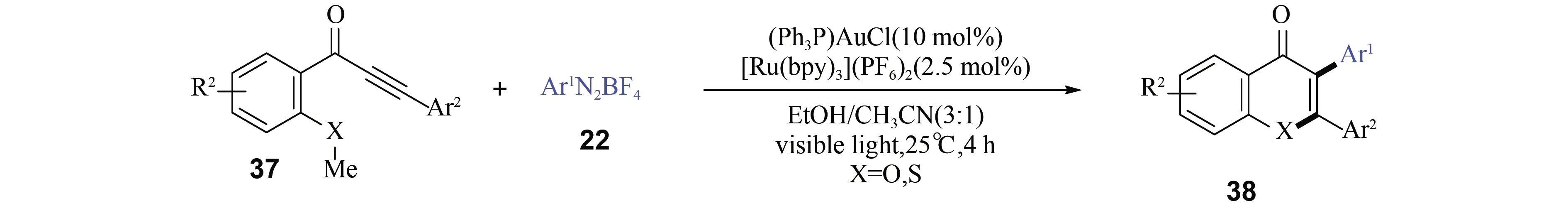
图10 2,3-二芳基(硫杂)黄酮类化合物的合成
2019年,华侨大学宋秋玲课题组[31]以2-甲硫(硒)基芳炔酮(37)为反应底物,发展了一系列反应方法合成各类官能团化的3-取代硫(硒)杂黄酮类化合物,极大的丰富了硫(硒)杂黄酮类化合物的合成方法(图11). 例如,通过银催化、氧化剂、光催化等手段可以引发二芳基膦氧(15)、芳基硫醇(40)、溴代二氟乙酸乙酯(42)、芳基醛(44)等自由基前体产生相应的膦酰自由基、芳基硫自由基、.CF2CO2Et自由基、芳酰基自由基,并发生自由基加成、串联环化等步骤,以良好的收率生成相应的3-膦酰化(39)、3-芳基硫醚化(41)、3-二氟乙酸乙酯化(43)、3-酰化(45)硫(硒)杂黄酮类化合物.
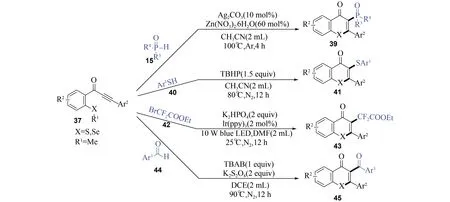
图11 3-取代硫(硒)杂黄酮类化合物的合成
此外,2-甲硫基芳炔酮(37)与三氟甲基硫醇银(19)在过硫酸铵为氧化剂的作用下反应12 h,可以合成3-甲硫基化硫杂黄酮(46)(图12)[23]. 该反应中,三氟甲基硫醇银(19)在氧化剂的作用下,产生三氟甲基硫基自由基中间体(47),自由基(47)与2-甲硫基芳炔酮(37)经历与上文类似的自由基加成/串联环化历程,生成3-甲硫基化硫杂黄酮(46).
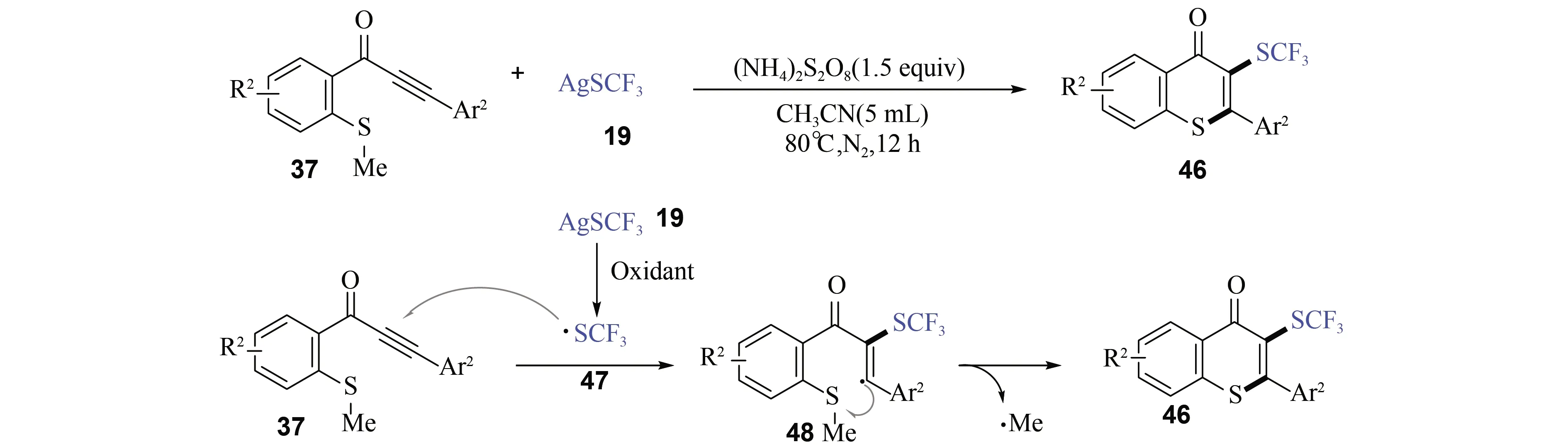
图12 2-三氟甲硫基化硫杂黄酮类化合物的合成
虽然上述研究工作为3-位官能团化硫杂黄酮的合成提供了高效的合成方法,但是上述方法都在传统有机溶剂中进行,并且多数催化体系中需要使用金属催化剂或者高温. 针对前人方法中的局限,我们课题组结合绿色化学和光合成方面的基础,采用绿色溶剂为反应介质在可见光诱导下实现了3-位官能团化硫杂黄酮的合成.例如,在可见光诱导下以2,4,5,6-四(9-咔唑基)-间苯二腈(4CzIPN)为光敏剂,过氧化十二酰(LPO)为氧化剂,可以实现水相中3-膦酰化硫杂黄酮的合成(图13)[32]. 该反应的关键在于在可见光照射下基态光敏剂(4CzIPN)受激发,产生相应的激发态 [4CzIPN]*. 由于[4CzIPN]*具有较高的氧化还原电势(E1/2(P*/P-)=+ 1.35 VvsSCE)[33,34],可以对二芳基氧膦(15)进行单电子氧化,产生膦酰基自由基(17)和[4CzIPN].-. 随后过氧化十二酰(LPO)将[4CzIPN].-氧化为基态光敏剂4CzIPN,完成光催化循环. 值得一提的是,水作为绿色溶剂可以回收再使用. 这种水相光催化体系不仅适用于3-膦酰化硫杂黄酮的合成,还适用于膦酰化含氮杂环的合成(包括氧化吲哚、喹啉二酮以及苯并噻唑等).

图13 3-膦酰化硫杂黄酮类化合物的水相合成
此外,基于我们对磺酰化反应的研究[35],最近我们使用乙二醇(EG)为绿色溶剂,在蓝光诱导下,以[Acr+-Mes] ClO4-作为无金属光敏剂,过硫酸钾或者氧气为氧化剂,实现了2-甲硫基芳炔酮(37)与芳基磺酰肼(50)的自由基串联环化反应,成功合成3-磺酰化硫杂黄酮类化合物(51)[36]. 荧光淬灭实验表明反应物(37)为该反应中的淬灭剂. 因此,结合实验提出如图14的反应机理,基态的光敏剂(Acr+-Mes)在蓝光照射下产生激发态的光敏剂中间体(Acr•-Mes•+). 在Acr•-Mes•+作用下,反应物(37)经过单电子氧化生成中间体(52). 另一方面,芳基磺酰肼(50)在过硫酸钾氧化下产生磺酰基自由基(4). 随后中间体(4)通过单电子还原生成磺酰负离子ArSO2-(53). 关键中间体(52)和(53)经过自由基加成、分子内环化产生目标产物3-磺酰化硫杂黄酮类化合物(51). 类似地,我们也发现该方法具有良好的普适性,相同条件下能以良好的收率合成3-磺酰化氧化吲哚和3-磺酰化喹啉衍生物.
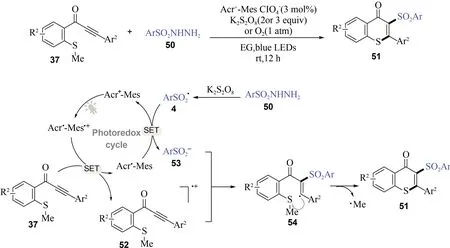
图14 3-磺酰化硫杂黄酮类化合物的合成
3 结论与展望
综上所述,2-甲硫基芳炔和2-甲硫基芳炔酮类化合物具有丰富的反应性:通过化学催化和光催化等手段产生各类自由基(如膦酰自由基、磺酰基自由基、酰基自由基、芳基自由基等),对2-甲硫基芳炔类化合物中的C≡C键加成,随后发生分子内环化,可以生成3-取代苯并呋喃、3-取代苯并噻吩、3-取代苯并硒吩、3-取代黄酮、3-取代硫杂黄酮、3-取代硒杂黄酮等杂环化合物. 虽然这方面的研究已经取得不错的进展,但是现有方法中采用的均相催化剂无法回收,绿色溶剂的应用相对较少. 从绿色可持续发展的角度看,对于2-甲硫基芳炔、2-甲硫基芳炔酮类化合物的自由基串联环化反应,仍然需要开发出溶剂绿色、催化剂廉价易得可回收、反应条件温和的高效催化体系. 此外,虽然光催化等手段在该领域已经有所利用,但是电催化方法目前尚无报道. 相信在不久的将来,2-甲硫基芳炔类化合物的自由基串联环化反应可以更加绿色高效,为多种杂环化合物的合成提供新方法.

