‘东方美人’茶茶渣对甲基紫的吸附性能
刘成顺, 段淑敏, 王树茂, 谢振邦, 韩 华, 柯子星
(1.福建农林大学安溪茶学院,福建 安溪 362406;2.浙江大学茶叶研究所,浙江 杭州 310000)
甲基紫(也称结晶紫、龙胆紫等)是一种三苯甲烷类碱性染料,在生产、生活中用途广泛,常用于印染工业、纺织工业、金属冶炼、医用消毒和化学品分析[1-2]。甲基紫常见于染料废水,在自然条件下很难降解,并对人体有潜在毒性和致癌作用[3]。目前处理印染废水的方法有吸附法[4]、生物法[5]、电化学法[6]、膜分离法[7]等。吸附法能耗较低、操作简单且无二次污染,因此被普遍应用。
‘东方美人’茶是台湾名茶,加工工艺独特,是发酵程度最高的乌龙茶,发酵程度介于一般乌龙茶和红茶之间。在制作及冲泡过程中,茶叶叶片表面的蜡质和可溶于水的小分子被消除掉,原有的致密结构发生改变,暴露出网状的纤维结构和一些特定的具有螯合或吸附功能的基团,因此具备较好的吸附潜能[8]。废弃茶渣作为一种生物吸附剂,广泛应用于孔雀绿[9]、酸性橙Ⅱ[10]等染料和重金属离子[11]的废水处理。本试验以‘东方美人’茶茶渣为吸附剂,研究其对甲基紫的吸附性能。
1 材料与方法
1.1 主要仪器和材料
1.1.1 主要仪器 UV-1750紫外可见光分光光度计(日本岛津);PRACTUM224-1CN电子天平(北京赛多利斯科学仪器有限公司);Eppendorf 5430/5430R高速冷冻离心机(德国艾本德股份有限公司);IS-RDD3台式恒温振荡器(美国精骐有限公司);电热鼓风干燥箱(上海一恒科学仪器有限公司)。
1.1.2 材料 ‘东方美人’茶干茶,购于东和农业有限公司;甲基紫,购于天津市北辰方正试剂厂;七水合硫酸锌、五水合硫酸铜和硫酸铵镍等试剂为分析纯;实验用水为蒸馏水。
1.2 茶渣的处理和茶渣粉末的制备
将试验所需的‘东方美人’茶干茶充分浸煮并不断更换滤液至滤液无色,收集茶渣用烘箱在120 ℃下干燥;将烘干后的茶渣用茶叶粉碎机粉碎呈粉末状,过80目分样筛。将处理好的茶渣粉末用封口袋密封,并放入干燥皿保存。
1.3 吸附实验
用电子天平准确称取一定量的茶渣粉末,放入150 mL的锥形瓶中,加入50 mL一定浓度的甲基紫溶液,一定温度下200 r·min-1振荡60 min(吸附时间试验除外),振荡后用离心机分离,5 000 r·min-1离心5 min。离心后取上清液,放入紫外可见光分光光度计,在波长为584 nm处测定吸光值并代入标准曲线,计算吸附率和吸附量(qe)。
吸附率/%=(C0-Ce)/C0×100
(1)
qe=V×(C0-Ce)/m
(2)
式中,C0为甲基紫溶液的初始浓度/(mg·L-1);Ce为吸附平衡时溶液中甲基紫的浓度/(mg·L-1);qe为茶渣吸附容量/(mg·g-1);V为甲基紫溶液的体积/L;m为茶渣质量/g。
2 结果与分析
2.1 吸附时间对甲基紫吸附效果的影响
在150 mL锥形瓶中加入0.2 g茶渣,再分别加入50 mL 100、300、600 mg·L-1甲基紫溶液,在25 ℃下恒温振荡吸附。振荡一定时间后取出离心,测定吸附率和吸附量(图1)。从图1可见,吸附率和吸附量与吸附时间呈正相关关系,随着吸附时间的延长,吸附量最高可达142.70 mg·g-1,表明茶粉是良好的生物吸附剂。从图1还可见,120 min时基本达到平衡,因此确定120 min为吸附平衡时间。虽然120 min时达到吸附平衡最大值,但60 min时吸附量已经接近最大值,60 min后增长幅度很小。综合考虑时间成本和经济效益,选定60 min为吸附时间。
2.2 茶渣粉末添加量对甲基紫吸附效果的影响
分别将0.05、0.1、0.2、0.3、0.4、0.5 g茶渣粉末与50 mL 100、600和1 500 mg·L-1甲基紫溶液混合,25 ℃下振荡60 min,离心测定不同茶渣粉末添加量对甲基紫吸附性能的影响。从图2可知,吸附率随投茶量的增加而升高,而吸附量随添加量增加而下降。当茶渣粉末达到0.5 g时,吸附量和吸附率基本达到平衡。由于随着茶渣粉末的增加,茶渣粉末的比表面积增大,可利用的吸附位增多,有利于与甲基紫充分结合,因此吸附率增加明显;茶渣粉末的增加可能导致茶渣粉末吸附位点的重叠或聚集,使得能够与甲基紫结合的总面积减少,因此吸附量下降[12]。试验中,0.1 g茶渣粉末吸附效果比0.2 g更好。由于0.1 g茶粉质量太小且茶粉比重较轻,为了后续方便对茶粉的光谱分析,综合考虑经济成本和吸附效果,以0.2 g为茶渣粉末添加量。
2.3 温度对甲基紫吸附效果的影响
50 mL初始浓度为100、600和1 500 mg·L-1的甲基紫溶液中加入0.2 g茶渣粉末进行振荡吸附,分别在15、25、30、40和50 ℃下恒温振荡60 min后离心。从图3可知,随着温度升高,茶渣对甲基紫的吸附量有较小增长,推测茶渣对甲基紫的吸附过程为吸热反应,温度升高有利于吸附。
2.4 金属离子浓度对甲基紫吸附效果的影响
添加不同浓度的Cu2+和Zn2+模拟废水中的重金属离子。常温下,分别将含有10 mg·L-1Cu2+、50 mg·L-1Zn2+的甲基紫溶液(600 mg·L-1,50 mL)加入0.2 g茶渣粉末恒温振荡60 min。从图4可知,随着金属离子浓度的提高,吸附率和吸附量均降低;加入Zn2+的吸附率和吸附量下降更明显。纵向比较150、300 mg·L-1可知,相同条件下,Zn2+对吸附效果影响更不利,Cu2+影响小,这可能是由于2种金属离子的金属活性不同(金属活性:Zn2+>Cu2+)。金属活性越高,金属离子与染料阳离子竞争吸附越激烈,破坏了原有的吸附平衡,导致茶渣对甲基紫的吸附率和吸附量下降[13]。
2.5 茶渣对甲基紫的吸附性能
2.5.1 热力学参数 根据公式(3)和(4)计算甲基紫的吸附热力学方程。根据公式(5)对甲基紫在茶渣粉末上的吸附平衡数据进行拟合,计算吸附焓变(△H)和吸附熵变(△S)(表1)。从表1可见,△H在4.44~5.81 kJ·mol-1之间,说明吸附甲基紫的过程为物理吸附过程[14];△S>0,表明为吸附熵增过程;△G<0,表明吸附过程可以自发进行;△G负值随温度升高而增大,表明高温有利于反应的自发进行。
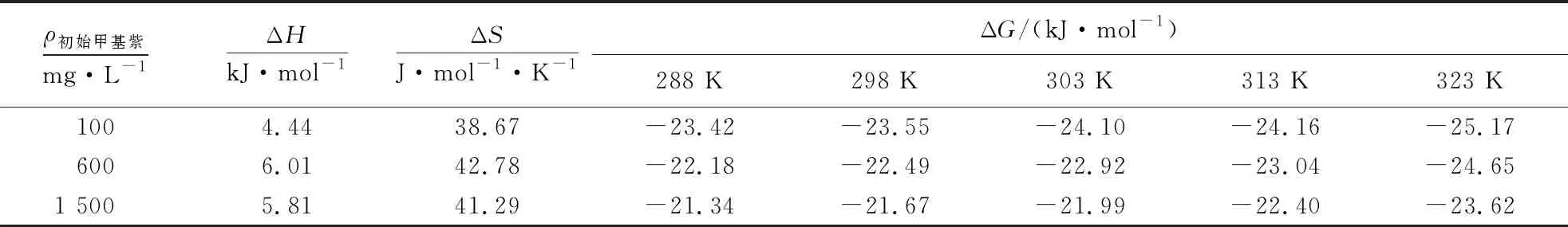
表1 甲基紫吸附的热力学参数Table 1 Thermodynamic parameters for methyl violet adsorption
△G=-RTlnKd
(3)
(4)
(5)
式中,△G为吸附自由能变/(kJ·mol-1);R为气体常数(8.314 J·mol-1·K-1);T为绝对温度/K;Kd为吸附平衡常数;Ca为平衡状态下吸附质在固相吸附剂上的浓度/(mg·L-1);Ce为吸附平衡时溶液中甲基紫的浓度/(mg·L-1);△H为吸附焓变/(kJ·mol-1);△S为吸附熵变/(J·mol-1·K-1)。
2.5.2 吸附等温线 Langmuir为单层分子吸附模型[15];Freundlich等温方程是个可应用于多层吸附情况的经验公式[16],其线性表达式见公式(6)、(7)。对吸附平衡数据进行拟合,相关参数的计算结果见表2。从表2可见,‘东方美人’茶茶渣对甲基紫的吸附等温线符合Langmuir和Freundlich吸附等温式,说明对甲基紫的吸附是一个由单层吸附到多层吸附的吸附过程。根据Freundlich理论,n=1.245 2,容易吸附[17]。

表2 Langmuir和Freundlich等温吸附模型相关参数Table 2 Simulation parameters of Langmuir and Freundlich isotherm adsorption models
(6)
(7)
式中,qm为单位吸附剂单分子层饱和吸附量/(mg·g-1);b为Langmuir常数/(L·mg-1);n为Freundlich参数;Kf为Freundlich参数/(mg·g-1)。
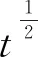

表3 甲基紫吸附的动力学模型相关参数Table 3 Fitting parameters of various kinetics models for methyl violet adsorption
(8)
(9)
(10)

3 结论
本研究于常温常压下,添加0.2 g‘东方美人’茶茶渣对50 mL甲基紫溶液进行吸附,于120 min达到吸附平衡点,其吸附效率可达90%以上。添加不同浓度的Cu2+和Zn2+模拟废水中的重金属离子,发现金属离子的加入对吸附产生不利影响,可能由于金属离子与染料阳离子竞争吸附,破坏了原有的吸附平衡,导致吸附率和吸附量下降。‘东方美人’茶茶渣和甲基紫之间的吸附行为符合Langmuir与Freundlich模型描述,表明对甲基紫的吸附行为主要发生在吸附剂表面的单分子层,同时伴随少量的多层吸附。通过动力学与热力学的分析表明,准二级动力学方程较适合茶粉对甲基紫的吸附,同时吸附过程为自发性的吸热反应,存在物理吸附和化学吸附。

