内镜下黏膜切除术治疗老年胃肠道息肉的临床效果及对血清炎症因子与预后的影响
魏 晟,董丽凤,胡艳婕,蒋大健,臧 杰,谢 俏
胃肠道息肉为胃肠道内出现的隆起病变,发病早期常无明显症状,若未接受治疗,后期容易导致消化道出血,甚至会发生癌变[1]。临床上治疗本病常应用内镜下电凝切除术,但是因为切除深度把握存在难度,常导致患者消化道穿孔或病灶切除不完全等,所以采用此种术式治疗胃肠道息肉效果与术者手术经验、技术关系密切[2-3]。老年患者因为身体器官功能退化,免疫力下降,围术期容易出现各种并发症,所以寻找一种治疗效果优异且安全性高的术式对于提高老年胃肠道息肉患者治疗效果意义重大。现内镜下黏膜切除术逐渐大量应用于胃肠道息肉治疗中,其将电凝切除与黏膜注射两种方式有机结合,具有微创、安全、易于开展等优势[4-5]。本研究比较老年胃肠道息肉患者行普通内镜电凝切除术与内镜下黏膜切除术治疗的效果,以明确内镜下黏膜切除术在老年胃肠道息肉治疗上的优劣,为临床应用提供参考。
1 资料与方法
1.1一般资料 选取2016年6月—2019年6月我院收治160例老年胃肠道息肉患者。纳入标准:①内镜确诊为胃肠道息肉;②具有普通内镜电凝切除术或内镜下黏膜切除术手术指征;③息肉直径5~22 mm;④患者同意参与本研究,并签署知情同意书。排除标准:①已接受过内镜下黏膜切除术治疗者;②内镜检查显示患者黏膜存在显著浸润;③存在内镜检查禁忌证者;④凝血功能异常者;⑤采用其他方式治疗者。依据手术方式的不同将160例患者均分为研究组和对照组。两组一般资料比较差异无统计学意义(P>0.05),具有可比性,见表1。本研究获得医院伦理委员会批准同意进行。
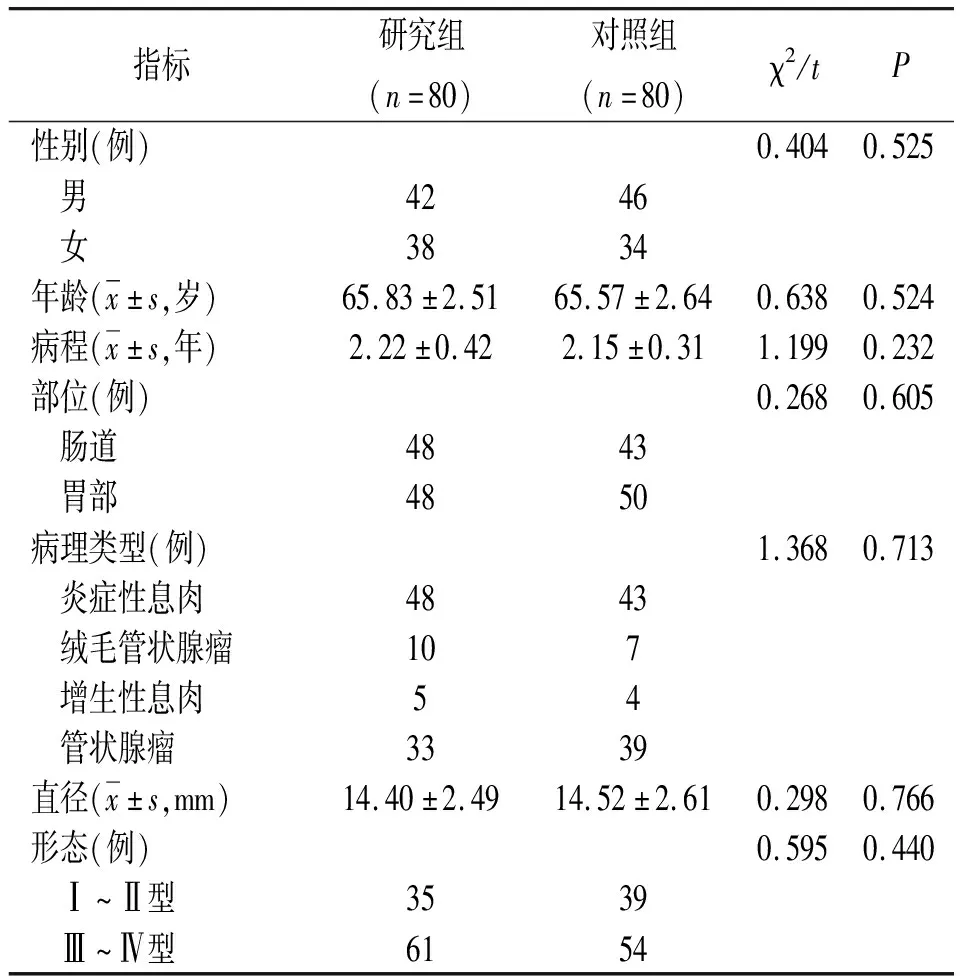
表1 不同术式治疗的老年胃肠道息肉两组一般资料比较
1.2治疗方法 ①对照组采用普通内镜电凝切除术治疗,将GIF-XQ230-2型胃镜(日本奥林巴斯公司生产)或VME-1300型电子结肠镜(上海涵飞医疗器械有限公司生产)置入后探查息肉,探查到息肉后在距离息肉边界2 mm处采用高频电刀进行切除操作,切除时注意达到黏膜上层但不要伤及肌层,后进行止血操作。②研究组采用内镜下黏膜切除术治疗,采用PCF-Q240Z型内镜(日本奥林巴斯公司生产)进行息肉探查与对照组相同,在息肉基底选择1~4个位点,将比例为1/10 000的肾上腺素/0.9%氯化钠注射液沿位点注入,待注射完成息肉基底完全隆起、肌层与黏膜分离后,将息肉基底采用套圈器套牢,选择高频电流切除息肉组织,较大息肉可行多次充分切除。手术完成后观察创面2 min,有出血情况发生及时止血,若出血轻微可用0.8%去甲肾上腺素溶液冲洗。
1.3观察指标 ①息肉切除情况:包括整块切除率与完整切除率。整块切除:镜下观察病变被整块切除,获得一个标本;完整切除:内镜观察息肉完全被切除,病理检查示切除样本基底及外侧边界未受到病变累及。②围术期指标:包括息肉切除时间、手术时间、出血量、术后开始进流食时间及住院时间,其中息肉切除时间为黏膜注射针插入后或高频电刀开始切除至息肉切除结束时间。③炎症因子:手术前与手术结束后收集两组晨起空腹静脉血离心后血清,采用酶联免疫吸附法测定降钙素原(PCT)、白细胞介素-6(IL-6)、C反应蛋白(CRP)、白细胞介素-17(IL-17)水平。④并发症:包括术后出血、感染、切口过深,其中切口过深为切口达基底黏膜肌层。⑤预后情况:两组患者术后均接受随访,随访终点为2019年12月31日,记录两组患者随访期间息肉复发情况。
2 结果
2.1两组息肉切除情况比较 研究组息肉整块切除率与完整切除率均高于对照组,差异有统计学意义(P<0.05或P<0.01),见表2。
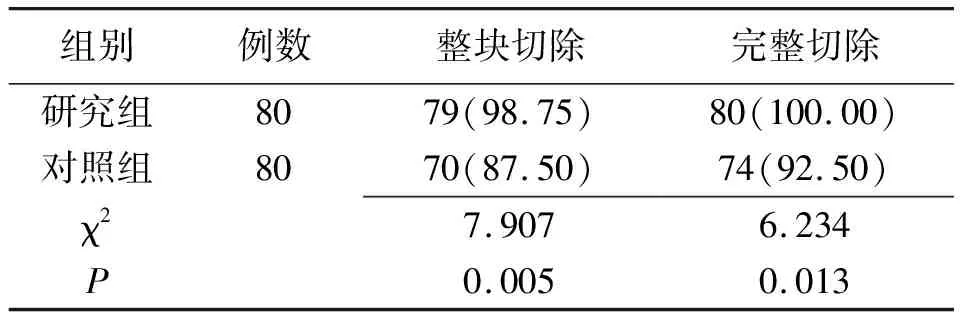
表2 不同术式治疗的老年胃肠道息肉两组息肉切除情况比较[例(%)]
2.2两组围术期相关指标比较 研究组息肉切除时间、手术时间、手术后开始进流食时间均短于对照组,出血量少于对照组,差异均有统计学意义(P<0.01),两组住院时间比较差异无统计学意义(P>0.05),见表3。

表3 不同术式治疗的老年胃肠道息肉两组围术期相关指标比较
2.3两组手术前后炎症因子水平比较 两组术前PCT、IL-6、CRP及IL-17水平比较差异无统计学意义(P>0.05)。术后两组PCT、IL-6、CRP及IL-17水平均显著上升,且研究组上述指标升高程度小于对照组,差异均有统计学意义(P<0.01)。见表4。

表4 不同术式治疗的老年胃肠道息肉两组手术前后炎症因子水平比较
2.4两组术后并发症比较 研究组术后并发症发生率为7.50%低于对照组术后并发症发生率22.50%,差异有统计学意义(χ2=7.059,P=0.008),见表5。

表5 不同术式治疗的老年胃肠道息肉两组术后并发症比较[例(%)]
2.5两组息肉复发情况比较 研究组随访期间息肉复发率为3.75%(3/80),对照组随访期间息肉复发率为0,两组随访期间息肉复发率比较差异无统计学意义(χ2=1.359,P=0.244)。
3 讨论
胃肠道息肉采用普通内镜电凝切除术治疗,虽然手术步骤简单,容易掌握,但是切除深度一直是该术式难点,切除过深会出现穿孔并发症,而切除过浅则易导致复发[6-8]。中老年群体胃肠道息肉发病率逐渐升高,由于老年患者身体机能下降,术后较易出现各种并发症,常导致患者手术治疗效果不佳[9-10]。
内镜下黏膜切除术为新型微创术式,其在黏膜下注射药物使息肉与正常组织分离,随后采用圈套器将其套好并切除,治疗效果优于普通内镜电凝切除术[11-13]。本研究组采用内镜下黏膜切除术治疗,患者息肉整块切除率与完整切除率均显著高于采用普通内镜电凝切除术治疗的对照组。内镜下黏膜切除术先采用黏膜下注射使病灶膨起,有效分离病灶黏膜及固有肌层,有利于圈套器圈套,便于其后息肉病灶切除[14-16]。本文发现,研究组息肉切除时间、手术时间、手术后开始进流食时间均短于对照组,出血量少于对照组。因电凝切除手术切除深度难以掌握,切除深度不当容易出现出血及穿孔等并发症,可能是造成本文对照组息肉切除时间、手术时间长及出血量多的原因之一。有研究显示,胃肠道息肉采用内镜治疗容易损伤胃肠道黏膜,组织内部炎症因子聚集,激活机体相关信号传导通路,炎症因子大量释放入血,使得患者血液中相关炎症因子水平显著升高[17-18]。本研究结果显示,术后两组PCT、IL-6、CRP及IL-17水平均显著上升,且研究组上述指标升高程度小于对照组,提示采用内镜下黏膜切除术治疗胃肠道息肉对于胃肠道黏膜损伤较轻,故能减弱炎性反应程度。
本文研究组术后并发症发生率为7.50%低于对照组术后并发症发生率22.50%,差异有统计学意义。电凝切除术切除深度不当容易导致患者息肉残留及出血发生,而内镜下黏膜切除术仅将息肉病灶黏膜切除,这可能是研究组术后出血及切口过深等并发症少的主要原因。有研究者认为,内镜下黏膜切除术整个过程中视野清晰,可清楚观察到病灶切除及出血情况并及时止血,是患者术后并发症发生率低的主要原因[19]。电凝切除术电凝时间过长容易导致患者黏膜下血管受损,同时由此所致的灼烧伤使得细胞出现变性坏死,这种坏死逐渐扩大造成术后出血及伤口感染风险增加[20]。本文还显示,两组随访期间息肉复发率比较差异无统计学意义。虽然研究组息肉切除效果较好,理论上说患者术后复发率较低,但是对于较扁平的黏膜层息肉,无明显蒂部结构,应适宜增加切除深度,减少残留以避免复发[21]。李倩等[22]研究认为,内镜下黏膜切除术可以有效提高息肉切除率,降低复发率。
综上,老年胃肠道息肉患者采用内镜下黏膜切除术治疗效果显著,患者炎性反应轻,息肉切除率高,术后并发症少,可以作为首选术式。

