中国大陆药物性肝损伤流行病学研究的现状分析*
杨 鸣 李志国 窦 豆 刘建平
1.北京中医药大学循证医学中心 (北京,100029) 2.北京中医药大学东直门医院 3.北京中医药大学中医学院
药物性肝损伤(DILI)是指由各类药物(包括化学药物、生物制剂、中草药、保健品、膳食补充剂)及其代谢产物乃至辅料等诱发的肝损伤[1,2]。由于DILI缺乏特异性的临床表现和病理特征,其诊断主要依靠排除法,即肝损伤发生前有药物应用史并排除病毒感染、酒精、免疫、遗传代谢等其他导致肝损伤的原因。我国《药物性肝损伤诊治指南(2015年版)》推荐因果关系评估法(RUCAM)用于药物和肝损伤之间因果关系的综合评价[1]。及时停用可疑伤肝药物是DILI最重要的初始治疗。
DILI是常见的药物不良反应,可导致肝功能衰竭甚至死亡。根据国外流行病学数据,DILI的发生率介于1/10万~20/10万[3,4]。最近一项研究表明,中国大陆DILI的发病率为23.8/10万,高于西方国家[5]。亚太的研究显示,中草药是韩国和新加坡引起DILI最为主要的药物[6]。我国多中心、大样本的临床回顾性研究表明,中药相关的肝损伤(HILI)在全部DILI中的构成比约为23.8%[5],其中关于HILI所占的构成比引起较大争议[7]。目前对中国大陆的DILI流行病学研究的整体情况尚不清楚,为深入了解国内DILI流行病学的研究现状,笔者基于中国知网(CNKI)和Pubmed数据库对中国大陆DILI的流行病学研究进行分析,现报道如下。
1 资料与方法
1.1 文献纳入标准 纳入的文献类型为流行病学研究,包括队列研究、病例对照研究、横断面研究、药物监测报告、数据库分析。研究目的为调查DILI的流行病学现状。无语言限制。
1.2 文献检索 中文文献的检索数据库是中国知网(CNKI),时间为从建库至2019年12月22日。检索式为:(TI=“药物性肝损伤”+“药物性肝病”+“药物性肝损害”+“药物性肝炎”+“DILI” OR AB=“药物性肝损伤”+“药物性肝病”+“药物性肝损害”+“药物性肝炎”+“DILI” OR KY=“药物性肝损伤”+“药物性肝病”+“药物性肝损害”+“药物性肝炎”+“DILI”) AND (TI =“流行病学”+“横断面”+“现况调查”+“问卷调查”+“抽样调查” +“现场调查”+“队列” OR AB =“流行病学”+“横断面”+“现况调查”+“问卷调查”+“抽样调查” +“现场调查”+“队列” OR KY =“流行病学”+“横断面”+“现况调查”+“问卷调查”+“抽样调查” +“现场调查”+“队列”)。英文文献的检索数据库是Pubmed(MEDLINE),时间为从建库至2019年12月27日。检索式为:[epidemiology (Title/Abstract)] AND [China(Title/Abstract)] AND [Chemical and Drug Induced Liver Injury (MeSH Terms)]。
1.3 图示分析 通过CNKI可视化功能,对检索的全部中文文献进行图示分析,包括发表年度、主题、研究机构,了解本领域的研究概况。
1.4 文献筛选与评价 将中、英文文献题录导入NoteExpress 3.0.4进行管理。通过阅读标题和摘要进行初筛后,进一步进行全文筛选。对文献研究特征进行归纳,主要内容包括第一作者、发表年份、研究类型、DILI的诊断和肝损伤的原因及排序。
2 结果
2.1 文献检索与CNKI可视化分析 共检索到128篇文献,其中CNKI 123篇,Pubmed 5篇。通过CNKI的可视化功能对中文文献的发表时间、主题词和发文机构进行统计。图1显示,DILI的流行病学研究从2001年开始出现,此后每年陆续有文章发表,呈现增长趋势。2016年CNKI可检索到18篇文章,达到最大值。截至目前,2019年发表文章与2016年基本持平。可见此领域越来越多地得到学界关注。
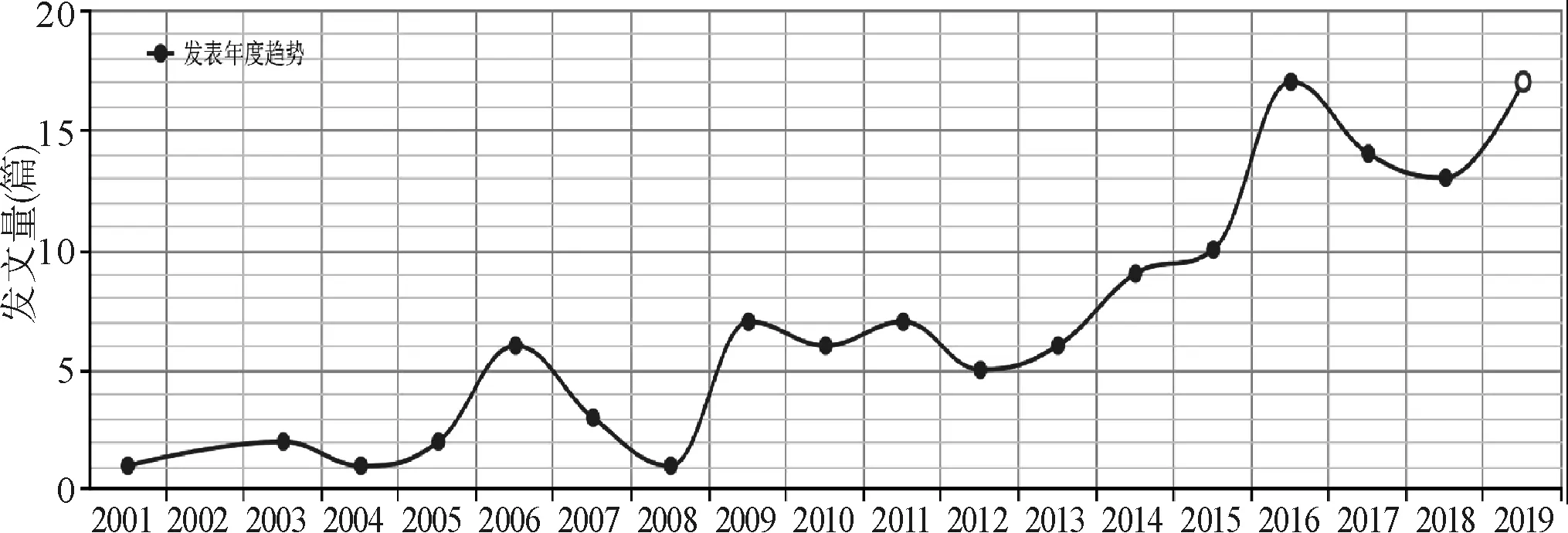
图1 CNKI DILI流行病学研究文章发表年度趋势
图2显示,排在前10位的主题词是药物性肝损伤、流行病学、DILI、肝损伤、病毒性肝炎、临床特点、抗结核药、药物性肝病、发病率和肝毒性。对于DILI的原因,抗结核药、抗感染药和中草药类别的研究较多。
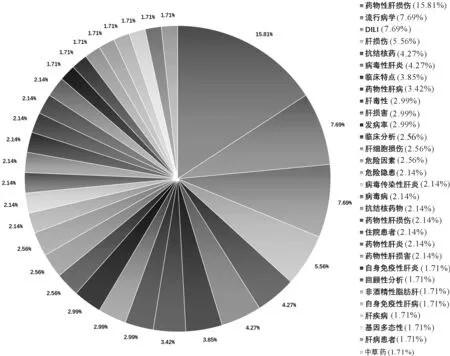
图2 CNKI DILI流行病学研究文章发表主题分布
发文机构的图表(图3)显示,复旦大学(不含附属医院)和深圳市孙逸仙心血管医院分别发文6篇,第三军医大学发文5篇,河北医科大学、北京中医药大学和郑州大学发文4篇。在中医院校中,北京中医药大学对DILI研究较多。
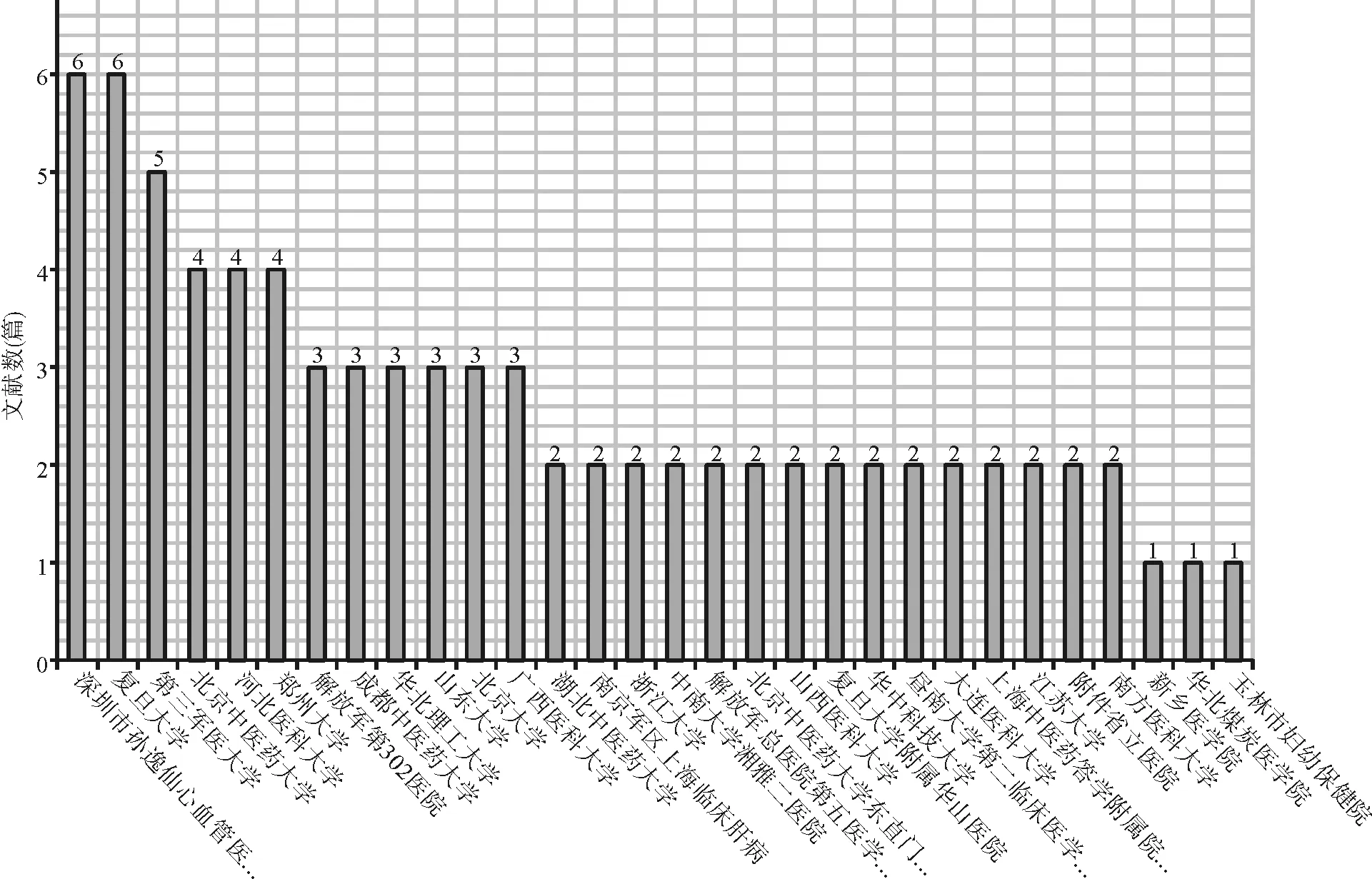
图3 CNKI DILI流行病学研究文章发表研究机构分布
2.2 纳入文献 经过题目和摘要浏览初筛,排除98篇文献,排除原因分别为综述20篇,基于文献的研究9篇,非药物所致肝损伤研究39篇,DILI的非流行病学研究4篇,无关研究25篇,重复发表1篇。经过全文浏览后,排除4篇非流行病学研究。最终纳入26篇研究进入分析。
2.3 研究特征分析
2.3.1 文献资料特征 纳入的26项研究中,中文发表24篇,英文发表2篇。2项为肺结核患者DILI的小样本前瞻性队列研究[8];1项为病例-对照研究[9];1项来源于中草药肝损伤研究云平台数据库(hilicloud.net)中三级甲等肝病专科医院的住院病例及不良反应自发上报的药物监测报告[10];其余22项为横断面研究,并对既往数据进行回顾性分析。在横断面研究中,19项研究是当地单个医院或该地区的多个医院病例资料回顾性分析,1项研究采用整群分层随机抽样方法查阅浙北地区8家医院的病例资料[9],1项研究的资料来源于东部、中部和西部的8个城市的48家医院新登记或曾经接受治疗的涂片阳性结核患者[11],1项研究的资料来源于中国大陆主要城市的308家医院[5]。各研究资料来源的时间从1995年至2017年,时间段6个月至12年。14项研究的调查总体为DILI,包括急性DILI和老年DILI,其余研究的调查总体包括白鲜皮制剂相关肝损伤、结核病患者、肝功能异常、“肝病”、非病毒性肝炎、肝炎病毒血清学阴性肝病患者及住院患者。调查总体人数为38~25 927例。
2.3.2 DILI诊断特征 6项研究(2项明确引用[12,13],4项经查证[14~17])参考了《新肝脏病学》中临床常用诊断标准[19],5项研究使用RUCAM量表[5,19~22],其中1项未报告该研究应用RUCAM量表诊断DILI的界值,2项纳入≥3分的患者,1项纳入≥6分的患者,1项纳入≥6分的患者和经临床专家小组判定的为DILI的RUCAM分数≥3分的患者;2项研究使用《药物性肝损伤诊治指南(2015年版)》[23,24],其中提及多种DILI诊断方法,但纳入研究仅引用该指南,未明确指出使用何工具进行诊断。姜慧芳[25]排除了入院有肝相关疾病诊断的病例,并根据住院期间最高ALT检测值结合药物性肝病的标准判断,葛斐林等[10]对白鲜皮制剂相关肝损伤的判断结合了患者诊断、《中草药相关肝损伤临床诊疗指南》和WHO-UMC的不良反应因果判断方法,1项研究诊断方法出处不明[9],4项研究以转氨酶升高至正常上限两倍诊断DILI[8,11,26,27],6项研究未提及如何诊断DILI[28~31]。
2.3.3 DILI发生率特征 抗结核治疗患者中DILI发生率在两项研究中分别为14.65%、20.1%,未发现其他前瞻性临床研究,无法获得可靠数据。姜慧芳[25]在住院患者3030例中鉴别出170例为DILI患者,现患率为5.61%。殷新光等[9]共调查住院患者23192 例,其中药物性肝病165例,现患率为0.71%。
2.3.4 DILI发生药物种类和不良反应 在纳入研究中,有14项研究列举了引起DILI的药物种类和不良反应事件数。大部分研究将中草药、中成药归为一类,甚至将食品补充剂与中药归为一类,西药按治疗不同疾病的方式分类。仅有1项研究将中西药分大类后,再各自对治疗不同疾病的药物进行分类研究[16]。综合13项研究的结果,各类别药物引起DILI的病例数构成比见图4(1项研究将中药和保健品归为一类,未对其结果与其他研究进行汇总[5])。其中,未分类的中药占30.0%,抗微生物药(包括抗生素、抗结核药、抗真菌药、抗病毒药)占20.4%,抗肿瘤药、解热镇痛药、心血管药和抗甲状腺药分别占6%~7%,激素类占3%,其他占21%。此外,7项研究显示,联合用药可引发DILI。见图4。

图4 各类别药物引起DILI的病例数构成比
2.3.5 不同药物在14项研究中出现的频次 见表1。中药和抗微生物药在14项研究中均被提及,抗肿瘤药、解热镇痛药和抗甲状腺药次之,心血管药物、激素和精神类药物出现在一半以上的研究中。

表1 不同药物类别在14项研究中出现的频次
2.3.6 研究机构特征情况 研究机构所在省市主要分布在华东地区,上海最多(7项),其次是浙江(3项)、四川(2项)、吉林(2项)、山东(2项)、广西(2项),其他省市如辽宁、内蒙古、北京、安徽、河南、湖北、广东、山西亦有研究发表。未见以中国大陆人群为研究总体的DILI流行病学研究。
3 讨论
本研究经过系统检索中国知网CNKI与Pubmed数据库,在流行病学研究方面,发现仅有抗结核治疗药物引起肝损伤的小样本前瞻性队列研究[8],未发现以中国大陆人群为研究总体的DILI现患率横断面研究或DILI在人群中发病率的队列研究。目前发表的研究均为基于单个、多个医院病历资料或区域性不良反应上报数据库的回顾性分析,无法得到具有全国代表性的DILI发生率。尽管病历或数据库中对于用药和肝损伤诊断信息有时间记录,但因为存在多次入院、检查未完善即开始用药、各种治疗联合应用等诸多情况,加之我国是肝病大国,不乏在原有肝病基础上的药物治疗,故此类研究难以推断用药与肝损伤的因果关系,可靠程度差。
由表1可知,调研DILI原因的大部分研究,将全部中药或全部中草药、中成药归为一类,而治疗不同系统疾病的西药则分别归类统计,这样的分类方法并不合适,可能会误导读者产生“中药是药物性肝损伤的主要原因”的错误认识。再者,在回顾性分析中,这种归类仅提供构成比,不能提供中药肝损伤的发生率。《中国的中医药》白皮书显示,2015年,全国中医类医疗卫生机构总诊疗人次达9.1亿,全国中医类医疗卫生机构出院人数2691.5万人。接受中药干预的人群在我国大陆数量庞大,有更多可能引起中药相关的肝损伤。此外,公众对药物安全性问题和DILI的认知尚不足,不按照说明书或医嘱服用中药,或服用来路不明的“偏方”“土方”,此均属于不合理用药的范畴,不能将由此造成的肝损伤笼统归因于中药。对此类情况应予以高度重视,加大对公众的宣教力度,严查各级医疗机构超规格、超剂量处方。笔者建议,可参考《国家基本药物目录(2018年版)》、《国家基本医疗保险、工伤保险和生育保险药品目录(2019年版)》的体系对DILI进行分类,在化学药品和生物制品、中成药和中药饮片三大类别之下,再分别归类。如将化学药和生物制品按临床药理学进行分类,中成药则根据功效分类,中药饮片则可用文字描述。保健品在我国是不能宣称具有任何治疗作用的,有必要对其单独分类。国家卫生健康委员会发布了药食同源的药物品种,在此范围内的中药保健品相对安全,其他类别在服用时仍需要谨慎对待。
国家食品药品监督管理局药品安全监管司在《药品不良反应报告和监测工作手册》(以下简称《手册》)中指出,药物不良反应的推断应遵循以下两点:停药或减量后,反应/事件是否消失或减轻;再次使用可疑药品后是否再次出现同样反应/事件。然而,目前的相关研究多为回顾性研究,无法按《手册》中的规定进行不良反应推断。RUCAM量表是当前常用的DILI诊断工具,在多项国内外大型DILI研究中均有使用。尽管RUCAM量表可应用于回顾性分析的研究,但受研究类型所限,难以提供准确资料进行评价,如用药至发病时间、停药后转氨酶的变化、非住院使用的伴随用药和再次用药反应,故在回顾性分析中应用该量表评估DILI因果关系的可靠性值得商榷。更新版本的RUCAM量表也更推荐其在前瞻性研究中使用,保证数据的完整性,无偏地对疾病做出专业的诊断[32]。虽然既往随机对照试验中大多都设计了如肝、肾功能等安全性的常规指标,但仅作为不良事件报告,仍缺乏相关信息做进一步的DILI不良反应因果推断;此外,随机对照试验受试者数量有限,随访时间较短,对于药物安全性的评价有局限。因此,DILI的大规模前瞻性队列研究是非常有必要的。
在探讨引起DILI的原因时,不同药物之间的相互作用不容忽视。药物相互作用是指一种药物的效应受到另一种药物的作用发生改变的现象[33]。即使单独用药时不会对肝功能产生影响,但在药物联合应用中,药物发生药效的靶点或药代动力学可能发生变化,从而产生药物性肝损伤。西药的相互作用研究信息相对完善,可查询相关专著或软件发现可能的相互作用[34]。中药与西药的相互作用研究信息目前比较缺乏,有待进一步探讨。对于DILI的流行病学研究设计而言,详细记录各种中西药的使用品种、用法用量、用药开始与结束的时间点、疗程和患者基本信息,有利于发现由药物相互作用带来的肝损伤。
未来对于DILI的流行病学研究需要全国性的大样本横断面调查,明确现患率。对于DILI的流行病学研究最佳设计是前瞻性队列研究,观察药物在更广泛人群中的使用情况。在药物干预的随机对照试验中,也可参考CONSORT Harms清单报告,提供更多信息以便进行不良反应推断[35]。
4 结论
目前未发现以中国大陆人群为研究总体的DILI横断面研究和前瞻性队列研究,无法得到DILI现患率、发生率等信息。了解中国大陆DILI的流行病学现状需要大样本的横断面研究和前瞻性队列研究,详细记录用药史,规范中西药品种分类方式,以及遵循不良反应推断原则对DILI进行诊断。

