金线莲呋甾皂苷26-O-β-葡萄糖苷酶基因克隆与表达分析
林江波,王伟英,邹 晖,戴艺民
(福建省农业科学院亚热带农业研究所,福建 漳州 363005)
0 引言
【研究意义】甾体皂苷是一类重要的生物活性物质,具有抗肿瘤、抗菌消炎、解痉挛和降血糖等多种药理活性[1],由甾体皂苷元骨架和1个或多个单糖或寡糖链缩合而成,结构复杂多样,主要存在于百合科(Liliaceae)[2-4]、薯蓣科(Dioscoreaceae)[5]等植物中。根据甾体皂苷元上F环结构的变化主要分为螺甾烷型、呋甾烷型和胆甾烷型等3类。呋甾皂苷 26-O-β-葡萄糖苷酶(furostanol glycoside 26-O-βglucosidase, F26G)催化呋甾烷型皂苷C-26糖苷键水解,形成螺甾烷型皂苷,是甾体皂苷代谢途径中的一个关键酶[6]。克隆金线莲(Anoectochilus roxburghii)F26G基因,分析其表达模式,对研究金线莲甾体皂苷的合成与代谢具有重要意义。【前人研究进展】黄楚君等[7]从兰科(Orchidaceae)石斛属(Dendrobium Sw.)的束花石斛(Dendrobium chrysanthumWall. ex Lindl.)中分离到变形螺甾烷醇类甾体皂苷。刘海等[8]从吉祥草 [Reineckia carnea(Andr.)Kunth]分离到3个甾体皂苷对人肾癌786-O细胞具有毒活性。Barile等[9]从葱属(Allium)植物A.minutiflorum中分离到3种具有抗菌活性的甾体皂苷,抗菌活性试验发现螺甾烷皂苷的抗菌活性比呋甾烷皂苷更强。闭鞘姜(Costus speciosus)的CSF26G基因编码562个氨基酸,与pET-22b连接后利用E. coliBL21能表达出高活性的F26G酶,催化呋甾烷型皂苷形成螺甾烷型皂苷[10-11]。Nakayasu 等[12]从Dioscorea esculenta中分离到DeF26G1的cDNA序列,编码566个氨基酸,属于GH1家庭β糖苷酶,能体外催化呋甾烷型皂苷形成螺甾烷型皂苷。金线莲是兰科(Orchidaceae)开唇兰属(Anoectochilus)植物,含有多糖、生物碱、黄酮、金线莲苷和甾体化合物等多种成分[13-16],是我国珍贵的中药材,具有保肝、降血压血糖、抗氧化和抗肿瘤等药理活性[17-18]。福建是全国金线莲种植和消费最大的省份,南靖、永安、武平等地都有较大规模的种植。目前,有关金线莲药效成分代谢相关基因的研究较少。【本研究切入点】F26G基因是甾体皂苷代谢途径中的一个关键酶,迄今为止,国内外还未有金线莲呋甾皂苷26-O-β-葡萄糖苷酶基因(ArF26G)的相关研究报道。【拟解决的关键问题】本研究通过金线莲转录组测序获得含有ArF26G基因5′末端的cDNA序列,利用RACE技术克隆金线莲ArF26G基因的cDNA全长,并分析不同温度和种植时间该基因在金线莲茎、叶中的表达,以期为进一步了解金线莲甾体皂苷的生物合成代谢调控机制提供参考。
1 材料与方法
1.1 试验材料及处理
试验材料由采自福建省龙岩市梅花山金线莲的种子,经过组织培养播种获得的组培生根苗。选取长势一致的组培生根瓶苗,用于种植和温度处理。2017年11月种植于温室大棚,基质为经过高压消毒的泥炭土,光照强度3 000~5 000 lx,空气相对湿度85%~90%,于种植 1、2、3、4、5、6个月各取样1次;生根瓶苗用培养箱5、15、25、35℃处理6 d后取样;每个样品随机选取长势一致的植株10株,分别取茎和叶,混匀,液氮速冻后-80℃保存备用。
1.2 金线莲ArF26G基因全长cDNA克隆
按照RNAiso Plus试剂说明书(TaKaRa)进行总RNA的提取,并利用分光光度计和琼脂糖凝胶电泳检验RNA的完整性和纯度。参照PrimeScriptTMReverse Transcriptase试剂说明书逆转录合成cDNA。
根据转录组测序信息设计3′RACE引物3F26-F1、3F26-F2 和 3′adaptor引物 dT-adapt、adapt,由生工生物工程(上海)股份有限公司合成(引物信息见表1,下同)。以3F26-F1和dT-adapt进行第一轮PCR,再以第一轮PCR产物为模板,以引物3F26-F2和adapt进行巢式PCR,PCR程序:94℃预变性5 min;94℃变性30 s,48℃退火30 s,72℃延伸50 s,30个循环;72℃延伸10 min。PCR产物经回收,与pMD19-T质粒载体连接后转化大肠杆菌DH5α感受态细胞,涂平板后37℃培养过夜,挑取单克隆于带Amp抗性的液体LB培养基37℃培养过夜,菌液经PCR鉴定后送生工生物工程(上海)股份有限公司测序。
1.3 生物信息学分析
在NCBI中用BLAST X和BLAST P程序分别搜索序列相似性和氨基酸保守结构域。利用ProtParam和在线工具SSPro(http://scratch.proteomics.ics.uci.edu/)预测ArF26G基因编码蛋白质产物的理化性质和二级结构,利用TargetP1.1(http://www.cbs.dtu.dk/services/TargetP/)预测蛋白质的亚细胞定位;采用MEGA 6.0软件分析、构建系统进化树[19]。

表1 PCR引物及其序列Table1 PCR primers and sequences
1.4 原核表达载体的构建与诱导表达
根据ArF26G基因开放阅读框(ORF)设计扩增上游引物F26-F(带BamHI酶切位点)和下游引物F26-R(带SacI酶切位点),PCR扩增程序:94℃预变性5 min;94℃变性30 s,58℃退火30 s,72℃延伸120 s,30个循环;72℃延伸10 min。胶回收PCR产物,回收产物和载体pET-28a(+)经BamHI和SacI双酶切,经胶回收、连接后转化大肠杆菌DH5α,挑取单克隆过夜培养,PCR验证后送上海生工生物工程有限公司测序。提取阳性克隆的质粒,获得重组原核表达质粒pET-28a-ArF26G。用冻融法把pET-28a-ArF26G转化大肠杆菌(E. coli)BL21(DE3),诱导表达和蛋白电泳参照林江波等[20]的方法。
1.5 表达分析
以提取的金线莲茎、叶总RNA为模板,使用PrimeScriptTMReverse Transcriptase逆转录合成cDNA,用超微量紫外可见光分光光度计(ND-1000)将cDNA浓 度定量为 100 ng·μL-1。根据 TaKaRa TB GreenTMPremixEx TaqTMⅡ(Tli RNaseH Plus)说明书及Roche LightCycler 96荧光定量PCR仪的操作要求进行实时荧光定量PCR。以ArF26G基因全长cDNA序列设计荧光定量PCR引物F26G-F和F26G-R。选择金线莲Actin为内参基因[21],引物为ArACT-F和ArACT-R。反应体系 20 μL:cDNA 模板3 μL,TB GreenTMPremix Ex TaqTMⅡ(Tli RNaseH Plus)10 μL,上游引物1 μL,下游引物1 μL,ddH2O 补充至 20 μL。反应程序:95℃预变性30 s;95℃变性10 s,60℃退火20 s,45个循环,每个处理设置3个生物学重复。
1.6 数据处理
方差分析利用DPS数据处理软件,多重比较采用新复极差法(Duncan法)。
2 结果与分析
2.1 金线莲ArF26G基因全长cDNA和ORF的克隆
以金线莲组培苗提取的总RNA反转录的cDNA为模板,利用巢式PCR扩增法,经二轮的PCR扩增后获得一条500 bp的清晰条带(图1A),经过克隆和测序,结果表明获得目的基因的3′末端。利用DNAMAN V6.0进行序列拼接和ORF分析,结果表明:cDNA全长1 982 bp(图2),含有1个1 764 bp的ORF,编码587个氨基酸,5′末端非翻译区60 bp,3′末端非翻译区 158 bp。
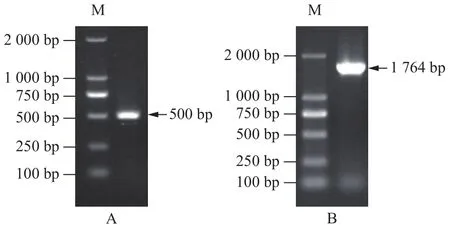
图1 PCR电泳结果Fig.1 PCR products by electrophoresis
以反转录的cDNA为模板,用引物F26-F和F26-R进行PCR扩增,PCR产物电泳结果显示在1 800 bp左右有一条亮带(图1B),测序结果表明:目的片段与拼接结果一致,获得了带BamHⅠ和SacⅠ酶切位点的ORF。
2.2 金线莲ArF26G蛋白生物信息学分析
通过Protparam在线分析ArF26G基因编码的氨基酸,结果表明:该蛋白质分子式为C2999H4554N782O902S15,分子量为66.48 kD,带负电氨基酸(Asp+Glu)76个,带正电氨基酸(Arg+Lys)63个,理论等电点(pI)为5.31,脂肪系数为75.08,总平均疏水性为-0.465,不稳定系数为37.92,属稳定蛋白。
SSPro(http://scratch.proteomics.ics.uci.edu/)在线工具对ArF26G蛋白质二级结构的预测结果(图3)表明,形成无规则卷曲的氨基酸残基有273个,占46.5%;形成α螺旋的氨基酸残基有215个,占36.63%;形成β折叠的氨基酸残基有99个,占16.87%。

图2 金线莲ArF26G基因cDNA序列及其推导的氨基酸序列Fig.2 The cDNA and its deduced amino acid sequence of ArF26G from Anoectochilus roxburhii
利用NCBI的BLAST P在线搜索ArF26G蛋白的保守结构域,相匹配的是Glycosyl hydrolase 1(GH1)superfamily结构域,E值为8.20×10-129,ArF26G蛋白的氨基酸序列与海枣(Phoenix dactylifera, XP_00 8791712)、芦笋(Asparagus officinalis, XP_020250593)、闭鞘姜(Cheilocostus speciosus, Q42707)的F26G氨基酸序列相似性分别为67%、69%和65%。利用TargetP1.1预测ArF26G蛋白的亚细胞定位,结果显示ArF26G定位于叶绿体,N端的33个氨基酸残基为叶绿体转运肽。
采用MEGA6.0软件对ArF26G的氨基酸序列和其他9个具有GH1保守结构域物种的氨基酸序列进行最大简约法聚类分析,结果表明(图4),10个物种聚为4类,金线莲与桃红蝴蝶兰(Phalaenopsisequestris)和深圳拟兰(Apostasia shenzhenica)等兰科植物聚为一类,与深圳拟兰的亲缘关系最近,闭鞘姜、芦笋和海枣聚为一类,藏红花(Crocus sativus)单独聚为一类,麻风树(Jatropha curcas)和荷花(Nelumbo nucifera)聚为一类。
2.3 原核表达载体的构建与诱导表达
与不携带质粒pET-28a-ArF26G诱导表达和携带质粒pET-28a-ArF26G不诱导表达的大肠杆菌BL21(DE3)相比,携带重组质粒pET-28a-ArF26G的大肠杆菌BL21(DE3)经诱导表达后出现1条约66.48 kD的粗蛋白条带,表明ArF26G基因能在大肠杆菌中有效表达(图5)。

图3 ArF26G蛋白的二级结构预测Fig.3 Predicted secondary structure of ArF26G

图4 ArF26G与其他物种GH1结构域蛋白的系统进化树Fig.4 Phylogenetic tree of ArF26G and GH1 domain proteins of other plants
2.4 ArF26G的表达分析
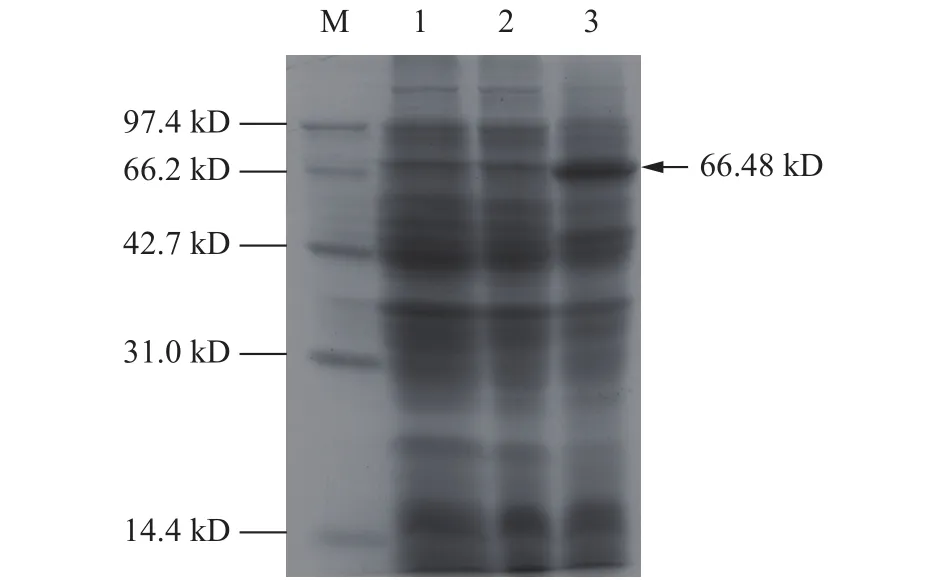
图5 ArF26G基因在大肠肝菌中表达的SDS-PAGE电泳Fig.5 SDS-PAGE of ArF26G expressed in Esherichia coli.
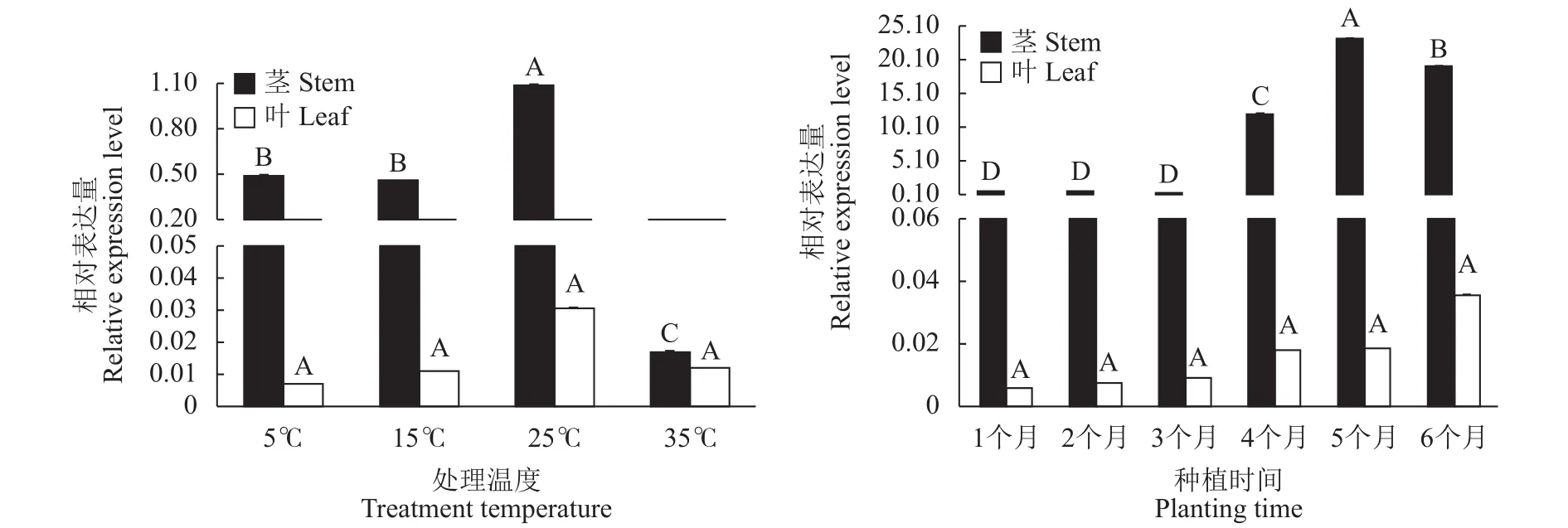
图6 不同处理温度和种植时间ArF26G在茎和叶中的相对表达量Fig.6 Relative expression of ArF26G in stem and leaf under different treatment temperature and planting time.
以25℃处理金线莲组培苗茎为参照,设ArF26G基因相对表达量为1,比较不同处理温度和种植时间ArF26G基因在茎和叶中的表达量。从图6可以看出,茎和叶都能检测到ArF26G基因的表达,但在叶片中的表达量很低。4种处理温度下,叶的ArF26G基因表达量差异不显著,茎25℃时表达量最高,与其他3个温度的表达量极显著差异。不同种植时间,叶ArF26G基因的表达量差异不显著,茎的ArF26G基因表达量差异极显著。种植后的前3个月ArF26G基因在茎中的表达量差异不显著,种植4个月,茎ArF26G基因的表达量急剧上升,4、5、6个月的表达量分别是25℃处理组培瓶苗的11.9、23.3和19.0倍,与种植1-3个月的表达量极显著差异。
3 讨论与结论
本研究克隆了金线莲ArF26G基因,编码587个氨基酸,细胞定位于叶绿体,N端的33个氨基酸残基为叶绿体转运肽,其推导的氨基酸序列具有1个GH1 superfamily,E值为 8.20×10-129,与海枣、芦笋、闭鞘姜的F26G氨基酸序列相似性分别为67%、69%和65%,推断该基因为金线莲的ArF26G基因。金线莲ArF26G基因在茎中的表达量极显著高于叶,金线莲组培苗经25℃处理的表达量最高。当金线莲种植时间达4个月时,ArF26G基因在茎中的表达量是25℃处理组培苗茎的11.9倍,种植5个月达到23.3倍,推测种植4个月后金线莲茎有螺甾烷型皂苷累积,这需要进一步分析金线莲甾体皂苷类化合物的组成和种植过程含量的变化来进一步验证。
植物GH1类β-葡萄糖苷酶参与了对微生物、昆虫和食草动物的防御反应[22]。甾体皂苷由作为糖苷配基的甾体骨架和与C3、C26羟基相连的低聚糖单元组成,当细胞受到损伤,F26G水解呋甾烷型皂苷C-26糖苷键,形成具有生物活性的螺甾烷型皂苷[12]。F26G的活性不受C-22的羟基、甲氧基、双键或C-3的葡萄糖链的影响,但C-23甲氧基会降低F26G的活性[23],不同植物来源F26G催化的底物和催化活性存在差异。闭鞘姜的CsF26G1以原纤细薯蓣皂苷和原薯蓣皂苷为底物水解形成纤细薯蓣皂苷和薯蓣皂苷[10]。NAKAYASU等[12]克隆了Dioscorea esculenta的DeF26G1基因,编码566个氨基酸,N端的80个氨基酸残基是叶绿体转运肽,成熟蛋白含486个氨基酸残基,属GH1 superfamily,水解原薯蓣皂苷C26糖苷键形成薯蓣皂苷,但不能水解C3糖苷键,成熟蛋白的催化活性强于完整蛋白;DeF26G1基因在叶中的表达量是块茎的6倍,表达模式与催化底物原薯蓣皂苷的分布模式一致。本研究克隆的金线莲ArF26G基因编码的氨基酸的N端也有叶绿体转运肽,但氨基酸残基比DeF26G1少,其催化活性和在金线莲中的催化底物及合成产物有待进一步研究。

